switch to new site
parent
16c2001886
commit
869a7a97d0
|
|
@ -7,3 +7,10 @@ indent_size = 2
|
|||
indent_style = space
|
||||
insert_final_newline = true
|
||||
trim_trailing_whitespace = true
|
||||
|
||||
[themes/tfsci/**/*.html]
|
||||
insert_final_newline = false
|
||||
|
||||
[scripts/Custom*.txt]
|
||||
indent_size = 1
|
||||
indent_style = tab
|
||||
|
|
|
|||
|
|
@ -0,0 +1,4 @@
|
|||
# https://github.com/github/linguist/blob/master/docs/overrides.md
|
||||
content/**/* linguist-documentation
|
||||
scripts/**/* linguist-vendored
|
||||
themes/**/* linguist-vendored
|
||||
|
|
@ -0,0 +1,32 @@
|
|||
name: Publish Site
|
||||
|
||||
on:
|
||||
push:
|
||||
branches:
|
||||
- main
|
||||
paths-ignore:
|
||||
- .github
|
||||
- README.md
|
||||
- LICENSE
|
||||
|
||||
jobs:
|
||||
deploy:
|
||||
runs-on: ubuntu-22.04
|
||||
if: "! contains(toJSON(github.event.commits.*.message), '[skip ci]')"
|
||||
steps:
|
||||
- uses: actions/checkout@v3
|
||||
- uses: actions/setup-node@v3
|
||||
- uses: peaceiris/actions-hugo@v2
|
||||
with:
|
||||
hugo-version: latest
|
||||
extended: true
|
||||
- run: sudo apt-get install opencc
|
||||
- run: npm ci
|
||||
- run: ./scripts/opencc.sh
|
||||
- run: hugo --minify
|
||||
env:
|
||||
HUGO_DISABLELANGUAGES: ''
|
||||
- run: npx wrangler pages publish public --project-name tfsci --branch main
|
||||
env:
|
||||
CLOUDFLARE_API_TOKEN: ${{ secrets.CF_API_TOKEN }}
|
||||
CLOUDFLARE_ACCOUNT_ID: ${{ secrets.CF_ACCOUNT_ID }}
|
||||
|
|
@ -0,0 +1,22 @@
|
|||
# Generated files by hugo
|
||||
/public/
|
||||
/resources/_gen/
|
||||
/assets/jsconfig.json
|
||||
hugo_stats.json
|
||||
|
||||
# Executable may be added to repository
|
||||
hugo.exe
|
||||
hugo.darwin
|
||||
hugo.linux
|
||||
|
||||
# Temporary lock file while building
|
||||
/.hugo_build.lock
|
||||
|
||||
# Node.js
|
||||
/node_modules
|
||||
|
||||
# I18n
|
||||
/content.zh-tw
|
||||
/content.zh-hk
|
||||
/data/*.zh-tw.yaml
|
||||
/data/*.zh-hk.yaml
|
||||
|
|
@ -0,0 +1,7 @@
|
|||
{
|
||||
"emphasis-style": false,
|
||||
"line-length": false,
|
||||
"no-blanks-blockquote": false,
|
||||
"no-inline-html": false,
|
||||
"no-emphasis-as-header": false
|
||||
}
|
||||
|
|
@ -0,0 +1,2 @@
|
|||
*.md
|
||||
*.html
|
||||
|
|
@ -0,0 +1,6 @@
|
|||
{
|
||||
"quoteProps": "consistent",
|
||||
"singleQuote": true,
|
||||
"printWidth": 120,
|
||||
"semi": false
|
||||
}
|
||||
|
|
@ -1,7 +0,0 @@
|
|||
{
|
||||
"recommendations": [
|
||||
"EditorConfig.EditorConfig",
|
||||
"esbenp.prettier-vscode",
|
||||
"DavidAnson.vscode-markdownlint"
|
||||
]
|
||||
}
|
||||
|
|
@ -3,5 +3,16 @@
|
|||
"editor.codeActionsOnSave": {
|
||||
"source.fixAll": true
|
||||
},
|
||||
"editor.defaultFormatter": "esbenp.prettier-vscode"
|
||||
"editor.defaultFormatter": "esbenp.prettier-vscode",
|
||||
"files.associations": {
|
||||
"**/archetypes/*": "plaintext",
|
||||
"*.xml": "plaintext",
|
||||
"_redirects": "plaintext",
|
||||
"_headers": "plaintext"
|
||||
},
|
||||
"search.exclude": {
|
||||
"**/node_modules": true,
|
||||
"/themes/**/*": true,
|
||||
"/scripts/**/*": true
|
||||
}
|
||||
}
|
||||
|
|
|
|||
|
|
@ -1,14 +1,14 @@
|
|||
# Transfeminine Science License
|
||||
# Transfeminine Science LICENSE
|
||||
|
||||
Transfeminine Science is [Copyright](https://en.wikipedia.org/wiki/Copyright) of [Aly W][aly-w].
|
||||
and the other authors of Transfeminine Science.
|
||||
|
||||
[All rights are reserved](https://en.wikipedia.org/wiki/All_rights_reserved).
|
||||
Please do not reproduce content from Transfeminine Science unless given direct permission from [Aly W][aly-w].
|
||||
|
||||
(e.g., for [translation projects](https://transfemscience.org/misc/#transfeminine-science-translations)).
|
||||
|
||||
If permission to reproduce content is granted, the content should be properly attributed and linked back to the original page(s) on Transfeminine Science.
|
||||
If permission to reproduce content is granted,
|
||||
the content should be properly attributed and linked back to the original page(s) on Transfeminine Science.
|
||||
|
||||
see <https://transfemscience.org/about/#license>
|
||||
|
||||
|
|
|
|||
88
README.md
88
README.md
|
|
@ -1,49 +1,65 @@
|
|||
# “女性倾向跨性别者科学”中文译本存档站
|
||||
# Transfeminine Science (MtF.wiki Chinese Copy)
|
||||
|
||||
“**女性倾向跨性别者科学**”是一个有关<u>女性倾向跨性别者激素疗法(transfeminine hormone therapy)</u>的原创信息资源站。对此类激素疗法,人们多称之为:女性化激素疗法(feminizing hormone therapy,FHT);用于女性倾向跨性别者的性别肯定激素疗法(gender-affirming hormone therapy,GAHT);以及男跨女(MtF)激素替代疗法(HRT)——后者在早年更为常见。该疗法需要服用女性性激素(包括雌激素及孕激素)和抗雄激素制剂,以达到跨性别女性及非二元性别(女性倾向)群体的女性化、去男性化、缓和性别焦虑的目的。
|
||||
→ *[English Introduction](#welcome)*
|
||||
|
||||
本站的文章由多位撰稿人编写,皆与女性倾向跨性别者激素疗法有关。撰稿人及其资料已列于“[关于本站][about]”页面的“[作者][authors-about]”一节。
|
||||
本站由跨性别者撰稿,为跨性别者及其医师服务。在“[文章][articles]”页面,可见本站文章的分类列表。此外,在“[最新文章][latest]”页面可见按发表时间倒序排列的文章列表。而在“[杂项][misc]”页面,则囊括了实用工具、重要的公开发表材料、网页链接等不同类型的内容。
|
||||
本站文章随时可更新及优化,即“活的文章”。本站所有新文章在发表之前会经过合伙撰稿人的非正式同行评议。
|
||||
欢迎来到 [MtF.wiki][wiki] 附属的“女性倾向跨性别者科学”(*[Transfeminine Science][origin]*)中文译本存档站。原文由一群非相关专业出身、却热情洋溢的多国跨性别人士所作,旨在为**女性化激素治疗**提供力所能及的指引,行文严谨、讨论细致、引经据典,具有相当的可信度。本项目则旨在**忠实转达**这些文章的内容和观点,以资参考。
|
||||
|
||||
## 译文分类一览
|
||||
为便于翻阅、减少翻译工作量,本站译者会从上百篇原文当中精心挑选一部分进行翻译;同时,边翻译边学习,促进 MtF.wiki 内容的完善。因此,本站内容可视作对 MtF.wiki 药物板块的先行或拓展参考。\
|
||||
由于原文内容随时会修订,而本站译者不一定有时间与精力实时跟进;因此,**译文修订间隔**暂定为 **3 - 12 个月**。如有不便,敬请谅解。
|
||||
|
||||
### 综合性文章
|
||||
> 本站除簡體中文外,還提供繁體中文版本,以便港澳台用戶閱覽;需要注意,此版本從簡體中文底稿自動轉換而來,或與港澳台地區語言習慣不符。
|
||||
|
||||
- [女性倾向跨性别者的激素治疗简介](articles/transfem-intro.md) (Aly W., 2018)
|
||||
- [对非二元女性倾向跨性别者的激素治疗可能性的探索](articles/nonbinary-transfem-overview.md) (Aly W., 2019)
|
||||
## 致谢
|
||||
|
||||
### 特定主题类
|
||||
本项目已得到 *Transfeminine Science* 的维护者兼撰稿人:[Aly W.][aly] 的二次创作许可。\
|
||||
本项目基于 [tfsci-sc/articles][origin-cn] 项目的早前工作而建。没有 ta 们的先行,就没有如今的这个项目。
|
||||
|
||||
#### 雌激素
|
||||
本站目前以 [Hugo][hugo] 构建,并部署于 [Cloudflare Pages][site-url]。
|
||||
|
||||
- [对女性倾向跨性别者舌下含服雌二醇以取代口服雌二醇的探索](articles/sublingual-e2-transfem.md) (Sam S., 2021)
|
||||
- [关于女性倾向跨性别者舌下含服戊酸雌二醇片剂的简介](articles/sublingual-ev.md) (Aly W., 2019)
|
||||
- [关于女性倾向跨性别者以阴囊及新阴唇给予透皮雌二醇可极大增强吸收率的简论](articles/genital-e2-application.md) (Aly W., 2019)
|
||||
- [性激素与性激素结合球蛋白的相互作用及其对女性化激素疗法的意义](articles/shbg.md) (Aly W., 2020)
|
||||
- [有关雌二醇注射剂的雌二醇浓度曲线的一次非正式荟萃分析](articles/injectable-e2-meta-analysis.md) (Aly W., 2021)
|
||||
## 联系方式
|
||||
|
||||
#### 抗雄激素制剂
|
||||
|
||||
- [低剂量的醋酸环丙孕酮足以最大限度地抑制女性倾向跨性别者的睾酮水平](articles/cpa-dosage.md) (Aly W., 2019)
|
||||
- [法国关于醋酸环丙孕酮和脑膜瘤风险的研究的最新进展以及对女性倾向跨性别者的影响](articles/cpa-meningioma.md) (Aly W., 2020)
|
||||
- [比卡鲁胺在女性化激素治疗方面的使用状况,以及医学界对其的接受情况](articles/bica-adoption.md) (Aly W., 2020)
|
||||
|
||||
#### 孕激素
|
||||
|
||||
- [口服孕酮及其引起的低孕酮水平与较弱效力的简论](articles/oral-p4-low-levels.md) (Aly W., 2018)
|
||||
|
||||
#### 激素治疗引起的普遍效果与风险
|
||||
|
||||
- [关于女性化激素疗法与乳腺癌风险的简述](articles/breast-cancer.md) (Aly W., 2020)
|
||||
如有任何对本站及诸译文的改进建议、勘误等,可发送邮件至专用邮箱 <tfsci@mtf.wiki>;不过,涉及到原文观点的应向 *Transfeminine Science* 的撰稿人直接反馈。\
|
||||
此外,还可通过提交 Pull Request 对译文、[简繁术语对照表](scripts/CustomTW.txt)等进行改进。
|
||||
|
||||
## 版权声明
|
||||
|
||||
[LICENSE](LICENSE.md)
|
||||
本站文章适用于 *Transfeminine Science* 的版权声明([原文][license]):
|
||||
|
||||
[author-en]: about.md#aly-w
|
||||
[about]: about.md
|
||||
[authors-about]: about.md#作者一览
|
||||
[articles]: #译文分类一览
|
||||
[latest]: https://transfemscience.org/articles-by-date/
|
||||
[misc]: https://transfemscience.org/misc/
|
||||
> 本站版权归 Aly W. 及本站其他撰稿人所有;保留一切权利。未经 Aly W. 允许,请勿对本站内容进行二次创作(如翻译项目)。如获得许可,请准确署名,并设置指向本站原文的链接。
|
||||
|
||||
此外,本站设计元素与其它补充内容的版权归 MtF.wiki 所有。
|
||||
|
||||
--------
|
||||
|
||||
## Welcome
|
||||
|
||||
Welcome to the Archive Site of Chinese Translations, a project under [MtF.wiki][wiki], to *[Transfeminine Science][origin]*. The original articles were written by non-professional but highly dedicated transgender individuals from several countries, for the purpose of providing useful information on *feminizing hormone therapy*, and with causal analysis, detailed discussions and enormous references, all of which have made them highly acceptable and reliable.\
|
||||
Accordingly, this project aims to bring these valued contents to Chinese readers, as accurately and fluently as possible, for reference.
|
||||
|
||||
For better experience and less workload for translation, the Translators would carefully pick up a subset of original articles to translate, and to further enhance the information on MtF.wiki. As such, this site can be considered as a reference or a pilot discussion for the subject of medications on MtF.wiki.\
|
||||
The original articles can be revised by their Authors *at any time*; also, the Translators may have little spare time or concentration on tracking such changes. Hence, **the interval of full revision** on translations has been determined to about **3 - 12 months**. The Translators would apologize for any inconvinience caused by out-dated contents.
|
||||
|
||||
## Thank you
|
||||
|
||||
The Translators would thank [Aly W.][aly], the maintainer and one of the authors of *Transfeminine Science*, for her permission on this project.\
|
||||
Also, the Translators would thank contributors from the previous translating project [tfsci-sc/articles][origin-cn]; without their previous fantastic work, this project might not be ever established.
|
||||
|
||||
The archive site is built with [Hugo][hugo], and deployed onto [Cloudflare Pages][site-url].
|
||||
|
||||
## Contact
|
||||
|
||||
For any recommendations or erratum on this site or translations, please send an e-mail to <tfsci@mtf.wiki>; however, for any discussion on ideas from the articles, please contact directly to their corresponding Authors.\
|
||||
Pull requests are welcomed as well.
|
||||
|
||||
## Licenses
|
||||
|
||||
All of the translations on this site comply under the [License][license] from *Transfeminine Science*.\
|
||||
The design and other supplements of this site are copyrights of MtF.wiki.
|
||||
|
||||
[wiki]: https://mtf.wiki
|
||||
[origin]: https://transfemscience.org
|
||||
[aly]: https://transfemscience.org/about/#aly-w
|
||||
[origin-cn]: https://github.com/tfsci-sc/articles
|
||||
[hugo]: https://gohugo.io
|
||||
[site-url]: https://tfsci.mtf.wiki
|
||||
[license]: LICENSE.md
|
||||
|
|
|
|||
|
|
@ -0,0 +1,12 @@
|
|||
{{- $created := .Date | time | dateFormat "2006-01-02" -}}
|
||||
---
|
||||
title: {{ .Name }}
|
||||
description: ''
|
||||
author: Aly W.
|
||||
published: {{ $created }}
|
||||
updated: {{ $created }}
|
||||
translated: {{ $created }}
|
||||
translators:
|
||||
- Bersella AI
|
||||
draft: true
|
||||
---
|
||||
|
|
@ -1,42 +0,0 @@
|
|||
# 一个综合女性化激素疗法信息的网站:“女性倾向跨性别者科学”建站声明
|
||||
|
||||
> - 作者 [Aly W.](https://transfemscience.org/articles-by-author/aly-w/)
|
||||
> + 首次发表于 2020 年 10 月 5 日
|
||||
> + 最后修改于 2022 年 1 月 21 日
|
||||
> + [原文出处](https://transfemscience.org/articles/announcement/)
|
||||
> - 译者 [Bersella AI](https://bersella-ai.cc/about-me/)
|
||||
> + 翻译于 2022 年 11 月 16 日
|
||||
|
||||
我们曾在 2017 年末在 Reddit 创建了新栏目 [r/MtFHRT][r-mtfhrt],旨在创建、收集、分享有关女性化激素疗法的资讯内容。该栏目最初接受任何相关内容的投稿;但投稿逐渐以原创文章为主。多年来该栏目内容得到了极大丰富。
|
||||
|
||||
读者可能已发现,最近数月里未曾有新内容在 r/MtFHRT 栏目投稿;其实,我们正全力专注于一个全新的项目:
|
||||
|
||||
**“女性倾向跨性别者科学”**(https://www.transfemscience.org/)
|
||||
|
||||
本站是有关女性化激素疗法的原创信息资源站。本站也是给 r/MtFHRT 栏目准备的全新升级的家,其中许多内容已迁移至本站,也有相当一些文章得到了重要修订。今后,由我们 r/MtFHRT 栏目团队撰写的内容将改为从本站发表。
|
||||
不过,我们当然仍将通过 r/MtFHRT 栏目分享新的内容,并同时发在 [r/TransDIY][r-transdiy] 和 [r/AskMtFHRT][r-askmtfhrt] 等其它栏目。我们还将在 Reddit 以外的社交平台(如 [Facebook][fb] 与 [Twitter][twi])发布新文章的链接。
|
||||
|
||||
为了克服 Reddit 作为我们的资讯内容发布平台的诸多局限,我们决定将内容迁移至本站。促成我们迁移的重要动机有:Reddit 上发表的内容可定制性与功能不足;Reddit 的编辑界面问题颇多、令人恼火;我们的内容也需要有一个专门、独立的发布平台;尤其重要的是,Reddit 帖子和评论有字数限制。
|
||||
|
||||
本站既已上线,我们的工作重点将回到资讯内容的创作上来。我们正筹备许多我们颇感兴趣的文章,正计划于本站发布;本站既有内容也会继续得到修订与优化。为符合本站的高标准,许多文章仍有待修订。
|
||||
|
||||
r/MtFHRT 栏目一直是欢迎任何人投稿的地方。不过有一点,我们决定只有特定的人能够在此发帖,并设置对新内容进行非正式同行评议的流程。这些措施旨在提高该栏目信息的质量与可靠度。不过很遗憾,我们启用这些措施之后,只有极少的新帖子由非团队成员的 Reddit 用户发布——这些帖子也无一符合可得到我们认可或完整同行评议的门槛。尽管如此,我们仍将接受原创文章的投稿,并进行同行评议;甚而可能发布到本站上。如果你有任何可能有所贡献的内容,欢迎[联系我们][contact]!
|
||||
|
||||
在此致谢所有关注我们的读者。希望读者们能在本站有所收获、怡然其中。
|
||||
|
||||
——“女性倾向跨性别者科学”运营团队:[Aly][aly], [Lain][lain] 与 [Sam][sam]
|
||||
|
||||
-------
|
||||
|
||||
**又记:**本站上线之后,r/MtFHRT 栏目转为本站的官方 Reddit 讨论区;本站有新文章发布时,其链接也于此处公布。不过,我们此后决定将我们的活动从 r/MtFHRT 转移至新栏目 [r/TransfemScience][r-tfsci]。
|
||||
|
||||
[r-mtfhrt]: https://reddit.com/r/MtFHRT/
|
||||
[r-transdiy]: https://reddit.com/r/TransDIY/
|
||||
[r-askmtfhrt]: https://www.reddit.com/r/AskMtFHRT/
|
||||
[fb]: https://www.facebook.com/TransfemScience
|
||||
[twi]: https://twitter.com/TransfemScience
|
||||
[contact]: ../about.md#联系我们
|
||||
[aly]: ../about.md#aly-w
|
||||
[lain]: ../about.md#lain-m
|
||||
[sam]: ../about.md#sam-s
|
||||
[r-tfsci]: https://reddit.com/r/TransfemScience
|
||||
|
|
@ -1,328 +0,0 @@
|
|||
# 关于女性倾向跨性别者以阴囊及新阴唇给予透皮雌二醇可极大增强吸收率的简论
|
||||
|
||||
> - 作者 [Aly W.][AUTHOR]
|
||||
> + 首次出版于 2019 年 3 月 29 日
|
||||
> + 最后修改于 2022 年 4 月 27 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [昭心][TRANSLATOR]、[Bersella AI][REVISOR]
|
||||
> + 翻译于 2022 年 11 月 14 日
|
||||
|
||||
[ORIGIN]: https://transfemscience.org/articles/genital-e2-application/
|
||||
[AUTHOR]: https://transfemscience.org/about/#aly-w
|
||||
[TRANSLATOR]: https://limelight.moe/u/昭心
|
||||
[REVISOR]: https://bersella-ai.cc/about-me/
|
||||
|
||||
## 译者按
|
||||
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
--------
|
||||
|
||||
## 摘要
|
||||
|
||||
> 外生殖器皮肤(如阴囊、阴茎和阴唇皮肤)的吸收能力似乎要强于其它皮肤区域。人们通常会将雌二醇、睾酮等透皮激素制剂应用于手臂、臀部和腹部等区域;不过对于外生殖器给药却鲜有研究。
|
||||
> 通常 100 μg/天剂量的雌二醇透皮贴片可引起平均约 100 pg/ml 的雌二醇水平。在阿根廷,有一项关于前列腺癌患者通过阴囊使用雌二醇贴片的临床研究发现,阴囊给药所提供的雌二醇水平比前臂给药高得多;在此 100 μg/天剂量的雌二醇透皮贴片能引起平均 500 pg/ml 的雌二醇水平。这与以下认知一致:阴囊给药的效率是常规皮肤部位的 5 倍。
|
||||
> 至于雌二醇透皮凝胶用于外生殖器的用法,至今尚未有文献评估;但有关睾酮凝胶与乳剂用于阴囊的研究已发现,相比于常规皮肤部位,阴囊给药引起的睾酮水平要高出 5-8 倍。由于雌二醇与睾酮的化学性质相似,且通过阴囊给予的雌二醇贴片同样可达到高雌二醇水平,故这项发现应该可推导至雌二醇凝胶。
|
||||
> 对于女性化激素治疗,外生殖器对雌二醇的高吸收率也许大有可为。如果女性倾向跨性别者通过透皮给药并不能达到理想的雌二醇水平,需要更高水平(例如在高剂量雌激素单药疗法当中)来抑制睾酮;那么可改为外生殖器给药。
|
||||
|
||||
## 前言
|
||||
|
||||
雌二醇可通过多种[形式][WIKI1]与[途径][WIKI2]给药<sup>([维基百科][WIKI3])</sup>。其中一种途径是[透皮给药][WIKI4],其形式包括[雌二醇贴片][WIKI3-TP]、[凝胶][WIKI3-TG]、[乳剂][WIKI3-OTF]与[喷雾剂][WIKI3-OTF];不过,贴片与凝胶是迄今使用最多的。传统上,透皮雌二醇会被应用于手臂、腹部等皮肤部位。
|
||||
每块 100 μg/天的雌二醇贴片通常可引起 50-100 pg/mL 左右的雌二醇水平;而每 3 mg/天的雌二醇凝胶引起的水平通常约为 100 pg/mL<sup>([Aly W., 2020][AW20-EED]; [维基百科][WIKI3])</sup>。不过,雌二醇水平[在个体间差别][WIKI4]显著<sup>([维基百科][WIKI3-VIP])</sup>;在透皮雌二醇的形式与剂量相同的情况下,某些人会有偏高或者偏低的雌二醇水平。对一部分人而言,其雌二醇水平可能低得不足以产生理想的疗效,对睾酮的抑制作用也不充分;如使用高剂量透皮雌二醇单药疗法,其也很难获得抑制睾酮所需的高雌二醇水平。
|
||||
|
||||
1960 年代,一篇有关[氢化可的松][WIKI6]用于人皮肤不同部位的透皮[吸收率][WIKI7]的临床研究论文公开发表<sup>([Feldmann & Maibach, 1967][FM67]; [相关材料][FM67-SUPPL])</sup>。(需要指出,氢化可的松——也称[皮质醇][WIKI6A]——作为一种[甾体激素][WIKI8],在结构上与[雌二醇][WIKI9]、[睾酮][WIKI10]等[性激素][WIKI11]很相似。)此研究将氢化可的松[用放射性同位素标记][WIKI12],并将其溶液涂抹于男性的不同皮肤部位,然后对用药后排出的尿液中的放射性物质(氢化可的松及其代谢物)之含量进行测定<sup>(Feldmann & Maibach, 1967)</sup>。
|
||||
研究者发现,尿液的放射性在不同用药部位之间有很大分别;其中,[阴囊][WIKI13]给药后所检出的放射性远远高于前臂及其它部位。不同部位用药后的尿液放射性系数分别为(以前臂为基准,由高到低)<sup>(Feldmann & Maibach, 1967)</sup>:
|
||||
|
||||
- 阴囊(42.0)
|
||||
- 下颌角(13.0)
|
||||
- 前额(6.0)
|
||||
- 腋下(3.6)
|
||||
- 头皮(3.5)
|
||||
- 背部(1.7)
|
||||
- **前臂(1.0)**
|
||||
- 手掌(0.8)
|
||||
- 脚踝(0.4)
|
||||
- 足底(0.1)
|
||||
|
||||
这是第一项表明了外生殖器(如阴囊)皮肤的透皮吸收率可显著高于其它皮肤部位的研究。
|
||||
|
||||
从阴囊对氢化可的松及其它药物吸收更佳的发现,也衍生出了一个问题:雌二醇与睾酮用于外生殖器是否也具有更大的[生物利用度][WIKI14]。其中睾酮已在 1980 年代被确认有此特性,此后睾酮的阴囊贴片(品牌 Testoderm)得以研发并于 1993 年在美国批准上市<sup>([Place et al., 1990][P90]; [Mazer et al., 1992][M92]; [Atkinson, Chang, & Snyder, 1998][ACS98])</sup>。
|
||||
与此相反的是,透皮雌二醇似乎从未被研究用于阴囊;这也许是因为雌激素极少用于男性。不过,最近笔者偶然发现了这篇很晦涩的、关于患[前列腺癌][WIKI15]的男性在[高剂量雌激素疗法][WIKI16]当中通过阴囊使用[雌二醇透皮贴片][WIKI17]的研究论文:
|
||||
|
||||
- Premoli, F., Re, I., Asenjo, G., Maximino, G., & Micheletti, L. (2005).
|
||||
Tratamiento del Cáncer de Próstata Avanzado con Estrógenos Transdérmicos Escrotales (ETE). [阴囊给药的透皮雌激素贴片(TSEP)在晚期前列腺癌治疗当中的应用]
|
||||
*Revista Argentina de Urología, 70*(4), 231–241.
|
||||
[[Google 学术][P05]] [[网页地址][P05-ARCHIVE]] [[PDF 文档][P05-PDF]] [[英译文][P05-ENG]]
|
||||
|
||||
这应该是第一项、也是迄今唯一一项调研阴囊给药的透皮雌二醇的研究。其论文并非以英语撰写,因此早前的文献检索并未发现之。
|
||||
在讨论该研究的结果之前,下文将会介绍关于阴囊给药的[透皮雌二醇][WIKI18]的一些背景和原理。如读者对研究结果更感兴趣,可跳转到“[研究结果](#研究结果)”一章。
|
||||
|
||||
## 背景
|
||||
|
||||
高剂量的[雌激素][WIKI19]有很强的[抗雄激素][WIKI20]效力,因此常作为一种[雄激素匮乏疗法][WIKI21],用于男性前列腺癌的治疗。具体而言,雌激素可通过其[抗促性腺激素][WIKI22]作用来抑制性腺[睾酮][WIKI23]的产生;同时,还可增加[性激素结合球蛋白][WIKI24] (SHBG) 的产生和血清水平,以降低游离(即具备生物活性)的[雄激素][WIKI25]之比例。大剂量雌激素疗法的抗雄效力,与[性腺切除术][WIKI26]和[促性腺激素释放激素][WIKI27] (GnRH) [激动剂][WIKI28]、[拮抗剂][WIKI29]相当,不过其具有独特的优缺点。
|
||||
雌激素疗法的优点包括减少[潮热][WIKI30]、保持[骨密度][WIKI31]、保留部分[性欲][WIKI32]、改善[生活质量][WIKI33]、以及低得多的成本。其缺点包括[女性化][WIKI34]、[男性乳房发育症][WIKI35](对顺性别男性来说乳房发育当然是不受欢迎的)、以及[心血管毒性][WIKI36]。
|
||||
相比于[口服][WIKI37]或非生物同质性雌激素(如[己烯雌酚][WIKI38]、[炔雌醇][WIKI39]和[结合雌激素][WIKI40]),使用[非肠胃途径][WIKI41]、具[生物同质性][WIKI42]的雌二醇是更好的选择——例如[注射用雌二醇酯][WIKI43]和透皮雌二醇。这是因为后者的心血管毒性倾向要低得多<sup>([Aly W.,2020][AW20-ECBC])</sup>。
|
||||
|
||||
注射雌二醇酯可以有效对抗前列腺癌,但传统上用于治疗的长效雌二醇酯(如[聚磷酸雌二醇][WIKI44]与[十一酸雌二醇][WIKI45])皆已停产。至于[戊酸雌二醇][WIKI46]、[环戊丙酸雌二醇][WIKI47]等短效雌二醇酯,尽管可作为替代,但其注射频率更频繁(例如每周注射一次),而且在全球多个地区的供应有限。此外,注射过程并不方便,且可能引起部分患者的痛苦和焦虑。
|
||||
透皮雌二醇贴片也较有效,但通常需要 3-4 个 100 μg/天的贴片才能完全抑制睾酮水平<sup>([Ockrim, Lalani, & Abel, 2006][OLA06]; [Langley et al., 2008][L08]; [Langley et al., 2021][L21])</sup>。同时使用多个贴片不仅可能带来不适,而且开销会很大。
|
||||
[透皮雌二醇凝胶][WIKI48]也曾被用于治疗前列腺癌,但其所需剂量很高(≥6 mg/天);并且即使如此,也只能有限地提高雌二醇水平,对睾酮的抑制也不完全<sup>([Aly W., 2019][AW19-HDTE])</sup>。
|
||||
|
||||
[透皮][WIKI4]药剂可经皮肤渗透吸收。不同皮肤部位的[吸收][WIKI7]能力有异。早在数十年前,人们便已认识到,阴囊皮肤对药剂的吸收能力远高于其它绝大多数部位<sup>([Feldmann & Maibach, 1967][FM67] [[相关材料][FM67-SUPPL]]; [维基百科][WIKI3-TA])</sup>。这里需要指出,最早用于医疗用途的[透皮睾酮贴片][WIKI49],是阴囊贴片;这是因为男性所需的睾酮不少。此后,非阴囊给药的睾酮贴片才得以推出,而且为提供基本等量的睾酮,其尺寸必须变得更大<sup>([Behre & Nieschlag, 2012][BN12]; [Khera, 2013][K13])</sup>。
|
||||
综上,考虑到雌二醇在结构上近似于睾酮,可以认为透皮雌二醇制剂用于阴囊时也有远高于常规部位的吸收率。
|
||||
|
||||
说回上文“[前言](#前言)”一章提及的 Premoli 等人 (2005) 的研究:其对在前列腺癌治疗中通过阴囊使用单个透皮雌二醇贴片的状况进行了评估。研究者均来自阿根廷;在这个贫困率很高的国家,大部分人口无力承担高昂的药费。因此,除了雌激素疗法相对于常规抗雄激素疗法的优势以外,经济方面的因素也成为他们研究的动机之一。
|
||||
他们的基本目标是:为了能够完全抑制睾酮水平、并治疗前列腺癌,通过非肠胃给药、毒性更小的途径来达到较高的雌二醇水平,同时维持较小的开销、和较好的便利性。除了治疗前列腺癌之外,这与许多女性倾向跨性别者的治疗目标非常相似。因此,这种疗法或许对女性化激素治疗也很有价值。
|
||||
|
||||
许多女性倾向跨性别者会为了达到更高的雌二醇水平并抑制睾酮,而选择将[口服雌二醇][WIKI50]片剂用于[舌下含服][WIKI51]。不过,舌下含服存在一些缺点,例如作用时间短、雌二醇水平波动大;同时还有一部分雌二醇会在肝脏内过度暴露,从而可能引起更高的健康风险(如血栓与心血管问题)<sup>([Sam S.,2021][SS21-SET];[维基百科][WIKI3-SA])</sup>。
|
||||
因此,如果有一种替代选项能够引起更稳定、持久的雌二醇水平,其应该会很受欢迎。
|
||||
|
||||
## 研究结果
|
||||
|
||||
Premoli 等人 (2005) 首先对两名患前列腺癌的男性进行了交叉型概念验证预实验,以评估阴囊对透皮雌二醇的吸收是否优于非阴囊部位。其中一名患者先以前臂使用 50 μg/天的雌二醇贴片,然后再以阴囊给药;另一名患者同样先以前臂、再以阴囊给药,不过使用的是 100 μg/天的雌二醇贴片。
|
||||
研究者发现,阴囊给药后的最大雌二醇水平远高于前臂:
|
||||
|
||||
> **「表一」** 在上述预实验中,前臂、阴囊给予雌二醇贴片之后的雌二醇水平:
|
||||
|
||||
| 患者 | 雌二醇贴片剂量 | 给药部位 | 最大雌二醇水平 | 差异 |
|
||||
| ------- | -------------- | -------- | -------------- | ------ |
|
||||
| 患者甲 | 50 μg/天 | 前臂 | 55 pg/mL | – |
|
||||
| | | 阴囊 | 200 pg/mL | 3.6 倍 |
|
||||
| 患者乙 | 100 μg/天 | 前臂 | 180 pg/mL | – |
|
||||
| | | 阴囊 | 500 pg/mL | 2.8 倍 |
|
||||
|
||||
下图将这项微型初期预实验的全过程结果可视化(受试者 2 人,交叉对照):
|
||||
|
||||
> ![][FIG1]
|
||||
>
|
||||
> **「图一」** 在交叉对照中,两名男性前列腺癌患者以阴囊给予透皮雌二醇贴片所引起的雌二醇水平<sup>(Premoli et al., 2005)</sup>。
|
||||
> 在本项初期预实验之后,研究者对 35 名男性前列腺癌患者以阴囊持续给予 100 μg/天的雌二醇透皮贴片,其观测到的平均雌二醇水平约为 500 pg/mL <sup>(Premoli et al., 2005)</sup>。
|
||||
|
||||
这项微型预实验结束之后,Premoli 等人展开了完整的研究,其中包括 35 名前列腺癌患者;每位患者每天经阴囊给予一个 100 μg/天的雌二醇透皮贴片。与预实验结果相似,所有受试者的平均雌二醇水平达 500 pg/ml 左右,范围则在 125 - 1,200 pg/mL 左右。范围幅度之大,恰与透皮途径的雌二醇在个体间可产生雌二醇水平的[巨大差异][WIKI5]的认识相吻合<sup>([维基百科][WIKI3-TA])</sup>。
|
||||
如通过常规皮肤部位给药,则单个 100 μg/天 的雌二醇贴片仅可产生平均约 100 pg/mL 的雌二醇水平<sup>([维基百科][WIKI3-TP];[图表][GRAPH1])</sup>。
|
||||
此外,一项研究显示,在使用 2-6 剂雌二醇贴片的情况下,平均雌二醇水平也只能达到 200 - 400 pg/mL<sup>([图表][GRAPH2];[Ockrim, Lalani, & Abel, 2006][OLA06])</sup>。
|
||||
综上,如将雌二醇透皮贴片用于阴囊,则其[生物利用度][WIKI14]应该有非阴囊部位的至少约 5 倍之大。此幅度与将口服雌二醇片剂用于舌下含服对生物利用度之提升的幅度(约 2-5 倍)相近<sup>([维基百科][WIKI3-SA])</sup>。
|
||||
|
||||
研究中观察到的雌二醇平均水平(即 500 pg/mL)已知足以强烈抑制性腺睾酮的产生、进而抑制血清睾酮水平;已知不小于 200 pg/mL 的雌二醇水平可将睾酮水平平均抑制 ≥90% <sup>([Aly W., 2018][AW18-INTRO-GS]; [维基百科][WIKI52-AE])</sup>。不过遗憾的是,Premoli 及其同行无法获得大多数受试者的睾酮抑制数据;因为几乎所有患者早已在研究开始前接受了常规的雄激素匮乏治疗(如性腺切除术和 GnRH 调节剂),其初始睾酮水平已很低(平均 28 ng/dL,范围 10-90 ng/dL)。
|
||||
无论如何,据研究者所述,仍有两名患者未事先接受常规的雄激素匮乏治疗,其初始睾酮水平仍在男性范围内;在其接受间歇性治疗期间,以阴囊给予雌二醇贴片时的睾酮水平为 10 - 30 ng/dL,停药时为 200 - 600 ng/dL。这与其它临床研究预期的高雌二醇水平对睾酮水平的强烈抑制是一致的。
|
||||
|
||||
|
||||
## 对女性倾向跨性别者的意义
|
||||
|
||||
Premoli 等人 (2005) 的发现很重要,因为他们提供的宝贵信息为在女性化激素治疗中提升雌二醇效力的一种新方法作了有力支持。如女性倾向跨性别者尚未接受[阴道成形术][WIKI53],可考虑将雌二醇透皮贴片用于阴囊;对于术后人群,则可用于[新阴唇][WIKI54]。如果通过常规皮肤部位仅可达到很低的雌二醇水平,那么这种方式应有助于提升雌二醇水平,从而降低贴片用量和成本;或者,用于高剂量雌二醇单药治疗等,以更高的雌二醇水平,起到抑制睾酮的作用。
|
||||
而且,如将雌二醇水平的稳定性(或许还有使用的便利性)纳入考虑,则这种方式应比[舌下含服][WIKI51]和[直肠给药][WIKI55]等其它方案更具优势。
|
||||
|
||||
除贴片之外,凝胶等其它雌二醇透皮制剂用于阴囊时也可大幅提升雌二醇水平。还需要指出,雌二醇凝胶应该无需大面积涂抹;因为根据一项研究的发现,雌二醇凝胶的涂抹面积越小,雌二醇水平就越高<sup>([Järvinen et al., 1997][J97]; [图表][GRAPH3])</sup>。不过,雌二醇凝胶用于阴囊或新阴唇是否更高效尚有待测试和证实;无论如何,如果属实,其将具有相较于贴片的一项显著优势——其仅需每日涂抹一次,而无需时刻往身上贴贴片。
|
||||
需要指出,有的 100 μg/天雌二醇贴片尺寸很大<sup>([表格][TABLE1])</sup>。阴囊睾酮贴片曾因尺寸过大、刺激性过强而被停用,因此雌二醇贴片的情况便显而易见了。不过,低剂量雌二醇贴片(如 50 或 75 μg/天)的尺寸更小<sup>([表格][TABLE1])</sup>,其用于阴囊时,不仅仍有可能引起高雌二醇水平,而且在实用性与耐受性上应优于高剂量贴片。
|
||||
|
||||
此外,还有个想法很有意思,即[透皮孕酮][WIKI56]也有潜在的医疗用途。使用孕酮透皮乳膏之后,可以观察到非常低但仍然显著的血清孕酮水平(~ 0.75 ng/mL)<sup>([维基百科][WIKI3-TA])</sup>。目前尚无任何透皮孕酮制剂被批准用于医学用途,因为其引起的孕酮水平很低,其临床效果也不明确。
|
||||
与雌二醇和睾酮类似,如将透皮孕酮用于阴囊,其可能也会更高效。不过,即使如此,其引起的血清孕酮水平仍将会过低;因此,虽然尚不清楚这是否会让透皮孕酮具备实质疗效,但这也许不大可能。
|
||||
还有一个问题是:外生殖器皮肤富含 [5α-还原酶][WIKI57]——即孕酮的主要[代谢酶][WIKI58]。
|
||||
无论如何,透皮孕酮用于阴囊的途径仍然非常值得探索。
|
||||
|
||||
总而言之,Premoli 等人 (2005) 的研究表明,透皮雌二醇用于阴囊时引起的雌二醇水平,远高于其它皮肤部位。睾酮在这方面已被证实,但对于雌二醇并无任何公开发表的数据佐证——直至此研究发表。
|
||||
|
||||
|
||||
## 关于经外生殖器给予雌二醇的附加讨论
|
||||
|
||||
### 贴片的大小和选择
|
||||
|
||||
透皮雌二醇贴片的品牌众多(例如 Climara、Vivelle、Vivelle-Dot 等),其尺寸、剂量(14 - 100 μg/天)和作用时间(每周一用或两用)也各有不同<sup>([表格][TABLE1])</sup>。
|
||||
其中,尺寸范围从小于十美分硬币(1.65 cm<sup>2</sup>)到几乎接近于通常的咖啡杯底座(44 cm<sup>2</sup>)不等。差距竟有 25 倍之多!尺寸依剂量也有不同:50 μg/天的贴片有 3.3 - 22 cm<sup>2</sup>不等的尺寸,而 100 μg/天的贴剂尺寸为 6.6 - 44 cm<sup>2</sup> 不等。在阴囊上使用非常大的透皮雌二醇贴片显然很困难,而且不舒适。
|
||||
前文所载表格链接,可帮助确定适合个人情况的最佳品牌和剂量。当然,贴片本身也可切分。
|
||||
|
||||
### 贴片的切分和粘贴
|
||||
|
||||
一部分(但并非所有)的雌二醇透皮贴片可以切成更小的尺寸。有的雌二醇贴片非常大,因此如用于外生殖器,切分贴片可能会很有用。详情见以下文献摘录<sup>([Matthews et al., 2017][M17]; [Klein et al., 2018][K18]; [Norjavaara, Ankarberg-Lindgren, & Kriström, 2016][NAK16]; [Rosenfield, Kiess, & Keizer-Schramad, 2006][RKK06])</sup>:
|
||||
|
||||
> 矩阵状的贴片可自粘,每 24 小时释放约 25 µg 的 17β-雌二醇。由于雌二醇均匀分布于整个贴片,故可切分贴片以提供所需的剂量。在实际使用时,贴片大多被切成两份或四份——其它更复杂的切割方式可能不够精确,且不切实际。未使用的部分贴片可放回原包装,并置于冰箱内至多一周。贴剂(或贴剂切片)应放置于清洁干燥的臀部皮肤,如有必要,应使用 Opsite®(透明粘合膜)以确保良好的附着力。[…]
|
||||
贴片切分后可能更难使用,因为它们可能会脱落,从而需要胶带支撑。
|
||||
|
||||
> 目前,市售雌二醇贴片当中最低剂量规格为 14 μg/天,而使用最多的低剂量贴片规格为 25 μg/天。有一种方法可减少贴片剂量,就是将其切为小片。矩阵状的贴片易于切分,但具有储层技术的贴片不应切分。切分贴片的缺点是:切片尺寸较小,可能很难使用,而且亦不为产品说明书所推荐。
|
||||
不过,迄今已有切分贴片的临床案例,尤其是在斯堪的纳维亚——有一个小组在夜间使用贴剂切片(25 微克贴剂四等分后,约等于 6.2 微克甚至更少)来模拟正常的清晨血浆雌二醇峰值;然后撕去贴片,几小时内即回落到基线。
|
||||
|
||||
> 可使用凝胶和贴片进行透皮给药;滴定雌二醇血浆水平显示,贴片切分后给药更为可靠,并且如要模仿自发性青春期早期的生理节律,只需在早晨将贴剂取下即可停止给药。 […]
|
||||
> 我们目前的建议是,尽可能使用矩阵状的雌二醇贴片。这种贴剂不仅稳定,而且雌二醇分布均匀,可按个人需求切分。然而,即使剂量相同,不同品牌的矩阵状贴剂的尺寸也各有别。贴片面积越大,按目标剂量切分越容易。
|
||||
>
|
||||
> 相比之下,储层式的贴剂则具有单独的药物层,这一层是包含药物溶液或悬浮液的隔室,由粘合层隔开。切开后,隔室将被破坏并导致药液泄漏。
|
||||
|
||||
> 目前尚不清楚如何将雌二醇剂量控制在低于 14 μg/天。欧洲生产的矩阵状贴片可轻松切为四片以便夜间提供雌激素;但美国的制造商建议不要这样做——以我们有限的经验来看,其会导致血浆雌二醇水平不稳定,这表明这些贴片内的雌二醇并未均匀浸透。
|
||||
|
||||
目前几乎所有市售雌二醇贴片,皆为矩阵状。唯一的例外是 Estraderm——一种储层状贴片;其已停止在美国上市,但在英国尚可一用。
|
||||
|
||||
Tegaderm 是一种透明薄膜敷料,可帮助固定贴片<sup>([Reddit 帖子][REDDIT1])</sup>。
|
||||
|
||||
|
||||
### 阴茎给药的情况
|
||||
|
||||
阴茎皮肤的吸收特性似乎与阴囊皮肤相似,也可提高透皮给药的吸收率。因此,它可以作为阴囊给予透皮雌二醇的补充或替代方式。有关阴茎给药的详情,见以下文献摘录<sup>([Hairston, Becher, & McVary, 2006][HBM06])</sup>:
|
||||
|
||||
> […] 必须考虑到局部阴茎治疗所特有的解剖学和生理学问题。在阴茎皮肤和海绵体之间,有几个解剖/筋膜层;其中,白膜有厚厚的胶原层,故被认为难以穿透。因此,局部治疗试验主要以龟头给药,因为其与海绵体有直接的静脉连通。
|
||||
阴茎皮肤本身具有角质层,故相对不透水。角质层的角质细胞与非常紧密的细胞间矩阵状脂质双层结合,这使得药物渗透很有难度。为克服这一障碍,研究者使用渗透促进剂渗透该层并到达皮下。可喜的是,在所有试验过的解剖部位当中,阴茎和阴囊最为独特:其角质层的可渗透性最强。有的测试药物用于这些局部区域时的吸收率几乎可达 100%(依其分子结构而定);龟头的角质层则更易于药物“突破”。而其它皮肤部位(例如背部和手掌)尤其不透水。
|
||||
另一个可能扰乱药物输送效果的因素是:真皮深层丰富的毛细血管,可能会将药物“偷到”体循环中。
|
||||
|
||||
因此,如需要通过更大的皮肤面积使用雌二醇凝胶或贴片,则阴茎皮肤可能是一个很好的选择。需要指出,大多数已接受阴道成形术(阴茎翻转法)的女性倾向跨性别者的阴道给药情况应也与此有关,因为其新阴道的内壁是阴茎皮瓣再造的。然而,尚未有研究表明经新阴道给药的有效性。
|
||||
|
||||
### 雌二醇凝胶和乳膏用于外生殖器的情况
|
||||
|
||||
迄今已有两项关于男性经阴囊使用睾酮凝胶和乳膏的临床研究发表:
|
||||
|
||||
- Iyer, R., Mok, S. F., Savkovic, S., Turner, L., Fraser, G., Desai, R., Jayadev, V., Conway, A. J., & Handelsman, D. J. (2017). Pharmacokinetics of testosterone cream applied to scrotal skin. [睾酮乳剂用于阴囊皮肤时的药代动力学] *Andrology, 5*(4), 725–731. [DOI:[10.1111/andr.12357][I17]]
|
||||
- Kuhnert, B., Byrne, M., Simoni, M., Kopcke, W., Gerss, J., Lemmnitz, G., & Nieschlag, E. (2005). Testosterone substitution with a new transdermal, hydroalcoholic gel applied to scrotal or non-scrotal skin: a multicentre trial. [多中心试验:一种新的透皮水醇凝胶作为睾酮替代品用于阴囊、非阴囊皮肤] *European Journal of Endocrinology, 153*(2), 317–326. [DOI:[10.1530/eje.1.01964][K05]]
|
||||
|
||||
第一篇论文的相关摘录如下(其中也简要描述了第二篇论文的发现):
|
||||
|
||||
> 阴囊皮肤薄、且甾体渗透性高,但关于睾酮用于阴囊皮肤途径的药代动力学尚未得到细致研究。本研究旨在阐明睾酮(乳膏)用于阴囊皮肤时的药代动力学。本研究是一项单中心、三阶段、交叉对照的药代动力学研究;具体为对性腺完好(eugonadal)的健康志愿者先施用癸酸诺龙抑制内源性睾酮,再以随机顺序提供三种不同剂量(12.5、25、50 mg)的睾酮乳膏,每次用药至少间隔 2 天。
|
||||
>
|
||||
> 睾酮用于阴囊皮肤时,其生物利用度显著高于腹部皮肤。本研究使用同种睾酮乳膏,并以液相色谱-质谱联用法(LC-MS)对甾体激素进行测定;发现经阴囊给药时只需最低剂量(12.5 mg)即可提供高达 4.6 ng/mL(16.0 nmol/L)的血药峰值浓度,而经腹部皮肤给药时需要 100mg 的睾酮乳膏方可使血药峰值浓度达到 4.7 ng/mL(16.3 nmol/L)。这表明睾酮用于阴囊时的生物利用度,比用于腹部皮肤高出约 8 倍。
|
||||
>
|
||||
> 一项早前的研究显示,用于阴囊时,睾酮凝胶的药代动力学与睾酮贴片相似;也与用于非阴囊部位、5 倍剂量的睾酮凝胶相似——这与透皮睾酮在阴囊的生物利用度高 5 倍相一致<sup>(Kuhnert et al., 2005)</sup>。
|
||||
> 其它一些评估了非阴囊给药的透皮睾酮的药代动力学的研究,则观测到峰值浓度时间 (T<sub>max</sub>)为 6-16 小时不等<sup>(Marbury et al., 2003; Miller et al., 2011; Olsson et al., 2014)</sup>,但峰值浓度(C<sub>max</sub>)与经阴囊给药时相似<sup>(Rolf et al., 2002; Bouloux, 2005; Olsson et al., 2014)</sup>。
|
||||
>
|
||||
> 我们总结认为,相比于非阴囊部位,将睾酮乳膏用于阴囊可提高其生物利用度,提高血清睾酮浓度峰值(依剂量而定),而且剂量的大幅减少也提高了其耐受性。
|
||||
|
||||
从上述发现可知,睾酮凝胶或乳膏用于阴囊时的睾酮浓度峰值,相当于非阴囊部位的约 5 - 8 倍。此幅度与睾酮贴片用于阴囊后的水平比非阴囊部位高 5 倍的认识相吻合。
|
||||
|
||||
雌二醇在化学结构和性质(例如亲脂性,可能也包括吸收特性)等方面与睾酮非常相似。因此,尽管目前尚无关于经阴囊/新阴唇使用雌二醇凝胶或乳膏、或者清楚表明其引起的雌二醇水平要高于常规透皮部位的研究;但是,我们可以从睾酮的现象来推断,雌二醇也会有类似性质——在当阴囊给药的透皮雌二醇贴片,被确认可引起远高于非阴囊部位的雌二醇水平之后,我们愈发确信这点。
|
||||
|
||||
因此,与雌二醇贴片类似,经阴囊/新阴唇使用雌二醇凝胶很可能成为一种可提供高雌二醇水平的强力选项。使用雌二醇透皮制剂时,与常规皮肤部位相比,如改为经阴囊/新阴唇给药,则应有更高的效力和明显更低的成本。
|
||||
此外,凝胶和乳膏每日只需给药一次,干燥得也非常迅速;如果换作贴片,其必须一直贴在身上,此时贴在阴囊/新阴唇就不及贴在常规部位来得舒适和便利了。而且,贴片需要先对阴囊/新阴唇进行脱毛方可使用,还会留下难以去除的粘合剂残留物、并引起局部皮肤反应;而凝胶和软膏则不会有这种问题。
|
||||
综上,雌二醇凝胶或软膏应是更适合用于阴囊/新阴唇的透皮制剂。
|
||||
|
||||
阴囊/新阴唇给药时可能需要注意:透皮雌二醇凝胶由水醇凝胶制成(内含酒精),因而涂抹于外生殖器时,可能会刺激皮肤、引起刺痛或灼伤。为此,可以改用仅含少量或不含酒精的透皮药物——例如乳膏(如复合非处方产品)和乳液(如 Estrasorb),而非水醇凝胶。此外,透皮雌二醇喷雾剂(品牌 Evamist)亦可作为替代方案。
|
||||
|
||||
总之,经阴囊给药的透皮睾酮凝胶或乳膏,相比于常规部位不仅吸收更好,而且睾酮水平高出约 5 - 8 倍。考虑到雌二醇的结构与睾酮相似,且阴囊给药的雌二醇贴片已被证明比常规部位明显吸收得更好,可以认为,透皮雌二醇凝胶和乳膏也有类似的效果。
|
||||
|
||||
### 雌二醇用于外生殖器的安全性
|
||||
|
||||
已有人表达了对雌二醇用于外生殖器之安全性的关注。例如,有人询问,雌二醇用于阴囊时是否会因其引起的局部雌二醇水平较高,而提高[睾丸癌][WIKI59]或[前列腺癌][WIKI15]的风险。
|
||||
现有的对正接受标准激素治疗的女性倾向跨性别者进行的大型观察性研究,并未发现睾丸癌<sup>([Bensley et al., 2021][B21]; [de Nie et al., 2021][N21])</sup>或前列腺癌<sup>([de Nie et al., 2020][N20])</sup>的风险升高。事实上,这些女性倾向跨性别者的前列腺癌风险反而大幅降低了<sup>(de Nie et al., 2020)</sup>。
|
||||
此外,对于顺性别男性,雄激素匮乏可降低前列腺癌的风险或发展;而高剂量雌激素疗法在很长时间内都用于治疗前列腺癌,且卓有成效<sup>([Ockrim, Lalani, & Abel, 2006][OLA06]; [Norman et al., 2008][N08]; [Langley et al., 2021][L21])</sup>。
|
||||
因此,对于睾丸或前列腺内的局部超高雌二醇浓度是否会提高患癌风险这个问题,尽管我们尚无相关数据可供回答,但现有的间接临床证据并不予以支持,故大可放心。
|
||||
|
||||
## 参考文献
|
||||
|
||||
略
|
||||
|
||||
<!-- 内置图片 -->
|
||||
[FIG1]: https://transfemscience.org/assets/images/s7qio1uxkaw21.png
|
||||
|
||||
<!-- 图表外链 -->
|
||||
[GRAPH1]: https://en.wikipedia.org/wiki/Template:Hormone_levels_with_transdermal_estradiol_patches
|
||||
[GRAPH2]: https://commons.wikimedia.org/wiki/File:Estradiol_and_testosterone_levels_with_high-dose_estradiol_patches_in_men.png
|
||||
[GRAPH3]: https://commons.wikimedia.org/wiki/File:Estradiol_levels_with_1_mg_per_day_transdermal_estradiol_gel_applied_to_different_amounts_of_area_in_postmenopausal_women.png
|
||||
|
||||
<!-- Reddit 外链 -->
|
||||
[REDDIT1]: https://www.reddit.com/r/TransDIY/comments/b7a0m6/psa_if_you_are_using_patches_you_should_be_using/
|
||||
|
||||
<!-- 表格外链 -->
|
||||
[TABLE1]: https://en.wikipedia.org/wiki/Template:Transdermal_estradiol_patches_marketed_in_the_United_States
|
||||
|
||||
<!-- 维基百科条目 -->
|
||||
[WIKI1]: https://en.wikipedia.org/wiki/Pharmaceutical_form
|
||||
[WIKI2]: https://en.wikipedia.org/wiki/Route_of_administration
|
||||
[WIKI3]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol
|
||||
[WIKI3-TP]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Transdermal_patches
|
||||
[WIKI3-TG]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Transdermal_gel
|
||||
[WIKI3-OTF]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Other_transdermal_formulations
|
||||
[WIKI3-VIP]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Variability_in_pharmacokinetics
|
||||
[WIKI3-TA]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Transdermal_administration
|
||||
[WIKI3-SA]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Sublingual_administration
|
||||
[WIKI4]: https://en.wikipedia.org/wiki/Transdermal_administration
|
||||
[WIKI5]: https://en.wikipedia.org/wiki/Interindividual_variability
|
||||
[WIKI6]: https://en.wikipedia.org/wiki/Hydrocortisone
|
||||
[WIKI6A]: https://en.wikipedia.org/wiki/Cortisol
|
||||
[WIKI7]: https://en.wikipedia.org/wiki/Absorption_(pharmacology)
|
||||
[WIKI8]: https://en.wikipedia.org/wiki/Steroid_hormone
|
||||
[WIKI9]: https://en.wikipedia.org/wiki/Estradiol_(medication)
|
||||
[WIKI10]: https://en.wikipedia.org/wiki/Testosterone_(medication)
|
||||
[WIKI11]: https://en.wikipedia.org/wiki/Sex_hormone
|
||||
[WIKI12]: https://en.wikipedia.org/wiki/Radioactive_tracer
|
||||
[WIKI13]: https://en.wikipedia.org/wiki/Scrotum
|
||||
[WIKI14]: https://en.wikipedia.org/wiki/Bioavailability
|
||||
[WIKI15]: https://en.wikipedia.org/wiki/Prostate_cancer
|
||||
[WIKI16]: https://en.wikipedia.org/wiki/High-dose_estrogen
|
||||
[WIKI17]: https://en.wikipedia.org/wiki/Transdermal_estradiol_patch
|
||||
[WIKI18]: https://en.wikipedia.org/wiki/Transdermal_estradiol
|
||||
[WIKI19]: https://en.wikipedia.org/wiki/Estrogen_(medication)
|
||||
[WIKI20]: https://en.wikipedia.org/wiki/Antiandrogen
|
||||
[WIKI21]: https://en.wikipedia.org/wiki/Androgen_deprivation_therapy
|
||||
[WIKI22]: https://en.wikipedia.org/wiki/Antigonadotropin
|
||||
[WIKI23]: https://en.wikipedia.org/wiki/Testosterone
|
||||
[WIKI24]: https://en.wikipedia.org/wiki/Sex%20hormone-binding%20globulin
|
||||
[WIKI25]: https://en.wikipedia.org/wiki/Androgen
|
||||
[WIKI26]: https://en.wikipedia.org/wiki/Gonadectomy
|
||||
[WIKI27]: https://en.wikipedia.org/wiki/Gonadotropin-releasing_hormone
|
||||
[WIKI28]: https://en.wikipedia.org/wiki/Gonadotropin-releasing_hormone_agonist
|
||||
[WIKI29]: https://en.wikipedia.org/wiki/Gonadotropin-releasing_hormone_antagonist
|
||||
[WIKI30]: https://en.wikipedia.org/wiki/Hot_flash
|
||||
[WIKI31]: https://en.wikipedia.org/wiki/Bone_density
|
||||
[WIKI32]: https://en.wikipedia.org/wiki/Sexual_desire
|
||||
[WIKI33]: https://en.wikipedia.org/wiki/Quality_of_life
|
||||
[WIKI34]: https://en.wikipedia.org/wiki/Feminization_(biology)
|
||||
[WIKI35]: https://en.wikipedia.org/wiki/Gynecomastia
|
||||
[WIKI36]: https://en.wikipedia.org/wiki/Cardiovascular_disease
|
||||
[WIKI37]: https://en.wikipedia.org/wiki/Oral_administration
|
||||
[WIKI38]: https://en.wikipedia.org/wiki/Diethylstilbestrol
|
||||
[WIKI39]: https://en.wikipedia.org/wiki/Ethinylestradiol
|
||||
[WIKI40]: https://en.wikipedia.org/wiki/Conjugated_estrogens
|
||||
[WIKI41]: https://en.wikipedia.org/wiki/Parenteral_administration
|
||||
[WIKI42]: https://en.wikipedia.org/wiki/Bioidentical
|
||||
[WIKI43]: https://en.wikipedia.org/wiki/Injectable_estradiol_esters
|
||||
[WIKI44]: https://en.wikipedia.org/wiki/Polyestradiol_phosphate
|
||||
[WIKI45]: https://en.wikipedia.org/wiki/Estradiol_undecylate
|
||||
[WIKI46]: https://en.wikipedia.org/wiki/Estradiol_valerate
|
||||
[WIKI47]: https://en.wikipedia.org/wiki/Estradiol_cypionate
|
||||
[WIKI48]: https://en.wikipedia.org/wiki/Transdermal_estradiol_gel
|
||||
[WIKI49]: https://en.wikipedia.org/wiki/Transdermal_testosterone_patch
|
||||
[WIKI50]: https://en.wikipedia.org/wiki/Oral_estradiol
|
||||
[WIKI51]: https://en.wikipedia.org/wiki/Sublingual_estradiol
|
||||
[WIKI52-AE]: https://en.wikipedia.org/wiki/Pharmacodynamics_of_estradiol#Antigonadotropic_effects
|
||||
[WIKI53]: https://en.wikipedia.org/wiki/Vaginoplasty
|
||||
[WIKI54]: https://en.wikipedia.org/wiki/Neolabia
|
||||
[WIKI55]: https://en.wikipedia.org/wiki/Rectal_estradiol
|
||||
[WIKI56]: https://en.wikipedia.org/wiki/Transdermal_progesterone
|
||||
[WIKI57]: https://en.wikipedia.org/wiki/5%CE%B1-Reductase
|
||||
[WIKI58]: https://en.wikipedia.org/wiki/Enzyme
|
||||
[WIKI59]: https://en.wikipedia.org/wiki/Testicular_cancer
|
||||
|
||||
|
||||
<!-- 参考文献外链 -->
|
||||
[AW20-EED]: https://transfemscience.org/articles/e2-equivalent-doses/
|
||||
[FM67]: https://doi.org/10.1038/jid.1967.29
|
||||
[FM67-SUPPL]: https://doi.org/10.1038/jid.1967.29
|
||||
[P90]: https://doi.org/10.1007/978-3-662-00814-0_9
|
||||
[M92]: https://doi.org/10.1016/0168-3659(92)90089-A
|
||||
[ACS98]: https://doi.org/10.1007/978-3-642-72185-4_13
|
||||
[P05]: https://scholar.google.com/scholar?cluster=3203160436559309066
|
||||
[P05-ARCHIVE]: https://web.archive.org/web/20201112031803/https://www.sau-net.org/publicaciones/abstracts_70_4.html
|
||||
[P05-PDF]: https://revistasau.org/index.php/revista/article/viewFile/3224/3168
|
||||
[P05-ENG]: https://docs.google.com/document/d/1dteNhG9wewvNX5zj0YcXrVAuQFZdtcqWmUWVvgI5uKs/view
|
||||
|
||||
[AW20-ECBC]: https://transfemscience.org/articles/estrogens-coagulation-blood-clots/
|
||||
[OLA06]: https://doi.org/10.1038/ncponc0602
|
||||
[L08]: https://doi.org/10.1111/j.1464-410X.2008.07583.x
|
||||
[AW19-HDTE]: https://transfemscience.org/articles/high-dose-transdermal-e2/
|
||||
[BN12]: https://books.google.com/books?id=MkrAPaQ4wJkC&pg=PA324
|
||||
[K13]: https://doi.org/10.1007/978-1-62703-179-0_10
|
||||
[SS21-SET]: sublingual-e2-transfem.md
|
||||
|
||||
[OLA06]: https://doi.org/10.1038/ncponc0602
|
||||
[AW18-INTRO-GS]: transfem-intro.md#对性腺的抑制作用
|
||||
|
||||
[J97]: https://doi.org/10.1111/j.1471-0528.1997.tb11562.x
|
||||
|
||||
[M17]: https://doi.org/10.1136/archdischild-2016-311372
|
||||
[K18]: https://doi.org/10.1210/jc.2017-02183
|
||||
[NAK16]: https://doi.org/10.1159/000438892
|
||||
[RKK06]: https://doi.org/10.1016/j.ics.2006.07.003
|
||||
|
||||
[HBM06]: https://doi.org/10.1007/978-1-59745-155-0_14
|
||||
[I17]: https://doi.org/10.1111/andr.12357
|
||||
[K05]: https://doi.org/10.1530/eje.1.01964
|
||||
|
||||
[B21]: https://doi.org/10.1016/j.urology.2021.11.014
|
||||
[N21]: https://doi.org/10.1111/bju.15575
|
||||
[N20]: https://doi.org/10.1210/clinem/dgaa412
|
||||
[N08]: https://doi.org/10.1038/sj.bjc.6604230
|
||||
[L21]: https://doi.org/10.1016/S0140-6736(21)00100-8
|
||||
|
|
@ -1,784 +0,0 @@
|
|||
# 有关雌二醇注射剂的雌二醇浓度曲线的一次非正式荟萃分析
|
||||
|
||||
> - 作者 [Aly W.][AUTHOR]
|
||||
> + 首次发表于 2021 年 7 月 16 日
|
||||
> + 最后修改于 2022 年 2 月 5 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [Bersella AI][TRANSLATOR]
|
||||
> + 翻译完成于 2022 年 5 月 22 日
|
||||
|
||||
[AUTHOR]: https://transfemscience.org/about/#aly-w
|
||||
[ORIGIN]: https://transfemscience.org/articles/injectable-e2-meta-analysis/
|
||||
[TRANSLATOR]: https://bersella-ai.cc/about-me/
|
||||
|
||||
## 译者按
|
||||
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. **长文注意:本译文共计约 1.8 万个汉字。** 读者如希望立即翻阅分析结果的汇总,请[点此跳转](#所有雌二醇注射剂的汇总图表);如希望了解本文作者推荐的剂量,可查阅[此小节](#对临床指南和剂量建议的剖析)。
|
||||
1. 原文还简短讨论了[睾酮注射剂](#环戊丙酸雌二醇ec油溶液与庚酸雌二醇een的持续时间比较)。
|
||||
1. 以下《指南》《跨性别……指南》等应当皆指代同一事物,原文如此。
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
-----
|
||||
|
||||
## 摘要
|
||||
|
||||
> 戊酸雌二醇、环戊丙酸雌二醇(油溶液)等雌二醇注射剂,常用作女性化激素治疗中的雌激素来源。不过,这些制剂在女性倾向跨性别者身上的特性知之甚少;而《跨性别护理指南》对其使用量的建议也更多地基于专家观点,而非临床数据。本文对既有临床数据当中,与常用的雌二醇注射剂相关的雌二醇浓度—时间曲线,进行了非正式的荟萃分析;旨在帮助厘清注射用雌二醇之特性、以及让女性倾向跨性别者更好地了解并考虑其使用量。
|
||||
纳入分析的雌二醇制剂包括:苯甲酸雌二醇(油溶液)、戊酸雌二醇(油溶液)、环戊丙酸雌二醇(油溶液或悬浮液)、庚酸雌二醇(油溶液)、十一酸雌二醇(油溶液)以及聚磷酸雌二醇。本文从各种文献当中收集并分析了临床上有关以上制剂的雌二醇浓度—时间数据。
|
||||
荟萃分析当中,每种制剂的数据皆被处理并拟合到药代动力学模型上;此外,还测定了一些指定的药代动力学参数。分析结果则就雌二醇注射剂之特性进行了讨论,包括曲线形状、持续时间、雌激素之暴露、不同个体及研究当中的差异等。
|
||||
基于现有结果,本文也探讨了《跨性别护理指南》对雌二醇注射剂之使用建议。现有《指南》的建议用量似乎过多,而注射间隔则显得过长。基于本次荟萃分析,这些《指南》应该重新评估其用量建议。
|
||||
最终,此次分析所拟合的雌二醇浓度曲线,被整合到一个基于可互动网页的注射用雌二醇模拟器,以供女性倾向跨性别者及服务她们的医疗工作者使用,帮助指导医疗决策。
|
||||
|
||||
## 前言
|
||||
|
||||
雌二醇是女性化激素治疗中主要的雌激素来源;针对不同用药途径,业已有了相应形态。最常见的形态包括口服片、舌下含服片剂、透皮剂以及注射剂。在许多国家(例如欧洲大部分地区),雌二醇注射剂已停产,因此无法用于女性化激素治疗 <sup>([Glintborg et al., 2021][G21])</sup>;然而,不少女性倾向跨性别者仍在使用,尤其在美国和自行用药(DIY)的群体中。常用的注射剂包括:戊酸雌二醇(EV)、环戊丙酸雌二醇(EC)和庚酸雌二醇(EEn),皆为油溶液。注射剂相较其它雌二醇形态,具有以下特点:更低的开销、更容易达到高雌二醇浓度以便压制睾酮的能力、更少的用药频率、以及理论上更小的健康风险(相对口服同等剂量而言,例如可避免肝脏首过效应);这些特点使得其在女性化激素治疗当中广受欢迎。注射带来的高雌二醇浓度对于单服雌二醇疗法也大有裨益:这避免了抗雄制剂的使用。
|
||||
|
||||
临床上使用的雌二醇注射剂,由雌二醇酯组成,而非雌二醇本身。这些雌二醇酯作为油溶液或水晶体悬浮液被注射到肌肉或脂肪下之后,会从注射位点缓慢释放。释放之后,其作为雌二醇的前体,被迅速代谢为雌二醇。如果用于肌注的是雌二醇本身(水溶液或油溶液),其很快就被吸收,持续时间也很短。由于具有亲脂性,临床使用的注射用雌二醇酯之脂溶性,比雌二醇更高 <sup>(通过测定油水分配系数而知,[表格][TABLE_1A])</sup>;当作为油溶液被肌注或皮下注射,其亲脂性会减缓其释放速率,因此持续时间也更长。对于脂肪酸酯(例如 EV、EEn、十一酸雌二醇等),酯的分子链越长,亲脂性越高,释放速率也更慢,从而达到浓度峰值所需时间和作用时间更长 <sup>([Edkins, 1959][E59]; [Sinkula, 1978][SINKULA78]; [Chien, 1981][CHIEN81]; [Kuhl, 2005][K05]; [Kalicharan, 2017][K17]; [Vhora et al., 2019][V19])</sup>。尽管注射剂的持续时间,皆取决于雌二醇酯的类型(尤其是物化特性);但其性状各异,注射后产生的效果亦有不同<sup>([Enever et al., 1983][E83]; [Aly W., 2019][ALYW19_AQUA])</sup>。其中,油溶液的持续时间,依雌二醇酯的类型与所用油载体而定;而水溶液则取决于雌二醇酯晶格的性状与体积<sup>(Chien, 1981; Enever et al., 1983; [Aly W., 2019][ALYW19_AQUA])</sup>。聚磷酸雌二醇,作为一种聚合酯,具有相较雌二醇更高的亲水性(水溶性),其表现亦与其它注射剂有异。其由多个通过磷酸酯链接的雌二醇分子构成(一个大分子平均包含 13 个雌二醇分子),注射后分解很慢,因此持续时间也很长。雌二醇酯用于注射,的确可以延长雌二醇作用时间;根据其成分,持续时长从数日到数月不等 <sup>([表格][TABLE_1B])</sup>。
|
||||
|
||||
在有关跨性别健康的文献当中,对雌二醇注射剂之药代动力学的研究与评述相当少见。现有的《跨性别激素治疗指南》关于注射剂仅有简略的介绍与用量建议,而这貌似基本上出自专家观点 <sup>(例如 [Deutsch, 2016a][D16a]; [Hembree et al., 2017][H17])</sup>。迄今已有许多关于评估雌二醇注射剂之药代动力学与雌二醇浓度—时间关系的研究成果发表,但其研究对象仅限于顺性别者,而非跨性别者。这些研究成果散落于各处文献,尚未被综合起来评述与分析。有一些评述文章,记录雌二醇注射剂用于激素节育法、更年期激素疗法<sup>(对于顺性别妇女, 例如 [Düsterberg & Nishino, 1982][DN82]; [Kuhl, 1986][K86]; [Kuhl, 1990][K90]; [Garza-Flores, 1994][GF94]; [Kuhl, 2005][K05])</sup>以及雄激素阻断治疗<sup>(对于患有前列腺癌的顺性别男性, 例如 [Gunnarsson & Norlén, 1988][GN88])</sup>时的药代动力学。然而,这些文章的研究范围相当有限。关于多次使用雌二醇注射剂的数据,尽管愈加稀少,但业已见诸报端 <sup>(例如 [Gooren, 1984][G84]; [表格][TABLE_1C])</sup>。至于对多次注射的模拟,迄今已有对于聚磷酸雌二醇的模拟结果 <sup>([Henriksson et al., 1999][H99]; [Johansson & Gunnarsson, 2000][JG00])</sup>;但对于其它雌二醇注射剂,则尚未有所探索。与此相反的是,有关睾酮注射剂,已有了充足的评述文献与模拟<sup>(例如 [Behre, Oberpenning, & Nieschlag, 1990][BON90]; [Behre & Nieschlag, 1998][BN98]; [Behre et al., 2004][B04]; [Nieschlag & Behre, 2010][NB10]; [Nieschlag & Behre, 2012][NB12])</sup>。
|
||||
|
||||
笔者为女性倾向跨性别者及为之服务的医疗工作者,开发了一款基于网页的[注射用雌二醇模拟器][WEB_1A],以帮助其理解使用注射剂时的雌二醇浓度—时间关系。在模拟器的制作过程中,雌二醇水平与曲线形状在不同研究之间的差异昭然若揭(甚至同一种雌二醇酯的结果也有差别)。起初,此模拟器仅基于一项关于苯甲酸雌二醇(EB)、EV、EC 在药代动力学之直接比较的知名研究,进行曲线的模拟。然而,鉴于不同研究当中雌二醇水平与曲线的明显差异,让该项目仅依赖一项研究的数据,是站不住脚的;需要整合多项研究的成果,使模拟结果更贴合已有数据。加入更多研究成果,也意味着可向模拟器添加更多雌二醇注射剂的选项。本文的工作正是为该模拟器项目而开展的。
|
||||
|
||||
## 研究方法
|
||||
|
||||
首先在文献中检索报告了和主要雌二醇注射剂(见表一)相关的雌二醇浓度—时间关系的研究项目。这些注射剂均已在世界不同地区至少一次用于女性化激素治疗,而其中戊酸雌二醇(油溶液)、环戊丙酸雌二醇(油溶液)如今正广泛使用。需要注意的是,部分注射剂现已停产。采用的数据包括雌二醇平均浓度、每名受试者单独的雌二醇浓度数据、平均峰值浓度(C<sub>max</sub>)以及达峰所需时间(T<sub>max</sub>)。检索过程在 PubMed, Google Scholar, 以及 WorldCat 等数据库上进行,使用了与此关联的关键词(如雌二醇酯名称、种类等,以及主要品牌名)。存在关联者被收录,以收集数据。其中,会被采用的,只有单次用药的数据,以及间隔时间足以使雌二醇水平回落至基准线的多次用药数据(例如间隔一个月用药的注射用复方避孕药)。收录文献时,并未将受试者的下丘脑-垂体-性腺轴(HPG 轴)之状态纳入考虑。部分注射剂资料稀缺,为此放宽了文献收录标准,以尽可能多地收集数据;但如果涉及同一注射剂的研究较多,其中仅包含 1\~2 名受试者的价值较低的研究文献会被排除。如果数据以附图的形式出现在文献中(这种情况很常见),其会通过 [WebPlotDigitizer][WEB_2A] 被提取出来。
|
||||
|
||||
> 【表一】主要注射用雌二醇形式(按持久性从低到高排序):
|
||||
>
|
||||
> | 雌二醇酯 | 缩写 | 形态 | 主要品牌名 |
|
||||
> |-|-|-|-|
|
||||
> | 苯甲酸雌二醇 | EB | 油溶液 | Progynon-B |
|
||||
> | 戊酸雌二醇 | EV | 油溶液 | Delestrogen, Mesigyna<sup>(1)</sup>, Progynon Depot<sup>(2)</sup> |
|
||||
> | 环戊丙酸雌二醇 | EC | 油溶液 | Depo-Estradiol |
|
||||
> | | | 水溶悬浮液<sup>(3)</sup> | Cyclofem<sup>(1)</sup>, Lunellea<sup>(1)</sup> |
|
||||
> | 庚酸雌二醇 | EEn | 油溶液 | Perlutal<sup>(1)</sup>, Topasela<sup>(1)</sup> |
|
||||
> | 十一酸雌二醇<sup>(4)</sup> | EU | 油溶液 | Delestrec, Progynon Depot 100 |
|
||||
> | 聚磷酸雌二醇<sup>(4)</sup> | PEP | 水溶液 | Estradurin |
|
||||
>
|
||||
>(1) 作为注射用复方避孕药,也包含一种孕激素(醋酸炔诺酮、醋酸甲羟孕酮或苯乙酮缩二羟孕酮等)
|
||||
>(2) 俗称“富士日雌”——译者注
|
||||
>(3) 含微晶颗粒
|
||||
>(4) 不再上市
|
||||
|
||||
收集后的数据会经过一系列整合、建模等处理过程。所有数据均对雌二醇的内源性分泌做了修正:一般来说,会减去雌二醇水平之基准值;但某些情况下,则需减去 *(受试者)* 的雌二醇浓度谷底值,或者参照组的雌二醇浓度。之后,依用药量做了标准化,并依样本规模进行加权。为尽可能收录数据,在许多事例中,部分缺失的特定信息(如雌二醇浓度基准线、达峰用时,受试者体重等)使用了合理的估计量。
|
||||
其后,数据汇总为平均雌二醇浓度曲线(而非单名受试者的曲线;排除了仅含一名受试者的个别研究项目)。再根据引自多篇论文的一级吸收与消除动力学资料<sup>(例如 [Colburn, 1981][COLB81]; [Wagner, 1993][W93]; [Fisher & Shafer, 2007][FS07]; [Lixoft, 2008][L08]; [Abuhelwa, Foster, & Upton, 2015][AFU15]; [Certara, 2020][C20])</sup>,对各种注射剂所对应的曲线做了最小二乘回归,以契合一室、二室、三室药代动力学模型;这些模型反过来和大多数研究项目各自的曲线相吻合。
|
||||
针对每种注射剂,也额外对所有相关研究项目之曲线做了拟合,以便改进拟合结果;这里没有直接用数据进行拟合,是因为此法加大了采样次数多的研究项目之权重,而用曲线则可避免该问题。Akaike 信息准则(AIC)也被用于协助拟合过程中的模型选择上。拟合过程使用了基于 Levenberg-Marquardt(LM) 算法的 Python 程序库 [Lmfit][WEB_2B]。雌二醇浓度峰值(C<sub>max</sub>)因其性质与平均浓度曲线不同,而被排除在拟合过程之外;除非有关特定注射剂的数据量过少。异常数据也被排除,以便平衡各拟合曲线下方的面积;这里有一项准则:如果某曲线下方的面积显著有异于同种注射剂的一般水平(达 ±50% 以上),那么该曲线将被排除在外。
|
||||
|
||||
接下来,依据每种注射剂的单次用药曲线、以及对其药代动力学的分室分析,计算了一些特定的药代动力学参数。这些参数包括:单次用药(以 5mg 计)后的雌二醇浓度峰值(C<sub>max</sub>)、达峰所需时间(T<sub>max</sub>)、曲线下方的总面积(AUC<sub>0-∞</sub>),以及雌二醇消除半衰期(t<sub>1/2</sub>)、消除90%所需时间(t<sub>90%</sub>,以 t<sub>1/2</sub> × 3.322 计)。
|
||||
另外,针对多次用药(每隔 7 天注射 5mg)并达到稳态的情况,也使用单次用药时的拟合曲线及其药代动力学的分室分析,估算了部分药代动力学参数。这些参数包括:雌二醇浓度达峰所需时间(T<sub>max</sub>)、峰值(C<sub>max</sub>)、谷值(C<sub>min</sub>)、峰谷之差(PTD,也即 C<sub>max</sub> - C<sub>min</sub>)、峰谷比值(PTR,也即 C<sub>max</sub> ÷ C<sub>min</sub>),以及综合平均浓度(C<sub>avg</sub>)。
|
||||
多次用药的模拟,通过堆积多个雌二醇浓度曲线的方式进行。模拟过程所采用的 T<sub>max</sub> 与 C<sub>max</sub> 数据取自上述拟合后的曲线,而非各受试者的平均值;这是因为,大多数研究仅提供了雌二醇平均浓度曲线,使得后者无法计算。
|
||||
上述计算过程,各采用了相应的药代动力学方程,并与基于 Microsoft Excel 的插件 [PKSolver][Z10] <sup>(Zhang et al., 2010)</sup>的计算结果进行了比对。
|
||||
|
||||
## 分析结果
|
||||
|
||||
以下小节所示图表,显示了来自各项研究、经内源性分泌量修正、并统一了摄入量的雌二醇浓度;以及对这些数据的拟合曲线(对于 EEn、EU、PEP 注射剂),或者对各项目曲线的拟合(对于 EB、EC 注射剂)。至于 EV,这两种拟合方式的结果几乎一致,故采用了基于数据拟合的曲线。拟合过程排除了研究 C<sub>max</sub> 的项目(但数据量奇缺的 EEn 除外)。由于源数据和三室药代动力学模型最为契合<sup>([Desmos][WEB_30A]; [V3C Fitter][WEB_30B])</sup>,因此该模型被用于所有注射剂的拟合过程。
|
||||
|
||||
### 苯甲酸雌二醇(EB)
|
||||
|
||||
EB 注射剂曾被广泛用于科学研究,尤其是在阐释 HPG 轴的功能及动力学上。EB 会用于雌激素激发试验,以测试 HPG 轴的功能。因其科研用途,相关的雌二醇浓度—时间关系数据很丰富。这里找到了来自 26 篇著述(表二)的 355 人次注射的数据。
|
||||
|
||||
> 【表二】和 EB 注射剂相关的研究项目:
|
||||
>
|
||||
> | 项目代号 | 注射人次 | 受试对象 | 用药量 | 参考文献 |
|
||||
> |-|-|-|-|-|
|
||||
> | G75 | 3 | 已去势、或已绝经妇女 | 27.6mg | [Geppert (1975)][G75];<br/> [Leyendecker et al. (1975)][L75] |
|
||||
> | K75 | 10 | 正常绝经前妇女 | ~0.15mg | [Keye & Jaffe (1975)][KL75] |
|
||||
> | S75a | 10 | 患有月经不调的绝经前妇女 | 1mg | [Shaw et al. (1975)][S75] |
|
||||
> | S75b1 | 5 | 正常绝经前妇女 | 0.5mg | [Shaw, Butt, & London (1975)][SBL75] |
|
||||
> | S75b2 | 5 | 正常绝经前妇女 | 1.5mg | 同上 |
|
||||
> | S75b3 | 5 | 正常绝经前妇女 | 2.5mg | 同上 |
|
||||
> | L76 | 3 | 正常绝经前妇女 | 3mg | [Leyendecker et al. (1976)][L76] |
|
||||
> | C78 | 22 | 患有无排卵性不孕症的绝经前妇女 | 1mg | [Canales et al. (1978)][C78] |
|
||||
> | S78 | 6 | 正常绝经前妇女 | 2.5mg | [Shaw (1978)][S78] |
|
||||
> | T78 | 19 | 患有高泌乳素血症的绝经前妇女 12 人,其中有 7 人的泌乳素恢复正常<br />(12 人中有 7 人注射两针) | 1mg | [Travaglini et al. (1978)][T78] |
|
||||
> | T79 | 18 | 患有高泌乳素血症的绝经前妇女 9 人<br/>(均注射两针,分别仅注射 EB 和同时注射孕激素) | 1mg | [Travaglini et al. (1979)][T79] |
|
||||
> | O80 | 10 | 正服用复方避孕药的绝经前妇女 | 5mg | [Oriowo et al. (1980)][O80]
|
||||
> | C81 | 14 | 产后哺乳期妇女 7 人(注射两针) | 3mg | [Canales et al. (1981)][C81] |
|
||||
> | W81 | 19 | 患有高泌乳素血症与垂体泌乳素瘤的绝经前妇女 | 1mg | [White et al. (1981)][W81] |
|
||||
> | S82 | 2 | 患有XX男性综合征的男性 | 5mg | [Schweikert et al. (1982)][S82] |
|
||||
> | B83 | 10 | 正常绝经前妇女 5 人(注射两次,分别在服用达那唑前后) | 5mg | [Braun, Wildt, & Leyendecker (1983)][BWL83] |
|
||||
> | K84 | 22 | 正服用复方激素药物的已去势的绝经前妇女 | 1mg | [Kemeter et al. (1984)][K84] |
|
||||
> | V84 | 7 | 酗酒、患有肝硬化或脂肪肝的绝经前妇女 | 5mg | [Välimäki et al. (1984)][V84] |
|
||||
> | G85 | 10 | 未接受激素治疗的女性倾向跨性别者 5 人,以及正常男性 5 人 | 2mg | [Goodman et al. (1985)][G85]
|
||||
> | A86 | 18 | 患排卵性不孕症和短暂性高泌乳素血症的绝经前妇女 9 人;<br />正常绝经前妇女 9 人 | ~5mg | [Aisaka et al. (1986)][A86] |
|
||||
> | C86 | 27 | 患有功能失调性子宫出血的更年期妇女 | 2mg | [Cano et al. (1986)][C86] |
|
||||
> | M87 | 5 | 正常绝经前妇女 | 10mg | [Messinis & Templeton (1987a)][MT87a];<br /> [Messinis & Templeton (1987b)][MT87b] |
|
||||
> | S87 | 11 | 正常绝经前妇女 | 1mg | [Sumioki (1987)][S87] |
|
||||
> | B89 | 20 | 患有排卵性不孕症的绝经前妇女 10 人<br/>(注射两针,分别在服用 GnRH 拮抗剂前后) | 2mg | [Bider et al. (1989)][B89] |
|
||||
> | V93 | 49 | 服用 GnRH 拮抗剂的绝经前妇女;<br />其中有妇科疾病者 15 人,正接受生育治疗者 6 人(每人 2\~3 针) | 2.5mg | [Vizziello et al. (1993)][V93] |
|
||||
> | E06 | 25 | 有经前情绪波动的绝经前妇女 13 人;<br />正常绝经前妇女 12 人 | ~2.5mg | [Eriksson et al. (2006)][E06] |
|
||||
|
||||
拟合曲线排除了显著有别于平均水平的部分研究项目的曲线。一些仅报告了总雌激素水平(而非雌二醇水平)的研究项目亦被排除<sup>([Akande, 1974][A74]; [Weiss, Nachtigall, & Ganguly, 1976][WNG76])</sup>。两项研究因年代久远、使用了过时且不准确的验血方法而被排除<sup>([Varangot & Cedard, 1957][VC57]; [Ittrich & Pots, 1965][IP65], [表格][TABLE_31A])</sup>。经处理的源数据与拟合曲线见图一。
|
||||
|
||||
> ![figure][FIG_1]
|
||||
>
|
||||
> 【图一】已发表的、单次肌注 EB 油溶液之后 7 日内的雌二醇浓度—时间曲线,及其拟合曲线(加粗黑/白线)。曲线已依内源性分泌量进行修正、并调整摄入量为 5mg,以与分室药代动力学模型相契合。各曲线随后也用相同的模型进行拟合。源数据在他处亦有提供<sup>([Google 文档][WEB_31A]; [Plotly 表格][WEB_31B])</sup>。
|
||||
|
||||
|
||||
### 戊酸雌二醇(EV)
|
||||
|
||||
EV 注射剂的相关浓度曲线资料来自:在更年期激素疗法、和其它需要雌激素的临床治疗当中的使用,注射用复方避孕药的使用,以及科研用途。这里找到了来自 28 篇著述(表三)的 309 人次注射的数据。
|
||||
|
||||
> 【表三】和 EV 注射剂相关的研究项目:
|
||||
>
|
||||
> | 项目代号 | 注射人次 | 受试对象 | 用药量 | 参考文献 |
|
||||
> |-|-|-|-|-|
|
||||
> | S7175 | 12 | 患有经期偏头痛的绝经前妇女 10 人;<br />曾有经期偏头痛史的闭经或已绝经妇女 2 人 | 5-20mg | [Somerville (1971)][S71];<br/> [Somerville (1972a)][S72a];<br/> [Somerville (1972b)][S72b];<br/> [Somerville (1972c)][S72c];<br/> [Somerville (1975)][SOMER75] |
|
||||
> | G75 | 3 | 已去势、或已绝经妇女 | 26.2mg | [Geppert (1975)][G75];<br/> [Leyendecker et al. (1975)][L75] |
|
||||
> | V75a | 4 | 不明/未描述 | 10mg | [Vermeulen (1975)][V75] |
|
||||
> | V75b | 2 | 不明/未描述 | 4mg | 同上 |
|
||||
> | O80 | 9 | 正服用复方避孕药的绝经前妇女 | 5mg | [Oriowo et al. (1980)][O80] |
|
||||
> | R80 | 6 | 已去势、或已绝经妇女 | 10mg | [Rauramo et al. (1980)][R80];<br/> [Rauramo, Punnonen, & Grönroos (1981)][RPG81] |
|
||||
> | B82 | 10 | 正在服用溴隐亭的正常绝经前妇女 | 20mg | [Blackwell, Boots, & Potter (1982)][BBP82] |
|
||||
> | D83 | 3 | 正常绝经前妇女 | 4mg | [Düsterberg, & Wendt (1983)][DW83] |
|
||||
> | A85 | 7 | 正常绝经前妇女 | 5mg | [Aedo et al. (1985)][A85]
|
||||
> | D85 | 2 | 已去势、或已绝经妇女 | 4mg | [Düsterberg & Nishino (1982)][DN82];<br/> [Düsterberg, Schmidt-Gollwitzer, & Hümpel (1985)][DSH85]
|
||||
> | R87 | 7 | 正常年轻男性 | 10mg | [Reimann et al. (1987)][R87] |
|
||||
> | S87a | 8 | 正常绝经前妇女 | 5mg | [Sang et al. (1987)][SANG87] |
|
||||
> | S87b | 8 | 正常绝经前妇女 | 2.5mg | 同上 |
|
||||
> | S87c | 20 | 已去势、或已绝经妇女 | 10mg | [Sherwin et al. (1987)][SHERW87]; [Sherwin (1988)][SHERW88] |
|
||||
> | G88 | 54 | 未接受激素治疗的、月经正常的男性倾向跨性别者 31 人;<br />未接受激素治疗的女性倾向跨性别者 14 人;<br />性腺完整、正服用雌激素药物的女性倾向跨性别者 9 人 | 10mg | [Goh & Ratnam (1988)][GR88] |
|
||||
> | G90 | 12 | 未接受激素治疗的、月经正常的男性倾向跨性别者 | 10mg | [Goh & Ratnam (1990)][GR90] |
|
||||
> | G94a | 8 | 正常绝经前妇女 | 5mg | [Garza-Flores (1994)][GF94] |
|
||||
> | G94c | 5 | 正常绝经前妇女 | 5mg | 同上 |
|
||||
> | J94 | 9 | 正常年轻男性 | 10mg | [Jilma et al. (1994)][J94] |
|
||||
> | G98 | 5 | 患有克氏综合征的男性 | 10mg | [Goh & Lee (1998)][GL98] |
|
||||
> | G02 | 17 | 正常已绝经妇女 | 5mg | [Göretzlehner et al. (2002)][G02] |
|
||||
> | K06 | 10 | 正常更年期妇女 | 2mg | [Kerdelhué et al. (2006)][K06] |
|
||||
> | V11 | 32 | 正常年轻男性 | 5mg | [Valle Alvarez (2011)][VA11] |
|
||||
> | S12 | 48 | 正常已绝经妇女<br />(注射两针,分别注射 Estradiol-Depot 与 Progynon Depot-10) | 10mg | [Schug, Donath, & Blume (2012)][SDB12] |
|
||||
|
||||
拟合曲线排除了显著有别于平均水平、或仅表示 C<sub>max</sub> 的部分研究项目的曲线。一项研究仅报告了雌酮水平(而非雌二醇水平)而被排除<sup>([Ibrahim, 1996][I96])</sup>。另一项研究因涉及伴随妊娠终止的孕妇而被排除<sup>([Garner & Armstrong, 1977][GA77])</sup>。还有一项研究被排除,原因是年代久远、使用了过时且不准确的验血方法<sup>([Ittrich & Pots, 1965][IP65], [表格][TABLE_32A])</sup>。经处理的源数据与拟合曲线见图二。
|
||||
|
||||
> ![figure][FIG_2]
|
||||
>
|
||||
> 【图二】已发表的、单次肌注 EV 油溶液之后 30 日内的雌二醇浓度—时间曲线,及源数据的拟合曲线(加粗黑/白线)。曲线已依内源性分泌量进行修正、并调整摄入量为 10mg,以与分室药代动力学模型相契合。由于对各曲线的拟合结果与此几乎一致,故直接用数据进行拟合。源数据在他处亦有提供<sup>([Google 文档][WEB_32A]; [Plotly 表格][WEB_32B])</sup>。
|
||||
|
||||
|
||||
### 环戊丙酸雌二醇(EC)油溶液
|
||||
|
||||
EC 油溶液用于更年期激素疗法,以及其它需要雌激素的治疗当中。然而,其使用率相对于其它注射剂(例如 EV)较低。关于该注射剂的研究项目屈指可数。此处找到了来自 4 篇著述(表四)的 49 人次注射的数据。
|
||||
|
||||
> 【表四】和 EC 油溶液注射剂相关的项目:
|
||||
>
|
||||
> | 项目代号 | 注射人次 | 受试对象 | 用药量 | 参考文献 |
|
||||
> |-|-|-|-|-|
|
||||
> | R73 | 6 | 性腺发育不良的青春期女生 | 1-2mg | [Rosenfield et al. (1973)][R73];<br/> [Rosenfield & Fang (1974)][RF74] |
|
||||
> | B80 | ~5 | 正常绝经前妇女 | 10mg | [Buckman et al. (1980)][B80] |
|
||||
> | O80 | 10 | 正服用复方避孕药的绝经前妇女 | 5mg | [Oriowo et al. (1980)][O80] |
|
||||
> | L96 | 28 | 注射前正服用雌激素药物、随后停药的已绝经妇女;<br />其中 16 人有激素性偏头痛史,另 12 人无此病史 | 5mg | [Lichten et al. (1996)][L96] |
|
||||
|
||||
拟合过程没有任何曲线被排除。经处理的源数据与拟合曲线见图三。
|
||||
|
||||
> ![figure][FIG_3]
|
||||
>
|
||||
>【图三】已发表的、单次肌注 EC 油溶液之后 30 日内的雌二醇浓度—时间曲线,及其拟合曲线(加粗黑/白线)。曲线已依内源性分泌量进行修正、并调整摄入量为 5mg,以与分室药代动力学模型相契合。各曲线随后也用相同的模型进行拟合。源数据在他处亦有提供<sup>([Google 文档][WEB_33A]; [Plotly 表格][WEB_33B])</sup>。
|
||||
|
||||
|
||||
### 环戊丙酸雌二醇(EC)悬浮液
|
||||
|
||||
EC 悬浮液仅用于注射用复方避孕药。许多高质量的相关研究项目因此被纳入。这里找到了来自 4 篇著述(表五)的 49 人次注射的数据。
|
||||
|
||||
> 【表四】和 EC 悬浮液注射剂相关的项目:
|
||||
>
|
||||
> | 项目代号 | 注射人次 | 受试对象 | 用药量 | 参考文献 |
|
||||
> |-|-|-|-|-|
|
||||
> | F82 | 11 | 正常绝经前妇女 | 5mg | [Fotherby et al. (1982)][F82] |
|
||||
> | A85 | 8 | 正常绝经前妇女 | 5mg | [Aedo et al. (1985)][A85] |
|
||||
> | G87a | 7 | 正常绝经前妇女 | 5mg | [Garza-Flores et al. (1987)][GF87];<br/> [Garza-Flores (1994)][GF94] |
|
||||
> | G87b | 8 | 正常绝经前妇女 | 5mg | 同上 |
|
||||
> | G87c | 7 | 正常绝经前妇女 | 5mg | 同上 |
|
||||
> | G87d | 8 | 正常绝经前妇女 | 2.5mg | 同上 |
|
||||
> | G87e | 8 | 正常绝经前妇女 | 2.5mg | 同上 |
|
||||
> | G87f | 6 | 正常绝经前妇女 | 2.5mg | 同上 |
|
||||
> | Z98 | 9 | 正常绝经前妇女 | 5mg | [Zhou et al. (1998)][Z98] |
|
||||
> | R99 | 14 | 经外科手术节育的健康绝经前妇女 | 5mg | [Rahimy & Ryan (1999)][RR99];<br/>[Rahimy, Ryan, & Hopkins (1999)][RRH99] |
|
||||
> | S11a | 15 | 正常绝经前妇女 | 5mg | [Sierra-Ramírez et al. (2011)][SR11] |
|
||||
> | S11b<sup>(1)</sup> | 15 | 正常绝经前妇女 | 5mg | 同上 |
|
||||
> | T13 | 15 | 正常绝经前妇女 | 5mg | [Thurman et al. (2013)][T13] |
|
||||
>
|
||||
> (1) 通过皮下注射,而非肌注。
|
||||
|
||||
有一项研究尽管使用了皮下注射,但其曲线和同项目内常规肌注方式的曲线相当接近<sup>([Sierra-Ramírez et al., 2011][SR11], [表格][TABLE_34A])</sup>。拟合过程中,一些仅含 C<sub>max</sub> 的项目被排除;此外,还排除了一项仅测量了 EC 浓度(而非雌二醇浓度)的研究<sup>([Martins et al., 2019][M19], [表格][TABLE_34B])</sup>。经处理的源数据与拟合曲线见图四。
|
||||
|
||||
> ![figure][FIG_4]
|
||||
>
|
||||
>【图四】已发表的、单次肌注/皮下注射 EC 悬浮液之后 30 日内的雌二醇浓度—时间曲线,及其拟合曲线(加粗黑/白线)。曲线已依内源性分泌量进行修正、并调整摄入量为 5mg,以与分室药代动力学模型相契合。各曲线随后也用相同的模型进行拟合。源数据在他处亦有提供<sup>([Google 文档][WEB_34A]; [Plotly 表格][WEB_34B])</sup>。
|
||||
|
||||
|
||||
### 庚酸雌二醇(EEn)
|
||||
|
||||
EEn 仅用作注射用复方避孕药的成分。一些相关研究项目因此被纳入。此处找到了来自 7 篇著述(表六)的 270 人次注射的数据。
|
||||
|
||||
> 【表六】和 EEn 注射剂相关的项目:
|
||||
>
|
||||
> | 项目代号 | 注射人次 | 受试对象 | 用药量 | 参考文献 |
|
||||
> |-|-|-|-|-|
|
||||
> | R86a | 1 | 正常绝经前妇女 | 5mg | [Recio et al. (1986)][R86] |
|
||||
> | R86b | 1 | 正常绝经前妇女 | 10mg | [Recio et al. (1986)][R86] |
|
||||
> | W86 | 3 | 正常绝经前妇女 | 10mg | [Wiemeyer et al. (1986)][W86];<br/> [Wiemeyer et al. (1987)][W87] |
|
||||
> | S88 | 14 | 正常绝经前妇女 | 10mg | [Schiavon et al. (1988)][S88] |
|
||||
> | G89 | 10 | 正常绝经前妇女 | 10mg | [Garza-Flores et al. (1989)][GF89] |
|
||||
> | G94a | 9 | 正常绝经前妇女 | 10mg | [Garza-Flores (1994)][GF94] |
|
||||
> | G94b | 9 | 正常绝经前妇女 | 5mg | 同上 |
|
||||
> | G94c | 7 | 正常绝经前妇女 | 10mg | 同上 |
|
||||
> | M95 | 216 | 正常绝经前妇女 | 10mg | [Martinez (1995)][M95] |
|
||||
|
||||
以上数据中,有 216 人次注射出自同一项目,且基本仅包含 C<sub>max</sub> 数据。在拟合过程中,来自 Wiemeyer 等人 (1986) 的论著因以较小样本数(3 人次)计算的曲线下面积异常偏高而被排除;因数据量稀缺,包含 C<sub>max</sub> 数据的项目也被纳入拟合。经处理的源数据与拟合曲线见图五。
|
||||
|
||||
> ![figure][FIG_5]
|
||||
>
|
||||
> 【图五】已发表的、单次肌注 EEn 之后 30 日内的雌二醇浓度—时间曲线,及源数据的拟合曲线(加粗黑/白线)。曲线已依内源性分泌量进行修正、并调整摄入量为 10mg,以与分室药代动力学模型相契合。源数据在他处亦有提供<sup>([Google 文档][WEB_35A]; [Plotly 表格][WEB_35B])</sup>。
|
||||
|
||||
|
||||
### 十一酸雌二醇(EU)
|
||||
|
||||
EU 曾用于前列腺癌的治疗、更年期激素疗法,以及其它需要雌激素的临床治疗当中。不过,其已停产多年,目前已不再使用。尽管如此,其仍然是雌二醇注射剂历史上一个重要的注脚。这里找到了来自 3 篇著述(表七)的 7 人次注射的数据。
|
||||
|
||||
> 【表七】和 EU 注射剂相关的项目:
|
||||
>
|
||||
> | 项目代号 | 注射人次 | 受试对象 | 用药量 | 参考文献 |
|
||||
> |-|-|-|-|-|
|
||||
> | G75 | 3 | 已去势、或已绝经妇女 | 32.3mg | [Geppert (1975)][GEPP75]/<br/>[Leyendecker et al. (1975)][L75], [表格][TABLE_36A]
|
||||
> | V75 | 4 | 不明/未描述 | 100mg | [Vermeulen (1975)][V75]/<br/>[Vermeulen (1977)][V77], [表格][TABLE_36B]
|
||||
|
||||
不幸的是,以上数据的质量特别低:不仅样本数少,而且雌二醇水平差别明显。此外,尽管 EU 的持续时间长达数月,但上述项目仅跟踪了注射后两周内的数据。因此,无法基于这些数据为 EU 拟合一个相对准确的曲线——而是基于一种提议,即 EU 的雌二醇浓度曲线下面积约为其它非聚合物雌二醇酯的三分之一。另外还存在少量的多次注射数据,但其无法被整合<sup>([Jacobi & Altwein, 1979][JA79], [表格][TABLE_36A]; [Jacobi et al., 1980][J80], [表格][TABLE_36B]; [Derra, 1981][D81], [表格][TABLE_36C])</sup>。经处理的源数据与拟合曲线见图六。
|
||||
|
||||
> ![figure][FIG_6]
|
||||
>
|
||||
> 【图六】已发表的、单次肌注 EU 油溶液之后 90 日内的雌二醇浓度—时间曲线,及源数据的拟合曲线(加粗黑/白线)。曲线已依内源性分泌量进行修正、并调整摄入量为 50mg,以与分室药代动力学模型相契合。源数据在他处亦有提供<sup>([Google 文档][WEB_36A]; [Plotly 表格][WEB_36B])</sup>。
|
||||
|
||||
|
||||
### 聚磷酸雌二醇(PEP)
|
||||
|
||||
PEP 主要用于前列腺癌的治疗,但也见于其它需要雌激素的临床治疗当中(包括乳腺癌治疗、更年期激素疗法)。其曾被广泛使用,近来似乎已然停产。此处找到了来自 11 篇著述(表八)的 114 人次注射的数据,均以患有前列腺癌的男性为对象。
|
||||
|
||||
> 【表六】和 PEP 注射剂相关的项目:
|
||||
>
|
||||
> | 项目代号 | 注射人次 | 受试对象 | 用药量 | 参考文献 |
|
||||
> |-|-|-|-|-|
|
||||
> | J76 | 16 | 患有前列腺癌的男性 | 160mg | [Jönsson (1976)][J76] |
|
||||
> | L79 | 10 | 患有前列腺癌的男性 | 80mg | [Leinonen et al. (1979)][L79] |
|
||||
> | L80 | 8 | 患有前列腺癌的男性 | 80mg | [Leinonen (1980)][L80] |
|
||||
> | J82 | 4 | 患有前列腺癌的男性 | 80mg | [Jacobi (1982)][J82] |
|
||||
> | N87a | 3 | 患有前列腺癌的男性 | 80mg | [Norlén (1987)][N87];<br/> [Gunnarsson & Norlén (1988)][GN88] |
|
||||
> | N87b | 3 | 患有前列腺癌的男性 | 160mg | 同上 |
|
||||
> | N87c | 3 | 患有前列腺癌的男性 | 240mg | 同上 |
|
||||
> | N87d | 4 | 患有前列腺癌的男性 | 80mg | 同上 |
|
||||
> | N87e | 4 | 患有前列腺癌的男性 | 160mg | 同上 |
|
||||
> | N87f | 4 | 患有前列腺癌的男性 | 240mg | 同上 |
|
||||
> | S88a | 9 | 患有前列腺癌的男性 | 160mg | [Stege et al. (1988)][STEGE88];<br/> [Stege et al. (1989)][STEGE89] |
|
||||
> | S88b | 9 | 患有前列腺癌的男性 | 240mg | 同上 |
|
||||
> | S88c | 9 | 患有前列腺癌的男性 | 320mg | 同上 |
|
||||
> | S96 | 11 | 患有前列腺癌的男性 | 320mg | [Stege et al. (1996)][STEGE96] |
|
||||
> | H99 | 17 | 患有前列腺癌的男性 | 240mg | [Henriksson et al. (1999)][H99];<br/> [Johansson & Gunnarsson (2000)][JG00] |
|
||||
|
||||
拟合过程中,几项年代较远而且数据偏移过大的研究被排除在外。经处理的源数据与拟合曲线见图七。
|
||||
|
||||
> ![figure][FIG_7]
|
||||
>
|
||||
> 【图七】已发表的、单次肌注 PEP 水溶液之后 90 日内的雌二醇浓度—时间曲线,及源数据的拟合曲线(加粗黑/白线)。为更好地观察本图,浓度最大值被裁剪至 600 pg/mL (~2200 pmol/L)。曲线已依内源性分泌量进行修正、并调整摄入量为 160mg,以与分室药代动力学模型相契合。源数据在他处亦有提供<sup>([Google 文档][WEB_37A]; [Plotly 表格][WEB_37B])</sup>。
|
||||
|
||||
|
||||
### 其它雌二醇注射剂种类
|
||||
|
||||
在搜索文献时,一批有关其它雌二醇注射剂种类的临床项目也被发现 *(参考文献略)*:
|
||||
|
||||
- 雌二醇油溶液,或水溶液(可能是微晶水悬浮液),或微球(例如 Juvenum-E);
|
||||
- 雌二醇/孕酮微晶水悬浮液;
|
||||
- 雌二醇/醋酸甲地孕酮微晶水悬浮液(Mego-E,一种在中国使用的不知名的注射用复方避孕药);
|
||||
- 二丙酸雌二醇油溶液(Agofollin);
|
||||
- 苯甲酸雌二醇/苯丙酸雌二醇油溶液(Dimenformon Prolongatum);
|
||||
- 苯甲酸雌二醇/苯丙酸雌二醇/丙酸睾酮/苯丙酸睾酮/异己酸睾酮油溶液(Estandron Prolongatum);
|
||||
- 苯甲酸雌二醇/二壬酸雌二醇/庚酸苯甲酸腙睾酮油溶液(Climacteron)。
|
||||
|
||||
这些注射剂因其知名度低、数据量少,而未纳入本次荟萃分析。此外,为含有多种雌二醇成分的剂型以及微球剂型匹配已有药代动力学模型,是存在难度的。
|
||||
|
||||
有些特定的雌二醇制剂,并未找到相应的雌二醇浓度—时间关系数据;诸如雌二醇水溶液、苯甲酸雌二醇微晶水悬浮液(Agofollin Depot; Ovocyclin M 等)、丁酸苯甲酸雌二醇/苯乙酮缩二羟孕酮油溶液(Redimen, Soluna, Unijab)等等。
|
||||
|
||||
|
||||
### 所有雌二醇注射剂的汇总图表
|
||||
|
||||
图八汇总了各注射剂的雌二醇浓度拟合曲线(以摄入量 5mg 计)。聚磷酸雌二醇(PEP)除外:其摄入量需相对于其它注射剂高出约 6.5 倍,方可达到相似的雌二醇暴露量;图中其曲线下面积远小于其它雌二醇注射剂(见“讨论”一节)。十一酸雌二醇(EU)因其数据量过少,无法准确获取其曲线,故排除在图八之外。
|
||||
|
||||
> ![figure][FIG_8]
|
||||
>
|
||||
> 【图八】对已发表的、单次肌注后 20 日内的雌二醇浓度—时间曲线进行拟合的汇总结果。曲线已调整摄入量为 5mg;但其中 PEP 在相同剂量下,雌二醇水平要低 6\~7 倍,故调整其剂量为其它雌二醇酯的 6.5 倍。
|
||||
本图的[另一个版本][FIG_8_ALT]将 X 轴(时间线)延长至 30 天,并排除了苯甲酸雌二醇。
|
||||
|
||||
图九显示了各类雌二醇注射剂每 7 日使用 5 mg(或等价)剂量,达到稳态之后的模拟曲线。类似于图八,PEP 的剂量也调整为较其它注射剂高出 6.5 倍;EU 则仍被排除。
|
||||
|
||||
> ![figure][FIG_9]
|
||||
>
|
||||
> 【图九】各类雌二醇注射剂重复使用并达到稳态之后,三个肌注周期内的模拟曲线。该模拟结果基于已发表的、单次肌注后的雌二醇浓度—时间曲线的拟合结果。其中 PEP 在相同剂量下,雌二醇水平要低 6\~7 倍,故调整其剂量为其它雌二醇酯的 6.5 倍。
|
||||
本图的[另一个版本][FIG_9_ALT]排除了苯甲酸雌二醇。
|
||||
|
||||
如需更多重复用药后的雌二醇浓度—时间模拟曲线,请参见附属的[可互动的模拟器网页][WEB_1A]。
|
||||
|
||||
|
||||
### 一些特定的药代动力学参数之汇总
|
||||
|
||||
下表显示了从各雌二醇注射剂的拟合曲线截取的一些特定药代动力学参数。
|
||||
十一酸雌二醇(EU)因其数据量过少,无法准确获取其曲线及相关参数,故排除在外。
|
||||
|
||||
> 【表九】各雌二醇注射剂单次肌注 5 mg 之后,雌二醇的一些特定药代动力学参数:
|
||||
>
|
||||
> | 雌二醇注射剂 | 达峰用时(T<sub>max</sub>)<br />(天) | 浓度峰值(C<sub>max</sub>)<br />(pg/mL) | 消除半衰期(t<sub>1/2</sub>)<br />(天) | 消除90%用时(t<sub>90%</sub>)<br />(天) | 曲线下面积(AUC<sub>0-∞</sub>)<br />(pg•d/mL) |
|
||||
> |-|-|-|-|-|-|
|
||||
> | 苯甲酸雌二醇(油溶液) | 0.65 | 971 | 1.2 | 3.9 | 2410 |
|
||||
> | 戊酸雌二醇(油溶液) | 2.1 | 295 | 3.0 | 9.9 | 1886 |
|
||||
> | 环戊丙酸雌二醇(油溶液) | 4.3 | 155 | 6.7 | 22.3 | 2150 |
|
||||
> | 环戊丙酸雌二醇(水悬浮液) | 1.2 | 241 | 5.1 | 16.9 | 2096 |
|
||||
> | 庚酸雌二醇(油溶液) | 6.5 | 160 | 4.6 | 15.1 | 2183 |
|
||||
> | 聚磷酸雌二醇<sup>(1)</sup> | 18.0 | 34 | 28.4 | 94.2 | 2117 |
|
||||
>
|
||||
> (1) 剂量调整为单次 32.5 mg(相当于其它雌二醇酯的 6.5 倍)。
|
||||
|
||||
下表显示了从各类雌二醇注射剂重复使用并达到稳态的模拟曲线截取的一些特定药代动力学参数。
|
||||
与表九类似,EU 被排除在外。
|
||||
|
||||
> 【表十】各雌二醇注射剂每 7 日肌注 5 mg(或等价)剂量并达到稳态之后,雌二醇的一些特定药代动力学参数:
|
||||
>
|
||||
> | 雌二醇注射剂 | 达峰用时(T<sub>max</sub>)<br />(天) | 浓度峰值(C<sub>max</sub>)<br />(pg/mL) | 浓度谷值(C<sub>min</sub>)<br />(pg/mL) | 峰谷之差<br />(pg/mL) | 峰谷比值 | 综合平均浓度(C<sub>avg</sub>)<br />(pg/mL) |
|
||||
> |-|-|-|-|-|-|-|
|
||||
> | 苯甲酸雌二醇(油溶液) | 0.64 | 990 | 29 | 962 | 35 | 344 |
|
||||
> | 戊酸雌二醇(油溶液) | 1.9 | 384 | 142 | 242 | 2.7 | 269 |
|
||||
> | 环戊丙酸雌二醇(油溶液) | 3.1 | 339 | 262 | 77 | 1.3 | 307 |
|
||||
> | 环戊丙酸雌二醇(水悬浮液) | 1.0 | 404 | 189 | 214 | 2.1 | 299 |
|
||||
> | 庚酸雌二醇(油溶液) | 4.0 | 329 | 288 | 41 | 1.1 | 312 |
|
||||
> | 聚磷酸雌二醇<sup>(1)</sup> | 3.2 | 304 | 299 | 5 | 1.0 | 302 |
|
||||
>
|
||||
> (1) 剂量调整为每次 32.5 mg(相当于其它雌二醇酯的 6.5 倍)。
|
||||
|
||||
消除半衰期(t<sub>1/2</sub>)是指当雌二醇的分布达到准平衡之后,雌二醇浓度减少 50 % 所需时间——*而非雌二醇酯注射过后消除半数所需时间* ;其仅计算雌二醇浓度—时间曲线的消除部分,而排除了雌二醇的吸收与分布时段<sup>([Toutain & Bousquet-Mélou, 2004][TB04])</sup>。由于贮存的注射剂有药代动力学的倒挂效应(flip–flop kinetics,即吸收速率比消除速率慢——译者注),并且雌二醇的血浆半衰期极短(\~0.5-2 小时);因此,“雌二醇注射剂的消除半衰期”所描述的,并非雌二醇从血浆清除的过程,而是雌二醇自注射位点吸收的过程<sup>(Toutain & Bousquet-Mélou, 2004; [Yáñez et al., 2011][Y11])</sup>。
|
||||
|
||||
|
||||
|
||||
## 讨论
|
||||
|
||||
### 数据的质量、局限性以及在各研究项目之间的差别
|
||||
|
||||
各雌二醇注射剂的拟合曲线之准确性,会被其已有数据所限制。各注射剂的数据之多少以及质量,皆有分别。例如,有关戊酸雌二醇(EV,油溶液)与环戊丙酸雌二醇(EC,水悬浮液)的数据相当完备;而有关 EC(油溶液)与庚酸雌二醇(EEn,油溶液)的数据则较为有限。有部分注射剂的浓度—时间曲线在特定时段的采样量不足,例如:苯甲酸雌二醇(EB,油溶液)在曲线的早期、EEn 油溶液在曲线的大部分时段、以及聚磷酸雌二醇(PEP)在曲线的后期。至于十一酸雌二醇(EU,油溶液),其数据量并不足以准确拟合其曲线。这些注射剂的拟合曲线与特定药代动力学参数,需要通过不完整的数据来解读;大多数情况下,其不应视为精准的定量,而应作为大致的估测,而且其势必会随更多、质量更好的数据而发生改变。事实上,这些曲线与参数常对特定研究项目表现出明显的敏感度。有关建模方面的抉择,诸如选择何种药代动力学模型、以及是否直接基于源数据进行拟合(而非基于各项目的曲线)等,这些都会对拟合曲线以及选定的药代动力学参数产生显著差别。
|
||||
|
||||
部分雌二醇注射剂的数据相当稀少;为此放宽了研究项目收录门槛,以尽可能多地收集数据,使拟合曲线结果更佳,尽管这要承担部分数据可能不可靠的风险。例如,收录项目时忽略了受试者的 HPG 轴状态;再例如,当数据量不足时,会将 C<sub>max</sub> 数据统计在内。
|
||||
关于 HPG 轴状态:一些针对有正常周期的妇女的项目会产生更大误差,这归咎于内源性分泌的雌二醇水平各异。此外,在性腺完整的妇女身上,突然升高的雌二醇水平,会促使促黄体生成素水平在数日内激增,并可导致雌二醇水平的增加延迟(delayed bump)。有关该现象更明显的例子,可见于使用 EB 的性腺完整的妇女<sup>([维基百科][WIKI_51A])</sup>。许多——若非大多数的话——有关 EB 的项目皆涉及到有完整 HPG 轴的妇女;此类项目相较有关其它种类注射剂的项目显得并不寻常。
|
||||
关于 C<sub>max</sub> 数据:有些 C<sub>max</sub> 数据代表“各受试者的雌二醇浓度峰值的平均值”,这和“所有受试者的平均雌二醇浓度曲线之峰值”是两回事。C<sub>max</sub> 会因检测规模与时机而与平均浓度曲线峰值产生差异<sup>(例如 [Oriowo et al., 1980][O80], [表格][TABLE_51A]; [Rahimy, Ryan, & Hopkins, 1999][RRH99])</sup>。关于其原因,举个例子,各受试者的雌二醇浓度并非都在同一时间达峰,而这种时间差会使得个体的浓度峰值在平均浓度曲线当中被稀释。不过,无论如何,C<sub>max</sub> 基本上与平均浓度曲线峰值较为接近。C<sub>max</sub> 数值在对 EEn 曲线的拟合过程中被囊括,而对于其它注射剂则被排除;这是因为,有关 EEn 等特定注射剂的雌二醇浓度曲线(平均的、各受试者的)数据相当有限,此时为更好地拟合其曲线,需引入 C<sub>max</sub>。
|
||||
还有,部分纳入了拟合过程的数据来自间隔一个月的多次用药;而有关间隔一个月多次使用注射用复方避孕药(含 EEn)的研究已发现,多次用药后,雌二醇浓度达峰时间可能发生推移<sup>([Schiavon et al., 1988][S88]; [Garza-Flores, 1994][GF94])</sup>。
|
||||
|
||||
即便使用同种雌二醇注射剂,在不同研究项目之间,雌二醇水平与浓度—时间曲线也会有显著差异。当下对于造成这些显著差异的原因,尚不完全明确;不过,有些潜在因素被认为可能产生这些差异。
|
||||
其中一些和制剂、注射方式有关,包括:剂型(如油溶剂、辅料和其它成分、药物浓度、颗粒大小等),注射量,注射位点(如臀部、大腿、上臂等),注射技术(如使用的力度,以及由此产生的贮存液滴尺寸),注射器死腔,等等。
|
||||
而另一些因素则与受试者、研究项目有关,包括:验血方法的差异,受试者样本特征的差异(如年龄、体重、性别、种族、运动能力、HPG 轴状态等),采样误差,等等<sup>([Sinkula, 1978][SINKULA78]; [Chien, 1981][CHIEN81]; [Minto et al., 1997][M97]; [Larsen & Larsen, 2009][LL09]; [Larsen et al., 2009][L09]; [Florence, 2010][F10]; [Larsen, Thing, & Larsen, 2012][LTL12]; [Kalicharan, 2017][K17])</sup>。对于一些年份更久远的项目,其验血结果的精确度可能更差,受试者人数也往往更少,这尤其增加了项目之间的差异性。这些项目的数据,相较年份更近、采样数更多的项目,会显得不大可靠。不过,本文的数据排除标准有助于排除这些异常结果。
|
||||
本次荟萃分析并未将不同项目之间差异背后的潜在因素纳入考虑;如果纳入考虑,会相当困难。这是因为,在许多情况下,各个项目并未披露有关这些差异的信息,而对于这些因素的准确影响与相对重要性的量化研究也很有限。
|
||||
|
||||
不过,从其它项目可以得知,不同的油溶剂在注射位点的溶解速度有所差异<sup>([Svendsen & Aaes‐Jørgensen, 1979][SA79]; [Schultz et al., 1998][S98]; [Larsen et al., 2001][L01])</sup>,而这会产生雌二醇浓度—时间曲线的差别<sup>([Ballard, 1978][B78], [摘要][B78_EXCERPT]; [Knudsen, Hansen, & Larsen, 1985][KHL85])</sup>。其原因被认为在于亲脂性和注射后释放速率的不同。油脂的粘稠度也被猜测可影响从注射位点逸出的速率<sup>([Schug, Donath, & Blume (2012)][SDB12])</sup>;然而,目前为止的研究并不支持此猜测<sup>([Larsen & Larsen, 2009][LL09]; [Larsen, Thing, & Larsen, 2012][LTL12])</sup>。不同注射剂所用油溶剂亦可能不一致,即便其包含同一种雌二醇酯。
|
||||
例如,在制药厂,戊酸雌二醇可制成芝麻油、蓖麻油、或葵花籽油溶液等剂型<sup>([表格][TABLE_51B])</sup>。需要留意,这三种油的亲脂性较为相似<sup>([表格][TABLE_51B])</sup>。
|
||||
而另一方面,为自行用药(DIY)的女性倾向跨性别者所采用的自制雌二醇注射剂,通常使用中链甘油三酯(MCT)作为油溶剂。这种油(以专利配方 Viscoleo 的形式)被发现,相较芝麻油和蓖麻油,其在动物体内的溶解速率显然要快得多<sup>([Svendsen & Aaes‐Jørgensen, 1979][SA79]; [Schultz et al., 1998][S98]; [Larsen et al., 2001][L01])</sup>。另外,尽管数据相当有限,但 MCT 已被发现可在人体内产生波动更大、持续时间更短的注射后浓度曲线<sup>([Knudsen, Hansen, & Larsen, 1985][KHL85])</sup>。因此,相较制药厂产品,以 MCT 作为溶剂的雌二醇注射剂,可能会产生截然不同的、不大有利的浓度—时间曲线。
|
||||
至于其它辅料(例如苯甲醇),或者注射位点、注射量等其它因素,也被发现可影响贮存的注射剂的药代动力学特性<sup>([Minto et al., 1997][M97]; [Kalicharan, Schot, & Vromans, 2016][KSV16])</sup>。根据剂型不同,油溶剂以外的辅料亦有不同<sup>([表格][TABLE_51B])</sup>。
|
||||
|
||||
不同项目之间差异所牵涉的还有:对于某种特定的雌二醇注射剂,其雌二醇浓度—时间曲线并非只有一条,而是有很多条;其变数包括剂型、用量/用法、受试者的状况,等等。因此,本次荟萃分析所测定的拟合曲线,仅仅代表对绝大多数情况下的一种预测;在特定情形下,某种注射剂的真实曲线很可能与此大相径庭。
|
||||
|
||||
对于某种特定的雌二醇注射剂,如果 *<u>先单独对各个项目的数据拟合其曲线,再将各曲线进行拟合</u>*,那么可获得相较 *<u>直接拟合所有原始数据</u>* 更加准确的结果;后者会因为某些项目的采样时间点多,而天然地增加其权重,继而扩大其对拟合结果的影响,因此存在局限性。而且,更大的问题是,由于不同项目对曲线的不同部分进行不同程度的采样,以及这些项目的曲线之间的系统性差异,故*直接拟合数据* 的方式可能会导致曲线形状的失真。这些问题皆可通过拟合各项目的拟合曲线而解决。不过,无法将所有项目都进行单独拟合;因为有些项目的采样时间点和曲线特征有限,这妨碍了其曲线的准确拟合。作为例子,C<sub>max</sub> 数据本身无法被正确拟合。综上,无法对所有雌二醇注射剂都进行对各项目之拟合曲线的拟合。结果就是,各雌二醇酯的拟合方式并非一致,其中有的选择了*直接拟合所有原始数据* (例如庚酸雌二醇、聚磷酸雌二醇)。
|
||||
|
||||
尽管存在各种局限性,但这种有关雌二醇注射剂的聚合分析与建模工作尚未有过先例。本次非正式荟萃分析提供了至今为止最详尽的、有关这些注射剂的雌二醇水平及其曲线的剖析。
|
||||
|
||||
### 持续时间和曲线形状
|
||||
|
||||
非聚合物类的注射用雌二醇酯油溶液的曲线形状,与其亲脂性高度相关。酯的亲脂性越强,则其造成的雌二醇水平峰值越低,浓度—时间曲线也拉得越长。例如,亲脂性最弱的雌二醇酯之一:苯甲酸雌二醇,拥有其中波动最大的曲线、最短的持续时间;而环戊丙酸雌二醇、庚酸雌二醇等亲脂性更强的雌二醇酯,则拥有相对更平滑、达峰更晚的曲线,以及更长的持续时间。
|
||||
|
||||
#### 戊酸雌二醇(EV)的持续时间
|
||||
|
||||
在本次荟萃分析中,来自 [Oriowo 等人 (1980)][O80] 的知名研究的注射用 EV 的浓度—时间曲线,较整体曲线的波动显著更大、且持续时间更短。在另一方面,来自年份更近、且质量可能更佳的数项研究的浓度—时间曲线,则更接近于 EV 的整体曲线<sup>(例如 [Göretzlehner 等人 (2002)][G02]; [Valle Alvarez 等人 (2011)][VA11]; [Schug, Donath, & Blume (2012)][SDB12])</sup>。值得一提的是,Oriowo 等人 (1980) 使用了一种基于花生油的 EV 剂型,而其与制药厂里通常以芝麻油或蓖麻油(及其它辅料)作为溶剂的注射用 EV 有所不同<sup>([表格][TABLE_51B])</sup>。此差异可能影响了 Oriowo 等人 (1980) 所描述的曲线。该研究的样本规模相较上述年份更近者也更少(其样本只有 9 人次,而另三项则分别有 17 人次、32 人次和 24×2 人次)。如果基于更新近的和全部数据,EV 显然拥有较 Oriowo 等人 (1980) 所描述的那样更平滑、更持久的曲线。
|
||||
|
||||
#### 环戊丙酸雌二醇(EC)油溶液与庚酸雌二醇(EEn)的持续时间比较
|
||||
|
||||
相比于其它几种注射剂,这两种注射剂可用的雌二醇浓度—时间关系数据更为稀少,至今也尚无二者之间的直接比较。基于一些有关这两种注射用雌二醇酯的文献——尤其是 [Oriowo 等人 (1980)][O80] 的讨论以及一篇对注射用复方避孕药的药代动力学的评述<sup>([Garza-Flores, 1994][GF94], [表格][TABLE_52A])</sup>,EEn 油溶液的持续时间似乎相较 EC 油溶液更长。不过,这项结论仅来自于有限的对相互独立、只能作间接比较之项目的研究。从 Garza-Flores (1994) 图表获取的 EC 油溶液相关数据,其实来自于 Oriowo 等人 (1980) <sup>([表格][TABLE_51A])</sup>;如果仅依赖这些数据,也需要当心。
|
||||
这里最大的顾虑是:正如本次荟萃分析所展示的那样,同一种雌二醇注射剂的曲线形状,在不同项目之间也可存在显著差异。其原因被认为仍未完全定论;不过,这些因素可能包括各项目(同种注射剂)所用剂型的不同。这方面需要提及的是:Oriowo 等人 (1980) 使用了有异于传统制药厂出品的 EC 油溶液注射剂的一种 EC 剂型;具体而言,该项目的剂型基于花生油(还包含其它几种杂项),而制药厂的上市产品则基于棉籽油<sup>([表格][TABLE_51B])</sup>。并且,该项目样本规模较少(仅 10 人次),故其样本误差可能较大。综上,兴许对于一些单独项目——尤其是像 Oriowo 等人 (1980) 这样的,需要格外谨慎地作出说明。
|
||||
|
||||
一项规模较小、却引人注目的有关注射用环戊丙酸睾酮油溶液(6 人次)、和庚酸睾酮油溶液(6 人次)之间直接比较的研究,和当下正在讨论的话题相关。该研究发现,使用同等剂量的、除睾酮成分外完全一致的剂型,可产生几乎一致的睾酮浓度—时间曲线<sup>([Schulte-Beerbühl & Nieschlag, 1980][SBN80], [表格][TABLE_52B])</sup>。此发现和环戊丙酸睾酮、庚酸睾酮之亲脂性(以[辛醇-水分配系数][WIKI_52A]预测法做测量)非常近似的事实相一致<sup>(例如,直接比较的话,用 [ALOGPS][WEB_52A] 计算得 5.1、5.11,用 [ChemAxon logP][WEB_52B] 计算得 6.29、6.11,用 [XLogP3][WEB_52C] 计算则得 6.4、6.3;[表格][TABLE_52C])</sup>。这无疑具有重要意义,因为亲脂性被认为是决定油基注射剂的释放动力学的关键因素<sup>([Sinkula, 1978][SINKULA78]; [Shah, 2007][S07]; [Larsen & Larsen, 2009][LL09]; [Larsen, Thing, & Larsen, 2012][LTL12]; [Shahiwala, Mehta, & Momin, 2018][SMM18])</sup>。
|
||||
将酯基部分相同的 EC 与 EEn 的亲脂性做比较,也可发现其几乎一致<sup>(例如,用 ALOGPS 预测辛醇-水分配系数得 6.47、6.45,用 XLogP3 计算则得 7.1、7.0;[表格][TABLE_52C])</sup>。故此,理论上,注射用 EC 和 EEn 会像环戊丙酸睾酮、庚酸睾酮那样,产生非常近似的曲线——至少假定剂型等其它一切变数皆恒定的情况下。
|
||||
|
||||
本次荟萃分析发现,相较于 Oriowo 等人 (1980) 的发现,EC 油溶液的整体曲线显著更平滑、更持久。这里需要提及的是:其它包含了 EC 油溶液的研究,皆仅使用了制药厂出品的 Depo-Estradiol,在其批准用于更年期激素疗法的注射间隔下——即每 3-4 周一次 1-5 mg<sup>([药品标签][WEB_52D])</sup>,其整体曲线显得更为稳定。
|
||||
此外,本次荟萃分析还发现,注射用 EC 油溶液、EEn 油溶液具有基本相似的平滑而又持久的雌二醇浓度—时间曲线。不过,油溶 EC 达峰时间更早;而在曲线的消除部分,油溶 EEn 被消除得更快。无论如何,关于这两种注射剂,可用的浓度—时间关系数据较为有限;而本次荟萃分析亦无法给出它们有什么药代动力学上的真正差异的结论,因为其曲线之间显而易见的差别有可能仅仅出于统计误差。
|
||||
综上所述,EC 油溶液可能具有较之 Oriowo 等人 (1980) 的发现更平滑、更持久的曲线;而 EC 油溶液、EEn 的曲线近似度可能较先前假设的那样更高。
|
||||
|
||||
#### 环戊丙酸雌二醇(EC)水悬浮液的曲线形状
|
||||
|
||||
尽管 EC 水悬浮液也是一种和 EC 油溶液、EEn 油溶液相似的长效型雌二醇注射剂,但其雌二醇浓度—时间曲线形状和后两者皆显得不同。较之于 EC 油溶液和其它长效型油基注射剂,EC 悬浮液的曲线达峰时间显然更早。这可能和注射用水悬浮液迥异的贮存原理和独特特性有关<sup>([Aly W., 2019][ALYW19_AQUA])</sup>。根据此论断,注射用醋酸甲羟孕酮悬浮液 (Depo-Provera) 也表现为达峰很早、但持续时间相当长(对于油基注射剂,更长的持续时间常关联于更晚的达峰时间)<sup>([多图表][TABLE_52D])</sup>。尽管作为注射剂时,水悬浮液往往相对于油溶液持续得更久<sup>([Enever et al., 1983][E83]; [Aly W., 2019][ALYW19_AQUA])</sup>;但并非所有情况皆如此。EC 悬浮液就显得相较 EC 油溶液持续得更短,这很有意思。
|
||||
|
||||
### 雌二醇暴露量与效力
|
||||
|
||||
将各种非聚合物类注射用雌二醇酯的剂量和注射间隔调整为每 7 天 5 mg之后,平均的雌二醇水平大约在 300 pg/mL (约合 1,100 pmol/L)。相比之下,在绝经前顺性别妇女体内,雌二醇分泌量在 200 μg/天 (或 6 mg 每月/每周期) 左右;而平均雌二醇水平则在 100 pg/mL (约合 370 pmol/L) 左右<sup>([Aly W., 2019][ALYW19_INTRO_N])</sup>。在根据雌二醇酯的摩尔质量进行调整后,特定剂量下的非聚合物类注射用雌二醇酯所达成的雌二醇水平,和绝经前顺性别妇女体内卵巢所分泌雌二醇达成的水平相一致(要达到综合平均 100 pg/mL 的雌二醇水平,需雌二醇酯约 1.2 mg/七天,或经卵巢分泌 1.4 mg/七天)。前述剂量和以下事实有关:注射用戊酸雌二醇被报告具有约 100% 的生物利用度(对于其它非聚合物类雌二醇酯,尽管此类描述更少,但情况应当类似)<sup>([Düsterberg & Nishino, 1982][DN82]; [Seibert & Günzel, 1994][SG94])</sup>。
|
||||
|
||||
尽管非聚合物类注射用雌二醇酯的雌二醇浓度—时间曲线不尽相同,但其曲线下面积皆显得颇为近似。这与不同雌二醇酯之间摩尔质量,以及雌二醇质量占比——所有纳入评估者皆介乎 62\~76%,而排除十一酸雌二醇后,则介乎 69\~76%——的差异较小的事实有关<sup>([表格][TABLE_1A])</sup>。本次荟萃分析中所展示的曲线下面积的差异,很可能只是出于统计误差的缘故;真正的差异则未能被证实。这种曲线下面积之近似意味着,同等剂量下,所有非聚合物类雌二醇酯皆可提供大致等量的雌二醇。
|
||||
|
||||
另一方面,聚磷酸雌二醇这种酯聚合物所产生的平均雌二醇水平、和曲线下面积,皆比非聚合物类雌二醇酯低了 6\~7 倍。这表明,聚磷酸雌二醇所含雌二醇的生物利用度并非 100%,其为临床上实际所用剂量(40-320 mg/月)相较非聚合物类雌二醇酯更高的事实所佐证;在更年期激素疗法、前列腺癌治疗等情况下也有相同迹象<sup>([维基百科][WIKI_53A]; [Estradurin 药品标签][WEB_53A])</sup>。迄今尚未有文献记载此现象,其缘故也尚不清楚。有这样一种可能:聚磷酸雌二醇在被分解成雌二醇之前,就有一部分被排出,因此这一部分也未表现出生物活性,从而使得为达到同等雌二醇水平与临床效果所需剂量变得更高。
|
||||
|
||||
对于某两种特定的雌二醇注射剂,即便可产生同等的总和雌二醇水平,也并不意味着它们必然具有同等雌激素效力——也即,一定剂量下的效力强度。似乎可信的是,在雌激素效力上,像苯甲酸雌二醇这样具有波动更大的雌二醇浓度—时间曲线的,总体弱于庚酸雌二醇这般具有波动更小之曲线的。这是因为,特定组织里的雌激素受体数目有限,从而会在一定节点上进入饱和状态。故此,波动更大、峰值更高的雌二醇水平,很可能会被“浪费”,在不同组织里,“浪费”的程度不一。
|
||||
另一方面,峰值更高、从而波动更大的雌二醇水平曲线,可能会对肝脏等需要较高雌二醇水平作用的组织产生更大影响(还伴随有凝血及其它健康风险)<sup>([Aly W., 2020][ALYW20_CLOT])</sup>。不过,这些可能性仅仅出于猜测和理论。诚然迄今已有一些文献提及该问题<sup>(例如 [Parkes, 1937][P37]; [Bradbury, Long, & Durham, 1953][BLD53])</sup>,但这方面的研究还很稀少。故此,当下无法将雌二醇水平在时间上的变化和曲线形状上的不同,纳入到对雌二醇注射剂(或其它雌二醇形态/路径)之间雌激素效力比较的评估上来。此外,需要提及的是,这些变化还取决于注射间隔,当注射间隔变短、雌二醇水平更稳定时,该变化会被削弱,这些皆应纳入考虑。
|
||||
|
||||
### 受试者个体之间的差异
|
||||
|
||||
即便采用同种雌二醇注射剂,个体之间也有总和雌二醇水平及其曲线形状上的很大不同。在本次荟萃分析中,并未纳入标准差、95%范围等一些衡量个体间差异的指标,因为这需要大幅增加工作量和工作时间——例如从所有项目和分析当中提取出误差线。不过,此次被收录的一些研究项目对上述指标都有体现<sup>(例如 [Oriowo et al., 1980][O80]; [Derra, 1981][D81], [图表][TABLE_36C]; [Aedo et al., 1985][A85], [图表][TABLE_54A]; [Sang et al., 1987][SANG87], [图表][TABLE_54B]; [Rahimy & Ryan, 1999][RR99], [图表][TABLE_54C]; [Valle Alvarez, 2011][VA11], [图表][TABLE_54D]; [Schug, Donath, & Blume, 2012][SDB12], [图表][TABLE_54E])</sup>。口服及透皮给予雌二醇所引起的雌二醇水平的高度差异,已被确定无疑<sup>([Kuhl, 2005][K05]; [维基百科][WIKI_54A])</sup>。
|
||||
注射用非聚合物类雌二醇酯在这方面的差异,应当会更小,因为其生物利用度看来皆接近完全。然而,似乎即便采用同样形态的注射用雌二醇,个体之间的差异仍相当大。比方说,单种注射用雌二醇剂型所适合的剂量和注射间隔,在每个个体上皆有显著差别。这就体现出验血的重要性:其可确保雌二醇注射剂的使用不会出现过量或不足的情况——过量会增加血栓等健康风险<sup>([Aly W., 2020][ALYW20_CLOT])</sup>,而剂量不足则会导致睾酮的压制和临床疗效欠佳。
|
||||
|
||||
### 对临床指南和剂量建议的剖析
|
||||
|
||||
一些《跨性别健康临床指南》<sup>(又见 [Aly W., 2020][ALYW20_GUIDE])</sup>提供了有关注射用戊酸雌二醇(油溶液)与环戊丙酸雌二醇(油溶液)之剂量、注射间隔的建议(见表十一);对于其它很少用于跨性别医学上的雌二醇注射剂,则未提供推荐剂量。在不同《指南》之间,戊酸雌二醇、环戊丙酸雌二醇的推荐剂量有较大差异;而推荐的注射间隔则恒定于每 1-2 周一次。戊酸雌二醇的剂量从 2-20 mg/周到 5-80 mg/两周不等;而环戊丙酸雌二醇的剂量从 <1 - 10 mg/周到 <2 - 80 mg/两周不等。
|
||||
作为参考,当下最主流的用于跨性别激素治疗的《临床指南》,来自于美国内分泌学会和加州大学旧金山分校(UCSF)<sup>([Aly W., 2020][ALYW20_GUIDE])</sup>;其中,美国内分泌学会版《指南》对这两种注射剂的推荐剂量皆为 2-10 mg/周、或 5-30 mg/两周<sup>([Hembree et al., 2017][H17])</sup>;UCSF 版《指南》则推荐使用 <20 - 40 mg/两周的戊酸雌二醇,以及 <2 - 5mg/两周的环戊丙酸雌二醇(如发生周期性不良反应,亦可缩短至一周并将剂量减半)<sup>([Deutsch, 2016a][D16a])</sup>。
|
||||
|
||||
> 【表十一】在《跨性别医学临床指南》中所推荐的雌二醇注射剂(尤指戊酸/环戊丙酸雌二醇)之用量与注射间隔<sup>(1)</sup>:
|
||||
>
|
||||
> | 指南 | 雌二醇酯 | 用量范围及注射间隔 |
|
||||
> |-|-|-|
|
||||
> | [美国内分泌学会 / Hembree et al. (2017)][H17] | 戊酸/环戊丙酸雌二醇 | 肌注 2-10 mg/周或 5-30 mg/两周 |
|
||||
> | [UCSF / Deutsch (2016b)][D16b] | 戊酸雌二醇 | 初始低剂量:肌注 <20 mg/两周<br/>初始剂量:肌注 20 mg/两周<br/>最高剂量:肌注 40 mg/两周<br/>备注①:“如有周期性症状,可将剂量与间隔减半”<br/>备注②:仅用于成年女性倾向跨性别者 |
|
||||
> | | 环戊丙酸雌二醇 | 初始低剂量:肌注 <2 mg/两周<br/>初始剂量:肌注 2 mg/两周<br/>最高剂量:肌注 5 mg/两周<br/>备注同上 |
|
||||
> | [UCSF / Olson-Kennedy et al. (2016)][OK16] | 戊酸雌二醇 | 5-20 mg/两周<br/>最高剂量:30-40 mg/两周<br/>备注:仅用于青年女性倾向跨性别者 |
|
||||
> | | 环戊丙酸雌二醇 | 2-10 mg/周<br/>备注:仅用于青年女性倾向跨性别者 |
|
||||
> | [芬威健康 / Cavanaugh et al. (2015)][C15]<sup>(2)</sup> | 戊酸雌二醇 | 初始剂量:肌注 5-10 mg/周<br/>通常剂量:肌注 20 mg/两周<br/>最高剂量:肌注 40 mg/两周 |
|
||||
> | | 环戊丙酸雌二醇 | 初始剂量:肌注 2.5 mg/两周<br/>通常剂量:肌注 5 mg/两周<br/>最高剂量:肌注 10 mg/两周 |
|
||||
> | [Callen-Lorde (2018)][CL18] | 戊酸雌二醇 | 初始剂量:肌注 10-20 mg/两周<br/>最高剂量:肌注 20-40 mg/两周 |
|
||||
> | | 环戊丙酸雌二醇 | 初始剂量:肌注 2.5 mg/两周<br/>最高剂量:肌注 5 mg/两周 |
|
||||
> | [Davidson et al. / Tom Waddell 健康中心 (2013)][D13] | 戊酸/环戊丙酸雌二醇 | 初始剂量:肌注 20-40 mg/两周<br/>平均剂量:肌注 40 mg/两周<br/>最高剂量:肌注 40-80 mg/两周 |
|
||||
> | [Bourns / 舍邦健康 / 安大略彩虹健康项目 (2019)][B19] | 戊酸雌二醇 | 初始剂量:3-4 mg/周或 6-8 mg/两周<br/>通常剂量:不定<br/>最高剂量:10 mg/周 |
|
||||
> | [不列颠哥伦比亚省跨性别护理服务,Trans Care BC (2021)][TCB21] | 戊酸雌二醇 | 初始剂量:肌注或皮下注射 5 mg/周<br/>通常剂量:肌注或皮下注射 10-20 mg/周<br/>部分人可接受每两周使用两倍剂量 |
|
||||
> | [Dahl et al. / 温哥华沿岸健康项目 (2015)][D15] | 戊酸雌二醇 | 肌注 20-40 mg/两周<br/>备注:“仅作 3-6 个月的雌激素替代治疗” |
|
||||
> | [欧洲性医学会 / T’Sjoen et al. (2020)][T20] | 戊酸雌二醇 | 肌注 5-30 mg 每周至每两周 |
|
||||
> | | 环戊丙酸雌二醇 | 肌注 2-10 mg/周 |
|
||||
> | [TransLine (2019)][T19] | 戊酸雌二醇 | 初始/通常剂量:肌注 5-10 mg/周<br/>最高剂量:肌注 20 mg/周 |
|
||||
> | | 环戊丙酸雌二醇 | 初始/通常剂量:肌注 1.25-2.5 mg/周<br/>最高剂量:肌注 5 mg/周 |
|
||||
>
|
||||
> (1) 还有些其它《指南》,其推荐剂量与间隔显然直接引用自美国内分泌学会版、或 UCSF 版《指南》,故未在此列出;但可于他处查阅<sup>([Aly W., 2020][ALYW20_GUIDE])</sup>。
|
||||
> (2) 芬威健康已于 2021 年更新了其《[指南][C15_NEW]》——译者注
|
||||
|
||||
在本次非正式荟萃分析中,随着将主流《跨性别临床指南》推荐的戊酸/环戊丙酸雌二醇剂量与使用间隔纳入考虑并加以比较,许多顾虑浮出了水面。基于本次分析,相较对其它途径、或形式(如口服、透皮等)的雌二醇推荐使用的剂量,显然,这些对于注射剂的推荐剂量与间隔会导致雌二醇暴露量更高。以 5 mg/周的剂量注射任意一种非聚合物类雌二醇酯之后,已可达到超生理的平均约 300 pg/mL (约合 1,100 pmol/L) 的雌二醇水平;然而,这些《指南》的推荐剂量可高达 *15-20 mg* 每周。根据本次荟萃分析,如此剂量所导致的平均雌二醇浓度,将大大超过同一篇指南对女性倾向跨性别者所建议的雌二醇水平范围;例如,10-20 mg/周剂量下,雌二醇水平范围可达约 600-1,200 pg/mL(约合 2,200-4,400 pmol/L,见图十),而建议的范围则在 50-200 pg/mL(约合 180-730 pmol/L)<sup>([表格][TABLE_55A])</sup>。考虑到绝经前顺性别妇女体内雌二醇的正常分泌量——约 1.4 mg/周,或 6 mg 每月或每周期(可提供平均约 100 pg/mL、约合 370 pmol/L 的雌二醇水平)<sup>([Aly W., 2019][ALYW19_INTRO_N])</sup>,那么如此高度超生理的雌二醇水平也就不出所料了。当前,关于高剂量注射用雌二醇酯(如戊酸、环戊丙酸雌二醇)的临床安全性数据尚有所欠缺,不过已知过大的雌激素暴露量可增加血栓等并发症的健康风险<sup>([Aly W., 2020][ALYW20_CLOT])</sup>。此类由《指南》推荐的超高剂量应当对其安全性作相当程度的保留。
|
||||
|
||||
> ![figure][FIG_10]
|
||||
>
|
||||
> 【图十】以当下主流的《跨性别护理指南》所优先推荐的剂量与间隔 (5-40 mg/两周) 注射戊酸雌二醇之后,雌二醇水平的模拟结果。在此间隔下,雌二醇水平在第二次或第三次注射后达到稳态,此后不再累积。
|
||||
本图的[另一个版本][FIG_10_ALT]将剂量与间隔减半,即 2.5-20 mg/周。
|
||||
|
||||
本文作者已于他处列出有关雌二醇注射剂在总和雌二醇暴露量上可与其它形态、路径大致相当的,用于女性倾向跨性别者的剂量<sup>([Aly W., 2020][ALYW20_DOSE])</sup>。其中对于注射用非聚合物类雌二醇酯,剂量从 1-6 mg/周不等,对应于“低剂量”到“超高剂量”疗法<sup>([图表][TABLE_55B])</sup>。相较于许多现有《指南》所推荐的那样,上述剂量范围应该更适合女性倾向跨性别者使用。在女性化激素治疗中,尽管在不服用抗雄制剂的情况下,较高的雌二醇水平对睾酮的抑制效力,可较正常生理水平更强;但是,这显然只需适度超生理的水平(约 200-300 pg/mL,合 730-1,100 pmol/L)便可形成强力压制<sup>([Aly W., 2020][ALYW19_INTRO_G]; [Langley et al., 2021][L21])</sup>。有鉴于此,注射用雌二醇的剂量无需过高。
|
||||
|
||||
有些像美国内分泌学会版这样的《指南》,会给戊酸、环戊丙酸雌二醇推荐相同的剂量与间隔;而 UCSF 版等其它《指南》则为其分别推荐不同的剂量。令人担忧的是,UCSF 版《指南》推荐剂量的差别可达一个数量级——即 <20 - 40 mg/两周(戊酸雌二醇)对比于 <2 - 5 mg/两周(环戊丙酸雌二醇);这两种雌二醇酯显然可产生相似的平均雌二醇水平(5 mg/周剂量下,可达 300 pg/mL 或 1,100 pmol/L),并且其雌二醇浓度—时间曲线形状差得不太多——差别只在,环戊丙酸雌二醇的稍微更平滑、更持久罢了。因此,对它们而言,采用相仿的剂量应该更合适。而这也得到以下事实的支持:在一次针对这两种雌二醇酯的集中临床开发计划里,顺性别妇女注射的复方避孕药所含戊酸、环戊丙酸雌二醇之剂量相当(均为每月一次 5 mg),而该剂量也是被仔细测定过的<sup>([Garza-Flores, 1994][GF94]; [Newton, d’Arcangues, & Hall, 1994][NAH94]; [Sang, 1994][SANG94]; [Toppozada, 1994][T94])</sup>。该计划还包含了一些关于不同剂量及直接比较的研究项目。基于本次荟萃分析,UCSF 版《指南》的推荐剂量可导致戊酸雌二醇摄入的显著过量,以及环戊丙酸雌二醇摄入的潜在不足。
|
||||
|
||||
《跨性别健康指南》对戊酸、环戊丙酸雌二醇(油溶液)之注射间隔的建议是每 1-2 周一次。其中,尽管在技术层面上,两周的间隔对于这两种注射剂皆可行;但如此间隔显然会引起雌二醇水平的大幅波动,即峰值很高、谷值很低。而对于短效性的戊酸雌二醇,该现象尤其明显(见图十、图十一)。这种大幅波动可能产生一些未知效应;而要达到适宜的睾酮压制作用,则有赖于持续较高的雌二醇水平。考虑到以上事实,应当建议,为这些注射剂优先推荐采用每周一次的注射间隔。这样会让雌二醇水平更加稳定,减少可能因其偏高、或偏低而产生的问题(见图十一)。
|
||||
当然,对于戊酸雌二醇,可采用更短的注射间隔(每 5 天一次),以进一步降低雌二醇水平的变化幅度;而另一方面,对于长效型的环戊丙酸(或庚酸)雌二醇油溶液,可采用每 10 天至两周一次的注射间隔——这里假定这些间隔时间皆可较好地被人体接受,且睾酮仍被充分抑制。(见图十一)
|
||||
在选用不同注射间隔时,需要按间隔之长短来相应调整剂量之高低,以确保雌二醇总暴露量相当;例如,对于非聚合物类雌二醇酯,高剂量下:3.5 mg/五天、5 mg/七天、7 mg/十天、或 10 mg/十四天。
|
||||
|
||||
> ![figure][FIG_11]
|
||||
>
|
||||
> 【图十一】高剂量戊酸雌二醇/环戊丙酸雌二醇(油溶液)在不同注射间隔下产生的雌二醇水平的模拟结果。剂量已依间隔之长短而相应调整,以使雌二醇总暴露量相当。
|
||||
|
||||
前述对《跨性别护理指南》建议的雌二醇注射剂用量、间隔产生的担忧,引出了一个问题:这些建议用量是如何确立的?很遗憾,现有《指南》基本没有描述它们是如何得出这些用量建议的,也不常引用外部资料来支持之。需要注意,UCSF 版《指南》所推荐的用量与间隔,和 1960 年代末 Christian Hamburger 及 Harry Benjamin 在最早一部和跨性别者有关的医学课本上所建议的相比较,几乎完全一致<sup>([Hamburger & Benjamin, 1969][HB69])</sup>。后者的推荐剂量为:10-40 mg/两周(戊酸雌二醇),和 2-5 mg/两周(环戊丙酸雌二醇);不过其作者还补充,在 4-8 个月过后,可每隔四周注射相同剂量。这些用量建议很明显是在对血浆雌二醇的检测得到普及、现代药代动力学的研究出现之前制定的;因此,至少在这些《指南》上的用量建议,显然主要基于过往专家建议和长期历史惯例,而非药代动力学或临床数据。早期为达到更长的持续时间、更便利的注射间隔,可能在特定雌二醇注射剂(即戊酸雌二醇)上采用了很高的剂量;但显然,当时尚未产生对过大的雌激素暴露量导致的风险(如血栓)的认知,而这些剂量也许从未经过修订。
|
||||
之所以针对女性倾向跨性别者的注射用雌二醇推荐用量长期保持不变,可能是因为:1. 相比于其它雌二醇形态,注射雌二醇并不常用;2. 不少医师使用它们时,只会测量雌二醇水平的谷值。需要提及的是:该谷值仅代表雌二醇注射剂所产生的曲线的最低点,其会相当程度地误导对平均、总和雌二醇暴露量的认识。无论如何,关于由当下为女性倾向跨性别者推荐的雌二醇注射剂用量,所造成的超高雌二醇水平,文献上已经有所察觉<sup>(例如 [Gooren, 2005][G05]; [Spack, 2013][S13]; [Deutsch, 2014][D14]; [Chantrapanichkul et al., 2021][C21]; [Glintborg et al., 2021][G21]; [Tassinari & Maranghi, 2021][TM21])</sup>。
|
||||
|
||||
在所有已被调查的跨性别激素治疗指南中,只有 UCSF 版《指南》<sup>(Deutsch, 2016b)</sup>和舍邦健康/安大略彩虹健康项目版《指南》<sup>([Bourns, 2019][B19])</sup>在其有关注射用雌二醇的讨论中引用了药代动力学文献。这些文献包括:[Düsterberg & Nishino (1982)][DN82];[Sierra-Ramírez 等人 (2011)][SR11];以及 [Thurman 等人 (2013)][T13]。看到一些《指南》谈到注射剂时会考虑已发表的药代动力学数据,值得赞赏;不过关于其引用的研究项目,有几点存在担忧。
|
||||
Düsterberg & Nishino (1982) 在其对注射用戊酸雌二醇的研究中,仅有极小规模的样本数(2 人次);其雌二醇水平结果因异常偏高,而被本次荟萃分析所排除。此外,该项目的发现并未在 UCSF 版《指南》的剂量建议中得到引用,因为一旦引用之,其建议剂量势必大幅减少;而另一方面,舍邦健康版《指南》引用了该项目,并将戊酸雌二醇的推荐剂量定为 3-4 mg/周或 6-8 mg/两周——这些剂量比其它《跨性别护理指南》所推荐的都要低,而根据本次荟萃分析,显然该剂量更适合女性倾向跨性别者使用。
|
||||
至于 Sierra-Ramírez 等人 (2011) 和 Thurman 等人 (2013) 的项目,尽管从质量而言优于 Düsterberg & Nishino (1982),但其描述的是环戊丙酸雌二醇 *<u>水悬浮液</u>*,而非其 *<u>油溶液</u>*。一般在女性化激素治疗当中使用的,都是其油溶液;而此二者之间存在很大不同,有关其水悬浮液的药代动力学研究不一定能推广到其油溶液。不过,无论如何,此二者的确可产生相似的雌二醇水平,因此其剂量应该是相当的。
|
||||
|
||||
本次荟萃分析只是一项非正式的、未公开发表的研究。此外,基于本次分析的结果以及前述讨论,当下大多数《跨性别临床指南》推荐的雌二醇注射剂之剂量显然高度过量、也不大安全,而且注射间隔显得过大。将来在雌二醇注射剂方面,《跨性别护理指南》应考虑对其用量建议重新进行评估;而跨性别医学界则应努力改善对其药代动力学、和针对女性倾向跨性别者的最佳使用方案的描述。鉴于今后短期内有关这些注射剂的临床数据都会很少,他们还可考虑引入已发表的药代动力学数据,以指导注射用雌二醇的剂量建议。在有关女性倾向跨性别者使用雌二醇注射剂的方面,有大量可更好地丰富《跨性别护理指南》信息的现成数据——正如本次荟萃分析所发现和收录的那样。
|
||||
|
||||
## 可交互的雌二醇注射剂模拟器网页
|
||||
|
||||
本次针对使用雌二醇注射剂后的雌二醇浓度—时间关系数据的非正式荟萃分析,是为了获得准确而典型的雌二醇水平曲线,并整合到一个基于网页的注射用雌二醇模拟器当中,供女性倾向跨性别者及其医师使用。该网页可模拟这些注射剂被单次注射和多次重复注射后的曲线。有关该模拟器的说明页,可于此处查阅:
|
||||
|
||||
- [An Interactive Web Simulator for Estradiol Levels with Injectable Estradiol Esters (Aly W., 2021)][ALYW21]
|
||||
|
||||
该模拟器本身可于此处访问:
|
||||
|
||||
- [Injectable Estradiol Simulator - Transfeminine Science][WEB_1A]
|
||||
|
||||
## 未来展望
|
||||
|
||||
本次项目将来还可能做进一步的工作。例如,本次荟萃分析可能将纳入对使用雌二醇注射剂的个体之间雌二醇水平的差异之评估;再例如,将本次荟萃分析(以及模拟器)延伸至其它激素类制剂,诸如睾酮注射剂以及其它雌二醇形态/路径(口服、舌下含服、小球)等等,应该相当容易,也具有价值。本文作者已经收集到其中部分制剂的药代动力学文献。不过,要完成这些,还需大量时间和精力。
|
||||
|
||||
## 特别鸣谢
|
||||
|
||||
这里要非常感谢 Violet 和 Lila;在本次项目的工作中,他们对于建模的数据导入和建议都是不可或缺的。此外,还要感谢 Violet 导出了为本次工作所用的特殊三室药代动力学模型。另外,不妨了解下 Violet 的个人项目 [Tilia][WEB_8A] 与 [TransKit][WEB_8B] ——前者提供的工具可助力跨性别者管理ta们的激素转变过程;后者则是为跨性别激素治疗量身打造的药代动力学模拟库,目前仍在制作中。最后,要感谢在本文发表前认真审议本文的所有审稿人。
|
||||
|
||||
## 辅助阅读材料
|
||||
|
||||
- [有关注射用雌二醇的研究项目,及雌二醇水平 - Google 表格][WEB_31A]
|
||||
- [基于可交互网页的 Violet 三室模型曲线拟合器][WEB_9A]
|
||||
- [注射用雌二醇的溶剂,及其成分与特性 - Google 文档][TABLE_51B]
|
||||
- [性激素酯的亲脂性 (Log P) 汇总表格 - Google 文档][TABLE_52C]
|
||||
|
||||
## 参考文献
|
||||
略
|
||||
|
||||
<!-- 第一章:前言 -->
|
||||
[E59]: https://doi.org/10.1111/j.2042-7158.1959.tb10412.x
|
||||
[V19]: https://doi.org/10.1007/978-981-13-3642-3_7
|
||||
[G21]: https://doi.org/10.1530/EJE-21-0059
|
||||
[ALYW19_AQUA]: https://transfemscience.org/articles/aqueous-suspensions/
|
||||
[D16a]: https://transcare.ucsf.edu/guidelines
|
||||
[H17]: https://doi.org/10.1210/jc.2017-01658
|
||||
[K86]: https://pubmed.ncbi.nlm.nih.gov/3817596/
|
||||
[K90]: https://doi.org/10.1016/0378-5122(90)90003-O
|
||||
[G84]: https://doi.org/10.1016/0306-4530(84)90004-0
|
||||
[H99]: https://doi.org/10.1002/(SICI)1097-0045(19990701)40:2%3C76::AID-PROS2%3E3.0.CO;2-Q
|
||||
[JG00]: https://doi.org/10.1002/1097-0045(20000615)44:1%3C26::AID-PROS4%3E3.0.CO;2-P
|
||||
[BON90]: https://doi.org/10.1007/978-3-662-00814-0_6
|
||||
[BN98]: https://doi.org/10.1007/978-3-642-72185-4_11
|
||||
[B04]: https://doi.org/10.1017/CBO9780511545221.015
|
||||
[NB10]: https://doi.org/10.1007/978-3-540-78355-8_21
|
||||
[NB12]: https://doi.org/10.1017/CBO9781139003353.016
|
||||
|
||||
[TABLE_1A]: https://en.wikipedia.org/wiki/Template:Structural_properties_of_selected_estradiol_esters
|
||||
[TABLE_1B]: https://en.wikipedia.org/w/index.php?title=Template:Potencies_and_durations_of_natural_estrogens_by_intramuscular_injection&oldid=964345939
|
||||
[TABLE_1C]: https://imgur.com/a/ef7b33G
|
||||
|
||||
[WEB_1A]: https://transfemscience.org/misc/injectable-e2-simulator/
|
||||
|
||||
<!-- 第二章:研究方法 -->
|
||||
[Z10]: https://doi.org/10.1016/j.cmpb.2010.01.007
|
||||
[COLB81]: https://doi.org/10.1007/bf01059272
|
||||
[W93]: https://books.google.com/books?id=gMuCDwAAQBAJ
|
||||
[FS07]: https://web.archive.org/web/20210717084442if_/https://wiki.ucl.ac.uk/download/attachments/23206987/Shafer%20NONMEM.pdf
|
||||
[L08]: http://mlxtran.lixoft.com/wp-content/uploads/sites/2/2016/02/PKPDlibrary.pdf
|
||||
[AFU15]: https://doi.org/10.1016/j.vascn.2015.03.004
|
||||
[C20]: https://onlinehelp.certara.com/phoenix/8.3/topics/pkmodelcalc.htm
|
||||
|
||||
[WEB_2A]: https://automeris.io/WebPlotDigitizer/
|
||||
[WEB_2B]: https://lmfit.github.io/lmfit-py/
|
||||
|
||||
<!-- 第三章:分析结果 -->
|
||||
|
||||
[WEB_30A]: https://www.desmos.com/calculator/ndgvp2avhj
|
||||
[WEB_30B]: https://alyw234237.github.io/v3c-fitter/
|
||||
|
||||
[G75]: https://www.worldcat.org/title/untersuchungen-zur-pharmakokinetik-von-ostradiol-17-beta-ostradiol-benzoat-ostradiol-valerianat-und-ostradiol-undezylat-bei-der-frau-der-verlauf-der-konzentrationen-von-ostradiol-17-beta-ostron-lh-und-fsh-im-serum/oclc/311708827
|
||||
[L75]: https://pubmed.ncbi.nlm.nih.gov/1150068/
|
||||
[KL75]: https://doi.org/10.1210/jcem-41-6-1003
|
||||
[S75]: https://doi.org/10.1111/j.1365-2265.1975.tb01534.x
|
||||
[SBL75]: https://doi.org/10.1111/j.1365-2265.1975.tb01537.x
|
||||
[L76]: https://doi.org/10.1007/BF00667679
|
||||
[C78]: https://doi.org/10.1016/S0015-0282(16)43271-1
|
||||
[S78]: https://doi.org/10.1016/S0300-595X(78)80008-5
|
||||
[T78]: https://doi.org/10.1007/BF03346769
|
||||
[T79]: https://doi.org/10.1007/BF03349341
|
||||
[O80]: https://doi.org/10.1016/S0010-7824(80)80018-7
|
||||
[C81]: https://doi.org/10.1016/0020-7292(81)90043-6
|
||||
[W81]: https://doi.org/10.1016/S0140-6736(81)92571-X
|
||||
[S82]: https://doi.org/10.1210/jcem-54-4-745
|
||||
[BWL83]: https://doi.org/10.1016/S0015-0282(16)47174-8
|
||||
[K84]: https://doi.org/10.1007/BF00570759
|
||||
[V84]: https://doi.org/10.1210/jcem-59-1-133
|
||||
[G85]: https://doi.org/10.1007/BF01541659
|
||||
[A86]: https://doi.org/10.1507/endocrine1927.62.5_662
|
||||
[C86]: https://doi.org/10.1016/0028-2243(86)90125-5
|
||||
[MT87a]: https://doi.org/10.1111/j.1365-2265.1987.tb01173.x
|
||||
[MT87b]: https://doi.org/10.1530/jrf.0.0790549
|
||||
[S87]: https://doi.org/10.1507/endocrine1927.63.10_1289
|
||||
[B89]: https://doi.org/10.1016/S0015-0282(16)60602-7
|
||||
[V93]: https://pubmed.ncbi.nlm.nih.gov/8506068/
|
||||
[E06]: https://doi.org/10.1016/j.psyneuen.2005.10.004
|
||||
[A74]: https://doi.org/10.1111/j.1471-0528.1974.tb00383.x
|
||||
[WNG76]: https://journals.lww.com/greenjournal/abstract/1976/04000/induction_of_an_lh_surge_with_estradiol_benzoate_.6.aspx
|
||||
[VC57]: https://pubmed.ncbi.nlm.nih.gov/13547587/
|
||||
[IP65]: https://docs.google.com/document/d/18BUGz-BuVOjc3eODsha5yWodifabu-uRuhxEUxUu7Go/view
|
||||
|
||||
[FIG_1]: https://transfemscience.org/assets/images/injectable-e2/eb_v3c.svg
|
||||
[TABLE_31A]: https://imgur.com/a/62NBGrw
|
||||
[WEB_31A]: https://docs.google.com/spreadsheets/d/108SmQhbk_gmG22WBvEcGs4tkT43AzwSBfrgPfDjlePk/view#gid=1819977282
|
||||
[WEB_31B]: https://chart-studio.plotly.com/~transfemscience/1/#/
|
||||
|
||||
[S71]: https://unsworks.unsw.edu.au/fapi/datastream/unsworks:65652/SOURCE01?view=true#page=167
|
||||
[S72a]: https://doi.org/10.1212/WNL.22.4.355
|
||||
[S72b]: https://doi.org/10.1111/j.1526-4610.1972.hed1203093.x
|
||||
[S72c]: https://doi.org/10.5694/j.1326-5377.1972.tb93039.x
|
||||
[SOMER75]: https://doi.org/10.1212/wnl.25.3.239
|
||||
[V75]: https://doi.org/10.1080/17843286.1975.11716973
|
||||
[R80]: https://doi.org/10.1016/0378-5122(80)90060-2
|
||||
[RPG81]: https://doi.org/10.1016/0378-5122(81)90010-4
|
||||
[BBP82]: https://doi.org/10.1016/S0015-0282(16)46042-5
|
||||
[DW83]: https://doi.org/10.1159/000179680
|
||||
[A85]: https://doi.org/10.1016/0010-7824(85)90081-2
|
||||
[DN82]: https://doi.org/10.1016/0378-5122(82)90064-0
|
||||
[DSH85]: https://doi.org/10.1159/000180039
|
||||
[R87]: https://doi.org/10.1007/BF00544558
|
||||
[SANG87]: https://doi.org/10.13699/j.cnki.1001-6821.1987.01.002
|
||||
[SHERW87]: https://doi.org/10.1016/0002-9378(87)90295-X
|
||||
[SHERW88]: https://doi.org/10.1016/0165-0327(88)90061-4
|
||||
[GR88]: https://doi.org/10.3109/09513598809023624
|
||||
[GR90]: https://doi.org/10.1007/BF02442351
|
||||
[GF94]: https://doi.org/10.1016/0010-7824(94)90032-9
|
||||
[J94]: https://doi.org/10.1210/jcem.79.6.7527406
|
||||
[GL98]: https://doi.org/10.1159/000023266
|
||||
[G02]: https://www.kup.at/journals/summary/1071.html
|
||||
[K06]: https://www.nel.edu/short-term-changes-in-melatonin-and-cortisol-serum-levels-after-a-single-administration-of-estrogen-to-menopausal-women-1766/
|
||||
[VA11]: https://repositoriodigital.ipn.mx/handle/123456789/12490
|
||||
[SDB12]: https://doi.org/10.5414/cp201589
|
||||
[I96]: https://www.worldcat.org/oclc/722383126
|
||||
[GA77]: https://doi.org/10.1016/0002-9378(77)90026-6
|
||||
|
||||
[FIG_2]: https://transfemscience.org/assets/images/injectable-e2/ev_v3c.svg
|
||||
[TABLE_32A]: https://imgur.com/a/62NBGrw
|
||||
[WEB_32A]: https://docs.google.com/spreadsheets/d/108SmQhbk_gmG22WBvEcGs4tkT43AzwSBfrgPfDjlePk/view#gid=0
|
||||
[WEB_32B]: https://chart-studio.plotly.com/~transfemscience/17/#/
|
||||
|
||||
[R73]: https://doi.org/10.1210/jcem-37-4-574
|
||||
[RF74]: https://doi.org/10.1016/S0022-3476(74)80355-0
|
||||
[B80]: https://doi.org/10.1016/0026-0495(80)90117-1
|
||||
[L96]: https://doi.org/10.1046/j.1526-4610.1996.3606367.x
|
||||
|
||||
[FIG_3]: https://transfemscience.org/assets/images/injectable-e2/ec_oil_v3c.svg
|
||||
[WEB_33A]: https://docs.google.com/spreadsheets/d/108SmQhbk_gmG22WBvEcGs4tkT43AzwSBfrgPfDjlePk/view#gid=675753324
|
||||
[WEB_33B]: https://chart-studio.plotly.com/~transfemscience/5/#/
|
||||
|
||||
[F82]: https://doi.org/10.1016/0010-7824(82)90049-X
|
||||
[GF87]: https://doi.org/10.1016/0010-7824(87)90093-X
|
||||
[Z98]: https://doi.org/10.1016/S0010-7824(98)00048-1
|
||||
[RR99]: https://doi.org/10.1016/s0010-7824(99)00081-5
|
||||
[SR11]: https://doi.org/10.1016/j.contraception.2011.03.014
|
||||
[T13]: https://doi.org/10.1016/j.contraception.2012.11.010
|
||||
[M19]: https://doi.org/10.1016/j.jpba.2019.03.053
|
||||
|
||||
[FIG_4]: https://transfemscience.org/assets/images/injectable-e2/ec_susp_v3c.svg
|
||||
[TABLE_34A]: https://commons.wikimedia.org/wiki/File:Estradiol_levels_after_a_single_subcutaneous_or_intramuscular_injection_of_5_mg_estradiol_cypionate.png
|
||||
[TABLE_34B]: https://commons.wikimedia.org/wiki/File:Estradiol_cypionate_levels_after_a_single_intramuscular_injection_of_5_mg_microcrystalline_estradiol_cypionate_in_aqueous_suspension_in_women.png
|
||||
[WEB_34A]: https://docs.google.com/spreadsheets/d/108SmQhbk_gmG22WBvEcGs4tkT43AzwSBfrgPfDjlePk/view#gid=1561713713
|
||||
[WEB_34B]: https://chart-studio.plotly.com/~transfemscience/7/#/
|
||||
|
||||
[R86]: https://doi.org/10.1016/0010-7824(86)90046-6
|
||||
[W86]: https://pubmed.ncbi.nlm.nih.gov/3814225/
|
||||
[W87]: https://pesquisa.bvsalud.org/portal/resource/en/lil-42873
|
||||
[S88]: https://doi.org/10.1016/0010-7824(88)90005-4
|
||||
[GF89]: https://doi.org/10.1016/0010-7824(89)90107-8
|
||||
[M95]: https://doi.org/10.1007/BF02436100
|
||||
|
||||
[FIG_5]: https://transfemscience.org/assets/images/injectable-e2/een_v3c.svg
|
||||
[WEB_35A]: https://docs.google.com/spreadsheets/d/108SmQhbk_gmG22WBvEcGs4tkT43AzwSBfrgPfDjlePk/view#gid=1683725929
|
||||
[WEB_35B]: https://chart-studio.plotly.com/~transfemscience/9/#/
|
||||
|
||||
[GEPP75]: https://www.worldcat.org/oclc/632312599
|
||||
[JA79]: https://doi.org/10.1159/000280272
|
||||
[J80]: https://doi.org/10.1111/j.1464-410X.1980.tb02961.x
|
||||
[D81]: https://www.worldcat.org/oclc/774239518
|
||||
[V77]: https://scholar.google.com/scholar?cluster=5963522046259984312
|
||||
|
||||
[FIG_6]: https://transfemscience.org/assets/images/injectable-e2/eu_v3c.svg
|
||||
[TABLE_36A]: https://commons.wikimedia.org/wiki/File:Estradiol_levels_after_injections_of_estradiol,_estradiol_benzoate,_estradiol_valerate,_and_estradiol_undecylate_in_women.png
|
||||
[TABLE_36B]: https://commons.wikimedia.org/wiki/File:Estradiol_levels_after_a_single_intramuscular_injection_of_10_mg_estradiol_valerate_and_100_mg_estradiol_undecylate.png
|
||||
[TABLE_36C]: https://imgur.com/a/ZYgpTsh
|
||||
[WEB_36A]: https://docs.google.com/spreadsheets/d/108SmQhbk_gmG22WBvEcGs4tkT43AzwSBfrgPfDjlePk/view#gid=467757621
|
||||
[WEB_36B]: https://chart-studio.plotly.com/~transfemscience/11/#/
|
||||
|
||||
[J76]: https://doi.org/10.1016/S0083-6729(08)60965-6
|
||||
[L79]: https://pubmed.ncbi.nlm.nih.gov/571863/
|
||||
[L80]: https://doi.org/10.1016/0022-4731(80)90225-3
|
||||
[J82]: https://scholar.google.com/scholar?cluster=5512908264284113489
|
||||
[N87]: https://doi.org/10.1159/000472772
|
||||
[GN88]: https://doi.org/10.1002/pros.2990130405
|
||||
[STEGE88]: https://doi.org/10.1097/00000421-198801102-00024
|
||||
[STEGE89]: https://doi.org/10.1002/pros.2990140211
|
||||
[STEGE96]: https://doi.org/10.1002/(SICI)1097-0045(199605)28:5%3C307::AID-PROS6%3E3.0.CO;2-8
|
||||
|
||||
[FIG_7]: https://transfemscience.org/assets/images/injectable-e2/pep_v3c.svg
|
||||
[WEB_37A]: https://docs.google.com/spreadsheets/d/108SmQhbk_gmG22WBvEcGs4tkT43AzwSBfrgPfDjlePk/view#gid=1263215142
|
||||
[WEB_37B]: https://chart-studio.plotly.com/~transfemscience/13/#/
|
||||
|
||||
[FIG_8]: https://transfemscience.org/assets/images/injectable-e2/all_v3c.svg
|
||||
[FIG_8_ALT]: https://transfemscience.org/assets/images/injectable-e2/all_v3c_no_eb.svg
|
||||
[FIG_9]: https://transfemscience.org/assets/images/injectable-e2/all_v3c_repeated.svg
|
||||
[FIG_9_ALT]: https://transfemscience.org/assets/images/injectable-e2/all_v3c_repeated_no_eb.svg
|
||||
|
||||
[TB04]: https://doi.org/10.1111/j.1365-2885.2004.00600.x
|
||||
[Y11]: https://doi.org/10.4155/tde.11.19
|
||||
|
||||
<!-- 第四章:讨论 -->
|
||||
|
||||
[RRH99]: https://doi.org/10.1016/S0010-7824(99)00086-4
|
||||
[SINKULA78]: https://scholar.google.com/scholar?cluster=12842077211931556704
|
||||
[CHIEN81]: https://journal.pda.org/content/35/3/106.short
|
||||
[M97]: https://jpet.aspetjournals.org/content/281/1/93.short
|
||||
[LL09]: https://doi.org/10.1208/s12248-009-9153-9
|
||||
[L09]: https://doi.org/10.1517/17425240903307431
|
||||
[F10]: https://books.google.com/books?id=5wcyP2OBPhoC&pg=PA80
|
||||
[LTL12]: https://doi.org/10.1007/978-1-4614-0554-2_7
|
||||
[K17]: https://dspace.library.uu.nl/handle/1874/348465
|
||||
[SA79]: https://doi.org/10.1111/j.1600-0773.1979.tb02404.x
|
||||
[S98]: https://doi.org/10.1016/S0378-5173(98)00121-5
|
||||
[L01]: https://doi.org/10.1016/S0378-5173(01)00860-2
|
||||
[B78]: https://scholar.google.com/scholar?cluster=7643602853178335452
|
||||
[B78_EXCERPT]: https://imgur.com/a/XXQEw8O
|
||||
[KHL85]: https://doi.org/10.1111/j.1600-0447.1985.tb08535.x
|
||||
[KSV16]: https://doi.org/10.1016/j.ejps.2015.12.011
|
||||
|
||||
[TABLE_51A]: https://commons.wikimedia.org/wiki/File:Estradiol_levels_after_a_single_5_mg_intramuscular_injection_of_estradiol_esters.png
|
||||
[TABLE_51B]: https://docs.google.com/document/d/1XJRvPikYmJtxcjBV3ssK3C5v-N6gFrQXCIIVz1amK8o/view#bookmark=id.4o16xc1yn2yk
|
||||
|
||||
[WIKI_51A]: https://en.wikipedia.org/wiki/Estrogen_provocation_test
|
||||
|
||||
[SBN80]: https://doi.org/10.1016/S0015-0282(16)44543-7
|
||||
[S07]: https://doi.org/10.1007/978-0-387-49785-3_9
|
||||
[SMM18]: https://doi.org/10.1201/b22448-9
|
||||
[E83]: https://doi.org/10.1016/0039-128x(83)90109-5
|
||||
|
||||
[TABLE_52A]: https://commons.wikimedia.org/wiki/File:Idealized_curves_of_estradiol_levels_after_injection_of_different_estradiol_esters_in_women.png
|
||||
[TABLE_52B]: https://imgur.com/a/15LxI3o
|
||||
[TABLE_52C]: https://docs.google.com/document/d/1nidcOcLjt4jIRUMv3rPgyrY_3zUz8Oa0B_noWnGPm4Q/view
|
||||
[TABLE_52D]: https://en.wikipedia.org/wiki/Medroxyprogesterone_acetate#Time%E2%80%93concentration_curves
|
||||
[WEB_52A]: http://www.vcclab.org/lab/alogps/
|
||||
[WEB_52B]: https://docs.chemaxon.com/display/docs/logp-plugin.md
|
||||
[WEB_52C]: http://www.sioc-ccbg.ac.cn/skins/ccbgwebsite/software/xlogp3/
|
||||
[WEB_52D]: https://www.accessdata.fda.gov/drugsatfda_docs/label/2005/085470s015lbl.pdf
|
||||
[WIKI_52A]: https://en.wikipedia.org/wiki/Octanol-water_partition_coefficient
|
||||
|
||||
[ALYW19_INTRO_N]: https://transfemscience.org/articles/transfem-intro/#normal-hormone-levels
|
||||
[SG94]: https://doi.org/10.1016/0010-7824(94)90030-2
|
||||
[ALYW20_CLOT]: https://transfemscience.org/articles/estrogens-blood-clots/
|
||||
[P37]: https://doi.org/10.1042/bj0310579
|
||||
[BLD53]: https://doi.org/10.1016/S0015-0282(16)31145-1
|
||||
|
||||
[WEB_53A]: https://web.archive.org/web/20180102072958/http://pharmanovia.com/product/estradurin/
|
||||
[WIKI_53A]: https://en.wikipedia.org/wiki/Polyestradiol_phosphate#Medical_uses
|
||||
|
||||
[K05]: https://doi.org/10.1080/13697130500148875
|
||||
|
||||
[TABLE_54A]: https://imgur.com/a/qhDYTKX
|
||||
[TABLE_54B]: https://imgur.com/a/NcmDDLV
|
||||
[TABLE_54C]: https://imgur.com/a/nmkQhzV
|
||||
[TABLE_54D]: https://imgur.com/qR2C2Zj
|
||||
[TABLE_54E]: https://imgur.com/a/lh5Hpto
|
||||
[WIKI_54A]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol
|
||||
|
||||
[ALYW20_GUIDE]: https://transfemscience.org/articles/transfem-hormone-guidelines/
|
||||
[D16b]: https://transcare.ucsf.edu/guidelines/feminizing-hormone-therapy
|
||||
[OK16]: https://transcare.ucsf.edu/guidelines/youth
|
||||
[C15]: https://www.lgbtqiahealtheducation.org/publication/transgender-sod/
|
||||
[C15_NEW]: https://www.lgbtqiahealtheducation.org/publication/medical-care-of-trans-and-gender-diverse-adults-2021/
|
||||
[CL18]: https://callen-lorde.org/transhealth/
|
||||
[D13]: https://www.sfdph.org/dph/comupg/oservices/medSvs/hlthCtrs/TransGendprotocols122006.pdf
|
||||
[B19]: https://www.rainbowhealthontario.ca/product/4th-edition-sherbournes-guidelines-for-gender-affirming-primary-care-with-trans-and-non-binary-patients/
|
||||
[TCB21]: http://www.phsa.ca/transcarebc/Documents/HealthProf/Primary-Care-Toolkit.pdf
|
||||
[D15]: http://www.phsa.ca/transcarebc/Documents/HealthProf/BC-Trans-Adult-Endocrine-Guidelines-2015.pdf
|
||||
[T20]: https://doi.org/10.1016/j.jsxm.2020.01.012
|
||||
[T19]: https://transline.zendesk.com/hc/en-us/articles/229373288-TransLine-Hormone-Therapy-Prescriber-Guidelines
|
||||
[ALYW20_DOSE]: https://transfemscience.org/articles/e2-equivalent-doses/
|
||||
[ALYW19_INTRO_G]: https://transfemscience.org/articles/transfem-intro/#gonadal-suppression
|
||||
[L21]: https://doi.org/10.1016/S0140-6736(21)00100-8
|
||||
[NAH94]: https://doi.org/10.3109/01443619409027641
|
||||
[SANG94]: https://doi.org/10.1016/0010-7824(94)90033-7
|
||||
[T94]: https://doi.org/10.1016/0010-7824(94)90029-9
|
||||
[HB69]: https://scholar.google.com/scholar?cluster=17287240145299798098
|
||||
[G05]: https://doi.org/10.1159/000087751
|
||||
[S13]: https://doi.org/10.1001/jama.2012.165234
|
||||
[D14]: https://books.google.com/books?id=EuB_AwAAQBAJ&pg=PA241
|
||||
[C21]: https://doi.org/10.4158/EP-2020-0414
|
||||
[TM21]: https://doi.org/10.3390/ijerph182312640
|
||||
|
||||
[FIG_10]: https://transfemscience.org/assets/images/injectable-e2/ev_guidelines.svg
|
||||
[FIG_10_ALT]: https://transfemscience.org/assets/images/injectable-e2/ev_guidelines_weekly.svg
|
||||
[FIG_11]: https://transfemscience.org/assets/images/injectable-e2/ev_ec_intervals.svg
|
||||
[TABLE_55A]: https://en.wikipedia.org/wiki/Template:Target_ranges_for_hormone_levels_in_hormone_therapy_for_transgender_women
|
||||
[TABLE_55B]: https://transfemscience.org/assets/images/injectable-e2/ev_better_doses.svg
|
||||
|
||||
<!-- 第六章:模拟器网页 -->
|
||||
[ALYW21]: https://transfemscience.org/articles/injectable-e2-simulator-release/
|
||||
|
||||
<!-- 第八和第九章:鸣谢、阅读材料 -->
|
||||
[WEB_8A]: https://github.com/tiliaqt/
|
||||
[WEB_8B]: https://github.com/tiliaqt/transkit/
|
||||
[WEB_9A]: https://alyw234237.github.io/v3c-fitter/
|
||||
|
|
@ -1,155 +0,0 @@
|
|||
# 舌下含服雌二醇及口服醋酸甲羟孕酮在女性倾向跨性别者中的应用(基于 Jain 等人的研究)
|
||||
|
||||
作者 [Aly W.](https://transfemscience.org/articles-by-author/aly-w/)
|
||||
|
||||
首次发表于 2019 年 6 月 15 日
|
||||
|
||||
最后修改于 2020 年 11 月 21 日
|
||||
|
||||
译者 [Sue-e89893](https://github.com/Sue-e89893)
|
||||
|
||||
翻译于 2021 年 9 月 26 日
|
||||
|
||||
注意: 本页 [最初是作为 Reddit 上 r/MtFHRT 的一个主题发布的](https://transfemscience.org/articles/announcement/),自从被转移到 Transfeminine Science 后,尚未进行适当或全面的修订。
|
||||
|
||||
## 介绍
|
||||
|
||||
Jain 和同事们在 2019 年 4 月末刊登了一篇关于跨性别女性舌下含服雌二醇合并使用或不合并使用醋酸甲羟孕酮(MPA)的研究:
|
||||
|
||||
- Jain, J., Kwan, D., & Forcier, M. (2019). Medroxyprogesterone Acetate in Gender-Affirming Therapy for Transwomen: Results from a Retrospective Study. The Journal of Clinical Endocrinology & Metabolism, jc.2018-02253. [DOI:[10.1210/jc.2018-02253][2]]
|
||||
|
||||
[2]: https://doi.org/10.1210/jc.2018-02253
|
||||
|
||||
这篇研究至关重要,不仅因为这是第一篇系统性地评估 MPA 在跨性别女性中的作用,而且,就我所知,这还是第一篇评定跨性别女性舌下含服雌二醇对睾酮水平的抑制作用。[编辑/更新:这实际上并不正确;[见下][3]] 这意味着,它能让我们知道,舌下含服雌二醇对睾酮的抑制效果,而且是在**很大**的雌二剂量范围内(见下)。
|
||||
|
||||
[3]: https://
|
||||
|
||||
## 研究概要
|
||||
|
||||
### 方法
|
||||
|
||||
这项研究对比了两组的雌二醇、睾酮和泌乳素水平及各种其他生化项目,一些自我报告的期望效果和不良反应:
|
||||
|
||||
1. 跨性别女性使用 2–12mg/天舌下含服雌二醇,100–200mg/天口服螺内脂。
|
||||
2. 跨性别女性使用 2–12mg/天舌下含服雌二醇,100–200mg/天口服螺内脂及 5–10mg/天舌下含服 MPA 或 150mg/3 月肌注 MPA。
|
||||
|
||||
雌二醇水平维持在 100 至 350pg/mL 的范围内,如果雌二醇水平稳定在 350pg/mL 以上,则减少舌下含服雌二醇的剂量。可惜,未给出何时、怎样测出雌二醇的水平这些细节。[编辑/更新:“取决于患者”,每天舌下含服一次或两次雌二醇;与作者私聊得知]患者依自己的喜好添加 MPA。
|
||||
|
||||
至于研究的设计和受试者,这项研究是对共 92 名跨性别女性 290 次随访的回顾性分析。在这 290 次随访中,102 次是服用 MPA 的(其中的 39 名患者),188 次未服用 MPA(其中的 53 名患者)。
|
||||
|
||||
### 结果
|
||||
|
||||
不出意料,这项研究在服用 MPA 的患者与未服用 MPA 的患者中未见雌二醇水平的差异(211pg/mL vs. 210pg/mL)。与此相反,他们注意到了,相比于不服用 MPA,服用 MPA 的患者的睾酮水平显著降低了(79ng/dL vs. 215ng/dL;降低 63%)。在两者中,未见泌乳素水平的差异。此外,这项研究还发现,在服用 MPA 的患者与未服用 MPA 的患者中,其他生化参数的差异很小。
|
||||
|
||||
在服用 MPA 的 39 名跨性别女性中,26 人(67%)报告了服用 MPA 后胸部发育得更好了,11 人(28%)报告了服用 MPA 后面部的毛发减少了,5 人(13%)报告了情绪波动。一名患者因情绪波动而停用 MPA。服用 MPA 后,未见血栓,心血管疾病,泌乳素瘤,溢乳、胆石症、乳腺癌或糖尿病。
|
||||
|
||||
### 讨论
|
||||
|
||||
作者总结道,他们发现了极少的副作用,雌二醇水平不变,睾酮水平降低以及其他与 MPA 相关的生化参数变化很小。
|
||||
|
||||
不过,作者强调,仍需进一步的研究来全面地评估 MPA 在跨性别女性中的作用。他们还做出如下声明:
|
||||
|
||||
> 跨性别群体将会受益于对 MPA 的更深入的研究[…]此外,MPA 和天然孕激素(prometrium)的对比研究也是必要的。因为 MPA 与天然孕激素的相对风险和益处在性别肯定激素治疗中尚不明确,而现有的临床建议很大程度上基于患者的偏好和/或轶事证据。那样,跨性别群体才会受益于如上所描述的未来的研究。[…]未来的研究应当确实我们的发现,系统地评价 MPA 的安全性,进一步研究 MPA 在跨性别人群中的作用。
|
||||
|
||||
## 评注
|
||||
|
||||
如前文所述,就我所知,这是第一篇评定舌下含服雌二醇对睾酮的抑制作用的研究。不仅如此,它在大范围的舌下含服雌二醇剂量(2-12)下评估了这种效果。
|
||||
|
||||
可惜,在论文的相关数据表中,研究者们并未列出在不同的舌下含服雌二醇的剂量下雌二醇和睾酮的平均值。而且,由于缺少数据,他们选择在相关图表中表现睾酮水平与雌二醇水平的相关性,而不是与舌下含服雌二醇的剂量的相关性(见下图)。所以,不同剂量的舌下含服雌二醇的作用不能轻易地弄明白。我已经发邮件给首要研究者,询问每一雌二醇剂量下平均的雌二醇/睾酮水平,正等待回信中。尽管需要费点功夫,手动地从论文的图表里提取这些信息也是可行的(类似于我之前做的——[Aly W., 2019][4])。(当我干完这事时,我会更新这篇文章。编辑/更新:我做完了。见下图/表)
|
||||
|
||||
[4]: https://transfemscience.org/articles/oral-e2-leinung-2018/
|
||||
|
||||
不管怎样,考虑到这项研究中用到的舌下含服雌二醇的剂量(2 到 12mg/天)以及合理且宽泛的雌二醇水平的容许范围(100 到 350pg/mL),未服用 MPA 的跨性别女性的睾酮水平居然惊人的高(215ng/dL)。虽然需要更多的分析来弄明白到底发生了什么,这显然对舌下含服雌二醇单药治疗对睾酮水平的抑制来讲并不是好消息。编辑/更新:分析完了,见下。
|
||||
|
||||
这项研究也评估了 5 到 10mg/天的舌下含服 MPA(也有 150mg/3 月的肌注 MPA)在跨性别女性中的作用。由于 MPA 有 100%的口服生物利用度,我们预计 5 到 10mg/天的口服 MPA 与 5 到 10mg/天的舌下含服 MPA 有着相同的效果。这项研究发现,使用相对低剂量的 MPA 和舌下含服雌二醇能很大程度地降低睾酮水平(-63%;215ng/dL 降至 79ng/dL)。
|
||||
|
||||
研究者们表示,67%的服用 MPA 的跨性别女性自我报告了胸部发育得更好了。然而,考虑到这些报告的主观性/逸闻性而非客观的测量,我们应当对这一发现抱有怀疑。如我在别处讨论过的那样,没有证据表明孕激素对胸部尺寸和形状的发育有正真的好处,同时,有理由认为孕激素没有这样的效果([Aly W., 2019][5];[Aly W., 2018][6];[Wiki][7])。
|
||||
|
||||
[5]: https://transfemscience.org/articles/p4-prior-review-fact-check/
|
||||
[6]: https://www.reddit.com/r/MtFHRT/comments/94naq0/oral_progesterone_achieves_very_low_levels_of/e3oljq8/
|
||||
[7]: https://en.wikipedia.org/wiki/Transgender_hormone_therapy_(male-to-female)#Progestogens
|
||||
|
||||
研究者们还表示,13%的服用 MPA 的跨性别女性(共 5 人)报告了情绪波动。不过,这些报告同样是主观的/逸闻的,而不是客观的。因此,我们也应该对此抱有怀疑。更加严谨高质量的临床研究证实 MPA 在顺性别女性中没有不好的情绪改变的风险([Wiki][8])。这很可能也适用于跨性别女性。
|
||||
|
||||
[8]: https://en.wikipedia.org/wiki/Medroxyprogesterone_acetate#Mood_changes
|
||||
|
||||
## 原图表
|
||||
|
||||
![Figure 9][9]
|
||||
|
||||
[9]: https://transfemscience.org/assets/images/s7m9rpt6bh431.png
|
||||
|
||||
“图 1。 血清雌二醇与雌二醇剂量之比,患者坚持服用雌二醇(E)和螺内脂(spiro),联用或不联用 MPA。图例:E+spiro+MPA(红),E+spiro(蓝)。”
|
||||
|
||||
![Figure 10][10]
|
||||
|
||||
[10]: https://transfemscience.org/assets/images/xf59gml7bh431.png
|
||||
|
||||
“图 2。 总血清睾酮与血清雌二醇之比,患者坚持服用雌二醇(E)和螺内脂(spiro),联用或不联用 MPA。图例:E+spiro+MPA(红),E+spiro(蓝)。”
|
||||
|
||||
## 重建的图表
|
||||
|
||||
我已经从论文中重建了两张图表,以便从中提取数据。可惜,并不完美;准确地获取点的位置几乎不可能,因为许多点重叠了。但不管怎样,数据相当接近。主要就是第一张图表的雌二醇+MPA 的趋势线(及延伸点)偏了。
|
||||
|
||||
![Figure 11][11]
|
||||
|
||||
[11]: https://transfemscience.org/assets/images/y4bpvkjsfj431.png
|
||||
|
||||
图一。 舌下含服雌二醇加螺内脂,联用或不联用醋酸甲羟孕酮。
|
||||
|
||||
![Figure 12][12]
|
||||
|
||||
[12]: https://transfemscience.org/assets/images/eza3v1gtfj431.png
|
||||
|
||||
图二。 舌下含服雌二醇加螺内脂,联用或不联用醋酸甲羟孕酮进行治疗期间,雌二醇水平和睾酮水平之间的关系。
|
||||
|
||||
## 新图表
|
||||
|
||||
下面是我用提取出的数据建的两个全新的图表:
|
||||
|
||||
![Figure 13][13]
|
||||
|
||||
[13]: https://transfemscience.org/assets/images/8dw4z9zmgj431.png
|
||||
|
||||
不同剂量的舌下含服雌二醇下雌二醇的水平。未具体说明给药后经过的时间。可能是随机的,因此雌二醇水平可能代表“平均”水平。编辑/更新:“取决于患者”,每天舌下含服一次或两次雌二醇。
|
||||
|
||||
![Figure 14][14]
|
||||
|
||||
[14]: https://transfemscience.org/assets/images/745m1pc8kj431.png
|
||||
|
||||
不同剂量的舌下含服雌二醇外加螺内脂和醋酸甲羟孕酮进行治疗期间,睾酮水平与不同的雌二醇水平。点代表上下 50pg/mL 内雌二醇的平均值。由于数据不足,未包含更高水平的雌二醇。
|
||||
|
||||
## 新表格
|
||||
|
||||
从图中的数据,我们可以作出如下舌下含服雌二醇的粗略表格:
|
||||
|
||||
| 舌下含服雌二醇剂量 | 雌二醇水平<sup>a</sup> | 睾酮水平 |
|
||||
| ------------------ | ---------------------- | ---------- |
|
||||
| 2 mg/day | ~50 pg/mL | ~235 ng/dL |
|
||||
| 4 mg/day | ~100 pg/mL | ~200 ng/dL |
|
||||
| 6 mg/day | ~150 pg/mL | ~115 ng/dL |
|
||||
| 8 mg/day | ~250 pg/mL | ~50 ng/dL |
|
||||
| 10 mg/day | ~300 pg/mL | ≤50 ng/dL |
|
||||
| 12 mg/day | ~500 pg/mL | ≤50 ng/dL |
|
||||
|
||||
<sup>a</sup>未具体说明给药后经过的时间及给药频率。[编辑/更新:“取决于患者”,每天舌下含服一次或两次雌二醇(私聊得知)。]假设舌下雌二醇给药后抽血的时间是随机的,在此,雌二醇水平可能代表“平均”水平。
|
||||
|
||||
## 附加评论
|
||||
|
||||
不得不说,这项研究中观测到的雌二醇水平及舌下含服雌二醇对睾酮的抑制比我预想的低得多。我不知道,是不是与这项研究出了问题或数据是否完全准确。不过,我到想到一件事,那就是作者并未提及服药规则,而患者很可能一天只舌下含服雌二醇一次[编辑/更新:“取决于患者”,每天舌下含服一次或两次雌二醇。]这很可能导致缺少持续稳定的雌二醇水平,最终造成低于预期的睾酮抑制。
|
||||
|
||||
## 更新
|
||||
|
||||
我只想更正并澄清这实际上**不是**第一项在跨性别女性中对舌下含服雌二醇的研究![这里][15],Madeline Deutsch 及其同事们的一项更早的研究评估了在 14 名跨性别女性舌下含服微粉化雌二醇(每天两次 2 毫克微粉化雌二醇,共计 4 毫克每天)外加 100 至 200mg/天的螺内脂。以下未结果(中间值):
|
||||
|
||||
[15]: https://doi.org/10.1097/AOG.0000000000000692
|
||||
|
||||
| | 基线 | 6 月 | # 6 个月中保持生理水平 |
|
||||
| ------------ | ---------- | --------- | ---------------------- |
|
||||
| 雌二醇水平 | 29 pg/mL | 258 pg/mL | 16/16 (100%) |
|
||||
| 总睾酮水平 | 405 ng/dL | 42 ng/dL | 10/15 (67%) |
|
||||
| 游离睾酮水平 | 11.4 ng/dL | 0.8 ng/dL | 14/15 (93%) |
|
||||
|
||||
不过,注意上表也包扩了两名**不**舌下含服雌二的跨性别女性;一位使用一片 100μg/天透皮雌二醇贴片,另一位每两周一次肌注 20mg 戊酸雌二醇。由于上表的数值是中间值及百分比,这两位对数据的影响应该没有那么大。
|
||||
|
||||
显而易见,在这项研究中睾酮的抑制情况好得多。
|
||||
|
|
@ -0,0 +1,65 @@
|
|||
title: 女性倾向跨性别者科学
|
||||
baseURL: https://tfsci.mtf.wiki
|
||||
theme: tfsci
|
||||
copyright: >
|
||||
© 2022
|
||||
[Transfeminine Science](https://transfemscience.org) and
|
||||
[MtF.wiki](https://mtf.wiki)
|
||||
|
||||
languageCode: zh-cn
|
||||
hasCJKLanguage: true
|
||||
defaultContentLanguage: zh-cn
|
||||
defaultContentLanguageInSubdir: true
|
||||
disableKinds: [taxonomy, term]
|
||||
disableLanguages: [zh-tw, zh-hk]
|
||||
enableGitInfo: true
|
||||
enableRobotsTXT: true
|
||||
googleAnalytics: G-TKT26VDTW3
|
||||
|
||||
author:
|
||||
name: MtF.wiki
|
||||
url: https://mtf.wiki
|
||||
email: tfsci@mtf.wiki
|
||||
|
||||
params:
|
||||
ContentSecurityPolicy:
|
||||
- default-src 'self'
|
||||
- img-src *
|
||||
- style-src 'self' 'unsafe-inline'
|
||||
- script-src 'self' https://www.googletagmanager.com
|
||||
- connect-src 'self' https://www.googletagmanager.com https://www.google-analytics.com
|
||||
|
||||
social:
|
||||
twitter: '@MtFwiki'
|
||||
telegram: '@MtFwiki'
|
||||
|
||||
markup:
|
||||
tableOfContents:
|
||||
endLevel: 4
|
||||
ordered: false
|
||||
startLevel: 2
|
||||
goldmark:
|
||||
renderer:
|
||||
unsafe: true
|
||||
|
||||
frontmatter:
|
||||
lastmod: [translated]
|
||||
date: [updated]
|
||||
publishDate: [published]
|
||||
|
||||
languages:
|
||||
zh-cn:
|
||||
title: 女性倾向跨性别者科学
|
||||
contentDir: content
|
||||
languageName: 大陆简体
|
||||
weight: 1
|
||||
zh-tw:
|
||||
title: 女性傾向跨性別者科學
|
||||
contentDir: content.zh-tw
|
||||
languageName: 臺灣正體
|
||||
weight: 2
|
||||
zh-hk:
|
||||
title: 女性傾向跨性別者科學
|
||||
contentDir: content.zh-hk
|
||||
languageName: 香港繁體
|
||||
weight: 3
|
||||
|
|
@ -0,0 +1,28 @@
|
|||
---
|
||||
title: 首页
|
||||
description: 欢迎来到 MtF.wiki 附属的“女性倾向跨性别者科学”(Transfeminine Science)中文译本存档站。
|
||||
---
|
||||
|
||||
欢迎来到 <https://MtF.wiki> 附属的“女性倾向跨性别者科学”(*[Transfeminine Science](https://transfemscience.org)*)中文译本存档站。原文由一群非相关专业出身、却热情洋溢的多国跨性别人士所作,旨在为**女性化激素治疗**提供力所能及的指引,行文严谨、讨论细致、引经据典,具有相当的可信度。本项目则旨在**忠实转达**这些文章的内容和观点,以资参考。\
|
||||
译文源代码现托管于 [GitHub](https://github.com/mtf-wiki/transfeminine-science)。
|
||||
|
||||
为便于翻阅、减少翻译工作量,本站译者会从上百篇原文当中精心挑选一部分进行翻译;同时,边翻译边学习,促进 MtF.wiki 内容的完善。因此,本站内容可视作对 MtF.wiki 药物板块的先行或拓展参考。\
|
||||
由于原文内容随时会修订,而本站译者不一定有时间与精力实时跟进;因此,译文修订间隔暂定为 3 - 12 个月。如有不便,敬请谅解。
|
||||
|
||||
可见“[关于]({{< ref "about" >}})”一页以了解更多详情。
|
||||
|
||||
> 本站除簡體中文外,還提供繁體中文版本,以便港澳台用戶閱覽;需要注意,此版本從簡體中文底稿自動轉換而來,或與港澳台地區語言習慣不符。
|
||||
|
||||
## 原站简介
|
||||
|
||||
“**女性倾向跨性别者科学**”是一个有关<u>女性倾向跨性别者激素疗法(transfeminine hormone therapy)</u>的原创信息资源站。
|
||||
对此类激素疗法,人们多称之为:{{< abbr FHT >}};用于女性倾向跨性别者的{{< abbr GaHT >}};以及{{< abbr MtF >}}{{< abbr HRT >}}——后者在早年更为常见。
|
||||
该疗法需要服用女性性激素(包括雌激素及孕激素)和抗雄激素制剂,以达到跨性别女性及非二元性别(女性倾向)群体的女性化、去男性化、缓和性别焦虑的目的。
|
||||
|
||||
本站的文章由多位撰稿人编写,皆与女性倾向跨性别者激素疗法有关。
|
||||
撰稿人及其资料已列于“[关于本站]({{< ref "about" >}})”页面的“[作者]({{< ref "about#list-of-authors" >}})”一节。
|
||||
本站由跨性别者撰稿,为跨性别者及其医师服务。
|
||||
在“[文章]({{< ref "articles" >}})”页面,可见本站文章的分类列表。
|
||||
此外,在“[最新文章]({{< ref "archives" >}})”页面可见按发表时间倒序排列的文章列表。
|
||||
而在“[杂项]({{< ref "misc" >}})”页面,则囊括了实用工具、重要的公开发表材料、网页链接等不同类型的内容。
|
||||
本站文章随时可更新及优化,即“活的文章”。本站所有新文章在发表之前会经过合伙撰稿人的非正式同行评议。
|
||||
|
|
@ -1,125 +1,142 @@
|
|||
# 关于本站
|
||||
---
|
||||
title: 关于本站
|
||||
linkTitle: 关于
|
||||
description: 本站概况与介绍请见首页以下翻译自原站点“关于本站”页面
|
||||
weight: 4
|
||||
---
|
||||
|
||||
本站概况与介绍请见[首页][index]。
|
||||
> 本站概况与介绍请见[首页]({{< ref "/" >}})。\
|
||||
> 以下翻译自原站点“[关于本站](https://transfemscience.org/about/)”页面;关于本翻译项目请见[下文]({{< ref "#translation-project" >}})。
|
||||
|
||||
## 本站创立的由来
|
||||
## 本站创立的由来 {#history}
|
||||
|
||||
本站基于多名女性倾向跨性别者在社交网站 Reddit 创建的女性化激素疗法相关内容而创立。本站仍在 Reddit 栏目:[r/TransfemScience][r-tfsci] 继续保持活跃,有新文章发布时也会在此贴出链接。更多详情可见《[建站声明][announcement]》一文。
|
||||
本站基于多名女性倾向跨性别者在社交网站 Reddit 创建的女性化激素疗法相关内容而创立。\
|
||||
本站仍在 Reddit 栏目:<https://reddit.com/r/TransfemScience> 继续保持活跃,有新文章发布时也会在此贴出链接。\
|
||||
更多详情可见《[建站声明]({{< ref "announcement" >}})》一文。
|
||||
|
||||
## 作者一览
|
||||
## 作者一览 {#list-of-authors}
|
||||
|
||||
本站撰稿人有:[Aly][aly]、[Lain][lain]、[Sam][sam]、[Mitzi][mitzi] 以及 [Luna][luna]。
|
||||
本站撰稿人有:
|
||||
[Aly W.]({{< ref "#aly-w" >}})、
|
||||
[Lain M.]({{< ref "#lain-m" >}})、
|
||||
[Sam S.]({{< ref "#sam-s" >}})、
|
||||
[Mitzi]({{< ref "#luna" >}})
|
||||
以及
|
||||
[Luna]({{< ref "#luna" >}})。
|
||||
|
||||
### Aly W.
|
||||
### Aly W. {#aly-w}
|
||||
|
||||
Aly (代词:她)来自美国南加利福尼亚州,是一名跨性别女性。她对女性化激素疗法抱有浓厚兴趣。2012 年 Aly 开始了性别转变过程,此后热衷于探究跨性别医学文献的工作。她以优异成绩毕业于[加州大学尔湾分校][wiki-ucirvine]的心理系,并取得学士学位。Aly 还完成了若干医学预科课程,并在加州大学尔湾分校的认知科研实验室担任一年的助教。
|
||||
Aly (代词:她)来自美国南加利福尼亚州,是一名跨性别女性。她对女性化激素疗法抱有浓厚兴趣。2012 年 Aly 开始了性别转变过程,此后热衷于探究跨性别医学文献的工作。她以优异成绩毕业于[加州大学尔湾分校][wiki-ucirvine]的心理系,并取得学士学位。Aly 还完成了若干医学预科课程,并在加州大学尔湾分校的认知科研实验室担任一年的助教。\
|
||||
Aly 已作为志愿者在英文维基百科社区活跃多年。2015 至 2018 年,她连年位列维基百科医学栏目最佳编辑者前六名之内。\
|
||||
Aly 在性激素药理学方面耕耘多年,贡献颇多;从她的[编辑历史][aly-stat]、[最佳条目][aly-top]、[新建文章][aly-create]与[已上传图片][aly-image]<sup>([备用链接][aly-image-alt])</sup>等记录中可见一斑。Aly 有时也在维基百科上简短引用本站内容,其中绝大部分来自她本人的文章。\
|
||||
Aly 多年来持续活跃于 Reddit 与 Discord 等平台上跨性别网络社群。在 Reddit 的数年间,她曾领导 <https://reddit.com/r/MtFHRT> 栏目(现为 <https://reddit.com/r/TransfemScience> 栏目)的运转;参与 <https://reddit.com/r/AskMtFHRT> 和 <https://reddit.com/r/TransBreastTimelines> 栏目的创立;也曾担任 <https://reddit.com/r/TransDIY> 栏目的版主。
|
||||
|
||||
Aly 已作为志愿者在英文维基百科社区活跃多年。2015 至 2018 年,她连年位列维基百科医学栏目最佳编辑者前六名之内。
|
||||
Aly 在性激素药理学方面耕耘多年,贡献颇多;从她的[编辑历史][aly-stat]、[最佳条目][aly-top]、[新建文章][aly-create]与[已上传图片][aly-image]<sup>([备用链接][aly-image-alt])</sup>等记录中可见一斑。Aly 有时也在维基百科上简短引用本站内容,其中绝大部分来自她本人的文章。
|
||||
如需联系 Aly,可发送邮件到 <aly@transfemscience.org> 。如需询问有关激素治疗的事项(如治疗建议),不妨移步至[网络社群][misc-com]。
|
||||
|
||||
Aly 多年来持续活跃于 Reddit 与 Discord 等平台上跨性别网络社群。在 Reddit 的数年间,她曾领导 [r/MtFHRT][r-mtfhrt] 栏目(现为 [r/TransfemScience][r-tfsci] 栏目)的运转;参与 [r/AskMtFHRT][r-askmtfhrt] 和 [r/TransBreastTimelines][r-tbt] 栏目的创立;也曾担任 [r/TransDIY][r-transdiy] 栏目的版主。
|
||||
|
||||
如需联系 Aly,可发送邮件到 `aly@transfemscience.org` 。如需询问有关激素治疗的事项(如治疗建议),不妨移步至[网络社群][misc-com]。
|
||||
|
||||
### Lain M.
|
||||
### Lain M. {#lain-m}
|
||||
|
||||
Lain (代词:Ta)是一名非二元(女性倾向)跨性别者。Ta 在纽约[罗彻斯特理工学院][wiki-rit]获得应用数学学士学位,学习了生物信息学与计算生物学。Ta 后来退出了博士学位的攻读,随后迁至气候温暖的旧金山湾区,在科技岗位述职。
|
||||
|
||||
作为扎根于夜生活(尤其是狂欢舞会)社群的人,Lain 重整了 [DanceSafe][dancesafe] 湾区分会,并运营了长达三年。(DanceSafe 是一项旨在减少夜生活里滥用药物——多为毒品——对健康之损害的非盈利项目。)Ta 在 DanceSafe 发表了倡导减少夜生活相关的药物之损害的文献,并在多场聚会与狂欢节上组织宣传展台。Lain 带领志愿者们,在主动接触夜生活社群的过程中,进行一对一的药物教育、性教育、咨询等,讨论其它密切相关的话题,以及掺杂物测试与用药[损害控制][wiki-harmredu]干预等等。
|
||||
作为扎根于夜生活(尤其是狂欢舞会)社群的人,Lain 重整了 [DanceSafe][dancesafe] 湾区分会,并运营了长达三年。(DanceSafe 是一项旨在减少夜生活里滥用药物——多为毒品——对健康之损害的非盈利项目。)Ta 在 DanceSafe 发表了倡导减少夜生活相关的药物之损害的文献,并在多场聚会与狂欢节上组织宣传展台。Lain 带领志愿者们,在主动接触夜生活社群的过程中,进行一对一的药物教育、性教育、咨询等,讨论其它密切相关的话题,以及掺杂物测试与用药[损害控制][wiki-harmredu]干预等等。\
|
||||
作为分会长,ta 提倡将药物损害控制手段标准化,并对药物管制政策进行改革;为此 ta 与美国[药物政策联盟][wiki-dpa](DPA)、[敏感药物政策学生组织][wiki-ssdp](SSDP)与[迷幻药综合学科研究会][wiki-maps](MAPS)等同行组织进行合作,还在湾区多场活动内进行了演说。
|
||||
|
||||
Lain 开始其医学转变过程之后,也开始热衷于对内分泌学与跨性别医学的研究上了。Lain 参与本站工作已有数年,期间撰写了数篇文章;不过,ta 后来离开了,不再与本站存在联系。
|
||||
|
||||
### Sam S.
|
||||
### Sam S. {#sam-s}
|
||||
|
||||
Sam (代词:她)来自英国伦敦,是一名跨性别女性。她未曾获得正式的医学或研究证书,但对循证医学有浓厚兴趣,也十分相信科学手段;她已在本站发布了数篇有关女性化激素疗法的文章。
|
||||
她的主要研究方向,是由女性倾向跨性别者的激素治疗引起的不寻常、以至罕见的副作用,例如血栓栓塞、冠心病等。具体而言,令她颇为关注的,是在性别肯定激素疗法当中,所用药物在不同类型与剂量下的差异如何。
|
||||
Sam (代词:她)来自英国伦敦,是一名跨性别女性。她未曾获得正式的医学或研究证书,但对循证医学有浓厚兴趣,也十分相信科学手段;她已在本站发布了数篇有关女性化激素疗法的文章。
|
||||
她的主要研究方向,是由女性倾向跨性别者的激素治疗引起的不寻常、以至罕见的副作用,例如血栓栓塞、冠心病等。具体而言,令她颇为关注的,是在性别肯定激素疗法当中,所用药物在不同类型与剂量下的差异如何。\
|
||||
自 2018 年开始激素转变过程起,她一直在涉猎并跟踪既有的和新发表的正式医学文献。
|
||||
|
||||
Sam 参与本站工作已有数年,期间撰写了数篇文章;不过,她后来离开了,不再为本站撰稿。
|
||||
|
||||
如需联系 Sam,可发送邮件至 `sam@transfemscience.org` 。
|
||||
如需联系 Sam,可发送邮件至 <sam@transfemscience.org>。
|
||||
|
||||
### Mitzi
|
||||
### Mitzi {#mitzi}
|
||||
|
||||
Mitzi (代词:她/Ta)来自英国伦敦,是一名非二元性别(女性倾向)人士。她在自行安排 HRT 用药(DIY)的社群中尤其活跃,在其中她作为指导者,向社群倡导在自行用药当中[减轻药物损害][wiki-harmredu]。
|
||||
Mitzi (代词:她/Ta)来自英国伦敦,是一名非二元性别(女性倾向)人士。她在自行安排 HRT 用药(DIY)的社群中尤其活跃,在其中她作为指导者,向社群倡导在自行用药当中[减轻药物损害][wiki-harmredu]。\
|
||||
Mitzi 常在线上和线下,对跨性别者遭遇无家可归、家庭暴力、医疗歧视与药物滥用等情况进行指引;还在一些基层组织(例如[跨性别医疗服务网络][twi-thn]、[性别形象确立工具包][gck]等)担任顾问。
|
||||
|
||||
Mitzi 对医学界有广泛兴趣,而对内分泌学与精神药理学尤为关注。她对英国的跨性别医疗系统作了直言不讳的批评,在其性别转变过程中也采取了自行用药的方式。
|
||||
|
||||
如需联系 Mitzi,可发送邮件到 `mitzi@transfemscience.org` 。
|
||||
如需联系 Mitzi,可发送邮件到 <mitzi@transfemscience.org>。
|
||||
|
||||
### Luna
|
||||
### Luna {#luna}
|
||||
|
||||
Luna(大青鲨型)(代词:她/Ta)来自英国,是一名女性和非二元跨性别者,也是计算机科学家。她对 [Aly W.][aly] 所作[注射用雌二醇模拟器][simulator]的代码做了[修改与优化][simulator-adv]。
|
||||
Luna(大青鲨型)(代词:她/Ta)来自英国,是一名女性和非二元跨性别者,也是计算机科学家。
|
||||
她对 [Aly W.]({{< ref "#aly-w" >}}) 所作[注射用雌二醇模拟器][simulator]的代码做了[修改与优化][simulator-adv]。
|
||||
|
||||
如需联系 Luna,可发送邮件至 `luna@transfemscience.org`。
|
||||
如需联系 Luna,可发送邮件至 <luna@transfemscience.org>。
|
||||
|
||||
## 联系我们
|
||||
## 联系我们 {#contact}
|
||||
|
||||
如需联系本站撰稿人,上文已列出各自的邮箱地址(例如联系 [Aly W.][aly] 可发至 `aly@transfemscience.org`)。此外,还可在 [Reddit][r-tfsci]、[推特][twi-tfsci] 与 [Discord][dc-tfsci] 等社交平台联系到诸撰稿人。我们欢迎任何关于我们的文章内容的反馈,以及其它重要的问询。
|
||||
如需联系本站撰稿人,上文已列出各自的邮箱地址(例如联系 [Aly W.]({{< ref "#aly-w" >}}) 可发至 <aly@transfemscience.org>)。此外,还可在 [Reddit][r-tfsci]、[推特][twi-tfsci] 与 [Discord][dc-tfsci] 等社交平台联系到诸撰稿人。我们欢迎任何关于我们的文章内容的反馈,以及其它重要的问询。\
|
||||
如需询问有关激素治疗的问题(如治疗建议),请移步至[跨性别网络社区][misc-com]。
|
||||
|
||||
## 免责声明
|
||||
## 免责声明 {#disclaimer}
|
||||
|
||||
本站的撰稿人<sup>(也包括译者)</sup>皆非医学专业或学术研究人士。本站文章已经过其他撰稿人的非正式[同行评议][wiki-pr],但从未正式发表或经过[学术同行评议][wiki-spr]。读者不应将本站内容奉为圭臬,而只应视为对现有[跨性别护理指南][guidelines]与[绝大部分医学文献][literature]的一种指引性或补充性资料。
|
||||
本站的撰稿人<sup>(也包括译者)</sup>皆非医学专业或学术研究人士。本站文章已经过其他撰稿人的非正式[同行评议][wiki-pr],但从未正式发表或经过[学术同行评议][wiki-spr]。读者不应将本站内容奉为圭臬,而只应视为对现有[跨性别护理指南][guidelines]与[绝大部分医学文献][literature]的一种指引性或补充性资料。建议应尽可能与专业医疗人士共同决定如何进行治疗。
|
||||
|
||||
建议应尽可能与专业医疗人士共同决定如何进行治疗。不过,我们知悉许多女性倾向跨性别者正在其激素治疗中[自行安排用药][wiki-diy],我们也打算帮助这些医疗资源匮乏的重要人群普及相关知识。
|
||||
不过,我们知悉许多女性倾向跨性别者正在其激素治疗中[自行安排用药][wiki-diy],我们也打算帮助这些医疗资源匮乏的重要人群普及相关知识。
|
||||
|
||||
## 版权声明
|
||||
## 版权声明 {#license}
|
||||
|
||||
[原文](LICENSE.md)
|
||||
[原文]({{< ref "license" >}})
|
||||
|
||||
> 本站版权归 Aly W. 及本站其他撰稿人所有;保留一切权利。未经 Aly W. 允许,请勿对本站内容进行二次创作(如翻译项目)。如获得许可,请准确署名,并设置指向本站原文的链接。
|
||||
> 本站版权归 Aly W. 及本站其他撰稿人所有;
|
||||
> 保留一切权利。未经 Aly W. 允许,请勿对本站内容进行二次创作(如翻译项目)。
|
||||
> 如获得许可,请准确署名,并设置指向本站原文的链接。
|
||||
|
||||
--------
|
||||
|
||||
## 关于此翻译项目
|
||||
## 关于此翻译项目 {#translation-project}
|
||||
|
||||
本站系对“女性倾向跨性别者科学”([Transfeminine Science][origin-en])网站之原创文章的中文翻译存档站点,2022 年十月创立。本站基于 GitHub 仓库:[tfsci-sc/articles][origin-cn] 的早前工作而建,现正由 MtF.wiki 工作组[自主维护][source]。
|
||||
原站撰稿人兼维护者:[Aly W.][aly] 已知悉本站工作,并授权本站仅存档简体中文内容。
|
||||
本站系对“女性倾向跨性别者科学”([Transfeminine Science](https://transfemscience.org))网站之原创文章的中文翻译存档站点,2022 年十月创立。\
|
||||
本站基于 GitHub 仓库:<https://github.com/tfsci-sc/articles> 的早前工作而建,现正由 MtF.wiki 工作组[自主维护](https://github.com/mtf-wiki/transfeminine-science)。
|
||||
|
||||
## 译者一览
|
||||
原站撰稿人兼维护者:[Aly W.]({{< ref "#aly-w" >}}) 已知悉本站工作,并授权本站仅存档简体中文内容。
|
||||
|
||||
### Bersella AI
|
||||
## 译者一览 {#list-of-translators}
|
||||
|
||||
跨性别女性,计算机系出身。自 2021 年十一月开始转变以来,密切关注跨性别医学动向,尤其是本站内容;至 2022 年十月止,在网络社区 [Limelight][llt] 总计发布 9 篇文章的翻译。
|
||||
随后加入 MtF.wiki 工作组,正式开始系统性整理工作。
|
||||
### Bersella AI {#bersella-ai}
|
||||
|
||||
如需联系 Bersella AI,可发送邮件至 `tfsci@mtf.wiki`。
|
||||
跨性别女性,计算机系出身。自 2021 年十一月开始转变以来,密切关注跨性别医学动向,尤其是本站内容;至 2022 年十月止,在网络社区 [Limelight](https://limelight.moe) 总计发布 9 篇文章的翻译。\
|
||||
随后加入 <https://MtF.wiki> 工作组,正式开始系统性整理工作。
|
||||
|
||||
### 其他来自 [tfsci-sc/articles][origin-cn] 的译者
|
||||
如需联系 Bersella AI,可发送邮件至 <tfsci@mtf.wiki>。
|
||||
|
||||
在此感谢 ta 们早前的卓越贡献。没有 ta 们先行,就没有如今的这个存档站。
|
||||
### 其他来自 tfsci-sc 项目的译者 {#list-of-tfsci-sc-translators}
|
||||
|
||||
#### yucandy
|
||||
在此感谢 ta 们早前的卓越贡献。没有 ta 们先行,就没有如今的这个存档站。\
|
||||
Ta 们目前与 MtF.wiki 尚无直接联系。
|
||||
|
||||
[Limelight](https://limelight.moe/u/yucandy) 与 [GitHub](https://github.com/yucandy) 用户,[tfsci-sc/articles][origin-cn] 项目的创始人。曾翻译两篇文章,也参与了“[性别烦躁指南](https://genderdysphoria.fyi/zh)”(This is Gender Dysphoria, FYI)的翻译。
|
||||
#### yucandy {#yucandy}
|
||||
|
||||
#### 昭心
|
||||
[Limelight](https://limelight.moe/u/yucandy) 与 [GitHub](https://github.com/yucandy) 用户,<https://github.com/tfsci-sc/articles> 项目的创始人。曾翻译两篇文章,也参与了“[性别烦躁指南](https://genderdysphoria.fyi/zh)”(*This is Gender Dysphoria, FYI*)的翻译。
|
||||
|
||||
#### 昭心 {#昭心}
|
||||
|
||||
[Limelight 用户](https://limelight.moe/u/昭心),曾翻译两篇文章。
|
||||
|
||||
#### Sue-e89893
|
||||
#### Sue-e89893 {#sue-e89893}
|
||||
|
||||
[GitHub 用户](https://github.com/Sue-e89893),曾翻译两篇文章。
|
||||
|
||||
## 本存档站技术支持
|
||||
## 联系译者 {#contact-translators}
|
||||
|
||||
#### [septs](https://github.com/septs)
|
||||
如有任何对本站及诸译文的改进建议、勘误等,可发送邮件至专用邮箱 <tfsci@mtf.wiki>;不过,涉及到原文观点的应向 *Transfeminine Science* 的撰稿人直接反馈。\
|
||||
此外,还可通过提交 [Pull Request](https://github.com/mtf-wiki/transfeminine-science/pulls) 对译文、简繁术语对照表等进行改进。
|
||||
|
||||
MtF.wiki 工作组成员,高级前端工程师。设计并开发 wiki 主站、[2345.LGBT][2345] 等站点。
|
||||
## 本存档站技术支持 {#supports}
|
||||
|
||||
[septs](https://github.com/septs)
|
||||
|
||||
<https://MtF.wiki> 与 <https://FtM.wiki> 工作组成员,高级前端工程师。设计并开发 wiki 主站、<https://2345.LGBT> 等站点。
|
||||
|
||||
<!-- 页内跳转 -->
|
||||
[aly]: #aly-w
|
||||
[lain]: #lain-m
|
||||
[sam]: #sam-s
|
||||
[mitzi]: #mitzi
|
||||
[luna]: #luna
|
||||
|
||||
<!-- 站内其它页面 -->
|
||||
[index]: README.md
|
||||
[announcement]: articles/announcement.md
|
||||
|
||||
[misc-com]: https://transfemscience.org/misc/#communities
|
||||
[simulator]: https://transfemscience.org/misc/injectable-e2-simulator/
|
||||
[simulator-adv]: https://transfemscience.org/misc/injectable-e2-simulator-advanced/
|
||||
|
|
@ -127,6 +144,7 @@ MtF.wiki 工作组成员,高级前端工程师。设计并开发 wiki 主站
|
|||
[literature]: https://transfemscience.org/articles/research-trans-literature/
|
||||
|
||||
<!-- Aly 的贡献 -->
|
||||
|
||||
[aly-stat]: https://xtools.wmflabs.org/ec/en.wikipedia.org/Medgirl131
|
||||
[aly-top]: https://xtools.wmflabs.org/topedits/en.wikipedia.org/Medgirl131
|
||||
[aly-create]: https://xtools.wmflabs.org/pages/en.wikipedia.org/Medgirl131
|
||||
|
|
@ -134,13 +152,11 @@ MtF.wiki 工作组成员,高级前端工程师。设计并开发 wiki 主站
|
|||
[aly-image-alt]: https://commons.wikimedia.org/wiki/Category:Medication_time%E2%80%93concentration_curves
|
||||
|
||||
<!-- Reddit 栏目 -->
|
||||
[r-tfsci]: https://reddit.com/r/TransfemScience/
|
||||
[r-mtfhrt]: https://www.reddit.com/r/MtFHRT/
|
||||
[r-askmtfhrt]: https://www.reddit.com/r/AskMtFHRT/
|
||||
[r-tbt]: https://www.reddit.com/r/TransBreastTimelines/
|
||||
[r-transdiy]: https://www.reddit.com/r/TransDIY/
|
||||
|
||||
[r-tfsci]: https://reddit.com/r/TransfemScience
|
||||
|
||||
<!-- 维基百科条目 -->
|
||||
|
||||
[wiki-ucirvine]: https://en.wikipedia.org/wiki/University_of_California,_Irvine
|
||||
[wiki-rit]: https://en.wikipedia.org/wiki/Rochester_Institute_of_Technology
|
||||
[wiki-harmredu]: https://en.wikipedia.org/wiki/Harm_reduction
|
||||
|
|
@ -151,15 +167,10 @@ MtF.wiki 工作组成员,高级前端工程师。设计并开发 wiki 主站
|
|||
[wiki-spr]: https://en.wikipedia.org/wiki/Scholarly_peer_review
|
||||
[wiki-diy]: https://en.wikipedia.org/wiki/Self-medication
|
||||
|
||||
|
||||
<!-- 其它外链 -->
|
||||
|
||||
[dancesafe]: https://dancesafe.org/
|
||||
[twi-thn]: https://twitter.com/transhealthnet
|
||||
[gck]: https://genderkit.org.uk/
|
||||
[twi-tfsci]: https://twitter.com/TransfemScience
|
||||
[dc-tfsci]: https://discord.gg/76YN4Kvy3c
|
||||
[llt]: https://limelight.moe
|
||||
[origin-en]: https://transfemscience.org/
|
||||
[origin-cn]: https://github.com/tfsci-sc/articles
|
||||
[source]: https://github.com/mtf-wiki/transfeminine-science
|
||||
[2345]: https://2345.lgbt
|
||||
|
|
@ -0,0 +1,6 @@
|
|||
---
|
||||
title: 存档
|
||||
description: 本页面用于枚举本站所有已经译制的文章
|
||||
layout: archives
|
||||
weight: 2
|
||||
---
|
||||
|
|
@ -0,0 +1,36 @@
|
|||
---
|
||||
title: 译文分类一览
|
||||
linkTitle: 文章
|
||||
description: 本页面整理了已翻译文章的分类
|
||||
weight: 1
|
||||
layout: single
|
||||
---
|
||||
|
||||
## 综合性文章 {#general-articles}
|
||||
|
||||
- [女性倾向跨性别者的激素治疗简介]({{< ref "transfem-intro" >}}) (Aly W., 2018)
|
||||
- [对非二元女性倾向跨性别者的激素治疗可能性的探索]({{< ref "nonbinary-transfem-overview" >}}) (Aly W., 2019)
|
||||
|
||||
## 特定主题类 {#special-topics}
|
||||
|
||||
### 雌激素 {#estrogens}
|
||||
|
||||
- [对女性倾向跨性别者舌下含服雌二醇以取代口服雌二醇的探索]({{< ref "sublingual-e2-transfem" >}}) (Sam S., 2021)
|
||||
- [关于女性倾向跨性别者舌下含服戊酸雌二醇片剂的简介]({{< ref "sublingual-ev" >}}) (Aly W., 2019)
|
||||
- [关于女性倾向跨性别者以阴囊及新阴唇给予透皮雌二醇可极大增强吸收率的简论]({{< ref "genital-e2-application" >}}) (Aly W., 2019)
|
||||
- [性激素与性激素结合球蛋白的相互作用及其对女性化激素疗法的意义]({{< ref "shbg" >}}) (Aly W., 2020)
|
||||
- [有关雌二醇注射剂的雌二醇浓度曲线的一次非正式荟萃分析]({{< ref "injectable-e2-meta-analysis" >}}) (Aly W., 2021)
|
||||
|
||||
### 抗雄激素制剂 {#antiandrogens}
|
||||
|
||||
- [低剂量的醋酸环丙孕酮足以最大限度地抑制女性倾向跨性别者的睾酮水平]({{< ref "cpa-dosage" >}}) (Aly W., 2019)
|
||||
- [法国关于醋酸环丙孕酮和脑膜瘤风险的研究的最新进展以及对女性倾向跨性别者的影响]({{< ref "cpa-meningioma" >}}) (Aly W., 2020)
|
||||
- [比卡鲁胺在女性化激素治疗方面的使用状况,以及医学界对其的接受情况]({{< ref "bica-adoption" >}}) (Aly W., 2020)
|
||||
|
||||
### 孕激素 {#progestogens}
|
||||
|
||||
- [口服孕酮及其引起的低孕酮水平与较弱效力的简论]({{< ref "oral-p4-low-levels" >}}) (Aly W., 2018)
|
||||
|
||||
### 激素治疗引起的普遍效果与风险 {#general-effects-and-risks}
|
||||
|
||||
- [关于女性化激素疗法与乳腺癌风险的简述]({{< ref "breast-cancer" >}}) (Aly W., 2020)
|
||||
|
|
@ -0,0 +1,57 @@
|
|||
---
|
||||
title: 一个综合女性化激素疗法信息的网站:“女性倾向跨性别者科学”建站声明
|
||||
linkTitle: “女性倾向跨性别者科学”建站声明
|
||||
description: 介绍 Transfeminine Science 的建站缘由
|
||||
author: Aly W.
|
||||
published: 2020-10-05
|
||||
updated: 2022-01-21
|
||||
translated: 2022-11-16
|
||||
translators:
|
||||
- Bersella AI
|
||||
trackHash: 7378b09b623aaedc898e8e60a30a5035fb5d10d2
|
||||
---
|
||||
|
||||
我们曾在 2017 年末在 Reddit 创建了新栏目 <https://reddit.com/r/MtFHRT>,旨在创建、收集、分享有关女性化激素疗法的资讯内容。
|
||||
该栏目最初接受任何相关内容的投稿;
|
||||
但投稿逐渐以原创文章为主。
|
||||
多年来该栏目内容得到了极大丰富。
|
||||
|
||||
读者可能已发现,最近数月里未曾有新内容在 r/MtFHRT 栏目投稿;
|
||||
|
||||
其实,我们正全力专注于一个全新的项目:
|
||||
|
||||
**“女性倾向跨性别者科学”**(<https://www.transfemscience.org>)
|
||||
|
||||
本站是有关女性化激素疗法的原创信息资源站。
|
||||
本站也是给 r/MtFHRT 栏目准备的全新升级的家,其中许多内容已迁移至本站,也有相当一些文章得到了重要修订。
|
||||
今后,由我们 r/MtFHRT 栏目团队撰写的内容将改为从本站发表。
|
||||
不过,我们当然仍将通过 r/MtFHRT 栏目分享新的内容,并同时发在 <https://reddit.com/r/TransDIY> 和 <https://reddit.com/r/AskMtFHRT> 等其它栏目。
|
||||
我们还将在 Reddit 以外的社交平台(如 [Facebook](https://facebook.com/TransfemScience) 与 [Twitter](https://twitter.com/TransfemScience))发布新文章的链接。
|
||||
|
||||
为了克服 Reddit 作为我们的资讯内容发布平台的诸多局限,我们决定将内容迁移至本站。
|
||||
促成我们迁移的重要动机有:Reddit 上发表的内容可定制性与功能不足;
|
||||
Reddit 的编辑界面问题颇多、令人恼火;
|
||||
我们的内容也需要有一个专门、独立的发布平台;
|
||||
尤其重要的是,Reddit 帖子和评论有字数限制。
|
||||
|
||||
本站既已上线,我们的工作重点将回到资讯内容的创作上来。
|
||||
我们正筹备许多我们颇感兴趣的文章,正计划于本站发布;
|
||||
本站既有内容也会继续得到修订与优化。为符合本站的高标准,许多文章仍有待修订。
|
||||
|
||||
r/MtFHRT 栏目一直是欢迎任何人投稿的地方。
|
||||
不过有一点,我们决定只有特定的人能够在此发帖,并设置对新内容进行非正式同行评议的流程。这些措施旨在提高该栏目信息的质量与可靠度。
|
||||
不过很遗憾,我们启用这些措施之后,只有极少的新帖子由非团队成员的 Reddit 用户发布——这些帖子也无一符合可得到我们认可或完整同行评议的门槛。
|
||||
尽管如此,我们仍将接受原创文章的投稿,并进行同行评议;
|
||||
甚而可能发布到本站上。如果你有任何可能有所贡献的内容,欢迎[联系我们]({{< ref "about#contact" >}})!
|
||||
|
||||
在此致谢所有关注我们的读者。希望读者们能在本站有所收获、怡然其中。
|
||||
|
||||
—— “女性倾向跨性别者科学”运营团队:
|
||||
[Aly]({{< ref "about#aly-w" >}}),
|
||||
[Lain]({{< ref "about#lain-m" >}}) 与
|
||||
[Sam]({{< ref "about#sam-s" >}})
|
||||
|
||||
---
|
||||
|
||||
**又记:** 本站上线之后,r/MtFHRT 栏目转为本站的官方 Reddit 讨论区;本站有新文章发布时,其链接也于此处公布。
|
||||
不过,我们此后决定将我们的活动从 r/MtFHRT 转移至新栏目 <https://reddit.com/r/TransfemScience>。
|
||||
|
|
@ -1,42 +1,53 @@
|
|||
# 比卡鲁胺在女性化激素治疗方面的使用状况,以及医学界对其的接受情况
|
||||
---
|
||||
title: 比卡鲁胺在女性化激素治疗方面的使用状况,以及医学界对其的接受情况
|
||||
linkTitle: 比卡鲁胺在女性化激素治疗上的使用与接受情况
|
||||
description: >-
|
||||
比卡鲁胺尚未得到充分研究,其安全性也令人堪忧,使用范围仍很有限。
|
||||
author: Aly W.
|
||||
published: 2020-07-01
|
||||
updated: 2022-11-08
|
||||
translated: 2022-11-14
|
||||
translators:
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 比卡鲁胺
|
||||
- 抗雄激素制剂
|
||||
- 用药安全
|
||||
trackHash: 7378b09b623aaedc898e8e60a30a5035fb5d10d2
|
||||
---
|
||||
|
||||
> - 作者 [Aly W.](https://transfemscience.org/articles-by-author/aly-w/)
|
||||
> + 首次发表于 2020 年 7 月 1 日
|
||||
> + 最后修改于 2022 年 9 月 26 日
|
||||
> - 译者 [Bersella AI](https://bersella-ai.cc)
|
||||
> + 翻译于 2022 年 11 月 14 日
|
||||
## 译者按 {#notice}
|
||||
|
||||
## 译者按
|
||||
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。 如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. **<u>⚠ 免责声明:本文不构成任何医疗、处方建议。 如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. 以下《指南》《跨性别……指南》等应当皆指代同一事物,原文如此。
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
---
|
||||
|
||||
## 摘要
|
||||
## 摘要 {#abstract}
|
||||
|
||||
> 比卡鲁胺是一种抗雄制剂,多年前其被推出时曾用于前列腺癌的治疗;但多年来,其因价格昂贵,未被推广至其它用途。不过,其价格已有所下降,现正广泛用于女性化激素治疗、以及其他群体(如顺性别妇女)由雄激素引起的症状的治疗上。
|
||||
> 比卡鲁胺存在一些风险,例如肝毒性等罕见的不良反应;这引起了对其安全性的担忧,从而限制了其在女性倾向跨性别者当中的使用。不过,在恰当的监测与临床管理下,这些风险相对较低——尽管仍很显著。最近,跨性别医学方面的一些著名学者,对比卡鲁胺在女性倾向跨性别者上的使用持开放态度,在其著述中亦对此做积极评价。
|
||||
> 比卡鲁胺是一种抗雄制剂,多年前其被推出时曾用于前列腺癌的治疗;但多年来,其因价格昂贵,未被推广至其它用途。不过,其价格已有所下降,现正广泛用于女性化激素治疗、以及其他群体(如顺性别妇女)由雄激素引起的症状的治疗上。\
|
||||
> 比卡鲁胺存在一些风险,例如肝毒性等罕见的不良反应;这引起了对其安全性的担忧,从而限制了其在女性倾向跨性别者当中的使用。不过,在恰当的监测与临床管理下,这些风险相对较低——尽管仍很显著。最近,跨性别医学方面的一些著名学者,对比卡鲁胺在女性倾向跨性别者上的使用持开放态度,在其著述中亦对此做积极评价。\
|
||||
> 比卡鲁胺也许会逐渐被认为在女性化激素治疗当中足够安全,就像螺内酯、醋酸环丙孕酮等风险很低的抗雄制剂一样;但是,在其被跨性别医学广泛接受前,可能还需更多的有关女性倾向跨性别者使用比卡鲁胺的研究与描述。
|
||||
|
||||
## 女性倾向跨性别者使用比卡鲁胺的历史
|
||||
## 女性倾向跨性别者使用比卡鲁胺的历史 {#history-of-bicalutamide-for-transfeminine-people}
|
||||
|
||||
比卡鲁胺(Casodex 品牌)是一种非甾体类抗雄制剂和选择性雄激素受体拮抗剂;最初在 1995 年推出时,其用于顺性别男性治疗前列腺癌。前列腺癌由雄激素引起,因此可被抗雄制剂治疗。相比于螺内酯(Aldactone 品牌)与醋酸环丙孕酮(Androcur 品牌)等抗雄制剂,在雄激素拮抗效力、临床疗效、药理选择性和可耐受度等方面,比卡鲁胺具有显著优势。而相较早期的非甾体类抗雄制剂(如氟他胺,Eulexin 品牌;尼鲁米特,Anandron 品牌),比卡鲁胺则有更好的效力、药代动力学特性以及可耐受度,安全性也大大提高。不过,直到最近,比卡鲁胺才作为抗雄制剂用于女性化激素治疗。
|
||||
比卡鲁胺(Casodex 品牌)是一种非甾体类抗雄制剂和选择性雄激素受体拮抗剂;最初在 1995 年推出时,其用于顺性别男性治疗前列腺癌。前列腺癌由雄激素引起,因此可被抗雄制剂治疗。相比于螺内酯(Aldactone 品牌)与醋酸环丙孕酮(Androcur 品牌)等抗雄制剂,在雄激素拮抗效力、临床疗效、药理选择性和可耐受度等方面,比卡鲁胺具有显著优势。而相较早期的非甾体类抗雄制剂(如氟他胺,Eulexin 品牌;尼鲁米特,Anandron 品牌),比卡鲁胺则有更好的效力、药代动力学特性以及可耐受度,安全性也大大提高。不过,直到最近,比卡鲁胺才作为抗雄制剂用于女性化激素治疗。\
|
||||
之所以多年来比卡鲁胺未被广泛用于女性倾向跨性别者,是因为比卡鲁胺曾受制药厂专利的保护,价格亦十分昂贵。不过,从 2007 至 2009 年开始出现的比卡鲁胺仿制品,改变了这一事实。此后,陆续推出的醋酸阿比特龙(Zytiga 品牌,在 2011 年)、恩杂鲁胺(Xtande 品牌,在 2012 年)等抗雄制剂具有更高效力,因而取代了比卡鲁胺,成为前列腺癌的标准治疗用药。新药的研发使得近十年内比卡鲁胺的价格大幅下降,而逐渐变得可以承受。
|
||||
|
||||
2015 年以前,只有极少的文献<sup>(见[相关文献一页][alyw19_lit])</sup>和一些网络传闻提到了女性倾向跨性别者使用比卡鲁胺。2011 年,Louis Gooren 率先在有关女性化激素治疗的文献中明确提及比卡鲁胺<sup>([Gooren, 2011][g11]; [Aly W., 2019][alyw19_lit])</sup>。Gooren 其人是跨性别医学领域的主要资深学者之一,曾参与美国内分泌学会《跨性别激素治疗指南》的编纂<sup>([Hembree et al., 2009][h09]; [Hembree et al., 2017][h17])</sup>。1980 年代末到 1990 年代初,在阿姆斯特丹自由大学医学中心(VUMC)的性别焦虑专家中心,Gooren 及其同行开展了有关尼鲁米特(Anandron、Nilandron 品牌)作为抗雄制剂用于女性倾向跨性别者的研究<sup>([de Voogt et al., 1987a][v87a]; [de Voogt et al., 1987b][v87b]; [Gooren et al., 1987][g87]; [Johannes et al., 1987][j87]; [Rao et al., 1988][r88]; A[sscheman, Gooren, & Peereboom-Wynia, 1989][agp89]; [van Kemenade et al., 1989][k89]; [维基百科][wiki_nilu])</sup>。不过,他们后来似乎放弃了尼鲁米特的研究;这可能出于其肺毒性发生率高、以及其它因脱靶效应带来的副作用之缘故。尽管如此,从 1990 年代开始,Gooren 还是在其发表的资料中将氟他胺与尼鲁米特纳入到可用于女性化激素治疗的潜在选项当中<sup>([Asscheman & Gooren, 1992][ag92]; [Gooren, 1999][g99]; 见[相关文献][alyw19_lit])</sup>;也正因如此,氟他胺被一些《跨性别健康指南》及其它出版物收录了,不过评价并不大积极<sup>(例如 [Israel & Tarver, 1997][it97]; [Levy, Crown, & Reid, 2003][lcr03]; [Dahl et al., 2006a][d06a]; [Dahl et al., 2006b][d06b]; Hembree et al., 2009; [Moreno-Pérez et al., 2012][mp12])</sup>。作为一名对女性倾向跨性别者使用的非甾体类抗雄制剂感兴趣的学者,Gooren 本应对安全性远胜于氟他胺与尼鲁米特的比卡鲁胺引起注意;但是 Gooren 及其同行从未进行有关比卡鲁胺用于女性倾向跨性别者的研究,在其发表的资料中也仅仅简单提及了这项用途。其他学者亦皆如是。
|
||||
|
||||
除了用于女性倾向跨性别者和患有前列腺癌的男性之外,比卡鲁胺还被研究用于治疗其他人群中由雄激素引起的症状。例如,其被用于治疗顺性别妇女的多毛症;部分人患有多囊卵巢综合征,其余则没有<sup>([Müderris, Bayram, & Güven, 1999][mbg99]; [Müderris et al., 2002][m02]; [Bahceci et al., 2004][b04]; [Müderris & Öner, 2009][mo09], [PDF][mo09_pdf], [英语译文][mo09_eng]; [Moretti et al., 2016][m16]; [Moretti et al., 2018][m18]; [维基百科][wiki_use_bica_s])</sup>。比卡鲁胺还被研究了结合阿那曲唑(Arimeidex 品牌;一种芳香化酶抑制剂)用于顺性别男孩的非促性腺激素相关性早熟的治疗上<sup>([Kreher et al., 2006][k06]; [Lewis et al., 2009][l09]; [Mitre & Lteif, 2009][ml09]; [Stenger et al., 2009][s09]; [Lenz et al., 2010][l10]; [Reiter et al., 2010][r10]; [Tessaris et al., 2012][t12]; [Özcabı et al., 2015][o15]; [Kor, 2018][k18]; [Arya & Davies, 2019][ad19]; [Nabhan & Eugster, 2019][ne19]; [Finkle et al., 2020][f20]; [Gurnurkar, DiLillo, & Carakushansky, 2021][gdc21]; [维基百科][wiki_use_bica_m])</sup>。此类性早熟很罕见,其中促性腺激素释放激素(GnRH)调节机制失去了作用。在美国,这种比卡鲁胺结合阿那曲唑的特定疗法已完成了二期临床试验,并提交了新药申请,但未获通过;原因是在主要疗效终点——限制身高上之效果的证据尚不充分<sup>([AstraZeneca, 2008][az08])</sup>。不过,尽管在适应症之外,比卡鲁胺仍被用于该疗法;而在经美国食品药品监管局(FDA)批准的 Casodex 药品标示中,亦提及了比卡鲁胺的这项用途<sup>([FDA, 2017][fda17])</sup>。
|
||||
除了用于女性倾向跨性别者和患有前列腺癌的男性之外,比卡鲁胺还被研究用于治疗其他人群中由雄激素引起的症状。例如,其被用于治疗顺性别妇女的多毛症;部分人患有多囊卵巢综合征,其余则没有<sup>([Müderris, Bayram, & Güven, 1999][mbg99]; [Müderris et al., 2002][m02]; [Bahceci et al., 2004][b04]; [Müderris & Öner, 2009][mo09], [PDF][mo09_pdf], [英语译文][mo09_eng]; [Moretti et al., 2016][m16]; [Moretti et al., 2018][m18]; [维基百科][wiki_use_bica_s])</sup>。\
|
||||
比卡鲁胺还被研究了结合阿那曲唑(Arimeidex 品牌;一种芳香化酶抑制剂)用于顺性别男孩的非促性腺激素相关性早熟的治疗上<sup>([Kreher et al., 2006][k06]; [Lewis et al., 2009][l09]; [Mitre & Lteif, 2009][ml09]; [Stenger et al., 2009][s09]; [Lenz et al., 2010][l10]; [Reiter et al., 2010][r10]; [Tessaris et al., 2012][t12]; [Özcabı et al., 2015][o15]; [Kor, 2018][k18]; [Arya & Davies, 2019][ad19]; [Nabhan & Eugster, 2019][ne19]; [Finkle et al., 2020][f20]; [Gurnurkar, DiLillo, & Carakushansky, 2021][gdc21]; [维基百科][wiki_use_bica_m])</sup>。此类性早熟很罕见,其中促性腺激素释放激素(GnRH)调节机制失去了作用。在美国,这种比卡鲁胺结合阿那曲唑的特定疗法已完成了二期临床试验,并提交了新药申请,但未获通过;原因是在主要疗效终点——限制身高上之效果的证据尚不充分<sup>([AstraZeneca, 2008][az08])</sup>。不过,尽管在适应症之外,比卡鲁胺仍被用于该疗法;而在经美国食品药品监管局(FDA)批准的 Casodex 药品标示中,亦提及了比卡鲁胺的这项用途<sup>([FDA, 2017][fda17])</sup>。
|
||||
|
||||
到了 2015 年中,比卡鲁胺在女性倾向跨性别者当中的使用和相关讨论稀少的事实,开始有了改变。维基百科上有关比卡鲁胺的内容,从最基本的页面逐步扩充了起来;现在有了更丰富的用药信息。此外,在网络圈子里,一些女性倾向跨性别者开始提倡本群体使用比卡鲁胺——例如正叙述其较之于现成选项的优势、以及其用于女性化激素治疗的优良潜力的笔者。
|
||||
到了 2015 年中,比卡鲁胺在女性倾向跨性别者当中的使用和相关讨论稀少的事实,开始有了改变。维基百科上有关比卡鲁胺的内容,从最基本的页面逐步扩充了起来;现在有了更丰富的用药信息。此外,在网络圈子里,一些女性倾向跨性别者开始提倡本群体使用比卡鲁胺——例如正叙述其较之于现成选项的优势、以及其用于女性化激素治疗的优良潜力的笔者。\
|
||||
今后一段时间里,许多开明的医务工作者,都开始接纳比卡鲁胺用在女性倾向跨性别者上。其中,最早的一项对女性倾向跨性别者使用比卡鲁胺的临床研究,开始于 2013 年;其论文摘要于 2017 年发表,全文则于 2019 年发表<sup>([Neyman, Fuqua, & Eugster, 2017][nfe17]; [Neyman, Fuqua, & Eugster, 2019][nfe19])</sup>。该研究是一项规模较小的回顾性图表总结,针对的是比卡鲁胺作为二线青春期阻断剂用于跨性别女孩——其保险拒绝给付其 GnRH 类似物的费用。目前为止,该研究仍为在比卡鲁胺用于女性倾向跨性别者方面的唯一数据来源。虽然从各方面而言,其数据并不出色,但起码还算正规。该研究的发起者早前还发表了有关患有非促性腺激素相关性早熟的男孩们使用比卡鲁胺作为青春期阻断剂的论文<sup>(例如 [Lenz et al., 2010][l10]; [Haddad & Eugster, 2012][he12])</sup>。Neyman, Fuqua 和 Eugster (2019) 的发现——尽管资料有限——有助于让医务工作者和学者对比卡鲁胺在女性化激素治疗当中的应用产生浓厚的兴趣。
|
||||
|
||||
无论如何,在当下,比卡鲁胺尚未在女性倾向跨性别者当中被广泛采用;这是因为,比卡鲁胺成为女性化激素治疗的一种选项的时间还不太久,而且关于女性倾向跨性别者使用之的研究与描述还很稀缺,其安全性亦引起担忧。事实上,《跨性别激素治疗指南》亦普遍未曾对此有过提及。目前,比卡鲁胺的使用基本上局限于一些思想更灵活的医务工作者、以及自行安排跨性别激素治疗用药(DIY)的人群里。
|
||||
|
||||
## 一些和比卡鲁胺有关的,限制了其使用率的担忧
|
||||
## 一些和比卡鲁胺有关的,限制了其使用率的担忧 {#concerns-about-bicalutamide-limiting-its-use}
|
||||
|
||||
目前为止,跨性别医学界并不大愿意认可比卡鲁胺在女性倾向跨性别者的使用。这是因为,关于女性倾向跨性别者使用之的研究与描述还很稀缺,尤其是在安全性方面。有一些担忧是和患有前列腺癌的男性当中由比卡鲁胺引起肝衰竭的罕见案例相关的。这些有关比卡鲁胺之肝毒性的已报告病例,一般发病很突然、且症状严重。对患有前列腺癌的男性而言,比卡鲁胺治疗其癌症的收益远大于概率极低的肝毒性之风险,因此这种风险足可容忍。不过,对一般既年轻而又健康的女性倾向跨性别者而言,比卡鲁胺并非用于治疗绝症;一旦因其患上肝衰竭而亡,那便得不偿失了。也正因如此,加州大学旧金山分校(UCSF)版《跨性别护理指南》警告,出于潜在肝脏风险的考虑,当下不应将比卡鲁胺用于女性倾向跨性别者<sup>([Deutsch, 2016][d16])</sup>。
|
||||
目前为止,跨性别医学界并不大愿意认可比卡鲁胺在女性倾向跨性别者的使用。这是因为,关于女性倾向跨性别者使用之的研究与描述还很稀缺,尤其是在安全性方面。有一些担忧是和患有前列腺癌的男性当中由比卡鲁胺引起肝衰竭的罕见案例相关的。这些有关比卡鲁胺之肝毒性的已报告病例,一般发病很突然、且症状严重。对患有前列腺癌的男性而言,比卡鲁胺治疗其癌症的收益远大于概率极低的肝毒性之风险,因此这种风险足可容忍。不过,对一般既年轻而又健康的女性倾向跨性别者而言,比卡鲁胺并非用于治疗绝症;一旦因其患上肝衰竭而亡,那便得不偿失了。也正因如此,加州大学旧金山分校(UCSF)版《跨性别护理指南》警告,出于潜在肝脏风险的考虑,当下不应将比卡鲁胺用于女性倾向跨性别者<sup>([Deutsch, 2016][d16])</sup>。\
|
||||
除了风险以外,目前还缺少可供指导适合女性倾向跨性别者使用的比卡鲁胺剂量之数据<sup>([Aly W., 2019][alyw19_dose])</sup>。目前普遍推荐使用的典型剂量,是 50 mg/天,但该剂量应该是缺少数据支持的情况下的主观臆断。
|
||||
|
||||
目前为止,已有 10 例和比卡鲁胺有关的严重肝毒性病例被报告<sup>([图表][table_2a])</sup>。这些病例皆为患有前列腺癌的男性,且皆在开始比卡鲁胺疗法的六个月内发病,其中两例随后死亡。尽管这些病例不多,看上去多少令人安心,但需要注意,已报告的不良反应病例数往往远低于其实际发生率。例如,对于醋酸环丙孕酮,迄今有大约 50 例脑膜炎病例被报告;但法国政府在近期的一项大规模研究发现,仅在法国就有超过 500 例和持续服用超过 8 年的高剂量醋酸环丙孕酮相关的脑膜炎病例*进行了手术*<sup>([Aly W., 2020][alyw20_meni])</sup>。相应地,截至撰稿时,在美国 FDA 的国际 [MedWatch/FAERS 数据库][faers]当中,共有 40 例和比卡鲁胺相关的肝衰竭病例,其中 25 例死亡;还有 240 例与其相关的肺间质病变病例,而已报告的只有 14 例<sup>([表格][table_2b])</sup>。但据估计,该数据库也仅报告了不足 10% 的严重不良反应现象<sup>([Graham, Ahmad, & Piazza-Hepp, 2002][gap02])</sup>。因此,实际病例数可能远大于此。这些案例不过出于巧合:迄今尚未确认比卡鲁胺和肝毒性之间是否存在因果关系。尽管如此,它们还是引起了不小担忧。传闻还有一件和比卡鲁胺相关的女性倾向跨性别者死亡病例,尽管不曾公开发表,但已在跨性别医学界当中口口相传。根据在跨性别医学领域的几位可靠人士所言,该病例是一名住在德克萨斯州的 20 岁跨性别女孩,服用比卡鲁胺后出现急性肝衰竭,且事前无任何征兆。该病例促使一些关注比卡鲁胺的医务工作者和学者,对比卡鲁胺在女性倾向跨性别者激素治疗中的使用,作出了保留意见。
|
||||
|
|
@ -45,18 +56,18 @@
|
|||
|
||||
在肝毒性风险上,比卡鲁胺远低于其类似物氟他胺<sup>(Kolvenbag & Blackledge, 1996; [Schellhammer et al., 1997][s97]; [Thole et al., 2004][t04]; [Manso et al., 2006][m06]; [表格][table_2c])</sup>;不过,其仍保有微弱的肝毒性风险——还可能附带严重并发症。故此,有必要谨慎使用之,每个服用它的人都需要注意监测肝功能。
|
||||
|
||||
## 近期进展及未来展望
|
||||
## 近期进展及未来展望 {#recent-developments-and-the-future}
|
||||
|
||||
比卡鲁胺在顺性别妇女改善和雄激素相关的皮肤及体毛状况上的使用,正被逐渐接受并加以描述。例如,在意大利进行的、有关比卡鲁胺用于多毛症的一项严谨的三期随机对照试验,近期已被公开发表<sup>([Moretti et al., 2018][m18])</sup>。此外,一项有关比卡鲁胺用于顺性别妇女脱发的回顾性图表总结,业已于近期公开发表<sup>([Fernandez-Nieto et al., 2019][fn19]; [Ismail et al., 2020][i20]; [Fernandez-Nieto et al., 2020][fn20]; [Moussa et al., 2021][m21])</sup>。这些有关体毛的研究发现了使用比卡鲁胺后的较低、但显著的肝功能病变发生率。
|
||||
|
||||
一些跨性别医学研究者也对比卡鲁胺产生了兴趣<sup>([Aly W., 2019][alyw19_lit])</sup>。其中可能尤其要关注的是,美国内分泌学会 2009、2017 年版《跨性别激素治疗指南》<sup>(Hembree et al., 2009; Hembree et al., 2017)</sup>的领衔作者:Wylie Hembree,在近期的评述中对比卡鲁胺用于女性倾向跨性别者做了积极评价<sup>([Fishman, Paliou, Poretsky, & Hembree, 2019][fpph19])</sup>。Hembree 及其同行提到了近期有关比卡鲁胺用于顺性别妇女多毛症的三期试验,以及有关比卡鲁胺作为青春期阻断剂用于跨性别女孩的研究,以支持将其用于女性倾向跨性别者的可能性。
|
||||
一些跨性别医学研究者也对比卡鲁胺产生了兴趣<sup>([Aly W., 2019][alyw19_lit])</sup>。其中可能尤其要关注的是,美国内分泌学会 2009、2017 年版《跨性别激素治疗指南》<sup>(Hembree et al., 2009; Hembree et al., 2017)</sup>的领衔作者:Wylie Hembree,在近期的评述中对比卡鲁胺用于女性倾向跨性别者做了积极评价<sup>([Fishman, Paliou, Poretsky, & Hembree, 2019][fpph19])</sup>。Hembree 及其同行提到了近期有关比卡鲁胺用于顺性别妇女多毛症的三期试验,以及有关比卡鲁胺作为青春期阻断剂用于跨性别女孩的研究,以支持将其用于女性倾向跨性别者的可能性。\
|
||||
另一位在跨性别医学领域的主要学者、美国内分泌学会版《指南》<sup>(Hembree et al., 2017; [Mitchell, 2020][m20])</sup>的联名作者:Guy T’Sjoen,在一篇与其同行创作的评述里,似乎也对比卡鲁胺持开放态度<sup>([Iwamoto et al., 2019][i19])</sup>。特别是在美国以外的学者,对比卡鲁胺的态度可能更开放,这归功于醋酸环丙孕酮——在美国以外使用最广泛的一种抗雄制剂——长期使用后引起的健康顾虑<sup>([Aly W., 2020][alyw20_meni])</sup>。密歇根州立大学的学者:John Randolph,同样对比卡鲁胺作出了积极评价<sup>([Randolph, 2018][r18])</sup>,不过此后他似乎改变了他的观点<sup>([Michigan Medicine, 2020][mm20])</sup>。而另一方面,其他学者并不那么欢迎比卡鲁胺在女性倾向跨性别者当中的使用<sup>(例如 [Hamidi & Davidge-Pitts, 2019][hdp19]; [Cocchetti et al., 2020][c20])</sup>。
|
||||
|
||||
只要给以适当的健康监测,比卡鲁胺较低的风险应可为跨性别医学界所接受。这种情况就跟有极低的严重不良反应发生率的其它药品一样:诸如螺内酯(高钾血症),醋酸环丙孕酮(良性脑膜瘤、血栓、乳腺癌、肝毒性),等等。考虑到其风险,比卡鲁胺可能最终不会被推荐用于一线治疗。不过,如果其它抗雄制剂的可行性因为某些缘故(例如,未按预期起效、耐受度低、有禁忌症、无法获取等)而变得更低、以至不具备,那么比卡鲁胺可作为二线治疗的一种选项。跨性别医学界做的还不够。在比卡鲁胺可被女性倾向跨性别者广泛接纳、或者为《跨性别激素治疗指南》所广泛推荐之前,可能需要更多的相关进展才行——也即,对真正的女性倾向跨性别者使用比卡鲁胺进行研究并加以描述。
|
||||
|
||||
## 后记
|
||||
## 后记 {#updates}
|
||||
|
||||
### 后记一
|
||||
### 后记一 {#update-1}
|
||||
|
||||
2021 年 3 月,芬威健康版《跨性别健康临床实践指南》自 2015 年 10 月以来首次获得更新<sup>([Aly W., 2020][aw20-guide])</sup>:
|
||||
|
||||
|
|
@ -70,7 +81,7 @@
|
|||
|
||||
在他处亦提供了从芬威健康版《指南》节选的有关女性倾向跨性别者使用比卡鲁胺的内容——还包括了对其安全性之监测的建议<sup>([Aly W., 2019][alyw19_lit_t])</sup>。
|
||||
|
||||
### 后记二
|
||||
### 后记二 {#update-2}
|
||||
|
||||
2021 年 9 月,南非洲艾滋病医师协会(SAHCS)首次发表了针对跨性别护理的《临床指南》:
|
||||
|
||||
|
|
@ -80,20 +91,84 @@
|
|||
|
||||
本站在他处亦提供了从该《指南》节选的有关女性倾向跨性别者使用比卡鲁胺的内容<sup>([Aly W., 2019][alyw19_lit_sahiv])</sup>。
|
||||
|
||||
### 后记三
|
||||
### 后记三 {#update-3}
|
||||
|
||||
2022 年 9 月,[世界跨性别人士健康专业协会][WPATH](WPATH)发布了第八版《[跨性别及性别多元化人群健康护理标准][SOC8]》(SOC8)<sup>([Coleman et al., 2022][C22])</sup>。该《标准》是现有最权威的跨性别护理指南之一,由健康护理专家担任顾问。此指南在以下两个片段中简要讨论了比卡鲁胺:
|
||||
2022 年 9 月,[世界跨性别人士健康专业协会][wpath](WPATH)发布了第八版《[跨性别及性别多元化人群健康护理标准][soc8]》(SOC8)<sup>([Coleman et al., 2022][c22])</sup>。该《标准》是现有最权威的跨性别护理指南之一,由健康护理专家担任顾问。此指南在以下两个片段中简要讨论了比卡鲁胺:
|
||||
|
||||
> 比卡鲁胺是一种抗雄制剂,用于治疗前列腺癌。其竞争性结合于雄激素受体,从而阻止雄激素与受体结合。有关比卡鲁胺用于女性倾向跨性别群体的数据非常稀少,其安全性资料也很缺乏。有一项小型研究探索了将 50 mg/天的比卡鲁胺作为青春期阻断剂,用于 23 名无法获得 GnRH 类似物治疗的青少年女性倾向跨性别者<sup>(Neyman et al., 2019)</sup>。这 23 人均发生了乳房发育——这与接受比卡鲁胺治疗的前列腺癌患者的普遍现象一致。
|
||||
比卡鲁胺已被指出可引起罕见的暴发性肝中毒,并导致死亡<sup>(O’Bryant et al., 2008)</sup>。考虑到比卡鲁胺用于女性倾向跨性别者的情况尚未得到充分研究,我们并不推荐其用于常规治疗。
|
||||
> 比卡鲁胺是一种抗雄制剂,用于治疗前列腺癌。其竞争性结合于雄激素受体,从而阻止雄激素与受体结合。有关比卡鲁胺用于女性倾向跨性别群体的数据非常稀少,其安全性资料也很缺乏。有一项小型研究探索了将 50 mg/天的比卡鲁胺作为青春期阻断剂,用于 23 名无法获得 GnRH 类似物治疗的青少年女性倾向跨性别者<sup>(Neyman et al., 2019)</sup>。这 23 人均发生了乳房发育——这与接受比卡鲁胺治疗的前列腺癌患者的普遍现象一致。\
|
||||
> 比卡鲁胺已被指出可引起罕见的暴发性肝中毒,并导致死亡<sup>(O’Bryant et al., 2008)</sup>。考虑到比卡鲁胺用于女性倾向跨性别者的情况尚未得到充分研究,我们并不推荐其用于常规治疗。
|
||||
|
||||
> 在药物的选择上,我们建议采用已被研究用于多名跨性别者的药物(如雌激素、醋酸环丙孕酮与 GnRH 激动剂),而非鲜少或从未经过有同行评议的科学研究的药物(如比卡鲁胺、直肠给药的孕酮等)<sup>(Angus et al., 2021; Butler et al., 2017; Efstathiou et al., 2019; Tosun et al., 2019)</sup>。
|
||||
|
||||
如上文所述,由于缺乏相关研究、且有潜在风险,《标准》并未建议将比卡鲁胺用于女性倾向跨性别者的常规治疗。本文也已提到,在比卡鲁胺得到主流《跨性别护理指南》的认可之前,可能还需要更多研究探索其用于女性倾向跨性别者的情况。
|
||||
|
||||
## 参考文献
|
||||
## 参考文献 {#references}
|
||||
|
||||
略
|
||||
- Anderson, J. (2003). The role of antiandrogen monotherapy in the treatment of prostate cancer. _BJU International_, _91_(5), 455–461. \[DOI:<https://doi.org/10.1046/j.1464-410X.2003.04026.x>\]
|
||||
- Arya, V. B., & Davies, J. H. (2019). Idiopathic gonadotropin-independent precocious puberty - is regular surveillance required? _Journal of Pediatric Endocrinology & Metabolism: JPEM_, _32_(4), 403–407. \[DOI:<https://doi.org/10.1515/jpem-2018-0419>\]
|
||||
- Asscheman, H., Gooren, L. J., & Peereboom-Wynia, J. D. (1989). Reduction in undesired sexual hair growth with anandron in male-to-female transsexuals—experiences with a novel androgen receptor blocker. _Clinical and Experimental Dermatology_, _14_(5), 361–363. \[DOI:<https://doi.org/10.1111/j.1365-2230.1989.tb02585.x>\]
|
||||
- Asscheman, H., & Gooren, L. J. (1992). Hormone Treatment in Transsexuals. In Bocking, W. O., Coleman, E. (Eds). _Gender Dysphoria: Interdisciplinary Approaches in Clinical Management_ (pp. 39–54). Binghamton: Haworth Press. / _Journal of Psychology & Human Sexuality_, _5_(4), 39–54. \[[Google Scholar](https://scholar.google.com/scholar?cluster=3926911364428297742)\] \[[Google Books](https://books.google.com/books?id=fny-DwAAQBAJ&pg=PT38)\] \[DOI:<https://doi.org/10.1300/J056v05n04_03>\]
|
||||
- AstraZeneca. (2008). _Clinical Review. NDA. 22-310/S-001. Casodex (bicalutamide) for Testotoxicosis._ Food and Drug Administration/AstraZeneca Pharmaceuticals. \[[URL](https://www.fda.gov/media/75809/)\] \[[PDF](https://www.fda.gov/media/75809/download)\]
|
||||
- Bahceci, M., Tuzcu, A., Canoruc, N., Tuzun, Y., Kidir, V., & Aslan, C. (2004). Serum C-reactive protein (CRP) levels and insulin resistance in non-obese women with polycystic ovarian syndrome, and effect of bicalutamide on hirsutism, CRP levels and insulin resistance. _Hormone Research in Paediatrics_, _62_(6), 283–287. \[DOI:<https://doi.org/10.1159/000081973>\]
|
||||
- Blackledge, G. R. P. (1996). Clinical progress with a new antiandrogen, Casodex™ (bicalutamide). _European Urology_, _29_(Suppl 2), 96–104. \[DOI:<https://doi.org/10.1159/000473847>\]
|
||||
- Cocchetti, C., Ristori, J., Romani, A., Maggi, M., & Fisher, A. D. (2020). Hormonal Treatment Strategies Tailored to Non-Binary Transgender Individuals. _Journal of Clinical Medicine_, _9_(6), 1609. \[DOI:<https://doi.org/10.3390/jcm9061609>\]
|
||||
- Dahl, M., Feldman, J. L., Goldberg, J. M., & Jaberi, A. (2006). Physical aspects of transgender endocrine therapy. _International Journal of Transgenderism_, _9_(3–4), 111–134. \[DOI:<https://doi.org/10.1300/J485v09n03_06>\]
|
||||
- Dahl, M., Feldman, J. L., Goldberg, J., & Jaberi, A. (2006). _Endocrine Therapy for Transgender Adults in British Columbia: Suggested Guidelines. Physical Aspects of Transgender Endocrine Therapy._ Vancouver: Vancouver Coastal Health. \[[Google Scholar](https://scholar.google.com/scholar?cluster=10288793516023166968)\] \[[PDF](https://www.cpath.ca/wp-content/uploads/2009/12/guidelines-endocrine.pdf)\]
|
||||
- de Voogt, H. J., Rao, B. R., Gooren, L. J. G., Geldof, A. A., & Bouman, F. G. (1987). Considerations About the Use of Anti-Androgenic Drugs in Male-to-Female Transsexuals. _Tenth International Symposium on Gender Dysphoria, Diagnosis and Treatment of Transsexualism, Vrije Universiteit Amsterdam, The Netherlands, June 9–12, 1987._ Harry Benjamin International Gender Dysphoria Association. \[[PDF](https://kinseyinstitute.org/pdf/HBIGDA_S10_1987OCR.pdf#page=55)\]
|
||||
- de Voogt, H. J., Rao, B. R., Geldof, A. A., Gooren, L. J. G., & Bouman, F. G. (1987). Androgen action blockade does not result in reduction in size but changes histology of the normal human prostate. _The Prostate_, _11_(4), 305–311. \[DOI:<https://doi.org/10.1002/pros.2990110403>\]
|
||||
- Deutsch, M. B. (2016). Overview of feminizing hormone therapy. In Deutsch, M. B. (Ed.). _Guidelines for the Primary and Gender-Affirming Care of Transgender and Gender Nonbinary People, 2nd Edition_ (pp. 26–48). San Francisco: University of California, San Francisco/UCSF Transgender Care. \[[URL](https://transcare.ucsf.edu/guidelines/feminizing-hormone-therapy)\] \[[PDF](https://transcare.ucsf.edu/sites/transcare.ucsf.edu/files/Transgender-PGACG-6-17-16.pdf#page=26)\]
|
||||
- Fernandez-Nieto, D., Saceda-Corralo, D., Rodrigues-Barata, R., Hermosa-Gelbard, A., Moreno-Arrones, O., Jimenez-Cauhe, J., Ortega-Quijano, D., & Vano-Galvan, S. (2019). Oral bicalutamide for female pattern hair loss: A pilot study. _Dermatologic Therapy_, _32_(6), e13096. \[DOI:<https://doi.org/10.1111/dth.13096>\]
|
||||
- Fernandez-Nieto, D., Saceda-Corralo, D., Jimenez-Cauhe, J., Moreno-Arrones, O. M., Rodrigues-Barata, R., Hermosa-Gelbard, A., & Vano-Galvan, S. (2020). Bicalutamide: A potential new oral antiandrogenic drug for female pattern hair loss. _Journal of the American Academy of Dermatology_, _83_(5), e355–e356. \[DOI:<https://doi.org/10.1016/j.jaad.2020.04.054>\]
|
||||
- Finkle, A., Zavertnik, S., Myers, S., Cormier, D., Heithaus, J., & Augustyn, M. (2020). Growing Up Fast: Managing Autism Spectrum Disorder and Precocious Puberty. _Journal of Developmental and Behavioral Pediatrics: JDBP_, _41_(9), 740–742. \[DOI:<https://doi.org/10.1097/DBP.0000000000000865>\]
|
||||
- Fishman, S. L., Paliou, M., Poretsky, L., & Hembree, W. C. (2019). Endocrine Care of Transgender Adults. In Poretsky, L., & Hembree, W. C. (Eds.). _Transgender Medicine_ (pp. 143–163). Cham: Humana Press. \[DOI:<https://doi.org/10.1007/978-3-030-05683-4_8>\]
|
||||
- Food and Drug Administration (FDA). (2017). _CASODEX (bicalutamide) tablet, for oral use._ \[[URL](https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=020498)\] \[[PDF](https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/020498s028lbl.pdf)\]
|
||||
- Gooren, L., Spinder, T., Spijkstra, J. J., Van Kessel, H., Smals, A., Rao, B. R., & Hoogslag, M. (1987). Sex steroids and pulsatile luteinizing hormone release in men. Studies in estrogen-treated agonadal subjects and eugonadal subjects treated with a novel nonsteroidal antiandrogen. _The Journal of Clinical Endocrinology & Metabolism_, _64_(4), 763–770. \[DOI:<https://doi.org/10.1210/jcem-64-4-763>\]
|
||||
- Gooren, L. J. G. (1999). Hormonal Sex Reassignment. _International Journal of Transgenderism_, _3_(3), 1–7. \[[Google Scholar](https://scholar.google.com/scholar?cluster=1501455977722930279)\] \[[URL](http://web.archive.org/web/20070430161048/http://www.symposion.com/ijt/ijt990301.htm)\] \[[Alt](http://www.tgmeds.org.uk/hormonal-sex-reassignment.html)\]
|
||||
- Gooren, L. J. (2011). Care of transsexual persons. _New England Journal of_ Medicine, _364_(13), 1251–1257. \[DOI:<https://doi.org/10.1056/NEJMcp1008161>\]
|
||||
- Graham, D. J., Ahmad, S. R., & Piazza‐Hepp, T. (2002). Spontaneous Reporting—USA. In Mann, R. D., & Andrews, E. B. (Eds.). _Pharmacovigilance_ (pp. 219–227). Chichester: John Wiley & Sons. \[DOI:<https://doi.org/10.1002/0470853093.ch17>\]
|
||||
- Gurnurkar, S., DiLillo, E., & Carakushansky, M. (2021). A Case of Familial Male-limited Precocious Puberty with a Novel Mutation. _Journal of Clinical Research in Pediatric Endocrinology_, _13_(2), 239–244. \[DOI:<https://doi.org/10.4274/jcrpe.galenos.2020.2020.0067>\]
|
||||
- Haddad, N. G., & Eugster, E. A. (2012). Peripheral Precocious Puberty: Interventions to Improve Growth. In Preedy, V. R. (Ed.). _Handbook of Growth and Growth Monitoring in Health and Disease_ (pp. 1199–1212). New York: Springer. \[DOI:<https://doi.org/10.1007/978-1-4419-1795-9_71>\]
|
||||
- Hamidi, O., & Davidge-Pitts, C. J. (2019). Transfeminine Hormone Therapy. _Endocrinology and Metabolism Clinics_, _48_(2), 341–355. \[DOI:<https://doi.org/10.1016/j.ecl.2019.02.001>\]
|
||||
- Hembree, W. C., Cohen-Kettenis, P., Delemarre-Van De Waal, H. A., Gooren, L. J., Meyer III, W. J., Spack, N. P., Tangpricha, V., & Montori, V. M. (2009). Endocrine treatment of transsexual persons: an Endocrine Society clinical practice guideline. _The Journal of Clinical Endocrinology & Metabolism_, _94_(9), 3132–3154. \[DOI:<https://doi.org/10.1210/jc.2009-0345>\]
|
||||
- Hembree, W. C., Cohen-Kettenis, P. T., Gooren, L., Hannema, S. E., Meyer, W. J., Murad, M. H., Rosenthal, S. M., Safer, J. D., Tangpricha, V., & T’Sjoen, G. G. (2017). Endocrine Treatment of Gender-Dysphoric/Gender-Incongruent Persons: An Endocrine Society Clinical Practice Guideline. _The Journal of Clinical Endocrinology and Metabolism_, _102_(11), 3869–3903. \[DOI:<https://doi.org/10.1210/jc.2017-01658>\] \[[PDF](https://academic.oup.com/jcem/article-pdf/102/11/3869/21533864/jc.2017-01658.pdf)\]
|
||||
- Ismail, F. F., Meah, N., de Carvalho, L. T., Bhoyrul, B., Wall, D., & Sinclair, R. (2020). Safety of oral bicalutamide in female pattern hair loss: A retrospective review of 316 patients. _Journal of the American Academy of Dermatology_, _83_(5), 1478–1479. \[DOI:<https://doi.org/10.1016/j.jaad.2020.03.034>\]
|
||||
- Israel, G. E., & Tarver, D. E. (1997). _Transgender Care: Recommended Guidelines, Practical Information, and Personal Accounts_ (p. 66). Philadelphia: Temple University Press. \[[Google Scholar](https://scholar.google.com/scholar?cluster=5451071852495304201)\] \[[Google Books](https://books.google.com/books?id=IlPX6E5glDEC&pg=PA66)\]
|
||||
- Iversen, P., Johansson, J. E., Lodding, P., Lukkarinen, O., Lundmo, P., Klarskov, P., Tammela, T. L., Tasdemir, I., Morris, T., Carroll, K., & Scandinavian Prostatic Cancer Group (2004). Bicalutamide (150 mg) versus placebo as immediate therapy alone or as adjuvant to therapy with curative intent for early nonmetastatic prostate cancer: 5.3-year median followup from the Scandinavian Prostate Cancer Group Study Number 6. _The Journal of Urology_, _172_(5 Part 1), 1871–1876. \[DOI:<https://doi.org/10.1097/01.ju.0000139719.99825.54>\]
|
||||
- Iwamoto, S. J., Defreyne, J., Rothman, M. S., Van Schuylenbergh, J., Van de Bruaene, L., Motmans, J., & T’Sjoen, G. (2019). Health considerations for transgender women and remaining unknowns: a narrative review. _Therapeutic Advances in Endocrinology and Metabolism_, _10_, 2042018819871166. \[DOI:[10.1177/2042018819871166](https://doi.org/10.1177%2F2042018819871166)\]
|
||||
- Johannes, F. L. M., van Kemenade, M. A., Cohen-Kettenis, P. T., Cohen, L., & Gooren, L. J. G. (1987). Effects of RU 23.903 (Anandron) on Lateralization and Spatial Ability in Male-to-Female-Transsexuals. _Tenth International Symposium on Gender Dysphoria, Diagnosis and Treatment of Transsexualism, Vrije Universiteit Amsterdam, The Netherlands, June 9–12, 1987._ Harry Benjamin International Gender Dysphoria Association. \[[PDF](https://kinseyinstitute.org/pdf/HBIGDA_S10_1987OCR.pdf#page=35)\]
|
||||
- Kolvenbag, G. J., & Blackledge, G. R. (1996). Worldwide activity and safety of bicalutamide: a summary review. _Urology_, _47_(1), 70–79. \[DOI:<https://doi.org/10.1016/S0090-4295(96)80012-4>\]
|
||||
- Kor, Y. (2018). Central precocious puberty in a case of late-diagnosed familial testotoxicosis and long-term treatment monitoring. _Hormones_, _17_(2), 275–278. \[DOI:<https://doi.org/10.1007/s42000-018-0029-1>\]
|
||||
- Kreher, N. C., Pescovitz, O. H., Delameter, P., Tiulpakov, A., & Hochberg, Z. E. (2006). Treatment of familial male-limited precocious puberty with bicalutamide and anastrozole. _The Journal of Pediatrics_, _149_(3), 416–420. \[DOI:<https://doi.org/10.1016/j.jpeds.2006.04.027>\]
|
||||
- Lenz, A. M., Shulman, D., Eugster, E. A., Rahhal, S., Fuqua, J. S., Pescovitz, O. H., & Lewis, K. A. (2010). Bicalutamide and third-generation aromatase inhibitors in testotoxicosis. _Pediatrics_, _126_(3), e728–e733. \[DOI:<https://doi.org/10.1542/peds.2010-0596>\]
|
||||
- Levy, A., Crown, A., & Reid, R. (2003). Endocrine intervention for transsexuals. _Clinical Endocrinology_, _59_(4), 409–418. \[DOI:<https://doi.org/10.1046/j.1365-2265.2003.01821.x>\]
|
||||
- Lewis, K. A., Lenz, A., Eugster, E. A., Fuqua, J. S., Pescovitz, O. H., Rahhal, S., & Shulman, D. (2009). Long term bicalutamide and 3rd generation aromatase inhibitor therapy in two boys with testotoxicosis. _Hormone Research \[in Paediatrics\]_, _72_(Suppl 3), 266–267 (PO2-189). \[[Google Scholar](https://scholar.google.com/scholar?cluster=5540864211259664143)\] \[DOI:<https://doi.org/10.1159/000239668>\]
|
||||
- Manso, G., Thole, Z., Salgueiro, E., Revuelta, P., & Hidalgo, A. (2006). Spontaneous reporting of hepatotoxicity associated with antiandrogens: data from the Spanish pharmacovigilance system. _Pharmacoepidemiology and Drug Safety_, _15_(4), 253–259. \[DOI:<https://doi.org/10.1002/pds.1168>\]
|
||||
- McLeod, D. G. (1997). Tolerability of Nonsteroidal Antiandrogens in the Treatment of Advanced Prostate Cancer. _The Oncologist_, _2_(1), 18–27. \[DOI:<https://doi.org/10.1634/theoncologist.2-1-18>\]
|
||||
- Michigan Medicine. (2020). _Feminizing Gender-Affirming Hormone Care: The Michigan Medicine Approach._ Ann Arbor: Michigan Medicine/University of Michigan. \[[URL](https://medicine.umich.edu/dept/obgyn/education/continuing-medical-education-cme/transgender-healthcare-curriculum)\] \[[PDF](http://www.med.umich.edu/1libr/ComprehensiveGenderServicesProgram/MMapproachFemGenderAffirmingHormones.pdf)\]
|
||||
- Mitchell, F. (2020). Guy T’Sjoen: collaborating to improve transgender wellbeing. _The Lancet Diabetes & Endocrinology_, _8_(7), 568–568. \[DOI:<https://doi.org/10.1016/S2213-8587(20)30192-3>\]
|
||||
- Mitre, N., & Lteif, A. (2009). Treatment of familial male-limited precocious puberty (testotoxicosis) with anastrozole and bicalutamide in a boy with a novel mutation in the luteinizing hormone receptor. _Journal of Pediatric Endocrinology and Metabolism_, _22_(12), 1163–1168. \[DOI:<https://doi.org/10.1515/JPEM.2009.22.12.1163>\]
|
||||
- Moreno-Pérez, Ó., De Antonio, I. E., & Grupo de Identidad y Diferenciación Sexual de la SEEN (GIDSEEN. (2012). Clinical practice guidelines for assessment and treatment of transsexualism. SEEN Identity and Sexual Differentiation Group (GIDSEEN). _Endocrinología y Nutrición (English Edition)_, _59_(6), 367–382. \[DOI:<https://doi.org/10.1016/j.endoen.2012.07.004>\]
|
||||
- Moretti, C. G., Guccione, L., Di Giacinto, P., Cannuccia, A., Meleca, C., Lanzolla, G., Andreadi, A., & Lauro, D. (2016). Efficacy and Safety of Myo-Inositol Supplementation in the Treatment of Obese Hirsute PCOS Women: Comparative Evaluation with OCP+Bicalutamide Therapy. _Endocrine Reviews_, _37_(2 Suppl 1) (SUN-153). \[[URL](https://endo.confex.com/endo/2016endo/webprogram/Paper26631.html)\] \[DOI:<https://doi.org/10.1093/edrv/37.supp.1>\]
|
||||
- Moretti, C., Guccione, L., Di Giacinto, P., Simonelli, I., Exacoustos, C., Toscano, V., Motta, C., De Leo, V., Petraglia, F., & Lenzi, A. (2018). Combined oral contraception and bicalutamide in polycystic ovary syndrome and severe hirsutism: a double-blind randomized controlled trial. _The Journal of Clinical Endocrinology & Metabolism_, _103_(3), 824–838. \[DOI:<https://doi.org/10.1210/jc.2017-01186>\]
|
||||
- Moussa, A., Kazmi, A., Bokhari, L., & Sinclair, R. D. (2021). Bicalutamide improves minoxidil-induced hypertrichosis in female pattern hair loss: A retrospective review of 35 patients. _Journal of the American Academy of Dermatology_, online ahead of print. \[DOI:<https://doi.org/10.1016/j.jaad.2021.10.048>\]
|
||||
- Muderris, I. I., Bayram, F., & Guven, M. (1999). Bicalutamide 25 mg/day in the treatment of hirsutism. _Human Reproduction_, _14_(Suppl 3), 366–366 (R-196). \[DOI:<https://doi.org/10.1093/humrep/14.Suppl_3.366-a>\]
|
||||
- Müderris, I. I., Bayram, F., Özçelik, B., & Güven, M. (2002). New alternative treatment in hirsutism: bicalutamide 25 mg/day. _Gynecological Endocrinology_, _16_(1), 63–66. \[DOI:<https://doi.org/10.1080/gye.16.1.63.66>\]
|
||||
- Müderris, İ. İ., & Öner, G. (2009). Hirsutizm Tedavisinde Flutamid ve Bikalutamid Kullanımı. \[Flutamide and Bicalutamide Treatment in Hirsutism.\] _Türkiye Klinikleri Endokrinoloji-Özel Dergisi_, _2_(2), 110–112. \[ISSN:[1308-0954](https://portal.issn.org/resource/ISSN/1308-0954)\] \[[URL](https://www.turkiyeklinikleri.com/article/en-hirsutizm-tedavisinde-flutamid-ve-bikalutamid-kullanimi-55753.html)\] \[[PDF](https://files.transfemscience.org/pdfs/M%C3%BCderris%20&%20%C3%96ner%20(2009)%20-%20Hirsutizm%20Tedavisinde%20Flutamid%20ve%20Bikalutamid%20Kullan%C4%B1m%C4%B1%20%5BFlutamide%20and%20Bicalutamide%20Treatment%20in%20Hirsutism%5D.pdf)\] \[[Translation](https://docs.google.com/document/d/1jwdHS1kUQk4pm4J1xVTtUehiFnrkIkpTMO1D1yI7fpI/view)\]
|
||||
- Nabhan, Z. M., & Eugster, E. A. (2019). Testotoxicosis with an episodic course: an unusual case within a series. _AACE Clinical Case Reports_, _5_(1), e50–e53. \[DOI:<https://doi.org/10.4158/ACCR-2018-0246>\]
|
||||
- Neyman, A., Fuqua, J. S., & Eugster, E. A. (2017). Bicalutamide as an Androgen Blocker with Secondary Effect of Promoting Feminization in Male to Female (MTF) Transgender Adolescents. 10th Individual Abstracts for International Meeting of Pediatric Endocrinology: Free Communication and Poster Sessions, Abstracts. _Hormone Research in Paediatrics_, _88_(Suppl 1), 1–628 (477; P3-605). \[DOI:<https://doi.org/10.1159/000481424>\] \[[PDF](https://files.transfemscience.org/pdfs/Neyman,%20Fuqua,%20&%20Eugster%20(2017)%20-%20Bicalutamide%20as%20an%20Androgen%20Blocker%20with%20Secondary%20Effect%20of%20Promoting%20Feminization%20in%20Male%20to%20Female%20(MTF)%20Transgender%20Adolescents.pdf#page=4)\]
|
||||
- Neyman, A., Fuqua, J. S., & Eugster, E. A. (2019). Bicalutamide as an androgen blocker with secondary effect of promoting feminization in male-to-female transgender adolescents. _Journal of Adolescent Health_, _64_(4), 544–546. \[DOI:<https://doi.org/10.1016/j.jadohealth.2018.10.296>\]
|
||||
- Özcabı, B., Ceylaner, S., Özcan, R., Büyükünal, C., Ercan, O., Tüysüz, B., & Evliyaoğlu, O. (2015). Testotoxicosis: Report of Two Cases, One with a Novel Mutation in LHCGR Gene. _Journal of Clinical Research in Pediatric Endocrinology_, _7_(3), 242–248. \[DOI:<https://doi.org/10.4274/jcrpe.2067>\]
|
||||
- Randolph Jr, J. F. (2018). Gender-Affirming Hormone Therapy for Transgender Females. _Clinical Obstetrics and Gynecology_, _61_(4), 705–721. \[DOI:<https://doi.org/10.1097/GRF.0000000000000396>\] \[[URL](https://www.ingentaconnect.com/content/wk/cobg/2018/00000061/00000004/art00008)\]
|
||||
- Rao, B. R., De Voogt, H. J., Geldof, A. A., Gooren, L. J. G., & Bouman, F. G. (1988). Merits and considerations in the use of anti-androgen. _Journal of Steroid Biochemistry_, _31_(4), 731–737. \[DOI:<https://doi.org/10.1016/0022-4731(88)90024-6>\]
|
||||
- Reiter, E. O., Mauras, N., McCormick, K., Kulshreshtha, B., Amrhein, J., De Luca, F., O’Brien, S., Armstrong, J., & Melezinkova, H. (2010). Bicalutamide plus anastrozole for the treatment of gonadotropin-independent precocious puberty in boys with testotoxicosis: a phase II, open-label pilot study (BATT). _Journal of Pediatric Endocrinology & Metabolism: JPEM_, _23_(10), 999–1009. \[DOI:<https://doi.org/10.1515/jpem.2010.161>\]
|
||||
- Schellhammer, P. F., Sharifi, R., Block, N. L., Soloway, M. S., Venner, P. M., Patterson, A. L., Sarosdy, M. F., Vogelzang, N. J., Schellenger, J. J., Kolvenbag, G. J., & Casodex Combination Study Group (1997). Clinical benefits of bicalutamide compared with flutamide in combined androgen blockade for patients with advanced prostatic carcinoma: final report of a double-blind, randomized, multicenter trial. _Urology_, _50_(3), 330–336. \[DOI:<https://doi.org/10.1016/s0090-4295(97)00279-3>\]
|
||||
- See, W. A., Wirth, M. P., McLeod, D. G., Iversen, P., Klimberg, I., Gleason, D., Chodak, G., Montie, J., Tyrrell, C., Wallace, D. M., Delaere, K. P., Vaage, S., Tammela, T. L., Lukkarinen, O., Persson, B. E., Carroll, K., Kolvenbag, G. J., & Casodex Early Prostate Cancer Trialist Group (2002). Bicalutamide as immediate therapy either alone or as adjuvant to standard care of patients with localized or locally advanced prostate cancer: first analysis of the early prostate cancer program. _The Journal of Urology_, _168_(2), 429–435. \[DOI:<https://doi.org/10.1016/S0022-5347(05)64652-6>\]
|
||||
- Stenger, P. J., Wagner, L., Egelhoff, J., & Rose, S. R. (2009). Bicalutamide and letrozole treatment of precocious puberty due to elevated levels of human chorionic gonadotropin (hCG). _Hormone Research_ \[_in Paediatrics_\], _72_(Suppl 3), 391–391 (PO3-149). \[[Google Scholar](https://scholar.google.com/scholar?cluster=9944726539277415138)\] \[DOI:<https://doi.org/10.1159/000239668>\]
|
||||
- Tessaris, D., Matarazzo, P., Mussa, A., Tuli, G., Verna, F., Fiore, L., & Lala, R. (2012). Combined treatment with bicalutamide and anastrozole in a young boy with peripheral precocious puberty due to McCune-Albright Syndrome. _Endocrine Journal_, _59_(2), 111–117. \[DOI:<https://doi.org/10.1507/endocrj.ej11-0214>\]
|
||||
- Thole, Z., Manso, G., Salgueiro, E., Revuelta, P., & Hidalgo, A. (2004). Hepatotoxicity induced by antiandrogens: a review of the literature. _Urologia Internationalis_, _73_(4), 289–295. \[DOI:<https://doi.org/10.1159/000081585>\]
|
||||
- Thompson, J., Hopwood, R. A., deNormand, S., & Cavanaugh, T. (2021). _Medical Care of Trans and Gender Diverse Adults._ Boston: Fenway Health. \[[URL](https://www.lgbtqiahealtheducation.org/publication/medical-care-of-trans-and-gender-diverse-adults-2021/)\] \[[PDF](https://www.lgbtqiahealtheducation.org/wp-content/uploads/2021/07/Medical-Care-of-Trans-and-Gender-Diverse-Adults-Spring-2021.pdf)\]
|
||||
- Tomson, A., McLachlan, C., Wattrus, C., Adams, K., Addinall, R., Bothma, R., Jankelowitz, L., Kotze, E., Luvuno, Z., Madlala, N., Matyila, S., Padavatan, A., Pillay, M., Rakumakoe, M. D., Tomson-Myburgh, M., Venter, W., & de Vries, E. (2021). Southern African HIV Clinicians’ Society gender-affirming healthcare guideline for South Africa. _Southern African Journal of HIV Medicine_, _22_(1), a1299. \[DOI:<https://doi.org/10.4102/sajhivmed.v22i1.1299>\] \[[PDF](https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8517808/pdf/HIVMED-22-1299.pdf)\]
|
||||
- van Kemenade, J. F., Cohen-Kettenis, P. T., Cohen, L., & Gooren, L. J. (1989). Effects of the pure antiandrogen RU 23.903 (anandron) on sexuality, aggression, and mood in male-to-female transsexuals. _Archives of Sexual Behavior_, _18_(3), 217–228. \[DOI:<https://doi.org/10.1007/BF01543196>\]
|
||||
|
||||
[alyw19_lit]: https://transfemscience.org/articles/bica-literature/
|
||||
[g11]: http://doi.org/10.1056/NEJMcp1008161
|
||||
|
|
@ -143,7 +218,7 @@
|
|||
[gap02]: https://doi.org/10.1002/0470853093.ch17
|
||||
[d16]: https://transcare.ucsf.edu/guidelines
|
||||
[alyw19_dose]: https://transfemscience.org/articles/bica-dosage/
|
||||
[alyw20_meni]: cpa-meningioma.md
|
||||
[alyw20_meni]: https://transfemscience.org/articles/cpa-meningioma/
|
||||
[a03]: https://doi.org/10.1046/j.1464-410X.2003.04026.x
|
||||
[i04]: https://doi.org/10.1097/01.ju.0000139719.99825.54
|
||||
[b96]: https://doi.org/10.1159/000473847
|
||||
|
|
@ -1,77 +1,95 @@
|
|||
# 关于女性化激素疗法与乳腺癌风险的简述
|
||||
---
|
||||
title: 关于女性化激素疗法与乳腺癌风险的简述
|
||||
linkTitle: 女性化激素疗法与乳腺癌风险
|
||||
description: >-
|
||||
长期使用雌激素与孕激素会极大提高患乳腺癌的风险。此外 X 染色体也可显著影响乳腺癌风险。
|
||||
author: Aly W.
|
||||
published: 2020-04-25
|
||||
updated: 2022-11-26
|
||||
translated: 2022-11-28
|
||||
translators:
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 用药安全
|
||||
- 雌激素
|
||||
- 孕激素
|
||||
trackHash: 7378b09b623aaedc898e8e60a30a5035fb5d10d2
|
||||
---
|
||||
|
||||
> **作者:[Aly W.][AUTHOR]**
|
||||
> - 首次发表于 2020 年 4 月 25 日
|
||||
> - 最后修改于 2022 年 1 月 27 日
|
||||
> - [原文出处](https://transfemscience.org/articles/breast-cancer/)
|
||||
>
|
||||
> **译者:[Bersella AI][TRANSLATOR]**
|
||||
> - 翻译于 2022 年 8 月 28 日
|
||||
|
||||
## 译者按
|
||||
## 译者按 {#notice}
|
||||
|
||||
1. 一些机构名称的链接,从维基百科的介绍页改为其官方网站。其余链接未作变动。
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
--------
|
||||
---
|
||||
|
||||
## 前言
|
||||
## 前言 {#introduction}
|
||||
|
||||
雌激素与孕激素可促进人类乳房发育。其中,雌激素在青春期乳房发育当中居主导作用;而孕激素在怀孕期间为准备泌乳和母乳喂养而产生的乳房变化当中居主导作用。较之于顺性别男性,乳腺癌在顺性别妇女当中尤其更为常见;激素被广泛认为是引起顺性别妇女的乳腺癌并发展的因素所在。据此可以合理推断:女性倾向跨性别者的激素疗法或可增加乳腺癌发病风险。本文就此观点以及既有相关研究项目进行论述。
|
||||
|
||||
## 乳腺癌风险相关因素:性别与年龄
|
||||
## 乳腺癌风险相关因素:性别与年龄 {#sex-and-age-as-breast-cancer-risk-factors}
|
||||
|
||||
对妇女而言,其患乳腺癌的终生概率通常约为 12.5%(即每 8 人有一人罹患)<sup>([Ban & Godellas, 2014][BG14])</sup>;而男性患病概率通常约为 0.1%(即每 1000 人有一人罹患)<sup>([Yousef, 2017][Y17])</sup>。男性乳腺癌的综合年化发病率约为每 100,000 人/年一例<sup>(Yousef, 2017; [Ottini & Capalbo, 2017][OC17])</sup>。在所有乳腺癌病例当中,男性占比不足 1%<sup>(Yousef, 2017; [Sun et al., 2017][S17])</sup>。综上,乳腺癌在妇女当中较常见,但在男性当中极为罕见。
|
||||
对妇女而言,其患乳腺癌的终生概率通常约为 12.5%(即每 8 人有一人罹患)<sup>([Ban & Godellas, 2014][bg14])</sup>;而男性患病概率通常约为 0.1%(即每 1000 人有一人罹患)<sup>([Yousef, 2017][y17])</sup>。男性乳腺癌的综合年化发病率约为每 100,000 人/年一例<sup>(Yousef, 2017; [Ottini & Capalbo, 2017][oc17])</sup>。在所有乳腺癌病例当中,男性占比不足 1%<sup>(Yousef, 2017; [Sun et al., 2017][s17])</sup>。综上,乳腺癌在妇女当中较常见,但在男性当中极为罕见。
|
||||
|
||||
除性别之外,年龄是乳腺癌的已知最大风险因素所在<sup>([Momenimovahed & Salehiniya, 2018][MS18])</sup>。对于绝经前妇女,乳腺癌风险随年龄增长呈指数级上升之势<sup>([Dix & Cohen, 1982][DC82])</sup>。女性乳腺癌风险在 15 岁时约为 1/600,000;在 20 岁时约为 1/75,000;在 30 岁时约为 1/1,500;到了 40 岁则约为 1/175<sup>([Anders et al, 2009][A09])</sup>。在其绝经后(通常在 50 岁),乳腺癌风险仍继续增长,但增幅有所放缓<sup>(Dix & Cohen, 1982; [Benz, 2008][B08]; [Colditz & Rosner, 2000][CR00])</sup>。其原因被认为在于,雌二醇与孕激素水平在绝经后大幅减少<sup>(Dix & Cohen, 1982)</sup>。据估算,如果不曾绝经,女性乳腺癌病例会多出六倍,也即大部分女性终其一生皆会罹患乳腺癌<sup>([Brisken, Hess, & Jeitziner, 2015][BHJ15])</sup>。男性的情况与女性类似,其乳腺癌发病率在大约 65 岁之前呈指数级上升之势,此后变为缓慢上升<sup>(Ottini & Capalbo, 2017; [Cancer Research UK][CRUK])</sup>。这可能和男性更年期及其导致的更低的睾酮与雌二醇水平有关<sup>([Satram, 2006][S06])</sup>。女性的乳腺癌确诊年龄通常在 60 岁左右,而男性通常在 65-70 岁<sup>([Ferzoco & Ruddy, 2016][FR16]; [Giordano, 2018][G18])</sup>。下图展示了女性及男性在不同年龄的乳腺癌发病风险<sup>(Ottini & Capalbo, 2017)</sup>。
|
||||
除性别之外,年龄是乳腺癌的已知最大风险因素所在<sup>([Momenimovahed & Salehiniya, 2018][ms18])</sup>。对于绝经前妇女,乳腺癌风险随年龄增长呈指数级上升之势<sup>([Dix & Cohen, 1982][dc82])</sup>。女性乳腺癌风险在 15 岁时约为 1/600,000;在 20 岁时约为 1/75,000;在 30 岁时约为 1/1,500;到了 40 岁则约为 1/175<sup>([Anders et al, 2009][a09])</sup>。在其绝经后(通常在 50 岁),乳腺癌风险仍继续增长,但增幅有所放缓<sup>(Dix & Cohen, 1982; [Benz, 2008][b08]; [Colditz & Rosner, 2000][cr00])</sup>。其原因被认为在于,雌二醇与孕激素水平在绝经后大幅减少<sup>(Dix & Cohen, 1982)</sup>。据估算,如果不曾绝经,女性乳腺癌病例会多出六倍,也即大部分女性终其一生皆会罹患乳腺癌<sup>([Brisken, Hess, & Jeitziner, 2015][bhj15])</sup>。男性的情况与女性类似,其乳腺癌发病率在大约 65 岁之前呈指数级上升之势,此后变为缓慢上升<sup>(Ottini & Capalbo, 2017; [Cancer Research UK][cruk])</sup>。这可能和男性更年期及其导致的更低的睾酮与雌二醇水平有关<sup>([Satram, 2006][s06])</sup>。女性的乳腺癌确诊年龄通常在 60 岁左右,而男性通常在 65-70 岁<sup>([Ferzoco & Ruddy, 2016][fr16]; [Giordano, 2018][g18])</sup>。下图展示了女性及男性在不同年龄的乳腺癌发病风险<sup>(Ottini & Capalbo, 2017)</sup>。
|
||||
|
||||
> 
|
||||
> 「图一」在不同年龄,男性、女性美国白人每十万人当中的乳腺癌发生率。数据源自美国国家癌症研究所(NCI)的统合监测、流行病学和最终结果项目(SEER,2003-2012年)<sup>(Ottini & Capalbo, 2017)</sup>。需要注意,男、女性所对应的 Y 坐标轴及刻度不同;女性的 Y 坐标轴(左)刻度为男性的 50 倍。
|
||||
<section class="box">
|
||||
|
||||
## 女性的激素暴露量与乳腺癌风险的关系
|
||||

|
||||
|
||||
除性别与年龄之外,有研究还强调了卵巢活动及其分泌的激素(如雌二醇与孕激素)是引起乳腺癌的主要风险因素<sup>([Ban & Godellas, 2014][BG14])</sup>。更晚的初潮、更早的更年期、以及母乳喂养,皆可让乳腺癌风险变得更低,因为上述现象可导致经卵巢分泌的激素总和暴露量更少<sup>(Ban & Godellas, 2014; Momenimovahed & Salehiniya, 2018)</sup>。如果在 40 岁以前摘除卵巢,可将乳腺癌的终生发病风险降低 50%<sup>(Ban & Godellas, 2014)</sup>。
|
||||
对于高患癌风险的已绝经妇女,可长期预防性服用选择性雌激素受体调节剂(SERMs,如三苯氧胺)、芳香化酶抑制剂(AIs,如阿那曲唑)等抗雌激素制剂,以预防乳腺癌;其可降低 50-70% 发病风险<sup>([Mocellin, Goodwin, & Pasquali, 2019][MGP19]; [Nelson et al., 2019][N19])</sup>。
|
||||
在灵长类动物当中,长期使用雌激素与孕激素疗法被发现可引起乳腺癌,而高剂量则让发病年龄较常规更早<sup>([Cline, 2007][C07])</sup>。
|
||||
**图 1**:在不同年龄,男性、女性美国白人每十万人当中的乳腺癌发生率。数据源自美国国家癌症研究所(NCI)的统合监测、流行病学和最终结果项目(SEER,2003-2012 年)<sup>(Ottini & Capalbo, 2017)</sup>。需要注意,男、女性所对应的 Y 坐标轴及刻度不同;女性的 Y 坐标轴(左)刻度为男性的 50 倍。
|
||||
|
||||
除增加乳腺癌发病风险之外,卵巢分泌的性激素还会促进活跃的乳腺癌之发展。抗雌激素制剂可有效治疗活跃当中的乳腺癌<sup>([Lumachi, Santeufemia, & Basso, 2015][LSB15])</sup>;而抗孕激素制剂(如奥那司酮、米非司酮等)亦可在乳腺癌的治疗当中取得初步成效<sup>([Palmieri et al., 2014][P14])</sup>。如患有乳腺癌的妇女服用生理剂量的雌激素,后者可加速肿瘤的发展<sup>([Herrmann, Adair, & Woodard, 1947][HAW47]; [Nathanson, 1947][N47]; [Gellhorn & Jones, 1949][GJ49]; [Nathanson, 1951][N51]; [Pearson et al., 1954][P54]; [Pearson & Lipsett, 1956][PL56]; [Kennedy, 1956][K56]; [Kennedy, 1957][K57]; [Dworin, 1961][D61]; [Kennedy, 1962][K62]; [Green, Sethi, & Lindner, 1964][GSL64]; [Kennedy, 1964][K64]; [Stoll, 1973][S73]; [Forrest, 1989][F89])</sup>。
|
||||
</section>
|
||||
|
||||
和公认的卵巢活动与乳腺癌风险之间关系相关联的是,更年期激素疗法亦可增加更年期、已绝经妇女的乳腺癌发病风险<sup>([乳腺癌激素相关因素合作研究小组(CGHFBC), 2019][CGHF19]; [图表][CGHF19-TABLE])</sup>。单服雌激素、或者合用雌激素与孕激素,皆会增加该风险,而后者增加的幅度更大<sup>(CGHFBC, 2019)</sup>。依据近期一项针对所有已有数据的大型荟萃分析,在更年期激素疗法引起的乳腺癌绝对风险上,单服雌激素达 20 年后,发病率将提高约 1.5 倍,而合用雌、孕可提高约 2.5 倍<sup>(CGHFBC, 2019)</sup>。因此,合用雌、孕疗法的乳腺癌发病风险高于单服雌激素疗法。在此之前,孕激素因其在乳房中对雌激素的拮抗效应,被认为可能对乳腺癌起抑制作用<sup>([Mauvais-Jarvis, Kuttenn, & Gompel, 1986][MKG86]; [Wren & Eden, 1996][WE96]; [Gompel et al., 2002][G02])</sup>;但上述荟萃分析推翻了该假设。
|
||||
美国[“妇女健康倡议”][WHI](WHI)项目似乎也和这种由更年期激素疗法引起的高乳腺癌风险有关系,至少在一项已使用的处方上(即 0.625mg/天的结合雌激素合并 2.5 mg/天的醋酸甲羟孕酮方案);使用该疗法 5 年后,发病风险增加 1.25 倍<sup>([WHI调查员编辑组, WGWHII, 2002][WHI02]; [Chlebowski, Aragaki, & Anderson, 2015][CAA15])</sup>。WHI 是迄今规模最大的激素疗法随机对照试验项目,其为评估关于激素药物所引起的长期健康效应之因果关系提供了宝贵机遇。
|
||||
## 女性的激素暴露量与乳腺癌风险的关系 {#hormone-exposure-in-women-and-breast-cancer-risk}
|
||||
|
||||
为了将更年期激素疗法引起的乳腺癌风险可视化,下图展示了乳腺癌风险和时间的关系;其基于[“护士健康研究”观察性项目][NHS](NHS)的数据与模型<sup>([Colditz & Rozner, 2000][CR00])</sup>。如图所示,更年期激素疗法可导致乳腺癌风险继续维持指数级增长,而该趋势本应在更年期开始之后减缓。
|
||||
除性别与年龄之外,有研究还强调了卵巢活动及其分泌的激素(如雌二醇与孕激素)是引起乳腺癌的主要风险因素<sup>([Ban & Godellas, 2014][bg14])</sup>。更晚的初潮、更早的更年期、以及母乳喂养,皆可让乳腺癌风险变得更低,因为上述现象可导致经卵巢分泌的激素总和暴露量更少<sup>(Ban & Godellas, 2014; Momenimovahed & Salehiniya, 2018)</sup>。如果在 40 岁以前摘除卵巢,可将乳腺癌的终生发病风险降低 50%<sup>(Ban & Godellas, 2014)</sup>。\
|
||||
对于高患癌风险的已绝经妇女,可长期预防性服用选择性雌激素受体调节剂(SERMs,如三苯氧胺)、芳香化酶抑制剂(AIs,如阿那曲唑)等抗雌激素制剂,以预防乳腺癌;其可降低 50-70% 发病风险<sup>([Mocellin, Goodwin, & Pasquali, 2019][mgp19]; [Nelson et al., 2019][n19])</sup>。\
|
||||
在灵长类动物当中,长期使用雌激素与孕激素疗法被发现可引起乳腺癌,而高剂量则让发病年龄较常规更早<sup>([Cline, 2007][c07])</sup>。
|
||||
|
||||
> 
|
||||
> 「图二」随年龄推移,不同激素治疗状态及类型的已绝经妇女的每十万人中乳腺癌年发生率。本图基于“护士健康研究”观察性项目的数据,使用了泊松回归模型。
|
||||
除增加乳腺癌发病风险之外,卵巢分泌的性激素还会促进活跃的乳腺癌之发展。抗雌激素制剂可有效治疗活跃当中的乳腺癌<sup>([Lumachi, Santeufemia, & Basso, 2015][lsb15])</sup>;而抗孕激素制剂(如奥那司酮、米非司酮等)亦可在乳腺癌的治疗当中取得初步成效<sup>([Palmieri et al., 2014][p14])</sup>。如患有乳腺癌的妇女服用生理剂量的雌激素,后者可加速肿瘤的发展<sup>([Herrmann, Adair, & Woodard, 1947][haw47]; [Nathanson, 1947][n47]; [Gellhorn & Jones, 1949][gj49]; [Nathanson, 1951][n51]; [Pearson et al., 1954][p54]; [Pearson & Lipsett, 1956][pl56]; [Kennedy, 1956][k56]; [Kennedy, 1957][k57]; [Dworin, 1961][d61]; [Kennedy, 1962][k62]; [Green, Sethi, & Lindner, 1964][gsl64]; [Kennedy, 1964][k64]; [Stoll, 1973][s73]; [Forrest, 1989][f89])</sup>。
|
||||
|
||||
同结合雌激素、醋酸甲羟孕酮等非生物同质性激素药物类似,诸如雌二醇、孕激素等具有生物同质性的激素,也和乳腺癌风险的增长有关<sup>(CGHFBC, 2019; [图表][CGHF19-TABLE])</sup>。服用雌二醇所造成的乳腺癌风险,和服用结合雌激素的风险并无二致<sup>(CGHFBC, 2019)</sup>。基于现有数据,口服孕激素(5 年以下)与乳腺癌风险的增长并无关联,这和合成孕酮制剂的情况截然相反<sup>(CGHFBC, 2019; [Stute, Wildt, & Neulen, 2018][SWN18]; [Mirkin, 2018][M18]; [Fournier et al., 2007][F07])</sup>。然而,一旦服用超过 5 年,口服孕激素将会助推乳腺癌风险的增长,其增长趋势在幅度上和服用醋酸甲羟孕酮的情况相似<sup>(CGHFBC, 2019; Stute, Wildt, & Neulen, 2018; Mirkin, 2018; Fournier et al., 2007)</sup>。口服孕激素初期相对较低的发病风险,可能与其产生的孕激素水平较低、从而使孕激素效力更低有关<sup>([Kuhl & Schneider, 2013][KS13]; [Davey, 2018][D18]; [维基百科][WIKI-1]; [图表][GRAPH-1])</sup>。因此,在口服孕激素引起的乳腺癌风险之增长足以被准确测定之前,可能需要更长的治疗时间(和/或更大的样本规模)<sup>(Kuhl & Schneider, 2013; Davey, 2018)</sup>。
|
||||
和公认的卵巢活动与乳腺癌风险之间关系相关联的是,更年期激素疗法亦可增加更年期、已绝经妇女的乳腺癌发病风险<sup>([乳腺癌激素相关因素合作研究小组(CGHFBC), 2019][cghf19]; [图表][cghf19-table])</sup>。单服雌激素、或者合用雌激素与孕激素,皆会增加该风险,而后者增加的幅度更大<sup>(CGHFBC, 2019)</sup>。依据近期一项针对所有已有数据的大型荟萃分析,在更年期激素疗法引起的乳腺癌绝对风险上,单服雌激素达 20 年后,发病率将提高约 1.5 倍,而合用雌、孕可提高约 2.5 倍<sup>(CGHFBC, 2019)</sup>。因此,合用雌、孕疗法的乳腺癌发病风险高于单服雌激素疗法。在此之前,孕激素因其在乳房中对雌激素的拮抗效应,被认为可能对乳腺癌起抑制作用<sup>([Mauvais-Jarvis, Kuttenn, & Gompel, 1986][mkg86]; [Wren & Eden, 1996][we96]; [Gompel et al., 2002][g02])</sup>;但上述荟萃分析推翻了该假设。\
|
||||
美国[“妇女健康倡议”][whi](WHI)项目似乎也和这种由更年期激素疗法引起的高乳腺癌风险有关系,至少在一项已使用的处方上(即 0.625mg/天的结合雌激素合并 2.5 mg/天的醋酸甲羟孕酮方案);使用该疗法 5 年后,发病风险增加 1.25 倍<sup>([WHI 调查员编辑组, WGWHII, 2002][whi02]; [Chlebowski, Aragaki, & Anderson, 2015][caa15])</sup>。WHI 是迄今规模最大的激素疗法随机对照试验项目,其为评估关于激素药物所引起的长期健康效应之因果关系提供了宝贵机遇。
|
||||
|
||||
为了将更年期激素疗法引起的乳腺癌风险可视化,下图展示了乳腺癌风险和时间的关系;其基于[“护士健康研究”观察性项目][nhs](NHS)的数据与模型<sup>([Colditz & Rozner, 2000][cr00])</sup>。如图所示,更年期激素疗法可导致乳腺癌风险继续维持指数级增长,而该趋势本应在更年期开始之后减缓。
|
||||
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 2**:随年龄推移,不同激素治疗状态及类型的已绝经妇女的每十万人中乳腺癌年发生率。本图基于“护士健康研究”观察性项目的数据,使用了泊松回归模型。
|
||||
|
||||
</section>
|
||||
|
||||
同结合雌激素、醋酸甲羟孕酮等非生物同质性激素药物类似,诸如雌二醇、孕激素等具有生物同质性的激素,也和乳腺癌风险的增长有关<sup>(CGHFBC, 2019; [图表][cghf19-table])</sup>。服用雌二醇所造成的乳腺癌风险,和服用结合雌激素的风险并无二致<sup>(CGHFBC, 2019)</sup>。基于现有数据,口服孕激素(5 年以下)与乳腺癌风险的增长并无关联,这和合成孕酮制剂的情况截然相反<sup>(CGHFBC, 2019; [Stute, Wildt, & Neulen, 2018][swn18]; [Mirkin, 2018][m18]; [Fournier et al., 2007][f07])</sup>。然而,一旦服用超过 5 年,口服孕激素将会助推乳腺癌风险的增长,其增长趋势在幅度上和服用醋酸甲羟孕酮的情况相似<sup>(CGHFBC, 2019; Stute, Wildt, & Neulen, 2018; Mirkin, 2018; Fournier et al., 2007)</sup>。口服孕激素初期相对较低的发病风险,可能与其产生的孕激素水平较低、从而使孕激素效力更低有关<sup>([Kuhl & Schneider, 2013][ks13]; [Davey, 2018][d18]; [维基百科][wiki-1]; [图表][graph-1])</sup>。因此,在口服孕激素引起的乳腺癌风险之增长足以被准确测定之前,可能需要更长的治疗时间(和/或更大的样本规模)<sup>(Kuhl & Schneider, 2013; Davey, 2018)</sup>。\
|
||||
当下对于非口服途径给药的孕激素对乳腺癌风险的影响,尚无任何现有数据提供<sup>(Stute, Wildt, & Neulen, 2018)</sup>。不过,一些研究者预计,无论是长期服用还是短期暴露,非口服途径、有完全效力的孕激素所引起的乳腺癌风险应和合成孕酮制剂相似<sup>(Kuhl & Schneider, 2013; Davey, 2018)</sup>。
|
||||
|
||||
尽管无论是前瞻性观察研究、还是随机对照试验所得到的证据皆表明,更年期妇女单服雌二醇的疗法可增加乳腺癌风险<sup>(CGHFBC, 2019)</sup>;但是已进行的随机对照试验(即 WHI)并未出现单服雌二醇会增加乳腺癌风险的情况,实际上风险反而大幅*降低* 了——相对风险率(RR)0.77,95% 可信区间 0.64-0.93<sup>(CGHFBC, 2019; [图表][CGHF19-TABLE2])</sup>。为了解释这种矛盾的现象,一些设想被提了出来。例如,在 WHI 项目的随机对照试验当中贡献了绝大部分数据的女性们有些不寻常之处,表现在其开始激素疗法的年龄较高(平均 64 岁)、超重和肥胖程度较大等<sup>(CGHFBC, 2019; [Kuhl, 2005][K05])</sup>。超重或肥胖的女性已处于更高的乳腺癌风险当中,可能不受单雌激素疗法的进一步影响<sup>(Kuhl, 2005)</sup>。此外,失去雌激素来源已有多年的妇女在接受治疗后可能会对其乳腺癌风险产生反常(paradoxical)的抑制效应,这和从更年期起接受治疗的妇女的情况截然相反;从观测数据亦可见之<sup>([Prentice, 2008][P08]; CGHFBC, 2019)</sup>。这种设想被称为“空档假设(gap hypthesis)”<sup>(Palmieri et al., 2014; [Mueck & Ruan, 2011][MR11])</sup>。
|
||||
尽管无论是前瞻性观察研究、还是随机对照试验所得到的证据皆表明,更年期妇女单服雌二醇的疗法可增加乳腺癌风险<sup>(CGHFBC, 2019)</sup>;但是已进行的随机对照试验(即 WHI)并未出现单服雌二醇会增加乳腺癌风险的情况,实际上风险反而大幅*降低* 了——相对风险率(RR)0.77,95% 可信区间 0.64-0.93<sup>(CGHFBC, 2019; [图表][cghf19-table2])</sup>。为了解释这种矛盾的现象,一些设想被提了出来。例如,在 WHI 项目的随机对照试验当中贡献了绝大部分数据的女性们有些不寻常之处,表现在其开始激素疗法的年龄较高(平均 64 岁)、超重和肥胖程度较大等<sup>(CGHFBC, 2019; [Kuhl, 2005][k05])</sup>。超重或肥胖的女性已处于更高的乳腺癌风险当中,可能不受单雌激素疗法的进一步影响<sup>(Kuhl, 2005)</sup>。此外,失去雌激素来源已有多年的妇女在接受治疗后可能会对其乳腺癌风险产生反常(paradoxical)的抑制效应,这和从更年期起接受治疗的妇女的情况截然相反;从观测数据亦可见之<sup>([Prentice, 2008][p08]; CGHFBC, 2019)</sup>。这种设想被称为“空档假设(gap hypthesis)”<sup>(Palmieri et al., 2014; [Mueck & Ruan, 2011][mr11])</sup>。\
|
||||
为验证这些设想,并查明雌激素对更年期乳腺癌风险的影响,尚需更多随机对照试验支持。
|
||||
|
||||
同样反常的是,在一些其它特定情形下,雌激素和/或孕激素的暴露亦可降低乳腺癌风险、抑制乳腺癌发展。例如,年轻妇女(35 岁以下)如怀孕超过 34 周,在短期(十年内)有更高的乳腺癌风险,但长期(20-25 年以上)风险反而变低了;其终生风险可降低至多 50%<sup>([Nichols et al., 2019][NICH19]; [Husby et al., 2018][H18])</sup>。怀孕期间,雌激素与孕激素可达到极高水平(例如,34 周后雌二醇可达 12,500 pg/mL以上)<sup>([图表][GRAPH-2])</sup>,而这些激素在动物实验当中被认为可起到抑制作用<sup>([Rajkumar et al., 2003][R03])</sup>。对于已绝经 5 年以上的妇女,高剂量雌激素疗法用于治疗乳腺癌很有效,与抗雌激素疗法基本相当<sup>([Bennink et al., 2017][B17])</sup>。与此相反的是,高剂量雌激素疗法对于绝经前妇女的乳腺癌并无作用,尽管其似乎在超大剂量下会起效<sup>(Bennink et al., 2017)</sup>。
|
||||
同样反常的是,在一些其它特定情形下,雌激素和/或孕激素的暴露亦可降低乳腺癌风险、抑制乳腺癌发展。例如,年轻妇女(35 岁以下)如怀孕超过 34 周,在短期(十年内)有更高的乳腺癌风险,但长期(20-25 年以上)风险反而变低了;其终生风险可降低至多 50%<sup>([Nichols et al., 2019][nich19]; [Husby et al., 2018][h18])</sup>。怀孕期间,雌激素与孕激素可达到极高水平(例如,34 周后雌二醇可达 12,500 pg/mL 以上)<sup>([图表][graph-2])</sup>,而这些激素在动物实验当中被认为可起到抑制作用<sup>([Rajkumar et al., 2003][r03])</sup>。对于已绝经 5 年以上的妇女,高剂量雌激素疗法用于治疗乳腺癌很有效,与抗雌激素疗法基本相当<sup>([Bennink et al., 2017][b17])</sup>。与此相反的是,高剂量雌激素疗法对于绝经前妇女的乳腺癌并无作用,尽管其似乎在超大剂量下会起效<sup>(Bennink et al., 2017)</sup>。\
|
||||
然而,雌、孕激素的这些益处只在反常情形下发生(例如超高激素水平/摄入、和/或在性激素不足之前推延之),与女性倾向跨性别者的关系并不密切。无论如何,这些话题都很有趣,笔者考虑将来另作文章来更全面地讨论它们。
|
||||
|
||||
## 男性的雌激素暴露与乳腺癌风险
|
||||
## 男性的雌激素暴露与乳腺癌风险 {#estrogen-exposure-in-men-and-breast-cancer-risk}
|
||||
|
||||
对于顺性别男性,睾酮暴露量较低、和/或雌激素暴露量较高的情形可提高其乳腺癌风险<sup>([Ferzoco & Ruddy, 2016][FR16])</sup>。这些情形包括:睾丸疾病、睾丸被摘除、肝脏疾病等等<sup>(Yousef, 2017)</sup>。其中,睾丸功能障碍、睾丸缺失可导致睾酮暴露量减少;而肝脏疾病会损害雌激素代谢功能,引起雌激素水平上升。此二种情形使得雌激素/雄激素比例增大,从而引起雌激素对乳房更大的刺激作用。乳腺癌风险的增长可能与其存在关联。同样地,男性发生的良性乳房疾病、男性女乳症等等也被发现和乳腺癌风险有关<sup>([Sasco, Lowenfels, & Pasker-De Jong, 1993][SLP93])</sup>,不过这些发现跟男性女乳症的风险混淆了<sup>([Giordano, 2005][G05])</sup>。除健康状况之外,顺性别男性用于治疗前列腺癌的高剂量雌激素疗法也被发现与乳腺癌风险的增加有关<sup>([Thellenberg et al., 2003][T03]; [Karlsson et al., 2006][K06])</sup>。
|
||||
对于顺性别男性,睾酮暴露量较低、和/或雌激素暴露量较高的情形可提高其乳腺癌风险<sup>([Ferzoco & Ruddy, 2016][fr16])</sup>。这些情形包括:睾丸疾病、睾丸被摘除、肝脏疾病等等<sup>(Yousef, 2017)</sup>。其中,睾丸功能障碍、睾丸缺失可导致睾酮暴露量减少;而肝脏疾病会损害雌激素代谢功能,引起雌激素水平上升。此二种情形使得雌激素/雄激素比例增大,从而引起雌激素对乳房更大的刺激作用。乳腺癌风险的增长可能与其存在关联。同样地,男性发生的良性乳房疾病、男性女乳症等等也被发现和乳腺癌风险有关<sup>([Sasco, Lowenfels, & Pasker-De Jong, 1993][slp93])</sup>,不过这些发现跟男性女乳症的风险混淆了<sup>([Giordano, 2005][g05])</sup>。除健康状况之外,顺性别男性用于治疗前列腺癌的高剂量雌激素疗法也被发现与乳腺癌风险的增加有关<sup>([Thellenberg et al., 2003][t03]; [Karlsson et al., 2006][k06])</sup>。
|
||||
|
||||
## 关于女性倾向跨性别者的乳腺癌风险的研究项目
|
||||
## 关于女性倾向跨性别者的乳腺癌风险的研究项目 {#studies-of-breast-cancer-risk-in-transfeminine-people}
|
||||
|
||||
本文将现有与女性化激素疗法引起的乳腺癌风险有关的研究项目,列入一份 Google 文档附件,其可于[此处][APP-1]查阅。截至目前,已有三个大型群体、数个较小群体研究评估了女性化激素治疗引起的乳腺癌风险。
|
||||
本文将现有与女性化激素疗法引起的乳腺癌风险有关的研究项目,列入一份 Google 文档附件,其可于[此处][app-1]查阅。截至目前,已有三个大型群体、数个较小群体研究评估了女性化激素治疗引起的乳腺癌风险。
|
||||
|
||||
### 阿姆斯特丹自由大学医学中心(VUMC)的研究
|
||||
### 阿姆斯特丹自由大学医学中心(VUMC)的研究 {#veterans-health-administration-vha-study}
|
||||
|
||||
附件中大部分研究项目由荷兰的阿姆斯特丹自由大学医学中心(VUMC)进行<sup>([Asscheman, Gooren, & Eklund, 1989][AGE89]; [van Kesteren et al., 1997][K97]; [Mueller & Gooren, 2008][MG08]; [Asscheman et al., 2011][A11]; [Gooren et al., 2013][G13]; [de Blok et al., 2018][B18]; [de Blok et al., 2019][B19])</sup>。该诊所为荷兰 95% 的跨性别者提供治疗<sup>(de Blok et al., 2019)</sup>。VUMC 的研究项目均大致基于同一批持续变化(evolving)的跨性别女性群体。数十年间,VUMC 仅报告了很低的乳腺癌发生率,并不比顺性别男性的高出许多——经过平均约 20 年的激素治疗,2300 名跨性别女性当中仅报告两起乳腺癌病例<sup>(Gooren et al., 2013)</sup>。该诊所通常采用的处方,是雌激素合并高剂量醋酸环丙孕酮。
|
||||
这些项目并未对乳腺癌做系统性筛查,对乳腺癌的诊断大都依赖于病人的报告,因此存在病例漏检的可能性<sup>([Feldman et al., 2016][F16])</sup>。
|
||||
附件中大部分研究项目由荷兰的阿姆斯特丹自由大学医学中心(VUMC)进行<sup>([Asscheman, Gooren, & Eklund, 1989][age89]; [van Kesteren et al., 1997][k97]; [Mueller & Gooren, 2008][mg08]; [Asscheman et al., 2011][a11]; [Gooren et al., 2013][g13]; [de Blok et al., 2018][b18]; [de Blok et al., 2019][b19])</sup>。该诊所为荷兰 95% 的跨性别者提供治疗<sup>(de Blok et al., 2019)</sup>。VUMC 的研究项目均大致基于同一批持续变化(evolving)的跨性别女性群体。数十年间,VUMC 仅报告了很低的乳腺癌发生率,并不比顺性别男性的高出许多——经过平均约 20 年的激素治疗,2300 名跨性别女性当中仅报告两起乳腺癌病例<sup>(Gooren et al., 2013)</sup>。该诊所通常采用的处方,是雌激素合并高剂量醋酸环丙孕酮。\
|
||||
这些项目并未对乳腺癌做系统性筛查,对乳腺癌的诊断大都依赖于病人的报告,因此存在病例漏检的可能性<sup>([Feldman et al., 2016][f16])</sup>。
|
||||
|
||||
2019 年,VUMC 又进行了一项跟踪性研究,不过这次使用了新的方式获得乳腺癌诊断史<sup>(de Blok et al., 2019)</sup>。研究者不再单纯询问病人是否被诊断出乳腺癌,而是通过遍及荷兰的一套电子病历信息系统:“[荷兰国家病理学/解剖学自动化档案馆][PALGA](PALGA)”来获取乳腺癌诊断史。这样一来,其报告的乳腺癌病例数从 2 例跃升至 15 例。这使得接受激素治疗平均达 15 年左右之后的乳腺癌相对风险率,相较先前期望的几乎翻了 50 倍之多,而绝对发生率约达 0.6%。这项发现推翻了该诊所早前所有研究的结论,也表明在早前研究中,VUMC 治疗的群体的乳腺癌真实病例数被大幅低估。可以认为,诸如肺癌风险、以及在本项研究骤增近 50 倍的乳腺癌病例等健康风险的大幅增长,应是符合逻辑的。故此,研究者以严谨行文,对这种增长做了详细描述<sup>(de Blok et al., 2019; [Reactions Weekly, 2019][RW19])</sup>。
|
||||
在此之前,女性化激素疗法所引起的乳腺癌风险之增长被认为很低,而今新的数据证明了其不一定属实<sup>([de Blok, Dreijerink, & Heijer, 2019][BDH19])</sup>。
|
||||
2019 年,VUMC 又进行了一项跟踪性研究,不过这次使用了新的方式获得乳腺癌诊断史<sup>(de Blok et al., 2019)</sup>。研究者不再单纯询问病人是否被诊断出乳腺癌,而是通过遍及荷兰的一套电子病历信息系统:“[荷兰国家病理学/解剖学自动化档案馆][palga](PALGA)”来获取乳腺癌诊断史。这样一来,其报告的乳腺癌病例数从 2 例跃升至 15 例。这使得接受激素治疗平均达 15 年左右之后的乳腺癌相对风险率,相较先前期望的几乎翻了 50 倍之多,而绝对发生率约达 0.6%。这项发现推翻了该诊所早前所有研究的结论,也表明在早前研究中,VUMC 治疗的群体的乳腺癌真实病例数被大幅低估。可以认为,诸如肺癌风险、以及在本项研究骤增近 50 倍的乳腺癌病例等健康风险的大幅增长,应是符合逻辑的。故此,研究者以严谨行文,对这种增长做了详细描述<sup>(de Blok et al., 2019; [Reactions Weekly, 2019][rw19])</sup>。\
|
||||
在此之前,女性化激素疗法所引起的乳腺癌风险之增长被认为很低,而今新的数据证明了其不一定属实<sup>([de Blok, Dreijerink, & Heijer, 2019][bdh19])</sup>。
|
||||
|
||||
### 美国退伍军人卫生管理局(VHA)的研究
|
||||
|
||||
另一组大型群体来自美国退伍军人卫生管理局(VHA)<sup>([Brown & Jones, 2015][BJ15]; [Brown, 2015][B15])</sup>。2015 年,一篇采用该群体数据的研究论文被发表。其中,研究者报告了在平均跟踪大约 10 年之后,出生指派性别为男的约 3500 人当中有 3 例乳腺癌病例。也就是说,平均治疗时长达 10 年时,发病率约为 0.09%。尽管其在平均跟踪时长上比 VUMC 的群体更短,但在总时长上与后者相近。VHA 的研究者还报告,乳腺癌发生率较先前预计的增长 33 倍。有些奇怪的是,其和 VUMC 于 2018 年报告的 46 倍并不一致(后者基于 2,300 人平均跟踪 15 年后有 15 人被确诊的事实)。VHA 总结认为,无论如何,女性倾向跨性别者的乳腺癌风险高于顺性别男性、也高于 VUMC 早前所报告的,但仍低于顺性别妇女。
|
||||
另一组大型群体来自美国退伍军人卫生管理局(VHA)<sup>([Brown & Jones, 2015][bj15]; [Brown, 2015][b15])</sup>。2015 年,一篇采用该群体数据的研究论文被发表。其中,研究者报告了在平均跟踪大约 10 年之后,出生指派性别为男的约 3500 人当中有 3 例乳腺癌病例。也就是说,平均治疗时长达 10 年时,发病率约为 0.09%。尽管其在平均跟踪时长上比 VUMC 的群体更短,但在总时长上与后者相近。VHA 的研究者还报告,乳腺癌发生率较先前预计的增长 33 倍。有些奇怪的是,其和 VUMC 于 2018 年报告的 46 倍并不一致(后者基于 2,300 人平均跟踪 15 年后有 15 人被确诊的事实)。VHA 总结认为,无论如何,女性倾向跨性别者的乳腺癌风险高于顺性别男性、也高于 VUMC 早前所报告的,但仍低于顺性别妇女。
|
||||
|
||||
VHA 的论文并未披露在激素疗法当中使用的药物及其剂量,不过考虑到其囊括了接受 VHA 系统的服务提供者治疗的所有患者,其处方应当千差万别。既然是在美国,通常的处方应该是雌激素合并螺内酯,无孕激素。
|
||||
|
||||
|
|
@ -80,182 +98,176 @@ VHA 的研究项目有一些问题需要探讨:
|
|||
- 同 VUMC 早前的研究项目一样,VHA 的研究也未对乳腺癌做系统性筛查,其诊断乳腺癌基本依赖病人的报告,从而存在病例漏检的可能性<sup>(Feldman et al., 2016)</sup>。
|
||||
- 该项目*未将激素疗法纳入考虑* <sup>(Feldman et al., 2016)</sup>。VHA 患者群体中只有少部分人正接受激素治疗,研究者并不知道多少人在接受治疗、多少人没有。此外,该群体中甚至有不明比例的人*不是跨性别者* ——研究者将 VHA 系统当中有“跨性别相关”诊断史(如“异装癖”,即变装者)的所有顺性别男性囊括其中。这些个体的绝大部分应当皆未接受激素治疗。
|
||||
- 对明确正接受激素治疗的人群的跟踪时长过短。在 VHA 患者群体当中,约有 1400 名明确正接受激素治疗的女性倾向跨性别者;对其的平均跟踪时长仅有 5.5 年,而其中近半数个体的跟踪时长尚未达 3 年。
|
||||
- VHA 的论文内容很不明晰,令人费解。例如,VHA 对跨性别者的称谓有误,按其出生时的性别“男性”或“女性”指代之并行文,如此很难分辨出谁是谁、谁在接受激素治疗与否。不仅如此,连一些针对该研究项目的评述文章也在讨论“男性”与“女性”的风险时错误地倒置身份<sup>(例如 [Dente et al., 2019][D19])</sup>。
|
||||
- 还有一点令人费解:VHA 研究者在相同时间点前后发表的两篇论文里,报告了包含出生指派性别为男、女的 5100 人的群体(两篇所指为同一组)出现 *33* 例乳腺癌病例<sup>([Brown & Jones, 2014][BJ14]; [Brown & Jones, 2016][BJ16])</sup>。作为对比,他们在 2015 年的论文中仅报告了 10 例(其中 3 例出生指派性别为男、7 例则为女)。造成这种差异的原因尚不清楚<sup>([Braun et al., 2017][BRAUN17])</sup>。
|
||||
- VHA 的论文内容很不明晰,令人费解。例如,VHA 对跨性别者的称谓有误,按其出生时的性别“男性”或“女性”指代之并行文,如此很难分辨出谁是谁、谁在接受激素治疗与否。不仅如此,连一些针对该研究项目的评述文章也在讨论“男性”与“女性”的风险时错误地倒置身份<sup>(例如 [Dente et al., 2019][d19])</sup>。
|
||||
- 还有一点令人费解:VHA 研究者在相同时间点前后发表的两篇论文里,报告了包含出生指派性别为男、女的 5100 人的群体(两篇所指为同一组)出现 _33_ 例乳腺癌病例<sup>([Brown & Jones, 2014][bj14]; [Brown & Jones, 2016][bj16])</sup>。作为对比,他们在 2015 年的论文中仅报告了 10 例(其中 3 例出生指派性别为男、7 例则为女)。造成这种差异的原因尚不清楚<sup>([Braun et al., 2017][braun17])</sup>。
|
||||
|
||||
出于上述问题的缘故,VHA 的项目的参考价值有限,应谨慎对待。VUMC 在 2019 年发表的数据远比其更具有价值。
|
||||
|
||||
### 凯撒医疗集团在加州和乔治亚州的研究
|
||||
### 凯撒医疗集团在加州和乔治亚州的研究 {#kaiser-permanente-in-california-and-georgia-study}
|
||||
|
||||
第三组、也是最后一组群体研究,来自[凯撒医疗集团][KAIS](Kaiser Permanente)在美国北加利福尼亚州、南加州和乔治亚州的分站<sup>([Silverberg et al., 2017][S17])</sup>。他们报告了来自上述三处分站、总计约 2800 名女性倾向跨性别者组成的群体的不同癌症发生率。对该群体的平均跟踪时长只有 4 年。研究者并未报告任何发生不足 5 例的癌症病例;而女性倾向跨性别者的乳腺癌既未出现在相关结果图表,亦未于讨论环节当中被提及。故此,该群体的乳腺癌病例应该少于 5 例。然而,由研究者 T’Sjoen 及其同行组成的跨性别医学研究领域权威团队,在其文章中援引凯撒集团的论文时指出,凯撒集团的团队发现了女性倾向跨性别者的乳腺癌风险较顺性别男性更高、但较顺性别女性更低<sup>([T’Sjoen et al., 2019][TS19])</sup>。如果此言属实(目前来看有很大概率),那么其应该是从和凯撒集团的研究者的私下交流当中取得的。
|
||||
第三组、也是最后一组群体研究,来自[凯撒医疗集团][kais](Kaiser Permanente)在美国北加利福尼亚州、南加州和乔治亚州的分站<sup>([Silverberg et al., 2017][s17])</sup>。他们报告了来自上述三处分站、总计约 2800 名女性倾向跨性别者组成的群体的不同癌症发生率。对该群体的平均跟踪时长只有 4 年。研究者并未报告任何发生不足 5 例的癌症病例;而女性倾向跨性别者的乳腺癌既未出现在相关结果图表,亦未于讨论环节当中被提及。故此,该群体的乳腺癌病例应该少于 5 例。然而,由研究者 T’Sjoen 及其同行组成的跨性别医学研究领域权威团队,在其文章中援引凯撒集团的论文时指出,凯撒集团的团队发现了女性倾向跨性别者的乳腺癌风险较顺性别男性更高、但较顺性别女性更低<sup>([T’Sjoen et al., 2019][ts19])</sup>。如果此言属实(目前来看有很大概率),那么其应该是从和凯撒集团的研究者的私下交流当中取得的。\
|
||||
凯撒集团的研究存在一定局限性,包括缺乏对乳腺癌风险的准确估计数字,以及跟踪时长非常短,等等。此外,癌症诊断史仅取自凯撒集团自有的信息系统;对于其癌症筛查的系统性如何,也尚不清楚。
|
||||
|
||||
凯撒集团的研究者计划进行的研究项目,将通过将其拓展至其它分站来扩大患者群体规模<sup>(Silverberg et al., 2017)</sup>。这种改进令人振奋,其有望提供更多和跨性别者健康风险有关的数据,包括乳腺癌风险。
|
||||
|
||||
### 其它较小的群体研究
|
||||
### 其它较小的群体研究 {#small-cohort-studies}
|
||||
|
||||
其余的针对女性倾向跨性别者之乳腺癌风险的科研项目规模均较小。其中一项是由比利时根特大学进行的,其跟踪了 50 名已进行性别重置手术的跨性别女性,平均跟踪时长 11.4 年;其未报告任何乳腺癌病例<sup>([Wierckx et al., 2012][W12])</sup>。另一项是由德国埃朗根大学医院进行的,其跟踪了 60 名跨性别女性;其同样未报告任何病例,不过她们的治疗时长仅有两年<sup>([Dittrich et al., 2005][D05])</sup>。最后一项是由 [Harry Benjamin][WIKI-2] 医生进行的;他在 1960 年代发表的文章里透露,其已为大约 150 名跨性别女性提供“中等至较大剂量的雌激素”治疗,期限从 3 个月到 12 年不等;其未曾接触到乳腺癌病例<sup>([Benjamin, 1964][B64]; [Benjamin, 1966][B66]; Gooren et al., 2013)</sup>。
|
||||
其余的针对女性倾向跨性别者之乳腺癌风险的科研项目规模均较小。其中一项是由比利时根特大学进行的,其跟踪了 50 名已进行性别重置手术的跨性别女性,平均跟踪时长 11.4 年;其未报告任何乳腺癌病例<sup>([Wierckx et al., 2012][w12])</sup>。另一项是由德国埃朗根大学医院进行的,其跟踪了 60 名跨性别女性;其同样未报告任何病例,不过她们的治疗时长仅有两年<sup>([Dittrich et al., 2005][d05])</sup>。最后一项是由 [Harry Benjamin][wiki-2] 医生进行的;他在 1960 年代发表的文章里透露,其已为大约 150 名跨性别女性提供“中等至较大剂量的雌激素”治疗,期限从 3 个月到 12 年不等;其未曾接触到乳腺癌病例<sup>([Benjamin, 1964][b64]; [Benjamin, 1966][b66]; Gooren et al., 2013)</sup>。\
|
||||
上述群体规模太小,难以对女性倾向跨性别者之乳腺癌风险进行有意义的量化。
|
||||
|
||||
### 关于既有研究项目的讨论
|
||||
### 关于既有研究项目的讨论 {#discussion-of-the-available-studies}
|
||||
|
||||
#### 由跟踪时长过短导致的对乳腺癌风险之量化的不确定性
|
||||
#### 由跟踪时长过短导致的对乳腺癌风险之量化的不确定性 {#inconclusive-quantification-of-breast-cancer-risk-due-to-short-follow-up-times}
|
||||
|
||||
由于跟踪时长不足,关于女性倾向跨性别者之乳腺癌风险的现有研究项目的结论并不充分<sup>(de Blok, Dreijerink, & Heijer, 2019; Mueller & Gooren, 2008; [Gooren, 2011][G11]; Gooren et al., 2013; Brown & Jones, 2015)</sup>。例如,在 VUMC 和 VHA 的研究里,平均跟踪时长仅有 10-20 年。对于顺性别妇女,其乳腺癌风险在停经前的数十年里呈指数级增长,但到了老年,增幅会非常低。顺性别妇女通常被确诊乳腺癌的年龄为 60 岁,这 60 年里包括停经前的 50 年激素暴露量、和绝经后 10 年的激素暴露量;如上文所示,这后 10 年里接受预防性抗雌激素疗法可大幅降低乳腺癌风险,因此其重要性不容忽视。综上,由于现有关于女性化激素疗法与乳腺癌风险的研究的跟踪时长过短,迄今尚不清楚我们(女性倾向跨性别者)真实的、或者说终生的乳腺癌风险到底如何<sup>(Mueller & Gooren, 2008)</sup>。
|
||||
由于跟踪时长不足,关于女性倾向跨性别者之乳腺癌风险的现有研究项目的结论并不充分<sup>(de Blok, Dreijerink, & Heijer, 2019; Mueller & Gooren, 2008; [Gooren, 2011][g11]; Gooren et al., 2013; Brown & Jones, 2015)</sup>。例如,在 VUMC 和 VHA 的研究里,平均跟踪时长仅有 10-20 年。对于顺性别妇女,其乳腺癌风险在停经前的数十年里呈指数级增长,但到了老年,增幅会非常低。顺性别妇女通常被确诊乳腺癌的年龄为 60 岁,这 60 年里包括停经前的 50 年激素暴露量、和绝经后 10 年的激素暴露量;如上文所示,这后 10 年里接受预防性抗雌激素疗法可大幅降低乳腺癌风险,因此其重要性不容忽视。综上,由于现有关于女性化激素疗法与乳腺癌风险的研究的跟踪时长过短,迄今尚不清楚我们(女性倾向跨性别者)真实的、或者说终生的乳腺癌风险到底如何<sup>(Mueller & Gooren, 2008)</sup>。
|
||||
|
||||
不过我们已知的是,女性倾向跨性别者在使用激素疗法(至少也有一种雌激素、一种形如醋酸环丙孕酮的孕激素)约 15 年后,其乳腺癌风险显然会大幅增加<sup>(de Blok, Dreijerink, & Heijer, 2019)</sup>。好在,其风险处于顺性别妇女和顺性别男性之间,并不会高于顺性别妇女。然而与此同时,其风险仍不容忽视,绝对发生率也必然随着跟踪时间延长而增大。
|
||||
不过我们已知的是,女性倾向跨性别者在使用激素疗法(至少也有一种雌激素、一种形如醋酸环丙孕酮的孕激素)约 15 年后,其乳腺癌风险显然会大幅增加<sup>(de Blok, Dreijerink, & Heijer, 2019)</sup>。好在,其风险处于顺性别妇女和顺性别男性之间,并不会高于顺性别妇女。然而与此同时,其风险仍不容忽视,绝对发生率也必然随着跟踪时间延长而增大。\
|
||||
关于终生风险,至少从 de Blok 等人 (2019) 的发现及其使用的激素治疗处方来看,女性倾向跨性别者的乳腺癌发生率大约就在几个百分点之多。
|
||||
|
||||
#### 和终生激素暴露量相关的乳腺癌风险
|
||||
#### 和终生激素暴露量相关的乳腺癌风险 {#breast-cancer-risk-in-relation-to-lifetime-hormone-exposure}
|
||||
|
||||
女性倾向跨性别者的乳腺癌风险应该低于顺性别妇女。这可能至少出于前者的终生激素暴露量更少的缘故<sup>(Mueller & Gooren, 2008)</sup>。事实上,至少从历史来看,女性倾向跨性别者开始接受激素治疗的平均年龄在 30-40 岁,而该年龄距离顺性别女性通常经历青春期的年龄段已过去数十年<sup>(Mueller & Gooren, 2008)</sup>。此外,青年人群可能在特定时间段里对乳腺癌易感<sup>([Biro & Wolff, 2011][BW11]; [Biro & Deardorff, 2013][BD13]; [Biro et al., 2020][B20])</sup>。然而,近年来女性倾向跨性别者启动激素治疗的年龄正在降低<sup>(Mueller & Gooren, 2008)</sup>,如今有不少人在十几到二十来岁便开始服用激素了<sup>([Aly W., 2019][AW19])</sup>。相较于早年里服用激素更晚的个体,这些个体的终生激素暴露量会更大,其乳腺癌风险也会更高。而且,到了顺性别妇女通常的更年期年龄,女性倾向跨性别者很少有意停止激素治疗<sup>(Mueller & Gooren, 2008)</sup>;其中许多人终其一生皆会维持治疗。这种额外的激素暴露量会使乳腺癌风险进一步升高<sup>(Mueller & Gooren, 2008)</sup>。
|
||||
女性倾向跨性别者的乳腺癌风险应该低于顺性别妇女。这可能至少出于前者的终生激素暴露量更少的缘故<sup>(Mueller & Gooren, 2008)</sup>。事实上,至少从历史来看,女性倾向跨性别者开始接受激素治疗的平均年龄在 30-40 岁,而该年龄距离顺性别女性通常经历青春期的年龄段已过去数十年<sup>(Mueller & Gooren, 2008)</sup>。此外,青年人群可能在特定时间段里对乳腺癌易感<sup>([Biro & Wolff, 2011][bw11]; [Biro & Deardorff, 2013][bd13]; [Biro et al., 2020][b20])</sup>。然而,近年来女性倾向跨性别者启动激素治疗的年龄正在降低<sup>(Mueller & Gooren, 2008)</sup>,如今有不少人在十几到二十来岁便开始服用激素了。相较于早年里服用激素更晚的个体,这些个体的终生激素暴露量会更大,其乳腺癌风险也会更高。而且,到了顺性别妇女通常的更年期年龄,女性倾向跨性别者很少有意停止激素治疗<sup>(Mueller & Gooren, 2008)</sup>;其中许多人终其一生皆会维持治疗。这种额外的激素暴露量会使乳腺癌风险进一步升高<sup>(Mueller & Gooren, 2008)</sup>。
|
||||
|
||||
#### 和孕激素及其剂量相关的乳腺癌风险
|
||||
#### 和孕激素及其剂量相关的乳腺癌风险 {#breast-cancer-risk-in-relation-to-progestogens-and-dosage}
|
||||
|
||||
现有的发现表明,顺性别妇女合并使用雌、孕激素时的乳腺癌风险,要高于单用雌激素;由此可以类推,女性倾向跨性别者合用雌、孕激素的激素疗法也会有更高的乳腺癌风险<sup>(Mde Blok, Dreijerink, & Heijer, 2019)</sup>。有这样一种可能:相较于已被 VUMC 研究过的合用雌激素与醋酸环丙孕酮疗法,如排除掉孕激素、仅用雌激素,则乳腺癌风险兴许会更低<sup>(Mde Blok, Dreijerink, & Heijer, 2019)</sup>。另外需要注意的是,VUMC 所用醋酸环丙孕酮的剂量会使得孕激素暴露量相当之高<sup>([Aly W., 2019][ALYW19]; [中文译本][ALYW19-CH])</sup>。
|
||||
乳腺癌风险与孕激素剂量之间的关联程度,目前尚不明确。类似地,乳腺癌风险是否受雌激素剂量影响,以及高雌激素剂量下是否有更高风险,目前也不明确。但无论如何,有绝经前妇女合用雌、孕激素的避孕疗法会增加乳腺癌风险的事实在先,可以认为,较高的雌/孕激素暴露量会增加一定程度的乳腺癌风险<sup>([Kahlenborn et al,, 2006][KAHL06]; [Zhu et al., 2012][Z12]; [Ji et al., 2019][J19])</sup>。
|
||||
另外,一项早年的调查性研究显示,绝经前妇女使用雌激素注射剂之后,乳腺癌风险相较口服雌激素、或未服用激素者增加了 4 倍<sup>([Hulka et al., 1982][H82]; [Coe & Parks, 1989][CP89])</sup>。需要注意,通常剂量的雌激素注射剂所提供的雌激素暴露量,是远大于口服雌激素和其它给药途径的<sup>([Göretzlehner et al., 2002][GORE02]; [Aly W., 2021][AW21]; [中文译本][AW21-CH])</sup>。
|
||||
现有的发现表明,顺性别妇女合并使用雌、孕激素时的乳腺癌风险,要高于单用雌激素;由此可以类推,女性倾向跨性别者合用雌、孕激素的激素疗法也会有更高的乳腺癌风险<sup>(Mde Blok, Dreijerink, & Heijer, 2019)</sup>。有这样一种可能:相较于已被 VUMC 研究过的合用雌激素与醋酸环丙孕酮疗法,如排除掉孕激素、仅用雌激素,则乳腺癌风险兴许会更低<sup>(Mde Blok, Dreijerink, & Heijer, 2019)</sup>。另外需要注意的是,VUMC 所用醋酸环丙孕酮的剂量会使得孕激素暴露量相当之高<sup>([Aly W., 2019][aw19-cd])</sup>。\
|
||||
乳腺癌风险与孕激素剂量之间的关联程度,目前尚不明确。类似地,乳腺癌风险是否受雌激素剂量影响,以及高雌激素剂量下是否有更高风险,目前也不明确。但无论如何,有绝经前妇女合用雌、孕激素的避孕疗法会增加乳腺癌风险的事实在先,可以认为,较高的雌/孕激素暴露量会增加一定程度的乳腺癌风险<sup>([Kahlenborn et al,, 2006][kahl06]; [Zhu et al., 2012][z12]; [Ji et al., 2019][j19])</sup>。\
|
||||
另外,一项早年的调查性研究显示,绝经前妇女使用雌激素注射剂之后,乳腺癌风险相较口服雌激素、或未服用激素者增加了 4 倍<sup>([Hulka et al., 1982][h82]; [Coe & Parks, 1989][cp89])</sup>。需要注意,通常剂量的雌激素注射剂所提供的雌激素暴露量,是远大于口服雌激素和其它给药途径的<sup>([Göretzlehner et al., 2002][gore02]; [Aly W., 2021][aw21-iema])</sup>。
|
||||
|
||||
## X 染色体与乳腺癌风险
|
||||
## X 染色体与乳腺癌风险 {#x-chromosomes-and-breast-cancer-risk}
|
||||
|
||||
人类性染色体包括 X 染色体和 Y 染色体。顺性别妇女通常有两条 X 染色体(即 46,XX 核型);而顺性别男性、女性倾向跨性别者通常有一条 X 染色体、一条 Y 染色体(即 46,XY 核型)。其中 46,XX 核型(即第二条 X 染色体的存在)可能会是乳腺癌风险的主要因素。X 染色体的获得(非整倍性)、以及其异常失活,已被发现和乳腺癌的发生及发展有关<sup>([Nakopoulou et al., 2007][N07]; [Di Oto et al., 2015][DO15]; [Lin et al., 2015][L15]; [Chaligné et al., 2015][C15]; [Di Oto et al., 2018][DO18])</sup>。此外,患有克氏综合征(即核型为 46,XXY)的男性的乳腺癌风险,也比 46,XY 核型的正常男性要高。
|
||||
与此相反的是,患有完全性雄激素不敏感综合征(CAIS)的女性,迄今未有乳腺癌病例报告——这还是在她们的乳房发育良好的情况下<sup>([Aly W., 2020][AW20])</sup>;其核型为 46,XY ,和女性倾向跨性别者相同<sup>([Hughes et al., 2012][H12]; [Tiefenbacher & Daxenbichler, 2008][TD08]; [Hughes, 2009][H09])</sup>。不过,克氏综合征与 CAIS 患者体内的激素异常现象,在乳腺癌风险上的作用可能有所不同,从而会造成一定迷惑性。尤其需要注意的是,患 CAIS 的女性的雌激素暴露量较少,体内孕激素也极少、以至不存在。无论如何,对于克氏综合征与 CAIS 患者的乳腺癌风险之差异,无法完全用激素异常来解释。
|
||||
综上,可以认为,女性倾向跨性别者*体内第二条 X 染色体的缺少\**,的确可能会在一定程度上降低乳腺癌风险。针对本话题有更深入的讨论,详见[此处][APP-2]。
|
||||
人类性染色体包括 X 染色体和 Y 染色体。顺性别妇女通常有两条 X 染色体(即 46,XX 核型);而顺性别男性、女性倾向跨性别者通常有一条 X 染色体、一条 Y 染色体(即 46,XY 核型)。其中 46,XX 核型(即第二条 X 染色体的存在)可能会是乳腺癌风险的主要因素。X 染色体的获得(非整倍性)、以及其异常失活,已被发现和乳腺癌的发生及发展有关<sup>([Nakopoulou et al., 2007][n07]; [Di Oto et al., 2015][do15]; [Lin et al., 2015][l15]; [Chaligné et al., 2015][c15]; [Di Oto et al., 2018][do18])</sup>。此外,患有克氏综合征(即核型为 46,XXY)的男性的乳腺癌风险,也比 46,XY 核型的正常男性要高。\
|
||||
与此相反的是,患有完全性雄激素不敏感综合征(CAIS)的女性,迄今未有乳腺癌病例报告——这还是在她们的乳房发育良好的情况下<sup>([Aly W., 2020][aw20])</sup>;其核型为 46,XY ,和女性倾向跨性别者相同<sup>([Hughes et al., 2012][h12]; [Tiefenbacher & Daxenbichler, 2008][td08]; [Hughes, 2009][h09])</sup>。不过,克氏综合征与 CAIS 患者体内的激素异常现象,在乳腺癌风险上的作用可能有所不同,从而会造成一定迷惑性。尤其需要注意的是,患 CAIS 的女性的雌激素暴露量较少,体内孕激素也极少、以至不存在。无论如何,对于克氏综合征与 CAIS 患者的乳腺癌风险之差异,无法完全用激素异常来解释。\
|
||||
综上,可以认为,女性倾向跨性别者*体内第二条 X 染色体的缺少*\*,的确可能会在一定程度上降低乳腺癌风险。针对本话题有更深入的讨论,详见[此处][app-2]。
|
||||
|
||||
> *\* 译者注:原文为“缺少的两条 X 染色体”(the lack of two X chromosomes)。*
|
||||
> _\* 译者注:原文为“缺少的两条 X 染色体”(the lack of two X chromosomes)。_
|
||||
|
||||
## 结语
|
||||
## 结语 {#summary-and-conclusions}
|
||||
|
||||
女性的乳腺癌风险显著高于男性。乳腺癌发生率随年龄增长呈指数级升高,但在年轻人群当中非常少见。有强力的证据支持以下观点,即雌激素与孕激素会增加乳腺癌发病风险;在因性别造成的乳腺癌风险差异当中,其可解释为主要成因机理。现有数据并未表明,在对乳腺癌风险的作用上,具生物同质性与不具生物同质性的激素有何明显差别。
|
||||
|
||||
早年有关女性化激素疗法与乳腺癌风险的研究发现,女性倾向跨性别者的乳腺癌发生率很低。然而,近期的一项研究采用了更好的研究方法,其发现的乳腺癌风险增加了近 50 倍。其患者群体所用的激素治疗处方,仅为雌激素合并醋酸环丙孕酮。目前尚不清楚其它激素处方(如单用雌激素,或雌激素合并非甾体类抗雄制剂)是否会有相似的风险。由于跟踪时长不足,有关女性倾向跨性别者之乳腺癌风险的现有数据存在局限性。因此,其终生乳腺癌风险尚未可知。
|
||||
早年有关女性化激素疗法与乳腺癌风险的研究发现,女性倾向跨性别者的乳腺癌发生率很低。然而,近期的一项研究采用了更好的研究方法,其发现的乳腺癌风险增加了近 50 倍。其患者群体所用的激素治疗处方,仅为雌激素合并醋酸环丙孕酮。目前尚不清楚其它激素处方(如单用雌激素,或雌激素合并非甾体类抗雄制剂)是否会有相似的风险。由于跟踪时长不足,有关女性倾向跨性别者之乳腺癌风险的现有数据存在局限性。因此,其终生乳腺癌风险尚未可知。\
|
||||
不过基于现有数据,可以预测未来的情况,即女性倾向跨性别者的终生乳腺癌风险率应有几个百分点之高。该风险率处于顺性别男性和顺性别妇女之间。
|
||||
|
||||
女性化激素疗法引起的乳腺癌风险会受到不同因素的影响。例如,累计用药时长,开始治疗的年龄,孕激素的长期服用,以及(可能的)雌/孕激素剂量,等等。我们(女性倾向跨性别者)体内第二条 X 染色体的缺少也许对乳腺癌起到了部分抑制作用。
|
||||
女性化激素疗法引起的乳腺癌风险会受到不同因素的影响。例如,累计用药时长,开始治疗的年龄,孕激素的长期服用,以及(可能的)雌/孕激素剂量,等等。我们(女性倾向跨性别者)体内第二条 X 染色体的缺少也许对乳腺癌起到了部分抑制作用。\
|
||||
尽管女性化激素疗法引起的乳腺癌风险是有必要予以关注的——特别是考虑到孕激素在其中的促进作用——,但放眼长期,乳腺癌的终生发生率应该很低,其风险显然也低于顺性别妇女。此外,乳腺癌的发生也需要经过长达多年的激素暴露,其一般也仅出现在老年。而且,乳腺癌容易治疗,患者生存时长可达 5-10 年。综上,基本可以肯定,考虑乳腺癌时不应将女性化激素疗法的情况排除在外。
|
||||
|
||||
女性化激素疗法引起乳腺癌的可能性,倒是凸显了对年龄与激素暴露量符合标准的女性倾向跨性别者定期进行乳腺癌筛查的重要性<sup>([Chowdhry & O’Connell, 2020][CO20])</sup>。在此建议长期进行激素治疗的女性倾向跨性别者,也像顺性别妇女的过程一样接受乳腺癌筛查<sup>(Chowdhry & O’Connell, 2020)</sup>。
|
||||
女性化激素疗法引起乳腺癌的可能性,倒是凸显了对年龄与激素暴露量符合标准的女性倾向跨性别者定期进行乳腺癌筛查的重要性<sup>([Chowdhry & O’Connell, 2020][co20])</sup>。在此建议长期进行激素治疗的女性倾向跨性别者,也像顺性别妇女的过程一样接受乳腺癌筛查<sup>(Chowdhry & O’Connell, 2020)</sup>。
|
||||
|
||||
[AUTHOR]: https://transfemscience.org/about/#aly-w
|
||||
[TRANSLATOR]: https://bersella-ai.cc/about-me
|
||||
--------
|
||||
|
||||
[BG14]: https://doi.org/10.1016/j.soc.2014.03.011
|
||||
[Y17]: https://doi.org/10.1053/j.seminoncol.2017.11.002
|
||||
[OC17]: https://doi.org/10.1007/978-3-319-48848-6_63
|
||||
[MS18]: https://doi.org/10.2147/BCTT.S176070
|
||||
[DC82]: https://pubmed.ncbi.nlm.nih.gov/7114800/
|
||||
[A09]: https://doi.org/10.1053/j.seminoncol.2009.03.001
|
||||
[B08]: https://doi.org/10.1016/j.critrevonc.2007.09.001
|
||||
[CR00]: https://doi.org/10.1093/aje/152.10.950
|
||||
[BHJ15]: https://doi.org/10.1210/en.2015-1392
|
||||
[CRUK]: https://perma.cc/GE2T-B68E
|
||||
[S06]: https://search.proquest.com/docview/305372484
|
||||
[FR16]: https://doi.org/10.1007/s11912-015-0487-4
|
||||
[G18]: http://doi.org/10.1056/NEJMra1707939
|
||||
## 译文修订记录
|
||||
|
||||
[BG14]: https://doi.org/10.1016/j.soc.2014.03.011
|
||||
[MGP19]: https://doi.org/10.1002/14651858.CD012191.pub2
|
||||
[N19]: http://doi.org/10.1001/jama.2019.5780
|
||||
[C07]: https://doi.org/10.1002/bdrb.20112
|
||||
[LSB15]: https://doi.org/10.4331/wjbc.v6.i3.231
|
||||
[P14]: https://doi.org/10.1016/j.mce.2013.08.001
|
||||
[HAW47]: http://doi.org/10.1001/archsurg.1947.01230070004001
|
||||
[N47]: https://doi.org/10.1016/S0039-6109(16)32241-1
|
||||
[GJ49]: https://doi.org/10.1016/0002-9343(49)90017-0
|
||||
[N51]: https://doi.org/10.1148/56.4.535
|
||||
[P54]: http://doi.org/10.1001/jama.1954.02940370046013
|
||||
[PL56]: https://doi.org/10.1016/S0025-7125(16)34564-3
|
||||
[K56]: https://books.google.com/books?id=BC3gBAAAQBAJ&pg=PA253
|
||||
[K57]: https://doi.org/10.1148/69.3.330
|
||||
[D61]: https://doi.org/10.3322/canjclin.11.2.48
|
||||
[K62]: https://doi.org/10.1002/1097-0142(196205/06)15:3%3C641::AID-CNCR2820150330%3E3.0.CO;2-9
|
||||
[GSL64]: https://doi.org/10.1016/0002-9610(64)90094-7
|
||||
[K64]: https://doi.org/10.7326/0003-4819-60-4-718_1
|
||||
[S73]: https://doi.org/10.1136/bmj.3.5877.446
|
||||
[F89]: https://doi.org/10.1017/S0269727000010502
|
||||
[CGHF19]: https://doi.org/10.1016/S0140-6736(19)31709-X
|
||||
[CGHF19-TABLE]: https://en.wikipedia.org/wiki/Template:Worldwide_epidemiological_evidence_on_breast_cancer_risk_with_menopausal_hormone_therapy
|
||||
[MKG86]: https://doi.org/10.1007/BF01807330
|
||||
[WE96]: http://doi.org/10.1097/00042192-199603010-00003
|
||||
[G02]: https://doi.org/10.1016/S0531-5131(01)00467-8
|
||||
[WHI]: https://www.whi.org/
|
||||
[WHI02]: http://doi.org/10.1001/jama.288.3.321
|
||||
[CAA15]: https://doi.org/10.6004/jnccn.2015.0106
|
||||
[NHS]: https://nurseshealthstudy.org
|
||||
[SWN18]: https://doi.org/10.1080/13697137.2017.1421925
|
||||
[M18]: https://doi.org/10.1080/13697137.2018.1455657
|
||||
[F07]: https://doi.org/10.1007/s10549-007-9523-x
|
||||
[KS13]: https://doi.org/10.3109/13697137.2013.768806
|
||||
[D18]: https://doi.org/10.1080/13697137.2018.1439915
|
||||
[WIKI-1]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_progesterone#Oral_administration
|
||||
[GRAPH-1]: https://web.archive.org/web/20220222215313/https://en.wikipedia.org/wiki/Template:Hormone_levels_with_oral_progesterone
|
||||
[CGHF19-TABLE2]: https://ars.els-cdn.com/content/image/1-s2.0-S014067361931709X-mmc1.pdf#page=29
|
||||
[K05]: https://doi.org/10.1016/j.maturitas.2005.02.018
|
||||
[P08]: https://doi.org/10.1007/978-0-387-69080-3_14
|
||||
[MR11]: https://doi.org/10.1515/HMBCI.2011.014
|
||||
[NICH19]: https://doi.org/10.7326/M18-1323
|
||||
[H18]: https://doi.org/10.1038/s41467-018-06748-3
|
||||
[GRAPH-2]: https://commons.wikimedia.org/wiki/File:Estrogen_and_progesterone_levels_during_pregnancy_in_women.png
|
||||
[R03]: https://doi.org/10.1186/bcr734
|
||||
[B17]: https://doi.org/10.1016/j.maturitas.2016.10.010
|
||||
- 2022 年 8 月 28 日——首次翻译。
|
||||
- 2022 年 11 月 28 日——移除一条已删除的原文链接。
|
||||
|
||||
[SLP93]: https://doi.org/10.1002/ijc.2910530403
|
||||
[G05]: https://doi.org/10.1634/theoncologist.10-7-471
|
||||
[T03]: https://doi.org/10.1097/01.ju.0000056706.88960.7c
|
||||
[K06]: https://doi.org/10.1016/j.juro.2006.03.036
|
||||
|
||||
[APP-1]: https://docs.google.com/document/d/1oqPdRM6gON2hwl6QO1e0GdseYoK5X0J5AtxDZ5hB5tk/view
|
||||
[AGE89]: https://doi.org/10.1016/0026-0495(89)90233-3
|
||||
[K97]: https://doi.org/10.1046/j.1365-2265.1997.2601068.x
|
||||
[MG08]: https://doi.org/10.1530/EJE-08-0289
|
||||
[A11]: https://doi.org/10.1530/EJE-10-1038
|
||||
[G13]: https://doi.org/10.1111/jsm.12319
|
||||
[B18]: https://web.archive.org/web/20201112033637/https://www.endocrine-abstracts.org/ea/0056/ea0056p955.htm
|
||||
[B19]: https://doi.org/10.1136/bmj.l1652
|
||||
[F16]: http://doi.org/10.1097/MED.0000000000000231
|
||||
[PALGA]: https://www.palga.nl/
|
||||
[RW19]: https://doi.org/10.1007/s40278-019-62242-2
|
||||
[BDH19]: https://doi.org/10.1016/j.ecl.2019.02.005
|
||||
[BJ15]: https://doi.org/10.1007/s10549-014-3213-2
|
||||
[B15]: https://doi.org/10.1089/lgbt.2014.0123
|
||||
[D19]: https://gmr.scholasticahq.com/article/7774-evaluating-risks-reported-cases-and-screening-recommendations-for-breast-cancer-in-transgender-patients
|
||||
[BJ14]: https://doi.org/10.1007/s40615-014-0032-4
|
||||
[BJ16]: https://doi.org/10.1089/lgbt.2015.0058
|
||||
[BRAUN17]: https://doi.org/10.1093/epirev/mxw003
|
||||
[KAIS]: https://healthy.kaiserpermanente.org/
|
||||
[S17]: https://doi.org/10.1016/j.annepidem.2017.07.007
|
||||
[TS19]: https://doi.org/10.1210/er.2018-00011
|
||||
[W12]: https://doi.org/10.1111/j.1743-6109.2012.02876.x
|
||||
[D05]: https://doi.org/10.1111/j.1743-6109.2012.02876.x
|
||||
[WIKI-2]: https://en.wikipedia.org/wiki/Harry_Benjamin
|
||||
[B64]: https://doi.org/10.1176/appi.psychotherapy.1964.18.3.458
|
||||
[B66]: https://books.google.com/books?id=S1iHGwAACAAJ
|
||||
[G11]: http://doi.org/10.1056/NEJMcp1008161
|
||||
[BW11]: https://doi.org/10.1007/978-1-4419-9896-5_2
|
||||
[BD13]: https://doi.org/10.1016/j.jadohealth.2012.09.019
|
||||
[B20]: https://doi.org/10.1016/j.jadohealth.2020.07.016
|
||||
[AW19]: https://transfemscience.org/articles/transition-skyrocketing/
|
||||
[ALYW19]: https://transfemscience.org/articles/cpa-dosage/
|
||||
[ALYW19-CH]: https://mtf-wiki.github.io/transfeminine-science/articles/cpa-dosage.html
|
||||
[KAHL06]: https://doi.org/10.4065/81.10.1290
|
||||
[Z12]: https://doi.org/10.3109/13625187.2012.715357
|
||||
[J19]: https://doi.org/10.1097/md.0000000000015719
|
||||
[H82]: https://doi.org/10.1016/0002-9378(82)90108-9
|
||||
[CP89]: https://doi.org/10.1353/pbm.1990.0026
|
||||
[GORE02]: https://www.kup.at/journals/summary/1071.html
|
||||
[AW21]: https://transfemscience.org/articles/injectable-e2-meta-analysis/
|
||||
[AW21-CH]: https://mtf-wiki.github.io/transfeminine-science/articles/injectable-e2-meta-analysis.html
|
||||
|
||||
[N07]: https://doi.org/10.1136/jcp.2006.037838
|
||||
[DO15]: https://doi.org/10.1016/j.humpath.2015.08.008
|
||||
[L15]: https://doi.org/10.1371/journal.pone.0118453
|
||||
[C15]: http://doi.org/10.1101/gr.185926.114
|
||||
[DO18]: https://doi.org/10.1007/s00428-018-2377-2
|
||||
[H12]: https://doi.org/10.1016/S0140-6736(12)60071-3
|
||||
[TD08]: https://doi.org/10.1159/000158055
|
||||
[H09]: https://doi.org/10.1002/9781444316728.ch9
|
||||
[AW20]: https://transfemscience.org/articles/cais-breast-dev-p4/
|
||||
[APP-2]: https://transfemscience.org/articles/breast-cancer-suppl/
|
||||
|
||||
[CANCER]: https://www.cancer.net/cancer-types/breast-cancer/statistics
|
||||
[CO20]: https://doi.org/10.1093/jbi/wbz092
|
||||
[bg14]: https://doi.org/10.1016/j.soc.2014.03.011
|
||||
[y17]: https://doi.org/10.1053/j.seminoncol.2017.11.002
|
||||
[oc17]: https://doi.org/10.1007/978-3-319-48848-6_63
|
||||
[ms18]: https://doi.org/10.2147/BCTT.S176070
|
||||
[dc82]: https://pubmed.ncbi.nlm.nih.gov/7114800/
|
||||
[a09]: https://doi.org/10.1053/j.seminoncol.2009.03.001
|
||||
[b08]: https://doi.org/10.1016/j.critrevonc.2007.09.001
|
||||
[cr00]: https://doi.org/10.1093/aje/152.10.950
|
||||
[bhj15]: https://doi.org/10.1210/en.2015-1392
|
||||
[cruk]: https://perma.cc/GE2T-B68E
|
||||
[s06]: https://search.proquest.com/docview/305372484
|
||||
[fr16]: https://doi.org/10.1007/s11912-015-0487-4
|
||||
[g18]: http://doi.org/10.1056/NEJMra1707939
|
||||
[mgp19]: https://doi.org/10.1002/14651858.CD012191.pub2
|
||||
[n19]: http://doi.org/10.1001/jama.2019.5780
|
||||
[c07]: https://doi.org/10.1002/bdrb.20112
|
||||
[lsb15]: https://doi.org/10.4331/wjbc.v6.i3.231
|
||||
[p14]: https://doi.org/10.1016/j.mce.2013.08.001
|
||||
[haw47]: http://doi.org/10.1001/archsurg.1947.01230070004001
|
||||
[n47]: https://doi.org/10.1016/S0039-6109(16)32241-1
|
||||
[gj49]: https://doi.org/10.1016/0002-9343(49)90017-0
|
||||
[n51]: https://doi.org/10.1148/56.4.535
|
||||
[p54]: http://doi.org/10.1001/jama.1954.02940370046013
|
||||
[pl56]: https://doi.org/10.1016/S0025-7125(16)34564-3
|
||||
[k56]: https://books.google.com/books?id=BC3gBAAAQBAJ&pg=PA253
|
||||
[k57]: https://doi.org/10.1148/69.3.330
|
||||
[d61]: https://doi.org/10.3322/canjclin.11.2.48
|
||||
[k62]: https://doi.org/10.1002/1097-0142(196205/06)15:3%3C641::AID-CNCR2820150330%3E3.0.CO;2-9
|
||||
[gsl64]: https://doi.org/10.1016/0002-9610(64)90094-7
|
||||
[k64]: https://doi.org/10.7326/0003-4819-60-4-718_1
|
||||
[s73]: https://doi.org/10.1136/bmj.3.5877.446
|
||||
[f89]: https://doi.org/10.1017/S0269727000010502
|
||||
[cghf19]: https://doi.org/10.1016/S0140-6736(19)31709-X
|
||||
[cghf19-table]: https://en.wikipedia.org/wiki/Template:Worldwide_epidemiological_evidence_on_breast_cancer_risk_with_menopausal_hormone_therapy
|
||||
[mkg86]: https://doi.org/10.1007/BF01807330
|
||||
[we96]: http://doi.org/10.1097/00042192-199603010-00003
|
||||
[g02]: https://doi.org/10.1016/S0531-5131(01)00467-8
|
||||
[whi]: https://www.whi.org/
|
||||
[whi02]: http://doi.org/10.1001/jama.288.3.321
|
||||
[caa15]: https://doi.org/10.6004/jnccn.2015.0106
|
||||
[nhs]: https://nurseshealthstudy.org
|
||||
[swn18]: https://doi.org/10.1080/13697137.2017.1421925
|
||||
[m18]: https://doi.org/10.1080/13697137.2018.1455657
|
||||
[f07]: https://doi.org/10.1007/s10549-007-9523-x
|
||||
[ks13]: https://doi.org/10.3109/13697137.2013.768806
|
||||
[d18]: https://doi.org/10.1080/13697137.2018.1439915
|
||||
[wiki-1]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_progesterone#Oral_administration
|
||||
[graph-1]: https://web.archive.org/web/20220222215313/https://en.wikipedia.org/wiki/Template:Hormone_levels_with_oral_progesterone
|
||||
[cghf19-table2]: https://ars.els-cdn.com/content/image/1-s2.0-S014067361931709X-mmc1.pdf#page=29
|
||||
[k05]: https://doi.org/10.1016/j.maturitas.2005.02.018
|
||||
[p08]: https://doi.org/10.1007/978-0-387-69080-3_14
|
||||
[mr11]: https://doi.org/10.1515/HMBCI.2011.014
|
||||
[nich19]: https://doi.org/10.7326/M18-1323
|
||||
[h18]: https://doi.org/10.1038/s41467-018-06748-3
|
||||
[graph-2]: https://commons.wikimedia.org/wiki/File:Estrogen_and_progesterone_levels_during_pregnancy_in_women.png
|
||||
[r03]: https://doi.org/10.1186/bcr734
|
||||
[b17]: https://doi.org/10.1016/j.maturitas.2016.10.010
|
||||
[slp93]: https://doi.org/10.1002/ijc.2910530403
|
||||
[g05]: https://doi.org/10.1634/theoncologist.10-7-471
|
||||
[t03]: https://doi.org/10.1097/01.ju.0000056706.88960.7c
|
||||
[k06]: https://doi.org/10.1016/j.juro.2006.03.036
|
||||
[app-1]: https://docs.google.com/document/d/1oqPdRM6gON2hwl6QO1e0GdseYoK5X0J5AtxDZ5hB5tk/view
|
||||
[age89]: https://doi.org/10.1016/0026-0495(89)90233-3
|
||||
[k97]: https://doi.org/10.1046/j.1365-2265.1997.2601068.x
|
||||
[mg08]: https://doi.org/10.1530/EJE-08-0289
|
||||
[a11]: https://doi.org/10.1530/EJE-10-1038
|
||||
[g13]: https://doi.org/10.1111/jsm.12319
|
||||
[b18]: https://web.archive.org/web/20201112033637/https://www.endocrine-abstracts.org/ea/0056/ea0056p955.htm
|
||||
[b19]: https://doi.org/10.1136/bmj.l1652
|
||||
[f16]: http://doi.org/10.1097/MED.0000000000000231
|
||||
[palga]: https://www.palga.nl/
|
||||
[rw19]: https://doi.org/10.1007/s40278-019-62242-2
|
||||
[bdh19]: https://doi.org/10.1016/j.ecl.2019.02.005
|
||||
[bj15]: https://doi.org/10.1007/s10549-014-3213-2
|
||||
[b15]: https://doi.org/10.1089/lgbt.2014.0123
|
||||
[d19]: https://gmr.scholasticahq.com/article/7774-evaluating-risks-reported-cases-and-screening-recommendations-for-breast-cancer-in-transgender-patients
|
||||
[bj14]: https://doi.org/10.1007/s40615-014-0032-4
|
||||
[bj16]: https://doi.org/10.1089/lgbt.2015.0058
|
||||
[braun17]: https://doi.org/10.1093/epirev/mxw003
|
||||
[kais]: https://healthy.kaiserpermanente.org/
|
||||
[s17]: https://doi.org/10.1016/j.annepidem.2017.07.007
|
||||
[ts19]: https://doi.org/10.1210/er.2018-00011
|
||||
[w12]: https://doi.org/10.1111/j.1743-6109.2012.02876.x
|
||||
[d05]: https://doi.org/10.1111/j.1743-6109.2012.02876.x
|
||||
[wiki-2]: https://en.wikipedia.org/wiki/Harry_Benjamin
|
||||
[b64]: https://doi.org/10.1176/appi.psychotherapy.1964.18.3.458
|
||||
[b66]: https://books.google.com/books?id=S1iHGwAACAAJ
|
||||
[g11]: http://doi.org/10.1056/NEJMcp1008161
|
||||
[bw11]: https://doi.org/10.1007/978-1-4419-9896-5_2
|
||||
[bd13]: https://doi.org/10.1016/j.jadohealth.2012.09.019
|
||||
[b20]: https://doi.org/10.1016/j.jadohealth.2020.07.016
|
||||
[aw19-cd]: https://transfemscience.org/articles/cpa-dosage/
|
||||
[kahl06]: https://doi.org/10.4065/81.10.1290
|
||||
[z12]: https://doi.org/10.3109/13625187.2012.715357
|
||||
[j19]: https://doi.org/10.1097/md.0000000000015719
|
||||
[h82]: https://doi.org/10.1016/0002-9378(82)90108-9
|
||||
[cp89]: https://doi.org/10.1353/pbm.1990.0026
|
||||
[gore02]: https://www.kup.at/journals/summary/1071.html
|
||||
[aw21-iema]: https://transfemscience.org/articles/injectable-e2-meta-analysis/
|
||||
[n07]: https://doi.org/10.1136/jcp.2006.037838
|
||||
[do15]: https://doi.org/10.1016/j.humpath.2015.08.008
|
||||
[l15]: https://doi.org/10.1371/journal.pone.0118453
|
||||
[c15]: http://doi.org/10.1101/gr.185926.114
|
||||
[do18]: https://doi.org/10.1007/s00428-018-2377-2
|
||||
[h12]: https://doi.org/10.1016/S0140-6736(12)60071-3
|
||||
[td08]: https://doi.org/10.1159/000158055
|
||||
[h09]: https://doi.org/10.1002/9781444316728.ch9
|
||||
[aw20]: https://transfemscience.org/articles/cais-breast-dev-p4/
|
||||
[app-2]: https://transfemscience.org/articles/breast-cancer-suppl/
|
||||
[co20]: https://doi.org/10.1093/jbi/wbz092
|
||||
|
|
@ -1,168 +1,179 @@
|
|||
# 低剂量的醋酸环丙孕酮足以最大限度地抑制女性倾向跨性别者的睾酮水平
|
||||
---
|
||||
title: 低剂量的醋酸环丙孕酮足以最大限度地抑制女性倾向跨性别者的睾酮水平
|
||||
linkTitle: 低剂量醋酸环丙孕酮足可高效抑制睾酮
|
||||
description: 本文探讨了以更低剂量服用 CPA,并深入论证了低剂量的合理性。
|
||||
author: Aly W.
|
||||
published: 2019-07-01
|
||||
updated: 2022-10-19
|
||||
translated: 2022-10-21
|
||||
translators:
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 醋酸环丙孕酮
|
||||
- 孕激素
|
||||
- 抗雄激素制剂
|
||||
- 用药安全
|
||||
- 用药途径与剂量
|
||||
trackHash: 93a11ce0ec1f970b0f395fd4013806ec94cfb88c
|
||||
---
|
||||
|
||||
> - 作者 [Aly W.][AUTHOR]
|
||||
> + 首次发表于 2019 年 7 月 1 日
|
||||
> + 最后修改于 2022 年 10 月 19 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [Bersella AI][TRANSLATOR]
|
||||
> + 翻译于 2022 年 3 月 2 日
|
||||
> + 修订于 2022 年 10 月 21 日
|
||||
## 译者按 {#notice}
|
||||
|
||||
[AUTHOR]: https://transfemscience.org/about/#aly-w
|
||||
[ORIGIN]: https://transfemscience.org/articles/cpa-dosage/
|
||||
[TRANSLATOR]: https://bersella-ai.cc/about-me/
|
||||
|
||||
## 译者按
|
||||
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. **<u>⚠ 免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
---
|
||||
|
||||
## 摘要
|
||||
## 摘要 {#abstract}
|
||||
|
||||
> 醋酸环丙孕酮(CPA)是一种孕激素与抗雄制剂,广泛用于女性化激素治疗。其作为孕激素的作用,远甚于作为雄激素受体拮抗剂的作用。一般作为孕激素用于顺性别妇女时,其剂量介乎 1\~2 mg/天;作为抗雄制剂时,其剂量介乎 50\~300 mg/天。但对于后者,会有强烈的孕激素过量影响,以及与之关联的副作用和风险。
|
||||
> CPA 因其孕激素作用可抑制睾酮水平,故也有拮抗促性腺激素之效应。单服 CPA 时,睾酮水平最大可压制 50% 至 70%;而结合小剂量雌激素服用时,其可完全抑制来自性腺的睾酮分泌,并将睾酮水平降低约 95%——正好落入女性范围。尽管历史上曾有女性倾向跨性别者每日服用 50\~100 mg 的 CPA,但目前已知的是,5\~10 mg/天的剂量足以最大程度(或接近最大程度)抑制睾酮水平。
|
||||
> 醋酸环丙孕酮(CPA)是一种孕激素与抗雄制剂,广泛用于女性化激素治疗。其作为孕激素的作用,远甚于作为雄激素受体拮抗剂的作用。一般作为孕激素用于顺性别妇女时,其剂量介乎 1\~2 mg/天;作为抗雄制剂时,其剂量介乎 50\~300 mg/天。但对于后者,会有强烈的孕激素过量影响,以及与之关联的副作用和风险。\
|
||||
> CPA 因其孕激素作用可抑制睾酮水平,故也有拮抗促性腺激素之效应。单服 CPA 时,睾酮水平最大可压制 50% 至 70%;而结合小剂量雌激素服用时,其可完全抑制来自性腺的睾酮分泌,并将睾酮水平降低约 95%——正好落入女性范围。尽管历史上曾有女性倾向跨性别者每日服用 50\~100 mg 的 CPA,但目前已知的是,5\~10 mg/天的剂量足以最大程度(或接近最大程度)抑制睾酮水平。\
|
||||
> CPA 本身通常以 50 mg/片的形式提供。这些片剂可被切药器切开,之后每日或隔日服用一次,这样日均剂量可减至 6.25 至 12.5 mg。低剂量 CPA 不仅可显著减少开销,而且有更好的耐受性及安全性。出于其低剂量仍保持的效用、以及和剂量相关的风险之考量,针对女性倾向跨性别者的 CPA 临床用量正在快速减少。
|
||||
|
||||
## 前言
|
||||
## 前言 {#introduction}
|
||||
|
||||
本文讨论醋酸环丙孕酮(CPA)的剂量。CPA 是一种孕激素与抗雄制剂,用于女性倾向跨性别者的激素治疗。本文探讨了以更低剂量服用 CPA,并深入论证了低剂量的合理性。
|
||||
如果读者只对推荐剂量感兴趣,可见[推荐剂量](#cpa-%E7%9A%84%E6%8E%A8%E8%8D%90%E5%89%82%E9%87%8F)一节。
|
||||
本文讨论醋酸环丙孕酮(CPA)的剂量。CPA 是一种孕激素与抗雄制剂,用于女性倾向跨性别者的激素治疗。\
|
||||
本文探讨了以更低剂量服用 CPA,并深入论证了低剂量的合理性。
|
||||
|
||||
## CPA 之效力、传统剂量与健康风险
|
||||
如果读者只对推荐剂量感兴趣,可见[推荐剂量]({{< ref "#recommended-dosages" >}})一节。
|
||||
|
||||
CPA 是一种强效孕激素,在顺性别妇女身上,1 mg/天的剂量即可抑制排卵,1\~3 mg/天即可使子宫内膜转化 <sup>([维基百科][WIKI-1]; [表格][TABLE-1]; [Endrikat et al., 2011][E11])</sup>。该剂量的 CPA 之效力,相当于处在黄体期的绝经前妇女自然产生的孕酮量(25 mg/天)以及孕酮水平(15 ng/mL)之效力。当作为孕激素用于顺性别妇女时(例如作为避孕药,或更年期激素疗法制剂),CPA 以每片 1/2 mg 的形式提供。
|
||||
## CPA 之效力、传统剂量与健康风险 {#potency-conventional-dosages-and-health-risks}
|
||||
|
||||
和其孕激素效力相反,CPA 作为雄激素受体(AR)拮抗剂之效力弱得多<sup>([维基百科][WIKI-1])</sup>。作为抗雄制剂,其剂量一般介乎 50\~300 mg/天,对于顺性别男女皆如此。对于女性,一般使用 50\~100 mg/天以改善受雄激素影响的皮肤与毛发之状况(例如痤疮与多毛症);而对于男性,则一般使用 100\~300 mg/天以治疗前列腺癌(若伴随手术/药物阉割,则使用 100\~200 mg/天;单服 CPA 疗法则需 200\~300 mg/天)<sup>([维基百科][WIKI-2])</sup>。为此,CPA 一般被制成 50mg 或 100mg 的片剂以供服用 <sup>([维基百科][WIKI-3])</sup>。CPA 作为抗雄制剂有双重机制:通过其低剂量下的孕激素作用来抑制睾酮水平,高剂量下还可直接阻止睾酮作用于 AR。
|
||||
CPA 是一种强效孕激素,在顺性别妇女身上,1 mg/天的剂量即可抑制排卵,1\~3 mg/天即可使子宫内膜转化 <sup>([维基百科][wiki-1]; [表格][table-1]; [Endrikat et al., 2011][e11])</sup>。该剂量的 CPA 之效力,相当于处在黄体期的绝经前妇女自然产生的孕酮量(25 mg/天)以及孕酮水平(15 ng/mL)之效力。当作为孕激素用于顺性别妇女时(例如作为避孕药,或更年期激素疗法制剂),CPA 以每片 1/2 mg 的形式提供。
|
||||
|
||||
和其孕激素效力相反,CPA 作为雄激素受体(AR)拮抗剂之效力弱得多<sup>([维基百科][wiki-1])</sup>。作为抗雄制剂,其剂量一般介乎 50\~300 mg/天,对于顺性别男女皆如此。对于女性,一般使用 50\~100 mg/天以改善受雄激素影响的皮肤与毛发之状况(例如痤疮与多毛症);而对于男性,则一般使用 100\~300 mg/天以治疗前列腺癌(若伴随手术/药物阉割,则使用 100\~200 mg/天;单服 CPA 疗法则需 200\~300 mg/天)<sup>([维基百科][wiki-2])</sup>。为此,CPA 一般被制成 50mg 或 100mg 的片剂以供服用 <sup>([维基百科][wiki-3])</sup>。CPA 作为抗雄制剂有双重机制:通过其低剂量下的孕激素作用来抑制睾酮水平,高剂量下还可直接阻止睾酮作用于 AR。
|
||||
|
||||
CPA 因其孕激素效力远甚于 AR 拮抗剂效力,使用传统临床剂量会有强烈的孕激素过量影响。有三篇文献摘录描述了这点:
|
||||
|
||||
> CPA 与其前身醋酸氯地孕酮相似,皆为强效孕激素,在 20\~30 mg 剂量下即可使子宫内膜转化。……
|
||||
> CPA 每个月为完全达到临床上的雄激素拮抗效果所需剂量的生理效力,应相当于一个月经周期内所产生孕酮之效力的三十倍。CPA 尽管是 _(抗雄)_ 这方面最有用的药物,但并非是理想的抗雄制剂,尤其是,某些副作用还与孕激素的过量摄入有关(而非其雄激素拮抗效应)。……
|
||||
> 在需要 CPA 完全发挥雄激素拮抗效应的场合,产生的诸如疲倦、无力、体重增加等不良反应皆可能与严重过量摄入的孕激素之效力有关。 ([Hammerstein et al., 1975][H75])
|
||||
> CPA 与其前身醋酸氯地孕酮相似,皆为强效孕激素,在 20\~30 mg 剂量下即可使子宫内膜转化。……\
|
||||
> CPA 每个月为完全达到临床上的雄激素拮抗效果所需剂量的生理效力,应相当于一个月经周期内所产生孕酮之效力的三十倍。CPA 尽管是 _(抗雄)_ 这方面最有用的药物,但并非是理想的抗雄制剂,尤其是,某些副作用还与孕激素的过量摄入有关(而非其雄激素拮抗效应)。……\
|
||||
> 在需要 CPA 完全发挥雄激素拮抗效应的场合,产生的诸如疲倦、无力、体重增加等不良反应皆可能与严重过量摄入的孕激素之效力有关。 ([Hammerstein et al., 1975][h75])
|
||||
|
||||
> Fixson (1963) 在已摘除卵巢、且事前服用了雌激素的妇女身上试用 CPA;20\~30 mg 的剂量可使子宫内膜转化,这说明其为一种强效孕激素。对于月经推迟的试验,其有效剂量不明,但估计应低于 1mg/天<sup>(Miller and Jacobs 1986)</sup>。
|
||||
> 相比于孕激素效力,CPA 的雄激素拮抗效应应被认为相当羸弱;为完全发挥该效应,需要每日服用 100mg,这相当于用于月经周期转化的剂量之三倍<sup>(Hammerstein and Cupceancu 1969)</sup>(值得一提的是,该数值相当于整个月经周期中黄体分泌的孕酮总量)。 ([Hammerstein, 1990][H90])
|
||||
> Fixson (1963) 在已摘除卵巢、且事前服用了雌激素的妇女身上试用 CPA;20\~30 mg 的剂量可使子宫内膜转化,这说明其为一种强效孕激素。对于月经推迟的试验,其有效剂量不明,但估计应低于 1mg/天<sup>(Miller and Jacobs 1986)</sup>。\
|
||||
> 相比于孕激素效力,CPA 的雄激素拮抗效应应被认为相当羸弱;为完全发挥该效应,需要每日服用 100mg,这相当于用于月经周期转化的剂量之三倍<sup>(Hammerstein and Cupceancu 1969)</sup>(值得一提的是,该数值相当于整个月经周期中黄体分泌的孕酮总量)。 ([Hammerstein, 1990][h90])
|
||||
|
||||
> 在内分泌学性质上,CPA 应具有较强的孕激素效力以及有限的雄激素拮抗效力。……
|
||||
> 关于其孕激素活性,每月(每周期)需要 20-30 mg 以转化受雌激素驱动(oestrogen-primed)的子宫内膜,该剂量和醋酸氯地孕酮以及其它强效孕激素相似。为完全发挥雄激素拮抗效力,每日须至少服用 50-100 mg 的 CPA,此剂量相当于女性在整个月经周期的孕酮暴露量的两到三倍。必须承认,这种孕激素的摄入已严重过量,除非大幅减少其用量以及效力。……
|
||||
> 已有人指出,CPA 并非一种有利于内分泌平衡的药物成分,因为其孕激素效力显著优于雄激素拮抗效力。有一种方法可以避免伴随高剂量反向序贯疗法而生的孕激素的严重过量:就是合并使用低剂量的避孕药和一种纯抗雄制剂(例如游离的环丙孕酮)。……
|
||||
> 必须强调的是,CPA 远不是一种用于多毛症的抗雄疗法的理想药物,因为其孕激素效力过强,局部作用也并不佳。因此,在未来值得为此寻找平衡性更好的抗雄制剂。 ([Hammerstein, 1979][H79])
|
||||
> 在内分泌学性质上,CPA 应具有较强的孕激素效力以及有限的雄激素拮抗效力。……\
|
||||
> 关于其孕激素活性,每月(每周期)需要 20-30 mg 以转化受雌激素驱动(oestrogen-primed)的子宫内膜,该剂量和醋酸氯地孕酮以及其它强效孕激素相似。为完全发挥雄激素拮抗效力,每日须至少服用 50-100 mg 的 CPA,此剂量相当于女性在整个月经周期的孕酮暴露量的两到三倍。必须承认,这种孕激素的摄入已严重过量,除非大幅减少其用量以及效力。……\
|
||||
> 已有人指出,CPA 并非一种有利于内分泌平衡的药物成分,因为其孕激素效力显著优于雄激素拮抗效力。有一种方法可以避免伴随高剂量反向序贯疗法而生的孕激素的严重过量:就是合并使用低剂量的避孕药和一种纯抗雄制剂(例如游离的环丙孕酮)。……\
|
||||
> 必须强调的是,CPA 远不是一种用于多毛症的抗雄疗法的理想药物,因为其孕激素效力过强,局部作用也并不佳。因此,在未来值得为此寻找平衡性更好的抗雄制剂。 ([Hammerstein, 1979][h79])
|
||||
|
||||
因高剂量 CPA 导致的孕激素摄入的高度过量,以及 CPA 高剂量下产生的已知不良反应与风险之间,存在一定关联<sup>([维基百科][WIKI-4])</sup>。这些副作用包括:疲倦、抑郁、体重增加、高泌乳素水平<sup>([维基百科][WIKI-5])</sup>、良性脑膜瘤<sup>([Aly W., 2020][AW20-MEN]; [维基百科][WIKI-6]; [表格 1][TABLE-2]; [表格 2][TABLE-3])</sup>、血栓<sup>([维基百科][WIKI-7])</sup>以及心血管问题<sup>([维基百科][WIKI-8])</sup>等。这些风险和剂量相关;迄今未发现每日 1/2 mg 的 CPA 与此存在关联(但有一项例外,即合用炔雌醇时会提高血栓风险)。CPA 的肝毒性同样与剂量相关:一般当剂量超过 20 mg/天时,肝转化酶水平会有升高;若超过 100 mg/天,有罕见概率出现肝衰竭<sup>([维基百科][WIKI-9]; [表格][TABLE-4])</sup>。低剂量能够尽量减少风险,这就是为何使用尽可能少的 CPA 的根本所在。
|
||||
因高剂量 CPA 导致的孕激素摄入的高度过量,以及 CPA 高剂量下产生的已知不良反应与风险之间,存在一定关联<sup>([维基百科][wiki-4])</sup>。这些副作用包括:疲倦、抑郁、体重增加、高泌乳素水平<sup>([维基百科][wiki-5])</sup>、良性脑膜瘤<sup>([Aly W., 2020][aw20-men]; [维基百科][wiki-6]; [表格 1][table-2]; [表格 2][table-3])</sup>、血栓<sup>([维基百科][wiki-7])</sup>以及心血管问题<sup>([维基百科][wiki-8])</sup>等。这些风险和剂量相关;迄今未发现每日 1/2 mg 的 CPA 与此存在关联(但有一项例外,即合用炔雌醇时会提高血栓风险)。CPA 的肝毒性同样与剂量相关:一般当剂量超过 20 mg/天时,肝转化酶水平会有升高;若超过 100 mg/天,有罕见概率出现肝衰竭<sup>([维基百科][wiki-9]; [表格][table-4])</sup>。低剂量能够尽量减少风险,这就是为何使用尽可能少的 CPA 的根本所在。
|
||||
|
||||
历史上,曾有女性倾向跨性别者每日服用 50\~100 mg 的 CPA。但在 2017 年,美国内分泌学会发布了最新一版针对跨性别者激素治疗的临床实践指南,其中将 CPA 的推荐用量从 50\~100 mg/天降至 25\~50 mg/天<sup>([Hembree et al., 2017][H17]; [Hembree et al., 2009][H09])</sup>。此举可能是受到了日渐明了的高剂量 CPA 之风险的驱动。不过,新的推荐用量似乎仍远超实际所需。
|
||||
历史上,曾有女性倾向跨性别者每日服用 50\~100 mg 的 CPA。但在 2017 年,美国内分泌学会发布了最新一版针对跨性别者激素治疗的临床实践指南,其中将 CPA 的推荐用量从 50\~100 mg/天降至 25\~50 mg/天<sup>([Hembree et al., 2017][h17]; [Hembree et al., 2009][h09])</sup>。此举可能是受到了日渐明了的高剂量 CPA 之风险的驱动。不过,新的推荐用量似乎仍远超实际所需。
|
||||
|
||||
## 低剂量或高剂量 CPA 对睾酮的抑制
|
||||
## 低剂量或高剂量 CPA 对睾酮的抑制 {#testosterone-suppression-with-low-and-high-doses}
|
||||
|
||||
像 CPA 一类的孕激素,可以显著抑制出生指派性别为男、性腺完整的人群当中的睾酮水平。从 1970 年代到 1980 年代初发表的一系列规模较小、质量较低的研究项目发现,健康年轻男性每日服用 5\~10 mg 的 CPA,可将睾酮水平抑制 40\~70%。其中,一些项目报告了使用 5 mg/天剂量的睾酮抑制程度,和使用 10 mg/天剂量的几乎一致(皆抑制了约 50%;[图表][GRAPH-1]);而 10 mg/天剂量的效果则与 20 mg/天相近(皆为约 60\~70%;[图表][GRAPH-2])。同一项目里即使 CPA 剂量加倍,也未能提高睾酮抑制率,这表明实际仅需 5 或 10 mg/天的 CPA 剂量,即可最大程度抑制睾酮。一项在 2002 年进行的、使用更现代和更可靠的血清睾酮定量方法的研究项目,发现了 10 mg/天用量的 CPA 可将睾酮水平抑制 66%(从约 600±150 ng/dL 压减至约 185 ng/dL;但未提供标准差数据)<sup>([Meriggiola et al., 2002a][M02a])</sup>。
|
||||
像 CPA 一类的孕激素,可以显著抑制出生指派性别为男、性腺完整的人群当中的睾酮水平。从 1970 年代到 1980 年代初发表的一系列规模较小、质量较低的研究项目发现,健康年轻男性每日服用 5\~10 mg 的 CPA,可将睾酮水平抑制 40\~70%。其中,一些项目报告了使用 5 mg/天剂量的睾酮抑制程度,和使用 10 mg/天剂量的几乎一致(皆抑制了约 50%;[图表][graph-1]);而 10 mg/天剂量的效果则与 20 mg/天相近(皆为约 60\~70%;[图表][graph-2])。同一项目里即使 CPA 剂量加倍,也未能提高睾酮抑制率,这表明实际仅需 5 或 10 mg/天的 CPA 剂量,即可最大程度抑制睾酮。一项在 2002 年进行的、使用更现代和更可靠的血清睾酮定量方法的研究项目,发现了 10 mg/天用量的 CPA 可将睾酮水平抑制 66%(从约 600±150 ng/dL 压减至约 185 ng/dL;但未提供标准差数据)<sup>([Meriggiola et al., 2002a][m02a])</sup>。
|
||||
|
||||
> 
|
||||
> 
|
||||
> 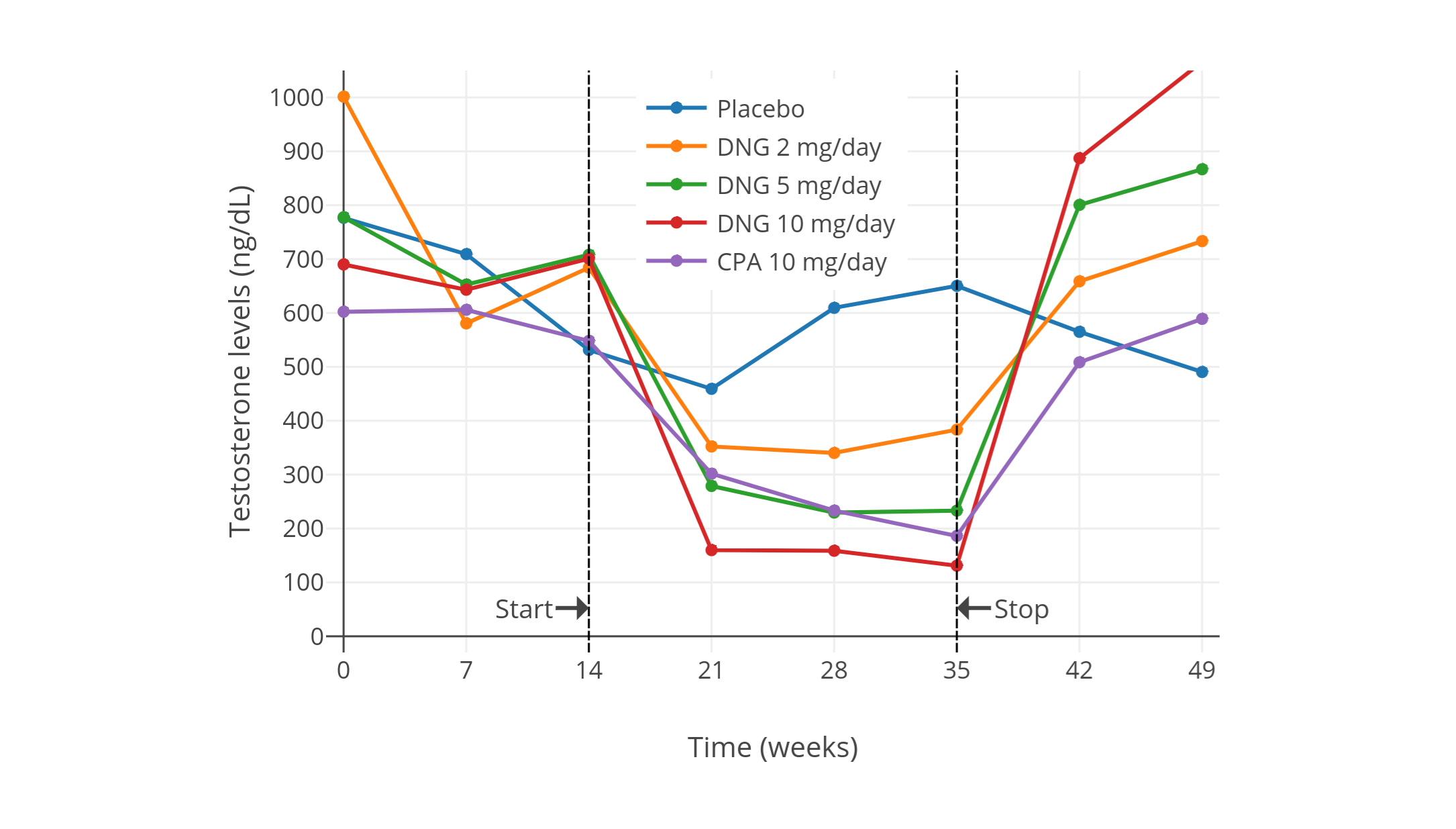
|
||||
>
|
||||
> ---
|
||||
>
|
||||
> 【多图表】男性单服低剂量 CPA 期间的睾酮水平。最下方的图表来自上述 2002 年的研究项目,使用了时间分辨荧光分析法(DELFIA)以测定睾酮水平。该项目还研究了不同剂量的地诺孕素(DNG);其仅需 1 mg/天剂量即可抑制排卵,这点与 CPA 相似。
|
||||
<section class="box">
|
||||
|
||||
有关其它孕激素之研究项目——诸如去氧孕烯、地诺孕素、醋酸氯地孕酮等,也同样发现:在男性身上可最大程度抑制睾酮水平的剂量,约为妇女抑制排卵所需剂量的 5\~10 倍<sup>(维基百科 [1][WIKI-10]; [2][WIKI-11]; [3][WIKI-12])</sup>。基于后者一般使用 1 mg/天的认知,可以认为 5\~10 mg/天剂量的 CPA 即可将睾酮的抑制效果最大化。该范围也与上述项目之发现相吻合。
|
||||

|
||||

|
||||

|
||||
|
||||
有关更高剂量 CPA 的研究项目则发现,高剂量下睾酮的抑制效果,仅略优于低剂量的表现。近年来一些针对健康的青春期及青年女性倾向跨性别者的研究项目,发现在单服 50\~100 mg/天的 CPA 的情况下,睾酮水平被抑制了 46~61%(在 4\~12 个月内,从 456–602 ng/dL 降至 226–294 ng/dL)。<sup>([Toorians et al., 2003][T03]; [Giltay et al., 2004][G04]; [T’Sjoen et al., 2005][T05]; [Tack et al., 2017][T17])</sup>
|
||||
针对患有前列腺癌的老年人群的研究则发现,单服高剂量 CPA 疗法——每日服用 50\~100 mg——可最多将睾酮水平抑制 70\~80%(降到了 50–200 ng/dL)。<sup>([Gräf, Brotherton, & Neumann, 1974][GBN74]; [Jacobi et al., 1980][J80] - [相关图表][J80-GRAPH]; [Knuth, Hano, & Nieschlag, 1984][KHN84] - [相关图表][KHN84-GRAPH]; [Schröder & Radlmaier, 2002][SR02]; [Nelson, 2011][N11])</sup>
|
||||
之所以在前列腺癌患者身上测出了更大的睾酮抑制率,可能是因为不同项目之间验血方法有所区别,以及/或者老年人群的 HPG 轴功能更弱、从而使睾酮水平更低。<sup>([Liu, Takahashi, & Veldhuis, 2017][LTV17]; [Winters, Wang, & Fortigel Study Group, 2010][WWF10])</sup>
|
||||
**多图表:** 男性单服低剂量 CPA 期间的睾酮水平。最下方的图表来自上述 2002 年的研究项目,使用了时间分辨荧光分析法(DELFIA)以测定睾酮水平。该项目还研究了不同剂量的地诺孕素(DNG);其仅需 1 mg/天剂量即可抑制排卵,这点与 CPA 相似。
|
||||
|
||||
目前已有人发现,长期使用单服孕激素疗法,会发生睾酮水平的“复原”或“逃逸”现象:尽管 _(前期)_ 其在最大有效剂量下即被显著抑制,但最终会逐渐回升。迄今该现象已在醋酸甲地孕酮上得到验证<sup>([维基百科][WIKI-13])</sup>;在 CPA 上亦有证实<sup>([Goldenberg & Bruchovsky, 1991][GB91]; [Saborowski, 1987][S87]; [Jacobi, Tunn, & Senge, 1982][JTS82])</sup>。其中一项研究显示,睾酮水平起初被抑制了 70% 左右;但在第 6\~12 个月疗程中,其回升至 50% 左右,并在此后至多 24 个月内维持稳定。采用单服孕激素疗法抑制睾酮时,需要关注到睾酮的逃逸现象。不过,迄今尚未发现合用雌激素与孕激素疗法与此现象存在关联。
|
||||
</section>
|
||||
|
||||
## 与雌激素合用时对睾酮的抑制作用
|
||||
有关其它孕激素之研究项目——诸如去氧孕烯、地诺孕素、醋酸氯地孕酮等,也同样发现:在男性身上可最大程度抑制睾酮水平的剂量,约为妇女抑制排卵所需剂量的 5\~10 倍<sup>(维基百科 [1][wiki-10]; [2][wiki-11]; [3][wiki-12])</sup>。基于后者一般使用 1 mg/天的认知,可以认为 5\~10 mg/天剂量的 CPA 即可将睾酮的抑制效果最大化。该范围也与上述项目之发现相吻合。
|
||||
|
||||
女性倾向跨性别者一般会将 CPA 与雌激素合用。雌激素同样可抑制睾酮水平。二者合用时,可产生抑制睾酮的协同作用,其剂量相较单服雌激素或孕激素时也更少。 _(如果单用雌激素,)_ 要将睾酮抑制到和经外科手术(即睾丸切除术)、或经药物(即 GnRH 拮抗剂)阉割相一致的水平,则要求相对较高的雌激素水平。当雌二醇浓度处在 200\~300 pg/mL 范围,其可抑制睾酮水平达 90% 左右(降至平均 50 ng/dL);如提高到 500 pg/mL 左右,则睾酮抑制率可达 95%(平均达 15 ng/dL)<sup>([维基百科][WIKI-14]; [图表][GRAPH-3])</sup>。由于需要超生理剂量的雌二醇方可最大程度(或接近最大程度)抑制睾酮,因此,往往采用低剂量雌二醇结合抗雄制剂/孕激素的方式来替代。
|
||||
有关更高剂量 CPA 的研究项目则发现,高剂量下睾酮的抑制效果,仅略优于低剂量的表现。近年来一些针对健康的青春期及青年女性倾向跨性别者的研究项目,发现在单服 50\~100 mg/天的 CPA 的情况下,睾酮水平被抑制了 46~61%(在 4\~12 个月内,从 456–602 ng/dL 降至 226–294 ng/dL)。<sup>([Toorians et al., 2003][t03]; [Giltay et al., 2004][g04]; [T’Sjoen et al., 2005][t05]; [Tack et al., 2017][t17])</sup>\
|
||||
针对患有前列腺癌的老年人群的研究则发现,单服高剂量 CPA 疗法——每日服用 50\~100 mg——可最多将睾酮水平抑制 70\~80%(降到了 50–200 ng/dL)。<sup>([Gräf, Brotherton, & Neumann, 1974][gbn74]; [Jacobi et al., 1980][j80] - [相关图表][j80-graph]; [Knuth, Hano, & Nieschlag, 1984][khn84] - [相关图表][khn84-graph]; [Schröder & Radlmaier, 2002][sr02]; [Nelson, 2011][n11])</sup>\
|
||||
之所以在前列腺癌患者身上测出了更大的睾酮抑制率,可能是因为不同项目之间验血方法有所区别,以及/或者老年人群的 HPG 轴功能更弱、从而使睾酮水平更低。<sup>([Liu, Takahashi, & Veldhuis, 2017][ltv17]; [Winters, Wang, & Fortigel Study Group, 2010][wwf10])</sup>
|
||||
|
||||
在 1980 和 1990 年代,针对前列腺癌患者的临床研究发现,将高剂量孕激素(例如每日服用 100\~300 mg 的 CPA、或 40\~160 mg 的醋酸甲地孕酮)结合低剂量雌激素(例如每日服用 0.1\~0.2 mg 的己烯雌酚、或 0.5\~1.5 mg 的雌二醇)使用,可完全抑制性腺分泌睾酮,并将睾酮水平减至阉割后的范围(小于 50 ng/dL)<sup>([Geller et al., 1981a][G81a]; [Geller et al., 1981b][G81b]; Geller & Albert, 1983; [Goldenberg et al., 1988][G88]; [Johnson et al., 1988][J88]; [Geller, 1988][GEL88]; [Venner et al., 1988][V88]; [Geller, 1991][G91]; Bruchovsky, 1991; [Bruchovsky et al., 1993][B93]; [Goldenberg et al., 1996][G96])</sup>。这里有一篇文献摘录对此做了详述:
|
||||
目前已有人发现,长期使用单服孕激素疗法,会发生睾酮水平的“复原”或“逃逸”现象:尽管 _(前期)_ 其在最大有效剂量下即被显著抑制,但最终会逐渐回升。迄今该现象已在醋酸甲地孕酮上得到验证<sup>([维基百科][wiki-13])</sup>;在 CPA 上亦有证实<sup>([Goldenberg & Bruchovsky, 1991][gb91]; [Saborowski, 1987][s87]; [Jacobi, Tunn, & Senge, 1982][jts82])</sup>。其中一项研究显示,睾酮水平起初被抑制了 70% 左右;但在第 6\~12 个月疗程中,其回升至 50% 左右,并在此后至多 24 个月内维持稳定。采用单服孕激素疗法抑制睾酮时,需要关注到睾酮的逃逸现象。不过,迄今尚未发现合用雌激素与孕激素疗法与此现象存在关联。
|
||||
|
||||
> 如前所述,CPA 并未完全抑制血浆睾酮浓度:其被抑制了 70% 左右,但数值仍相当于阉割后浓度的三倍。为系统研究该问题,Rennie 等 (59) 调查并对比了 12 种睾酮除去法。他们发现,将 CPA 与极低剂量的乙烯雌酚(0.1 mg/天)合用,可高效去除雄激素(例如血浆睾酮、组织内的双氢睾酮)。该团队 (60,61) 随后还发现,每日 200mg、甚至 100mg 的 CPA 足以获得相似的内分泌反馈,这也和其第二阶段临床治疗的相当正面的反馈具有关联性。出于内分泌学的视角,这项研究法不仅具有较多潜在优势,而且逻辑性很强:这种给药方案可结合两种制剂的抗雄效果;仅需少量雌激素,即可将血浆睾酮水平降低至经过阉割的程度。一旦睾酮达到阉割后水平,只需少量 CPA 即可中和剩余雄激素(主要来自肾上腺)的作用。在第三阶段疗程里,并未将合用低剂量 CPA 及乙烯雌酚的疗法,与常规疗法进行比较。考虑到内分泌反馈与观察结果,二者合用的疗法应该具有相对其它常规疗法的竞争力。([Schröder & Radlmaier, 2002][SR02])
|
||||
## 与雌激素合用时对睾酮的抑制作用 {#testosterone-suppression-in-combination-with-estrogen}
|
||||
|
||||
一项 2016 年的研究发现,在每日服用 50 mg 的 CPA、并涂抹 1\~2 mg 雌二醇透皮凝胶的女性倾向跨性别者当中,45 pg/mL 左右的雌二醇水平(结合 CPA)并不足以抑制睾酮到女性/阉割后范围;其睾酮水平约为 120\~190 ng/dL<sup>([Gava et al., 2016][G16]; [图表][GRAPH-4])</sup>。不过,85 pg/mL 左右的雌二醇水平(结合 CPA)则完全抑制了性腺的睾酮分泌,最终睾酮水平约在 20 ng/dL。因此,结合 CPA 来完全抑制睾酮所需的雌二醇浓度,需达到一个特定最小值。
|
||||
另一项在 2019 年进行、针对口服 CPA 与戊酸雌二醇的女性倾向跨性别者的研究显示,完全抑制睾酮水平所需的雌二醇浓度,中位数为 76 pg/mL,第 25 百分位数为 63 pg/mL<sup>([Angus et al., 2019][A19]; [图表][GRAPH-5])</sup>。
|
||||
女性倾向跨性别者一般会将 CPA 与雌激素合用。雌激素同样可抑制睾酮水平。二者合用时,可产生抑制睾酮的协同作用,其剂量相较单服雌激素或孕激素时也更少。 _(如果单用雌激素,)_ 要将睾酮抑制到和经外科手术(即睾丸切除术)、或经药物(即 GnRH 拮抗剂)阉割相一致的水平,则要求相对较高的雌激素水平。当雌二醇浓度处在 200\~300 pg/mL 范围,其可抑制睾酮水平达 90% 左右(降至平均 50 ng/dL);如提高到 500 pg/mL 左右,则睾酮抑制率可达 95%(平均达 15 ng/dL)<sup>([维基百科][wiki-14]; [图表][graph-3])</sup>。由于需要超生理剂量的雌二醇方可最大程度(或接近最大程度)抑制睾酮,因此,往往采用低剂量雌二醇结合抗雄制剂/孕激素的方式来替代。
|
||||
|
||||
> 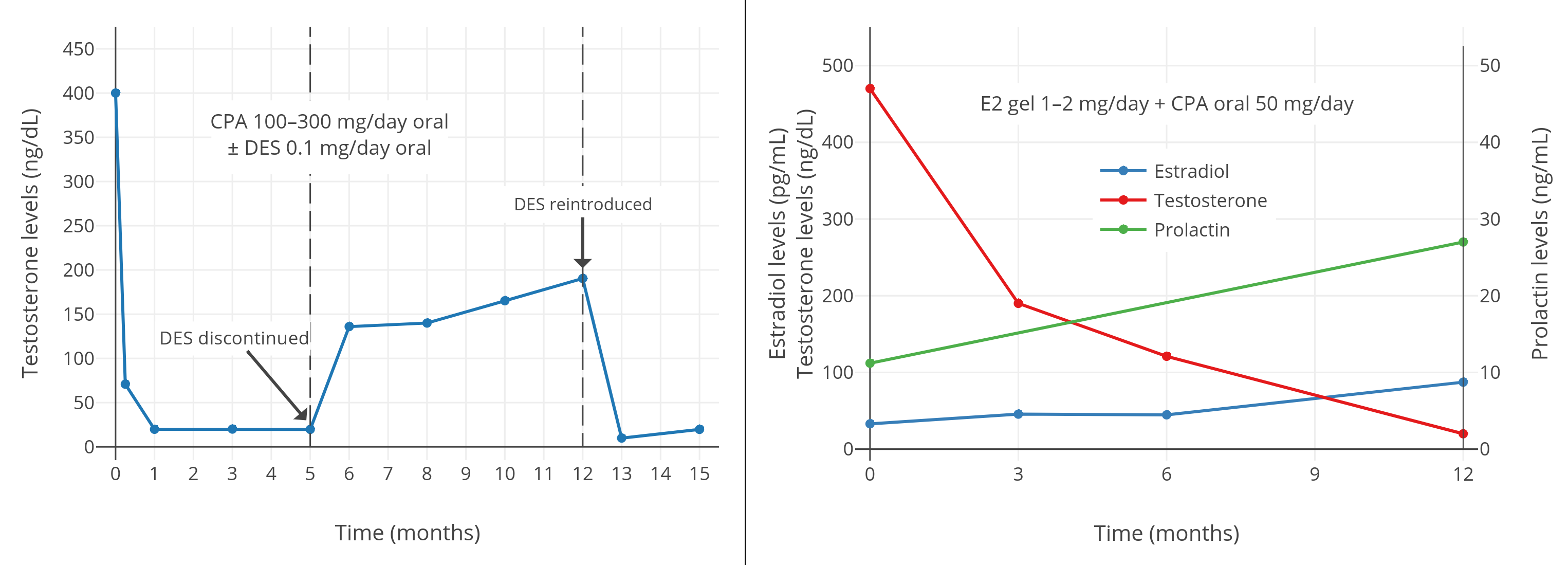
|
||||
> 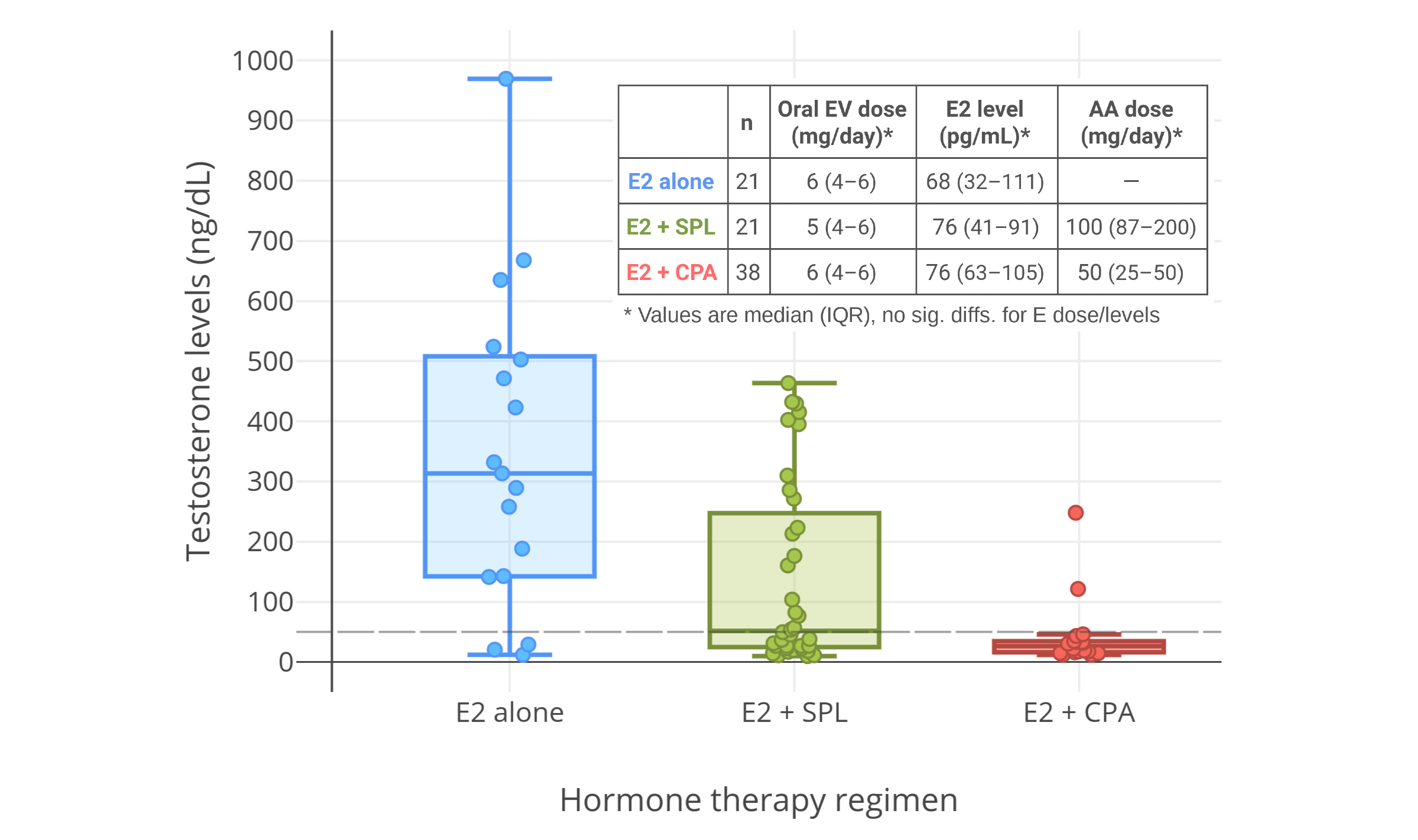
|
||||
> 
|
||||
>
|
||||
> ---
|
||||
>
|
||||
> 【多图表】男性、女性倾向跨性别者合用 CPA 与低剂量雌激素时的睾酮浓度。右上图附注:透皮雌二醇平均剂量在第 6\~12 个月有所提升。
|
||||
在 1980 和 1990 年代,针对前列腺癌患者的临床研究发现,将高剂量孕激素(例如每日服用 100\~300 mg 的 CPA、或 40\~160 mg 的醋酸甲地孕酮)结合低剂量雌激素(例如每日服用 0.1\~0.2 mg 的己烯雌酚、或 0.5\~1.5 mg 的雌二醇)使用,可完全抑制性腺分泌睾酮,并将睾酮水平减至阉割后的范围(小于 50 ng/dL)<sup>([Geller et al., 1981a][g81a]; [Geller et al., 1981b][g81b]; Geller & Albert, 1983; [Goldenberg et al., 1988][g88]; [Johnson et al., 1988][j88]; [Geller, 1988][gel88]; [Venner et al., 1988][v88]; [Geller, 1991][g91]; Bruchovsky, 1991; [Bruchovsky et al., 1993][b93]; [Goldenberg et al., 1996][g96])</sup>。这里有一篇文献摘录对此做了详述:
|
||||
|
||||
Fung 等人 (2017) 发现,女性倾向跨性别者结合 25/50 mg 每日的 CPA 与口服雌二醇(约 3.5 mg/天)或透皮雌二醇(约 3.5 mg/天的凝胶,或约 100 μg/天的贴片)使用,可完全、一致地抑制性腺的睾酮分泌,睾酮水平被抑制约 95%<sup>([Fung, Hellstern-Layefsky, & Lega, 2017][FHL17])</sup>。该剂量的雌二醇被认为可达到平均 100 pg/mL 的雌二醇水平<sup>([Aly W., 2020][AW20-E2-EQU]; [维基百科][WIKI-15])</sup>。Fung 等人 (2017) 的研究恰巧比美国内分泌学会的 2017 年版《指南》早发布六个月;该研究可能是促使后者所推荐的 CPA 剂量减少的原因(从 50\~100 mg/天降至 25\~50 mg/天)。
|
||||
> 如前所述,CPA 并未完全抑制血浆睾酮浓度:其被抑制了 70% 左右,但数值仍相当于阉割后浓度的三倍。为系统研究该问题,Rennie 等 (59) 调查并对比了 12 种睾酮除去法。他们发现,将 CPA 与极低剂量的乙烯雌酚(0.1 mg/天)合用,可高效去除雄激素(例如血浆睾酮、组织内的双氢睾酮)。该团队 (60,61) 随后还发现,每日 200mg、甚至 100mg 的 CPA 足以获得相似的内分泌反馈,这也和其第二阶段临床治疗的相当正面的反馈具有关联性。出于内分泌学的视角,这项研究法不仅具有较多潜在优势,而且逻辑性很强:这种给药方案可结合两种制剂的抗雄效果;仅需少量雌激素,即可将血浆睾酮水平降低至经过阉割的程度。一旦睾酮达到阉割后水平,只需少量 CPA 即可中和剩余雄激素(主要来自肾上腺)的作用。在第三阶段疗程里,并未将合用低剂量 CPA 及乙烯雌酚的疗法,与常规疗法进行比较。考虑到内分泌反馈与观察结果,二者合用的疗法应该具有相对其它常规疗法的竞争力。([Schröder & Radlmaier, 2002][sr02])
|
||||
|
||||
迄今罕有研究了结合低剂量 CPA 与中、低剂量雌激素对睾酮之抑制的项目。不过,基于单服 5\~10 mg/天的 CPA 已可最大程度抑制睾酮的事实,可以认为其效果与高剂量的类似。根据部分研究,结合使用 5\~12.5 mg/天的 CPA 与用于生理替代的睾酮的健康年轻男性,已检测不出促性腺激素(小于 0.5 IU/L),睾丸功能因此被完全抑制<sup>([Meriggiola et al., 1998][M98]; [Meriggiola et al., 2002b][M02b])</sup>。雌二醇的促性腺激素拮抗效应,相对睾酮也更强<sup>([维基百科][WIKI-16])</sup>,因此这些发现或许也适用于结合 CPA 与用于生理替代的雌二醇的情况(例如平均 100\~200 pg/mL 的雌二醇浓度)。
|
||||
一项 2016 年的研究发现,在每日服用 50 mg 的 CPA、并涂抹 1\~2 mg 雌二醇透皮凝胶的女性倾向跨性别者当中,45 pg/mL 左右的雌二醇水平(结合 CPA)并不足以抑制睾酮到女性/阉割后范围;其睾酮水平约为 120\~190 ng/dL<sup>([Gava et al., 2016][g16]; [图表][graph-4])</sup>。不过,85 pg/mL 左右的雌二醇水平(结合 CPA)则完全抑制了性腺的睾酮分泌,最终睾酮水平约在 20 ng/dL。因此,结合 CPA 来完全抑制睾酮所需的雌二醇浓度,需达到一个特定最小值。\
|
||||
另一项在 2019 年进行、针对口服 CPA 与戊酸雌二醇的女性倾向跨性别者的研究显示,完全抑制睾酮水平所需的雌二醇浓度,中位数为 76 pg/mL,第 25 百分位数为 63 pg/mL<sup>([Angus et al., 2019][a19]; [图表][graph-5])</sup>。
|
||||
|
||||
依据 [Meyer 等人 (2020)][M20] [[PDF][M20-PDF]] 对 155 名女性倾向跨性别者合用 CPA 与雌二醇进行的研究,10、25、50 mg/天剂量的 CPA 并未在睾酮水平上形成差异;三者皆达到较高抑制率(平均降至 15–20 ng/dL,落入女性正常范围的下限)。其中所用雌二醇形态包括:戊酸雌二醇口服片(剂量范围 3–10 mg/天、中位数 6 mg/天),以及雌二醇透皮贴片(100 μg/天)。雌二醇浓度平均达 100 pg/mL;而四分位间距(即第 25、第 75 百分位之差)则可达 100 pg/mL 左右。该研究表明,对于女性倾向跨性别者,如果其雌二醇水平合适,仅需不超过 10 mg/天的 CPA 即可完全抑制睾酮水平。
|
||||
另一项研究也发现,女性倾向跨性别者使用小于 20 mg/天、和大于 50 mg/天的 CPA,在睾酮抑制率上无任何区别<sup>([Even-Zohar et al., 2020][EZ20])</sup>。
|
||||
<section class="box">
|
||||
|
||||
在雌二醇水平合适的情况下,为抑制睾酮甚至仅需低于 5 mg/天剂量的 CPA(例如 2 mg/天),然而尚无任何研究予以证实。不过,这种概念在对其它孕激素的研究中已有先例。例如,在一项研究里,女性倾向跨性别者每日服用 10 mg 的醋酸甲羟孕酮(该剂量大致相当于可抑制绝经前妇女排卵的 CPA 剂量:1 mg/天<sup>([表格][TABLE-1])</sup>),其睾酮水平下降了 63%,达 215 ng/dL(相比之下,雌二醇—螺内酯联合疗法可达 79 ng/dL)<sup>([Jain, Kwan, & Forcier, 2019][JKF19])</sup>。因此,可以期望极低剂量的 CPA 也能达到类似效果;而且,这种剂量还具有将人体孕激素暴露量减至正常生理水平的益处。
|
||||

|
||||

|
||||

|
||||
|
||||
## 更低剂量 CPA 的临床应用
|
||||
**多图表:** 男性、女性倾向跨性别者合用 CPA 与低剂量雌激素时的睾酮浓度。右上图附注:透皮雌二醇平均剂量在第 6\~12 个月有所提升。
|
||||
|
||||
考虑到高剂量 CPA 的风险、以及其低剂量下较强的睾酮抑制能力,临床上低剂量 CPA 正更多地被用于女性化激素治疗。许多文献证实了这点,其中向女性倾向跨性别者推荐了更少的剂量<sup>(例如: [Lederbogen, 2009][L09]; [Fung, Hellstern-Layefsky, & Lega, 2017][FHL17]; [Heath & Wynne, 2019][HW19]; [Winkler-Crepaz et al., 2017][WC17]; [Mahfouda et al., 2018][M18]; [Oliphant et al., 2018][O18]; [Athanasoulia-Kaspar & Stalla, 2019][AKS19]; [Bourns, 2019][B19]; [Fuss et al., 2019][F19]; [Jacobeit, 2019][J19]; [Nota, den Heijer, & Gooren, 2019][NHG19]; [澳洲与新西兰临床试验登记系统, ANZCTR, 2020][A20]; [Meyer et al., 2020][M20] [[PDF][M20-PDF]]; [T’Sjoen et al., 2020][TS20])</sup>。其中,Nota, den Heijer, & Gooren (2019) 的文章将 CPA 推荐的、最低必要剂量定为 10\~50 mg/天,该剂量与先前过大的推荐及使用剂量(100 mg/天)<sup>([Asscheman & Gooren, 1993][AG93]; [Gooren, Giltay, & Bunck, 2008][GGB08])</sup>形成了鲜明反差。
|
||||
</section>
|
||||
|
||||
## 更高剂量 CPA 的雄激素受体拮抗效应
|
||||
Fung 等人 (2017) 发现,女性倾向跨性别者结合 25/50 mg 每日的 CPA 与口服雌二醇(约 3.5 mg/天)或透皮雌二醇(约 3.5 mg/天的凝胶,或约 100 μg/天的贴片)使用,可完全、一致地抑制性腺的睾酮分泌,睾酮水平被抑制约 95%<sup>([Fung, Hellstern-Layefsky, & Lega, 2017][fhl17])</sup>。该剂量的雌二醇被认为可达到平均 100 pg/mL 的雌二醇水平<sup>([Aly W., 2020][aw20-e2-equ]; [维基百科][wiki-15])</sup>。Fung 等人 (2017) 的研究恰巧比美国内分泌学会的 2017 年版《指南》早发布六个月;该研究可能是促使后者所推荐的 CPA 剂量减少的原因(从 50\~100 mg/天降至 25\~50 mg/天)。
|
||||
|
||||
迄今罕有研究了结合低剂量 CPA 与中、低剂量雌激素对睾酮之抑制的项目。不过,基于单服 5\~10 mg/天的 CPA 已可最大程度抑制睾酮的事实,可以认为其效果与高剂量的类似。根据部分研究,结合使用 5\~12.5 mg/天的 CPA 与用于生理替代的睾酮的健康年轻男性,已检测不出促性腺激素(小于 0.5 IU/L),睾丸功能因此被完全抑制<sup>([Meriggiola et al., 1998][m98]; [Meriggiola et al., 2002b][m02b])</sup>。雌二醇的促性腺激素拮抗效应,相对睾酮也更强<sup>([维基百科][wiki-16])</sup>,因此这些发现或许也适用于结合 CPA 与用于生理替代的雌二醇的情况(例如平均 100\~200 pg/mL 的雌二醇浓度)。
|
||||
|
||||
依据 [Meyer 等人 (2020)][m20] [[PDF][M20-PDF]] 对 155 名女性倾向跨性别者合用 CPA 与雌二醇进行的研究,10、25、50 mg/天剂量的 CPA 并未在睾酮水平上形成差异;三者皆达到较高抑制率(平均降至 15–20 ng/dL,落入女性正常范围的下限)。其中所用雌二醇形态包括:戊酸雌二醇口服片(剂量范围 3–10 mg/天、中位数 6 mg/天),以及雌二醇透皮贴片(100 μg/天)。雌二醇浓度平均达 100 pg/mL;而四分位间距(即第 25、第 75 百分位之差)则可达 100 pg/mL 左右。该研究表明,对于女性倾向跨性别者,如果其雌二醇水平合适,仅需不超过 10 mg/天的 CPA 即可完全抑制睾酮水平。\
|
||||
另一项研究也发现,女性倾向跨性别者使用小于 20 mg/天、和大于 50 mg/天的 CPA,在睾酮抑制率上无任何区别<sup>([Even-Zohar et al., 2020][ez20])</sup>。
|
||||
|
||||
在雌二醇水平合适的情况下,为抑制睾酮甚至仅需低于 5 mg/天剂量的 CPA(例如 2 mg/天),然而尚无任何研究予以证实。不过,这种概念在对其它孕激素的研究中已有先例。例如,在一项研究里,女性倾向跨性别者每日服用 10 mg 的醋酸甲羟孕酮(该剂量大致相当于可抑制绝经前妇女排卵的 CPA 剂量:1 mg/天<sup>([表格][table-1])</sup>),其睾酮水平下降了 63%,达 215 ng/dL(相比之下,雌二醇—螺内酯联合疗法可达 79 ng/dL)<sup>([Jain, Kwan, & Forcier, 2019][jkf19])</sup>。因此,可以期望极低剂量的 CPA 也能达到类似效果;而且,这种剂量还具有将人体孕激素暴露量减至正常生理水平的益处。
|
||||
|
||||
## 更低剂量 CPA 的临床应用 {#clinical-adoption-of-lower-doses}
|
||||
|
||||
考虑到高剂量 CPA 的风险、以及其低剂量下较强的睾酮抑制能力,临床上低剂量 CPA 正更多地被用于女性化激素治疗。许多文献证实了这点,其中向女性倾向跨性别者推荐了更少的剂量<sup>(例如: [Lederbogen, 2009][l09]; [Fung, Hellstern-Layefsky, & Lega, 2017][fhl17]; [Heath & Wynne, 2019][hw19]; [Winkler-Crepaz et al., 2017][wc17]; [Mahfouda et al., 2018][m18]; [Oliphant et al., 2018][o18]; [Athanasoulia-Kaspar & Stalla, 2019][aks19]; [Bourns, 2019][b19]; [Fuss et al., 2019][f19]; [Jacobeit, 2019][j19]; [Nota, den Heijer, & Gooren, 2019][nhg19]; [澳洲与新西兰临床试验登记系统, ANZCTR, 2020][a20]; [Meyer et al., 2020][m20] [[PDF][M20-PDF]]; [T’Sjoen et al., 2020][ts20])</sup>。其中,Nota, den Heijer, & Gooren (2019) 的文章将 CPA 推荐的、最低必要剂量定为 10\~50 mg/天,该剂量与先前过大的推荐及使用剂量(100 mg/天)<sup>([Asscheman & Gooren, 1993][ag93]; [Gooren, Giltay, & Bunck, 2008][ggb08])</sup>形成了鲜明反差。
|
||||
|
||||
## 更高剂量 CPA 的雄激素受体拮抗效应 {#androgen-receptor-antagonism-with-higher-doses}
|
||||
|
||||
CPA 的雄激素受体(AR)拮抗效应相对较弱。为达到有意义、或明显的 AR 拮抗效果,每日需服用 50\~300 mg。但很不幸,该剂量造成了孕激素的严重过度摄入,继而存在与更高风险及更多不良反应的关联。因此,不宜再推荐使用这种剂量。基于合理的角度,CPA 应仅作为孕激素,以较低剂量来抑制睾酮水平。例如,可最大程度抑制睾酮的 CPA 剂量,大约在 10 mg/天或以下;适宜女性倾向跨性别者的最大剂量,应接近该数值。(不过,一天 12.5 mg 的剂量亦可接受。)
|
||||
|
||||
需要强调的是:将 CPA 结合雌激素使用,可将睾酮水平轻松抑制到女性、或阉割后范围(往往还*低于* 女性平均水平),因此并不需要伴随 AR 拮抗作用。无论如何,如果仍需要、或期望通过 AR 拮抗作用来中和剩余的处在女性、或阉割后水平的睾酮(例如治疗顽固痤疮、或有其它目的),可以在 CPA 之外再补充少量非孕激素类 AR 拮抗剂,例如比卡鲁胺、螺内酯等,这些相对高剂量 CPA 而言更为安全。
|
||||
|
||||
## CPA 的推荐剂量
|
||||
## CPA 的推荐剂量 {#recommended-dosages}
|
||||
|
||||
### 抑制睾酮所需剂量
|
||||
### 抑制睾酮所需剂量 {#estrogen-plus-cyproterone-acetate}
|
||||
|
||||
> **如结合雌激素使用:**
|
||||
|
||||
对于女性倾向跨性别者,下表所示 CPA 剂量足以最大程度抑制睾酮水平:
|
||||
|
||||
| 剂型 | 最小剂量 | 最大剂量 | 用法 |
|
||||
| ---------- | ---------- | ---------- | -------------- |
|
||||
| 10 mg 片剂 | 5 mg/天 | 10 mg/天 | 每日半片到一片 |
|
||||
| 50 mg 片剂 | 6.25 mg/天 | 12.5 mg/天 | 每日 ⅛ 到 ¼ 片 |
|
||||
```csv
|
||||
剂型,最小剂量,最大剂量,用法
|
||||
10 mg 片剂,5 mg/天,10 mg/天,每日半片到一片
|
||||
50 mg 片剂,6.25 mg/天,12.5 mg/天,每日 ⅛ 到 ¼ 片
|
||||
```
|
||||
|
||||
最初一个月内,仅使用最小剂量。一个月过后,测量睾酮水平以确认其是否处在女性、或阉割后范围(小于 50 ng/dL)。如要完全抑制睾酮,需同时让雌二醇水平至少达到 65 pg/mL 左右(无关 CPA 剂量)。如果一个月后睾酮未被充分抑制、而雌二醇水平已足够,那么将 CPA 剂量加至最大推荐量,过一个月再测量睾酮水平。不过,作为替代,也可增加雌二醇用量;雌二醇水平越高,睾酮抑制率更佳。
|
||||
|
||||
> **如单服 CPA:**
|
||||
> **如单服 CPA:** 不建议单服 CPA 以抑制睾酮;因为其存在骨质疏松风险,以及其它由性激素缺乏引起的症状<sup>([维基百科][wiki-17]; [Aly W., 2019][aw19-nb])</sup>。无论如何,单服的推荐剂量基本等同于上述合用雌激素时的用量。不过,略高的剂量(10\~12 mg/天)不失为一种更好的选择。
|
||||
|
||||
不建议单服 CPA 以抑制睾酮;因为其存在骨质疏松风险,以及其它由性激素缺乏引起的症状<sup>([维基百科][WIKI-17]; [Aly W., 2019][AW19-NB])</sup>。无论如何,单服的推荐剂量基本等同于上述合用雌激素时的用量。不过,略高的剂量(10\~12 mg/天)不失为一种更好的选择。
|
||||
|
||||
### 孕激素作用所需剂量
|
||||
### 孕激素作用所需剂量 {#cyproterone-acetate-alone}
|
||||
|
||||
对于女性倾向跨性别者,下表所示 CPA 剂量基本与通常的孕激素生理暴露量(即排卵期内孕激素水平)相似:
|
||||
|
||||
| 剂型 | 剂量 | 用法 |
|
||||
| ---------- | ----------- | ------------ |
|
||||
| 10 mg 片剂 | 2.5 mg/天 | 每日 ¼ 片 |
|
||||
| 50 mg 片剂 | 3.125 mg/天 | 每日 1/16 片 |
|
||||
```csv
|
||||
剂型,剂量,用法
|
||||
10 mg 片剂,2.5 mg/天,每日 ¼ 片
|
||||
50 mg 片剂,3.125 mg/天,每日 1/16 片
|
||||
```
|
||||
|
||||
### 一些补充
|
||||
### 一些补充 {#additional-topics}
|
||||
|
||||
在合用 CPA 与雌激素治疗时,作为理想之举,应通过采血来测量睾酮水平,以确保其被充分抑制。
|
||||
|
||||
可以使用切药器来切割 CPA 片剂。另外,还可每过 2 日或 3 日服用一次 CPA(而非每日服用),这样可平摊日均剂量。有一点需要补充:CPA 的清除半衰期较长,一般为 1.5\~2 日,最长可达 4 日<sup>([维基百科][WIKI-18]; [图表][GRAPH-6])</sup>。因此,隔日服用、甚至每 3 日服用一次,是有市场的,也完全合情合理。
|
||||
可以使用切药器来切割 CPA 片剂。另外,还可每过 2 日或 3 日服用一次 CPA(而非每日服用),这样可平摊日均剂量。有一点需要补充:CPA 的清除半衰期较长,一般为 1.5\~2 日,最长可达 4 日<sup>([维基百科][wiki-18]; [图表][graph-6])</sup>。因此,隔日服用、甚至每 3 日服用一次,是有市场的,也完全合情合理。
|
||||
|
||||
如果已经用 CPA 与雌激素压制睾酮到了女性、或阉割后水平,但仍期望通过 AR 拮抗作用来中和剩余睾酮;那么可以补充少量 AR 拮抗剂,例如比卡鲁胺(6.25\~25 mg/天)或螺内酯(100\~200 mg/天)。
|
||||
|
||||
---
|
||||
|
||||
## 后记
|
||||
## 后记 {#updates}
|
||||
|
||||
### 后记一
|
||||
### 后记一 {#update-1}
|
||||
|
||||
澳大利亚昆士兰大学的 Judith Dean 博士,正进行一项名曰 [GoLoCypro][GLC] 的研究(2019-2022 年)。该项目会评估 120\~350 名女性倾向跨性别者合用 CPA 与雌二醇时,不同 CPA 剂量(每周两次 12.5 mg,隔日 12.5 mg,以及每日 12.5 mg、25 mg、50 mg)所产生的影响。CPA 剂量会被滴定到一个可维持睾酮水平在 0.5\~1.5 nmol/L(14\~43 ng/dL)的临床目标范围内的最小值。该项目是第一个研究女性倾向跨性别者使用不同剂量 CPA 的课题;其提供的有关可充分抑制睾酮的 CPA 最小剂量的宝贵资料亦备受关注。
|
||||
澳大利亚昆士兰大学的 Judith Dean 博士,正进行一项名曰 [GoLoCypro][glc] 的研究(2019-2022 年)。该项目会评估 120\~350 名女性倾向跨性别者合用 CPA 与雌二醇时,不同 CPA 剂量(每周两次 12.5 mg,隔日 12.5 mg,以及每日 12.5 mg、25 mg、50 mg)所产生的影响。CPA 剂量会被滴定到一个可维持睾酮水平在 0.5\~1.5 nmol/L(14\~43 ng/dL)的临床目标范围内的最小值。该项目是第一个研究女性倾向跨性别者使用不同剂量 CPA 的课题;其提供的有关可充分抑制睾酮的 CPA 最小剂量的宝贵资料亦备受关注。
|
||||
|
||||
### 后记二
|
||||
### 后记二 {#update-2}
|
||||
|
||||
2021 年 7 月,欧洲性别不一致调查组织网络(European Network for the Investigation of Gender Incongruence, ENIGI)在线发表了一篇有关女性倾向跨性别者使用低剂量 CPA 的研究论文:
|
||||
|
||||
- Kuijpers, S. M., Wiepjes, C. M., Conemans, E. B., Fisher, A. D., T’Sjoen, G., & den Heijer, M. (2021).
|
||||
Toward a lowest effective dose of cyproterone acetate in trans women: Results from the ENIGI study.
|
||||
The Journal of Clinical Endocrinology & Metabolism, 106(10), e3936–e3945. [[DOI:10.1210/clinem/dgab427][K21]]
|
||||
- Kuijpers, S. M., Wiepjes, C. M., Conemans, E. B., Fisher, A. D., T’Sjoen, G., & den Heijer, M. (2021).
|
||||
Toward a lowest effective dose of cyproterone acetate in trans women: Results from the ENIGI study.
|
||||
The Journal of Clinical Endocrinology & Metabolism, 106(10), e3936–e3945. \[DOI: <https://doi.org/10.1210/clinem/dgab427>]
|
||||
|
||||
该项目结合使用了雌二醇与 CPA,所用剂量如下:
|
||||
|
||||
|
|
@ -171,14 +182,15 @@ CPA 的雄激素受体(AR)拮抗效应相对较弱。为达到有意义、
|
|||
|
||||
在不服用 CPA 的实验组,睾酮的抑制并不充分;而所有服用 CPA 的实验组皆达到完全、且一致的睾酮抑制效果。结果如下:
|
||||
|
||||
| CPA 剂量 | 不服用 | 10 mg/天 | 25 mg/天 | 50 mg/天 | 100 mg/天 |
|
||||
| ------------------------------ | ------ | -------- | -------- | -------- | --------- |
|
||||
| 初始受试者人数 | 34 | 4 | 234 | 599 | 11 |
|
||||
| 提高剂量的人数 | 16 | 1 | 11 | 2 | 0 |
|
||||
| 降低剂量的人数 | 0 | 0 | 4 | 40 | 7 |
|
||||
| 睾酮水平(nmol/L) | 5.5 | 0.9 | 0.9 | 1.1 | 0.9 |
|
||||
| 睾酮水平(ng/dL) | \~160 | \~26 | \~26 | \~32 | \~26 |
|
||||
| 检出睾酮低于 2 nmol/L 次数占比 | 46.3% | 92.3% | 96.2% | 93.4% | 100% |
|
||||
```csv
|
||||
CPA 剂量,不服用,10 mg/天,25 mg/天,50 mg/天,100 mg/天
|
||||
初始受试者人数,34,4,234,599,11
|
||||
提高剂量的人数,16,1,11,2,0
|
||||
降低剂量的人数,0,0,4,40,7
|
||||
睾酮水平(nmol/L),5.5,0.9,0.9,1.1,0.9
|
||||
睾酮水平(ng/dL),\~160,\~26,\~26,\~32,\~26
|
||||
检出睾酮低于 2 nmol/L 次数占比,46.3%,92.3%,96.2%,93.4%,100%
|
||||
```
|
||||
|
||||
该项目并未提供受试者总人数,以及调整 CPA 剂量之后的验血结果。因此,10 mg/天实验组的实际人数与验血结果并不可靠。不过,基于以上“检出睾酮低于 2 nmol/L 次数占比”的数据,该实验组的验血次数应当至少有 13 次(92.3% 大致等于 12/13,但也可能是 24/26,以此类推)。论文作者考虑到该组别人数/验血次数较少,也作出了解释:
|
||||
|
||||
|
|
@ -188,69 +200,70 @@ CPA 的雄激素受体(AR)拮抗效应相对较弱。为达到有意义、
|
|||
|
||||
论文作者总结如下:
|
||||
|
||||
> 总而言之,对于这组跨性别女性群体,10 mg/天的 CPA 被发现足以将睾酮浓度降低至在顺性别妇女测出的范围内。该剂量 CPA 不仅和高剂量同样有效,而且对泌乳素浓度的影响更小,也能维持更高的高密度脂蛋白(胆固醇)水平。
|
||||
> 尽管相较 CPA,选择长期副作用更少的 GnRH 拮抗剂更佳;但如果 GnRH 拮抗剂有使用禁忌、无法获取、或者无法报销(reimbursed)的情况,那么依据本项目的发现,低剂量 CPA 也不失为一种选项。
|
||||
> 总而言之,对于这组跨性别女性群体,10 mg/天的 CPA 被发现足以将睾酮浓度降低至在顺性别妇女测出的范围内。该剂量 CPA 不仅和高剂量同样有效,而且对泌乳素浓度的影响更小,也能维持更高的高密度脂蛋白(胆固醇)水平。\
|
||||
> 尽管相较 CPA,选择长期副作用更少的 GnRH 拮抗剂更佳;但如果 GnRH 拮抗剂有使用禁忌、无法获取、或者无法报销(reimbursed)的情况,那么依据本项目的发现,低剂量 CPA 也不失为一种选项。\
|
||||
> 将来的研究重点,应该放在对更小剂量 CPA(例如 5 mg)之效力的评估、以及其潜在的长期副作用上。
|
||||
|
||||
围绕该论文的观点,论文作者之一:Guy T’Sjoen 及其他同行还在一篇对女性倾向跨性别者而言最佳的激素疗法之论述中,推荐 CPA 剂量应不高于 10 或 12.5 mg/天,且不应持续服用超过两年<sup>([Glintborg et al., 2021][G21])</sup>。值得一提的是,T’Sjoen 其人被视为跨性别医学方面首屈一指的专家之一;他也是美国内分泌学会《跨性别护理指南》的联名作者之一<sup>([Hembree et al., 2017][H17])</sup>。
|
||||
围绕该论文的观点,论文作者之一:Guy T’Sjoen 及其他同行还在一篇对女性倾向跨性别者而言最佳的激素疗法之论述中,推荐 CPA 剂量应不高于 10 或 12.5 mg/天,且不应持续服用超过两年<sup>([Glintborg et al., 2021][g21])</sup>。值得一提的是,T’Sjoen 其人被视为跨性别医学方面首屈一指的专家之一;他也是美国内分泌学会《跨性别护理指南》的联名作者之一<sup>([Hembree et al., 2017][h17])</sup>。
|
||||
|
||||
在 Kuijpers 及其同行发表论文后不久,以色列的 Even Zohar 及其同行也于 2021 年 7 月,发表了一篇有关女性倾向跨性别者使用低剂量 CPA 的研究论文(其最初在 2020 年 5 月,作为会议摘要发表):
|
||||
|
||||
- Even Zohar, N., Sofer, Y., Yaish, I., Serebro, M., Tordjman, K., & Greenman, Y. (2021).
|
||||
Low-Dose Cyproterone Acetate Treatment for Transgender Women.
|
||||
- Even Zohar, N., Sofer, Y., Yaish, I., Serebro, M., Tordjman, K., & Greenman, Y. (2021).\
|
||||
Low-Dose Cyproterone Acetate Treatment for Transgender Women.\
|
||||
The Journal of Sexual Medicine, 18(7), 1292–1298. [[10.1016/j.jsxm.2021.04.008][EZ21]]
|
||||
- 会议摘要:[Even-Zohar et al., 2020][EZ20]
|
||||
- 会议摘要:[Even-Zohar et al., 2020][ez20]
|
||||
|
||||
在该论文的前言部分,有如下叙述:
|
||||
|
||||
> 为协助医师对跨性别女性(transgender women)进行治疗,一些组织已发布了《治疗指南》。CPA 已被广泛用于给药方案当中。总的来说,近年来 CPA 的推荐剂量已在减小:在美国内分泌学会 2009 年版《指南》当中,CPA 推荐剂量为 50-100 mg/天;但到了 2017 年,该剂量修订为 25-50 mg/天。而在澳大利亚跨性别健康专业协会的 2019 年版《指南》所建议的 CPA 剂量,为 12.5-25 mg/天。至于由欧洲性医学会发布的 2020 年版《指南》,则将 CPA 剂量修订为 10-50 mg/天。迄今尚无有关不同 CPA 剂量的效力与安全性之间的对比数据的论文发表。
|
||||
|
||||
该论文的研究者发现,当合用雌二醇时,低剂量 CPA(10-20 mg/天)的睾酮抑制率与高剂量(50-100 mg/天)一致。睾酮水平降低到了(或接近)女性/阉割后范围(一般不大于 2 nmol/L 或 58 pg/mL)。
|
||||
有 38 名女性倾向跨性别者服用低剂量 CPA,其中 32 名(84%)的剂量为 10 mg/天、6 名(16%)的剂量为 20 mg/天,平均剂量 11.6 ± 3.7 mg/天。雌二醇则通过透皮贴片(平均剂量 83.7 ± 36.5 μg/天)、透皮凝胶(平均剂量 3.8 ± 1.2 g/天)或者口服(平均剂量 4.1 ± 1.7 mg/天)的形式给药。后续在低剂量、高剂量 CPA 组别当中,雌二醇浓度平均达到了约 110 到 350 pmol/L(或 ~30–95 pg/mL)。
|
||||
该论文的研究者发现,当合用雌二醇时,低剂量 CPA(10-20 mg/天)的睾酮抑制率与高剂量(50-100 mg/天)一致。睾酮水平降低到了(或接近)女性/阉割后范围(一般不大于 2 nmol/L 或 58 pg/mL)。\
|
||||
有 38 名女性倾向跨性别者服用低剂量 CPA,其中 32 名(84%)的剂量为 10 mg/天、6 名(16%)的剂量为 20 mg/天,平均剂量 11.6 ± 3.7 mg/天。雌二醇则通过透皮贴片(平均剂量 83.7 ± 36.5 μg/天)、透皮凝胶(平均剂量 3.8 ± 1.2 g/天)或者口服(平均剂量 4.1 ± 1.7 mg/天)的形式给药。后续在低剂量、高剂量 CPA 组别当中,雌二醇浓度平均达到了约 110 到 350 pmol/L(或 ~30–95 pg/mL)。\
|
||||
除睾酮抑制效果之外,研究还发现了:在 12 个月激素治疗过后,低剂量 CPA 组别的泌乳素水平(398 ± 69 mIU/mL)显著低于高剂量的水平(804 ± 121 mIU/mL)。
|
||||
|
||||
基于这些发现,论文作者叙述如下:
|
||||
|
||||
> 我们建议,现有的《临床实践指南》应修订其为跨性别女性推荐的 CPA 剂量。
|
||||
|
||||
这两篇论文皆声明,其为首次揭露女性倾向跨性别者服用低剂量 CPA 之疗效。不过,这项成就其实应该属于 [Meyer 等人 (2020)][M20] [[PDF][M20-PDF]];其于 2020 年 2 月便已发现,女性倾向跨性别者合用雌二醇与 10、25、50 mg/天的 CPA 时,可获得一致的睾酮抑制效果。
|
||||
这两篇论文皆声明,其为首次揭露女性倾向跨性别者服用低剂量 CPA 之疗效。不过,这项成就其实应该属于 [Meyer 等人 (2020)][m20] [[PDF][M20-PDF]];其于 2020 年 2 月便已发现,女性倾向跨性别者合用雌二醇与 10、25、50 mg/天的 CPA 时,可获得一致的睾酮抑制效果。
|
||||
|
||||
[Lim 等人 (2020)][L20] 在 2020 年 5/7 月发表了一篇论文;其研究课题并非与 CPA 及睾酮抑制效果有关,不过,其报告了 26 名女性倾向跨性别者分别使用口服与透皮雌二醇时,睾酮水平中位数(范围)分别为 0.6 (0.4–1.0) nmol/L、0.9 (0.7–1.6) nmol/L;她们还分为了合用雌二醇与低剂量 CPA(12.5-18.8 mg/天,中位数 12.5;共 14 人)、摘除性腺后单用雌二醇(共 9 人)、以及合用雌二醇与螺内酯(共 3 人)等组别。
|
||||
[Lim 等人 (2020)][l20] 在 2020 年 5/7 月发表了一篇论文;其研究课题并非与 CPA 及睾酮抑制效果有关,不过,其报告了 26 名女性倾向跨性别者分别使用口服与透皮雌二醇时,睾酮水平中位数(范围)分别为 0.6 (0.4–1.0) nmol/L、0.9 (0.7–1.6) nmol/L;她们还分为了合用雌二醇与低剂量 CPA(12.5-18.8 mg/天,中位数 12.5;共 14 人)、摘除性腺后单用雌二醇(共 9 人)、以及合用雌二醇与螺内酯(共 3 人)等组别。
|
||||
|
||||
### 后记三
|
||||
### 后记三 {#update-3}
|
||||
|
||||
一篇于 2021 年 12 月发表的论文报告了一起由低剂量 CPA 引起的致命肝衰竭病例:
|
||||
|
||||
- Kumar, P., Reddy, S., Kulkarni, A., Sharma, M., & Rao, P. N. (2021).
|
||||
Cyproterone acetate induced Acute liver failure: Case report and review of the literature.
|
||||
Journal of Clinical and Experimental Hepatology, 11(6), 739–741. [[DOI:10.1016/j.jceh.2021.01.003][KP21]]
|
||||
- Kumar, P., Reddy, S., Kulkarni, A., Sharma, M., & Rao, P. N. (2021).\
|
||||
Cyproterone acetate induced Acute liver failure: Case report and review of the literature.\
|
||||
Journal of Clinical and Experimental Hepatology, 11(6), 739–741. \[DOI: <https://doi.org/10.1016/j.jceh.2021.01.003>]
|
||||
|
||||
该病例描述了一名 30 岁顺性别妇女连续六个月服用 25 mg/天的 CPA 以治疗多毛症,但患上了急性肝衰竭;住院四天后不治身亡。这是迄今报告的第二起和低于 100 mg/天剂量的 CPA 之肝毒性有关的病例,也是第一起有关 CPA 对于顺性别妇女之肝毒性的病例。该病例表明,在肝毒性上,即便相对较低的 CPA 剂量:25 mg/天,也并非足够安全。
|
||||
该病例描述了一名 30 岁顺性别妇女连续六个月服用 25 mg/天的 CPA 以治疗多毛症,但患上了急性肝衰竭;住院四天后不治身亡。这是迄今报告的第二起和低于 100 mg/天剂量的 CPA 之肝毒性有关的病例,也是第一起有关 CPA 对于顺性别妇女之肝毒性的病例。该病例表明,在肝毒性上,即便相对较低的 CPA 剂量:25 mg/天,也并非足够安全。\
|
||||
该论文还强调了女性倾向跨性别者应使用最低有效剂量(不大于 10-12.5 mg/天)之重要性。
|
||||
|
||||
<!-- 以下为 2022 年 3 月以来的增补内容 -->
|
||||
|
||||
### 后记四
|
||||
### 后记四 {#update-4}
|
||||
|
||||
2022 年 9 月,[世界跨性别人士健康专业协会][WPATH](WPATH)发布了第八版《[跨性别及性别多元化人群健康护理标准][SOC8]》(SOC),其中首次为跨性别激素治疗提供建议<sup>([Coleman et al., 2022][C22])</sup>。其向女性倾向跨性别者推荐的 CPA 剂量为 10 mg/天<sup>([Coleman et al., 2022][C22])</sup>。此剂量远比早前发布的《跨性别护理指南》所建议的要低;这也是首次有主流《指南》推荐如此低的剂量。
|
||||
该《标准》提及了 [Kuijpers 等人 (2021)][K21] 并支持其推荐的剂量[但并未提及 [Even Zohar 等人 (2021)][EZ21] 与 [Meyer 等人 (2020)][M20]],同时还讨论了脑膜瘤和高泌乳素水平等与 CPA 剂量有关的风险<sup>([Coleman et al., 2022][C22])</sup>。
|
||||
2022 年 9 月,[世界跨性别人士健康专业协会][wpath](WPATH)发布了第八版《[跨性别及性别多元化人群健康护理标准][soc8]》(SOC),其中首次为跨性别激素治疗提供建议<sup>([Coleman et al., 2022][c22])</sup>。其向女性倾向跨性别者推荐的 CPA 剂量为 10 mg/天<sup>([Coleman et al., 2022][c22])</sup>。此剂量远比早前发布的《跨性别护理指南》所建议的要低;这也是首次有主流《指南》推荐如此低的剂量。\
|
||||
该《标准》提及了 [Kuijpers 等人 (2021)][k21] 并支持其推荐的剂量[但并未提及 [Even Zohar 等人 (2021)][ez21] 与 [Meyer 等人 (2020)][m20]],同时还讨论了脑膜瘤和高泌乳素水平等与 CPA 剂量有关的风险<sup>([Coleman et al., 2022][c22])</sup>。\
|
||||
考虑到 WPATH 的这篇《标准》在跨性别健康领域的重要地位和影响力,可以认为,全球范围内在女性化激素治疗当中使用低剂量 CPA 的情况将会更普遍。有当下公认的循证实践在先,不应再继续使用高剂量 CPA。
|
||||
|
||||
### 后记五
|
||||
### 后记五 {#update-5}
|
||||
|
||||
2022 年 10 月,一项对雌二醇与 CPA 的睾酮抑制效果进行细致评估的研究,公开发表了论文:
|
||||
|
||||
- Collet, S., Gieles, N., Wiepjes, C. M., Heijboer, A. C., Reyns, T., Fiers, T., Lapauw, B., den Heijer, M., & T’Sjoen, G. (2022).
|
||||
Changes in serum testosterone and adrenal androgen levels in transgender women with and without gonadectomy.
|
||||
The Journal of Clinical Endocrinology & Metabolism, advance online publication. [[DOI:10.1210/clinem/dgac576][CS20]]
|
||||
- Collet, S., Gieles, N., Wiepjes, C. M., Heijboer, A. C., Reyns, T., Fiers, T., Lapauw, B., den Heijer, M., & T’Sjoen, G. (2022).\
|
||||
Changes in serum testosterone and adrenal androgen levels in transgender women with and without gonadectomy.\
|
||||
The Journal of Clinical Endocrinology & Metabolism, advance online publication. \[DOI: <https://doi.org/10.1210/clinem/dgac576>]
|
||||
|
||||
该项目属于欧洲性别不一致调查组织网络(ENIGI)倡议之下的一部分,其中大多数患者来自荷兰阿姆斯特丹的诊所、以及比利时根特的诊所。
|
||||
|
||||
该项目中有 275 名女性倾向跨性别者接受雌二醇合并 CPA 治疗。她们的总睾酮、游离睾酮水平,以及由肾上腺分泌的雄激素——脱氢表雄酮(DHEA)、硫酸脱氢表雄酮(DHEA-S)与雄烯二酮(A4)等——之水平,以液相色谱-质谱联用法(LC-MS)进行测定;测定时间定于跟踪开始时、第 3 个月、第 12 个月、第 2-4 年以及经手术切除性腺之后(此时不再服用 CPA)。至于其雌二醇水平,则以 LC-MS(阿姆斯特丹方面)或免疫测定法(根特方面)进行测定。
|
||||
其所用雌二醇形式与剂量,通常为 4 mg/天的口服戊酸雌二醇或 100 μg/天的雌二醇透皮贴片;而 CPA 的剂量多为 25-50 mg/天。
|
||||
该项目中有 275 名女性倾向跨性别者接受雌二醇合并 CPA 治疗。她们的总睾酮、游离睾酮水平,以及由肾上腺分泌的雄激素——脱氢表雄酮(DHEA)、硫酸脱氢表雄酮(DHEA-S)与雄烯二酮(A4)等——之水平,以液相色谱-质谱联用法(LC-MS)进行测定;测定时间定于跟踪开始时、第 3 个月、第 12 个月、第 2-4 年以及经手术切除性腺之后(此时不再服用 CPA)。至于其雌二醇水平,则以 LC-MS(阿姆斯特丹方面)或免疫测定法(根特方面)进行测定。\
|
||||
其所用雌二醇形式与剂量,通常为 4 mg/天的口服戊酸雌二醇或 100 μg/天的雌二醇透皮贴片;而 CPA 的剂量多为 25-50 mg/天。\
|
||||
这些人当中有大约一半,在以激素治疗约两年之后都接受了性腺切除术。
|
||||
|
||||
结果显示:
|
||||
结果显示:
|
||||
|
||||
- 在不同跟踪时长下,以 LC-MS 和免疫测定法测定的雌二醇水平中位数,分别为 49-75 pg/mL(合 180–275 pmol/L)和 63-69 pg/mL(232–255 pmol/L)。
|
||||
- 在接受激素治疗达三个月之后,总睾酮水平从 536 ng/dL (18.6 nmol/L) 降至 12 ng/dL (0.40 nmol/L),降幅 97.1%;而游离睾酮水平从 109 pg/mL (378 pmol/L) 降至 2.0 pg/mL (7.1 pmol/L),降幅 98.3%;此后,总睾酮、游离睾酮水平维持稳定。
|
||||
- 至于 DHEA、DHEA-S 及 A4 等激素的水平,降幅则分别达 24.9-28.0%、20.1-23.5% 及 36.5%,到了激素治疗第 3-12 月之后也基本不变。
|
||||
|
|
@ -258,105 +271,104 @@ CPA 的雄激素受体(AR)拮抗效应相对较弱。为达到有意义、
|
|||
|
||||
论文作者指出,在本研究中,接受激素治疗的女性倾向跨性别者的睾酮水平,与顺性别妇女接近或稍低于之。
|
||||
|
||||
--------
|
||||
|
||||
[WIKI-1]: https://en.wikipedia.org/wiki/Pharmacology_of_cyproterone_acetate#Pharmacodynamics
|
||||
[TABLE-1]: https://en.wikipedia.org/wiki/Template:Oral_potencies_of_progestogens
|
||||
[E11]: https://doi.org/10.1016/j.contraception.2011.04.009
|
||||
[WIKI-2]: https://en.wikipedia.org/wiki/Cyproterone_acetate#Medical_uses
|
||||
[WIKI-3]: https://en.wikipedia.org/wiki/Cyproterone_acetate#Available_forms
|
||||
[H75]: https://doi.org/10.1016/0022-4731(75)90311-8
|
||||
[H90]: https://doi.org/10.1007/978-3-642-74612-3_35
|
||||
[H79]: https://books.google.com/books?id=waMTAQAAMAAJ
|
||||
[WIKI-4]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate
|
||||
[WIKI-5]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#High_prolactin_levels
|
||||
[AW20-MEN]: cpa-meningioma.md
|
||||
[WIKI-6]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Brain_tumors
|
||||
[TABLE-2]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_meningioma
|
||||
[TABLE-3]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_prolactinoma
|
||||
[WIKI-7]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Blood_clots
|
||||
[WIKI-8]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Cardiovascular_effects
|
||||
[WIKI-9]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Liver_toxicity
|
||||
[TABLE-4]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_liver_toxicity
|
||||
[H17]: https://doi.org/10.1210/jc.2017-01658
|
||||
[H09]: https://doi.org/10.1210/jc.2009-0345
|
||||
## 译文修订记录
|
||||
|
||||
[GRAPH-1]: https://commons.wikimedia.org/wiki/File:Testosterone_levels_with_5_or_10_mg_per_day_oral_cyproterone_acetate_in_men.png
|
||||
[GRAPH-2]: https://commons.wikimedia.org/wiki/File:Androgen_levels_with_10_or_20_mg_per_day_oral_cyproterone_acetate_in_men.png
|
||||
[M02a]: https://doi.org/10.1210/jcem.87.5.8514
|
||||
[WIKI-10]: https://en.wikipedia.org/wiki/Desogestrel#Antigonadotropic_effects
|
||||
[WIKI-11]: https://en.wikipedia.org/wiki/Dienogest#Antigonadotropic_effects
|
||||
[WIKI-12]: https://en.wikipedia.org/wiki/Medroxyprogesterone_acetate#Antigonadotropic_and_anticorticotropic_effects
|
||||
[T03]: https://doi.org/10.1210/jc.2003-030520
|
||||
[G04]: https://doi.org/10.1093/ajcn/80.5.1167
|
||||
[T05]: https://doi.org/10.1677/joe.1.06112
|
||||
[T17]: https://doi.org/10.1016/j.jsxm.2017.03.251
|
||||
[GBN74]: https://doi.org/10.1007/978-3-642-80859-3_7
|
||||
[J80]: https://doi.org/10.1111/j.1464-410X.1980.tb02961.x
|
||||
[J80-GRAPH]: https://commons.wikimedia.org/wiki/File:Testosterone_and_luteinizing_hormone_levels_with_100_mg_per_day_oral_cyproterone_acetate_in_men.png
|
||||
[KHN84]: https://doi.org/10.1210/jcem-59-5-963
|
||||
[KHN84-GRAPH]: https://commons.wikimedia.org/wiki/File:Testosterone_levels_with_300_mg_per_week_cyproterone_acetate_and_100_mg_per_month_estradiol_undecylate_by_intramuscular_injection.png
|
||||
[SR02]: https://doi.org/10.1007/978-1-59259-152-7_15
|
||||
[N11]: https://books.google.com/books?id=fu3BBwAAQBAJ&pg=PA2938
|
||||
[LTV17]: https://doi.org/10.1007/978-3-319-53298-1_16
|
||||
[WWF10]: https://doi.org/10.2164/jandrol.109.009035
|
||||
[WIKI-13]: https://en.wikipedia.org/wiki/Megestrol_acetate#Antigonadotropic_and_anticorticotropic_effects
|
||||
[GB91]: https://pubmed.ncbi.nlm.nih.gov/1825143/
|
||||
[S87]: https://www.worldcat.org/title/konservative-therapie-mit-cyproteronacetat-und-estradiolundecylat-beim-fortgeschrittenen-prostatacarcinom-e-5-jahres-studie/oclc/917571781
|
||||
[JTS82]: https://scholar.google.com/scholar?cluster=8992751753331497790
|
||||
- 2022 年 3 月 2 日——首次翻译。
|
||||
- 2022 年 10 月 21 日——第一次修订,增补“后记四”“后记五”内容,整理外链。
|
||||
|
||||
[WIKI-14]: https://en.wikipedia.org/wiki/Pharmacodynamics_of_estradiol#Effects_on_sex-hormone_levels
|
||||
[GRAPH-3]: https://en.wikipedia.org/wiki/Template:Antigonadotropic_effects_of_estradiol
|
||||
[G81a]: https://doi.org/10.1210/jcem-52-3-576
|
||||
[G81b]: https://www.ncbi.nlm.nih.gov/pubmed/6782738
|
||||
[G88]: https://doi.org/10.1016/S0022-5347(17)42073-8
|
||||
[J88]: https://doi.org/10.1016/0090-4295(88)90726-1
|
||||
[GEL88]: https://doi.org/10.1016/0090-4295(88)90402-5
|
||||
[V88]: https://www.ncbi.nlm.nih.gov/pubmed/3285485
|
||||
[G91]: https://www.ncbi.nlm.nih.gov/pubmed/1825145
|
||||
[B93]: https://doi.org/10.1002/1097-0142(19930901)72:5%3C1685::AID-CNCR2820720532%3E3.0.CO;2-3
|
||||
[G96]: https://doi.org/10.1016/S0090-4295(96)00048-9
|
||||
[G16]: https://doi.org/10.1111/cen.13050
|
||||
[GRAPH-4]: https://commons.wikimedia.org/wiki/File:Hormone_levels_with_low-dose_estradiol_gel_and_oral_cyproterone_acetate_in_transgender_women.png
|
||||
[A19]: https://doi.org/10.1530/EC-19-0272
|
||||
[GRAPH-5]: https://commons.wikimedia.org/wiki/File:Testosterone_levels_with_estradiol_alone,_estradiol_plus_spironolactone,_and_estradiol_plus_cyproterone_acetate_in_transfeminine_people.png
|
||||
[FHL17]: https://doi.org/10.1080/15532739.2017.1290566
|
||||
[AW20-E2-EQU]: https://transfemscience.org/articles/e2-equivalent-doses/
|
||||
[WIKI-15]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol
|
||||
[M98]: https://doi.org/10.1093/humrep/13.5.1225
|
||||
[M02b]: https://onlinelibrary.wiley.com/doi/abs/10.1002/j.1939-4640.2002.tb02311.x
|
||||
[WIKI-16]: https://en.wikipedia.org/wiki/Pharmacology_of_bicalutamide#Influences_on_hormone_levels
|
||||
[M20]: https://doi.org/10.1530/EJE-19-0463
|
||||
[M20-PDF]: https://files.transfemscience.org/pdfs/Meyer%20et%20al.%20(2020)%20-%20Safety%20and%20Rapid%20Efficacy%20of%20Guideline-Based%20Gender-Affirming%20Hormone%20Therapy_%20An%20Analysis%20of%20388%20Individuals%20Diagnosed%20with%20Gender%20Dysphoria.pdf
|
||||
[EZ20]: https://doi.org/10.1210/jendso/bvaa046.1412
|
||||
[JKF19]: https://doi.org/10.1210/jc.2018-02253
|
||||
|
||||
[L09]: http://doi.org/10.1055/s-0028-1090190
|
||||
[HW19]: https://books.google.com/books?id=-sCZDwAAQBAJ&pg=PA122
|
||||
[WC17]: https://doi.org/10.1007/s10304-016-0116-9
|
||||
[M18]: https://doi.org/10.1016/S2213-8587(18)30305-X
|
||||
[O18]: https://hdl.handle.net/10289/12160
|
||||
[AKS19]: http://doi.org/10.1055/a-0801-3319
|
||||
[B19]: https://www.rainbowhealthontario.ca/resources/4th-edition-sherbournes-guidelines-for-gender-affirming-primary-care-with-trans-and-non-binary-patients/
|
||||
[F19]: https://doi.org/10.1016/j.psyneuen.2019.02.023
|
||||
[J19]: https://doi.org/10.1007/s41969-019-00080-x
|
||||
[NHG19]: https://www.ncbi.nlm.nih.gov/books/NBK544426/
|
||||
[A20]: https://www.anzctr.org.au/Trial/Registration/TrialReview.aspx?id=379339
|
||||
[TS20]: https://doi.org/10.1016/j.jsxm.2020.01.012
|
||||
[AG93]: https://doi.org/10.1300/J056v05n04_03
|
||||
[GGB08]: https://doi.org/10.1210/jc.2007-1809
|
||||
|
||||
[WIKI-17]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Low_hormone_levels
|
||||
[AW19-NB]: nonbinary-transfem-overview.md
|
||||
[WIKI-18]: https://en.wikipedia.org/wiki/Pharmacology_of_cyproterone_acetate#Metabolism
|
||||
[GRAPH-6]: https://commons.wikimedia.org/wiki/File:Cyproterone_acetate_levels_with_100_mg_oral_cyproterone_acetate_per_day_in_women.png
|
||||
|
||||
[GLC]: https://researchers.uq.edu.au/research-project/38285
|
||||
[K21]: https://doi.org/10.1210/clinem/dgab427
|
||||
[G21]: https://doi.org/10.1530/EJE-21-0059
|
||||
[EZ21]: https://doi.org/10.1016/j.jsxm.2021.04.008
|
||||
[L20]: https://doi.org/10.1210/clinem/dgaa262
|
||||
[KP21]: https://doi.org/10.1016/j.jceh.2021.01.003
|
||||
[WPATH]: https://zh.wikipedia.org/wiki/%E4%B8%96%E7%95%8C%E8%B7%A8%E6%80%A7%E5%88%AB%E4%BA%BA%E5%A3%AB%E5%81%A5%E5%BA%B7%E4%B8%93%E4%B8%9A%E5%8D%8F%E4%BC%9A
|
||||
[SOC8]: https://en.wikipedia.org/wiki/Standards_of_Care_for_the_Health_of_Transgender_and_Gender_Diverse_People
|
||||
[C22]: https://doi.org/10.1080/26895269.2022.2100644
|
||||
[CS20]: https://doi.org/10.1210/clinem/dgac576
|
||||
[wiki-1]: https://en.wikipedia.org/wiki/Pharmacology_of_cyproterone_acetate#Pharmacodynamics
|
||||
[table-1]: https://en.wikipedia.org/wiki/Template:Oral_potencies_of_progestogens
|
||||
[e11]: https://doi.org/10.1016/j.contraception.2011.04.009
|
||||
[wiki-2]: https://en.wikipedia.org/wiki/Cyproterone_acetate#Medical_uses
|
||||
[wiki-3]: https://en.wikipedia.org/wiki/Cyproterone_acetate#Available_forms
|
||||
[h75]: https://doi.org/10.1016/0022-4731(75)90311-8
|
||||
[h90]: https://doi.org/10.1007/978-3-642-74612-3_35
|
||||
[h79]: https://books.google.com/books?id=waMTAQAAMAAJ
|
||||
[wiki-4]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate
|
||||
[wiki-5]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#High_prolactin_levels
|
||||
[aw20-men]: https://transfemscience.org/articles/cpa-meningioma/
|
||||
[wiki-6]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Brain_tumors
|
||||
[table-2]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_meningioma
|
||||
[table-3]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_prolactinoma
|
||||
[wiki-7]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Blood_clots
|
||||
[wiki-8]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Cardiovascular_effects
|
||||
[wiki-9]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Liver_toxicity
|
||||
[table-4]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_liver_toxicity
|
||||
[h17]: https://doi.org/10.1210/jc.2017-01658
|
||||
[h09]: https://doi.org/10.1210/jc.2009-0345
|
||||
[graph-1]: https://commons.wikimedia.org/wiki/File:Testosterone_levels_with_5_or_10_mg_per_day_oral_cyproterone_acetate_in_men.png
|
||||
[graph-2]: https://commons.wikimedia.org/wiki/File:Androgen_levels_with_10_or_20_mg_per_day_oral_cyproterone_acetate_in_men.png
|
||||
[m02a]: https://doi.org/10.1210/jcem.87.5.8514
|
||||
[wiki-10]: https://en.wikipedia.org/wiki/Desogestrel#Antigonadotropic_effects
|
||||
[wiki-11]: https://en.wikipedia.org/wiki/Dienogest#Antigonadotropic_effects
|
||||
[wiki-12]: https://en.wikipedia.org/wiki/Medroxyprogesterone_acetate#Antigonadotropic_and_anticorticotropic_effects
|
||||
[t03]: https://doi.org/10.1210/jc.2003-030520
|
||||
[g04]: https://doi.org/10.1093/ajcn/80.5.1167
|
||||
[t05]: https://doi.org/10.1677/joe.1.06112
|
||||
[t17]: https://doi.org/10.1016/j.jsxm.2017.03.251
|
||||
[gbn74]: https://doi.org/10.1007/978-3-642-80859-3_7
|
||||
[j80]: https://doi.org/10.1111/j.1464-410X.1980.tb02961.x
|
||||
[j80-graph]: https://commons.wikimedia.org/wiki/File:Testosterone_and_luteinizing_hormone_levels_with_100_mg_per_day_oral_cyproterone_acetate_in_men.png
|
||||
[khn84]: https://doi.org/10.1210/jcem-59-5-963
|
||||
[khn84-graph]: https://commons.wikimedia.org/wiki/File:Testosterone_levels_with_300_mg_per_week_cyproterone_acetate_and_100_mg_per_month_estradiol_undecylate_by_intramuscular_injection.png
|
||||
[sr02]: https://doi.org/10.1007/978-1-59259-152-7_15
|
||||
[n11]: https://books.google.com/books?id=fu3BBwAAQBAJ&pg=PA2938
|
||||
[ltv17]: https://doi.org/10.1007/978-3-319-53298-1_16
|
||||
[wwf10]: https://doi.org/10.2164/jandrol.109.009035
|
||||
[wiki-13]: https://en.wikipedia.org/wiki/Megestrol_acetate#Antigonadotropic_and_anticorticotropic_effects
|
||||
[gb91]: https://pubmed.ncbi.nlm.nih.gov/1825143/
|
||||
[s87]: https://www.worldcat.org/title/konservative-therapie-mit-cyproteronacetat-und-estradiolundecylat-beim-fortgeschrittenen-prostatacarcinom-e-5-jahres-studie/oclc/917571781
|
||||
[jts82]: https://scholar.google.com/scholar?cluster=8992751753331497790
|
||||
[wiki-14]: https://en.wikipedia.org/wiki/Pharmacodynamics_of_estradiol#Effects_on_sex-hormone_levels
|
||||
[graph-3]: https://en.wikipedia.org/wiki/Template:Antigonadotropic_effects_of_estradiol
|
||||
[g81a]: https://doi.org/10.1210/jcem-52-3-576
|
||||
[g81b]: https://www.ncbi.nlm.nih.gov/pubmed/6782738
|
||||
[g88]: https://doi.org/10.1016/S0022-5347(17)42073-8
|
||||
[j88]: https://doi.org/10.1016/0090-4295(88)90726-1
|
||||
[gel88]: https://doi.org/10.1016/0090-4295(88)90402-5
|
||||
[v88]: https://www.ncbi.nlm.nih.gov/pubmed/3285485
|
||||
[g91]: https://www.ncbi.nlm.nih.gov/pubmed/1825145
|
||||
[b93]: https://doi.org/10.1002/1097-0142(19930901)72:5%3C1685::AID-CNCR2820720532%3E3.0.CO;2-3
|
||||
[g96]: https://doi.org/10.1016/S0090-4295(96)00048-9
|
||||
[g16]: https://doi.org/10.1111/cen.13050
|
||||
[graph-4]: https://commons.wikimedia.org/wiki/File:Hormone_levels_with_low-dose_estradiol_gel_and_oral_cyproterone_acetate_in_transgender_women.png
|
||||
[a19]: https://doi.org/10.1530/EC-19-0272
|
||||
[graph-5]: https://commons.wikimedia.org/wiki/File:Testosterone_levels_with_estradiol_alone,_estradiol_plus_spironolactone,_and_estradiol_plus_cyproterone_acetate_in_transfeminine_people.png
|
||||
[fhl17]: https://doi.org/10.1080/15532739.2017.1290566
|
||||
[aw20-e2-equ]: https://transfemscience.org/articles/e2-equivalent-doses/
|
||||
[wiki-15]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol
|
||||
[m98]: https://doi.org/10.1093/humrep/13.5.1225
|
||||
[m02b]: https://onlinelibrary.wiley.com/doi/abs/10.1002/j.1939-4640.2002.tb02311.x
|
||||
[wiki-16]: https://en.wikipedia.org/wiki/Pharmacology_of_bicalutamide#Influences_on_hormone_levels
|
||||
[m20]: https://doi.org/10.1530/EJE-19-0463
|
||||
[m20-pdf]: https://files.transfemscience.org/pdfs/Meyer%20et%20al.%20(2020)%20-%20Safety%20and%20Rapid%20Efficacy%20of%20Guideline-Based%20Gender-Affirming%20Hormone%20Therapy_%20An%20Analysis%20of%20388%20Individuals%20Diagnosed%20with%20Gender%20Dysphoria.pdf
|
||||
[ez20]: https://doi.org/10.1210/jendso/bvaa046.1412
|
||||
[jkf19]: https://doi.org/10.1210/jc.2018-02253
|
||||
[l09]: http://doi.org/10.1055/s-0028-1090190
|
||||
[hw19]: https://books.google.com/books?id=-sCZDwAAQBAJ&pg=PA122
|
||||
[wc17]: https://doi.org/10.1007/s10304-016-0116-9
|
||||
[m18]: https://doi.org/10.1016/S2213-8587(18)30305-X
|
||||
[o18]: https://hdl.handle.net/10289/12160
|
||||
[aks19]: http://doi.org/10.1055/a-0801-3319
|
||||
[b19]: https://www.rainbowhealthontario.ca/resources/4th-edition-sherbournes-guidelines-for-gender-affirming-primary-care-with-trans-and-non-binary-patients/
|
||||
[f19]: https://doi.org/10.1016/j.psyneuen.2019.02.023
|
||||
[j19]: https://doi.org/10.1007/s41969-019-00080-x
|
||||
[nhg19]: https://www.ncbi.nlm.nih.gov/books/NBK544426/
|
||||
[a20]: https://www.anzctr.org.au/Trial/Registration/TrialReview.aspx?id=379339
|
||||
[ts20]: https://doi.org/10.1016/j.jsxm.2020.01.012
|
||||
[ag93]: https://doi.org/10.1300/J056v05n04_03
|
||||
[ggb08]: https://doi.org/10.1210/jc.2007-1809
|
||||
[wiki-17]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Low_hormone_levels
|
||||
[aw19-nb]: https://transfemscience.org/articles/nonbinary-transfem-overview/
|
||||
[wiki-18]: https://en.wikipedia.org/wiki/Pharmacology_of_cyproterone_acetate#Metabolism
|
||||
[graph-6]: https://commons.wikimedia.org/wiki/File:Cyproterone_acetate_levels_with_100_mg_oral_cyproterone_acetate_per_day_in_women.png
|
||||
[glc]: https://researchers.uq.edu.au/research-project/38285
|
||||
[k21]: https://doi.org/10.1210/clinem/dgab427
|
||||
[g21]: https://doi.org/10.1530/EJE-21-0059
|
||||
[ez21]: https://doi.org/10.1016/j.jsxm.2021.04.008
|
||||
[l20]: https://doi.org/10.1210/clinem/dgaa262
|
||||
[wpath]: https://zh.wikipedia.org/wiki/%E4%B8%96%E7%95%8C%E8%B7%A8%E6%80%A7%E5%88%AB%E4%BA%BA%E5%A3%AB%E5%81%A5%E5%BA%B7%E4%B8%93%E4%B8%9A%E5%8D%8F%E4%BC%9A
|
||||
[soc8]: https://en.wikipedia.org/wiki/Standards_of_Care_for_the_Health_of_Transgender_and_Gender_Diverse_People
|
||||
[c22]: https://doi.org/10.1080/26895269.2022.2100644
|
||||
|
|
@ -1,53 +1,47 @@
|
|||
# 法国关于醋酸环丙孕酮和脑膜瘤风险的研究的最新进展以及对女性倾向跨性别者的影响
|
||||
---
|
||||
title: 法国关于醋酸环丙孕酮和脑膜瘤风险的研究的最新进展以及对女性倾向跨性别者的影响
|
||||
linkTitle: 醋酸环丙孕酮和脑膜瘤风险
|
||||
description: >-
|
||||
在醋酸环丙孕酮的累积剂量较大的情况下,脑膜瘤风险会显著提高。减量或减少用药年限均可降低该风险。
|
||||
author: Aly W.
|
||||
published: 2020-04-24
|
||||
updated: 2022-10-19
|
||||
translated: 2022-10-20
|
||||
translators:
|
||||
- 昭心
|
||||
- Bersella AI
|
||||
trackHash: 7378b09b623aaedc898e8e60a30a5035fb5d10d2
|
||||
tags:
|
||||
- 用药安全
|
||||
- 醋酸环丙孕酮
|
||||
- 抗雄激素制剂
|
||||
- 孕激素
|
||||
---
|
||||
|
||||
> - 作者 [Aly W.][AUTHOR]
|
||||
> + 首次发表于 2020 年 4 月 24 日
|
||||
> + 最后修改于 2022 年 10 月 19 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [昭心][TRANSLATOR]
|
||||
> + 翻译于 2021 年 10 月 29 日
|
||||
> - 译文修订 [Bersella AI][REVISOR]
|
||||
> + 修订于 2022 年 10 月 20 日
|
||||
## 译者按 {#notice}
|
||||
|
||||
[AUTHOR]: https://transfemscience.org/about/#aly-w
|
||||
[ORIGIN]: https://transfemscience.org/articles/injectable-e2-meta-analysis/
|
||||
[TRANSLATOR]: https://limelight.moe/u/昭心
|
||||
[REVISOR]: https://bersella-ai.cc/about-me/
|
||||
|
||||
## 译者按
|
||||
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. **<u>⚠ 免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
--------
|
||||
---
|
||||
|
||||
## 摘要
|
||||
## 摘要 {#by-abstract}
|
||||
|
||||
> 醋酸环丙孕酮 (CPA) 是一种孕激素和抗雄激素制剂,常用于女性化激素治疗中。在通常为女性倾向跨性别者所用的剂量下,它具有极强的孕激素效力;其通常剂量可达 25 至 100mg/天——尽管仅需约 2 至 3 mg/天 的剂量就可提供与妇女整个黄体期相当的孕激素暴露量。
|
||||
> 2018 年,法国政府发表了一项大型流行病学研究的结果,其显示通常的高剂量 CPA 会带来与剂量相关的较高的脑膜瘤 (一种对激素敏感的脑肿瘤) 风险;如每个月有 20 天循环服用 50 mg 的 CPA 并持续超过 5 年、或服用 25 mg/天并持续 10 年以上,会使需手术处理的脑膜瘤风险提高 20 倍。后续的研究亦复现了这些结果。这些发现已使得 CPA 的临床应用受到限制,剂量也大大减少。
|
||||
> 醋酸环丙孕酮 (CPA) 是一种孕激素和抗雄激素制剂,常用于女性化激素治疗中。在通常为女性倾向跨性别者所用的剂量下,它具有极强的孕激素效力;其通常剂量可达 25 至 100mg/天——尽管仅需约 2 至 3 mg/天 的剂量就可提供与妇女整个黄体期相当的孕激素暴露量。
|
||||
> 2018 年,法国政府发表了一项大型流行病学研究的结果,其显示通常的高剂量 CPA 会带来与剂量相关的较高的脑膜瘤 (一种对激素敏感的脑肿瘤) 风险;如每个月有 20 天循环服用 50 mg 的 CPA 并持续超过 5 年、或服用 25 mg/天并持续 10 年以上,会使需手术处理的脑膜瘤风险提高 20 倍。后续的研究亦复现了这些结果。这些发现已使得 CPA 的临床应用受到限制,剂量也大大减少。
|
||||
> 不过所幸,对女性倾向跨性别者来说,CPA 大幅降低过后的剂量 (如 5-10 mg/天) 仍可高效抑制睾酮。尽管如此,考虑到脑膜瘤和其他各种并发症的风险,仍建议女性倾向跨性别者谨慎而有限度地使用 CPA;例如,仅对非脑膜瘤高风险人群在较短时间内 (如 2 年) 以低剂量使用。
|
||||
|
||||
## 引言
|
||||
## 引言 {#introduction}
|
||||
|
||||
[醋酸环丙孕酮][cpa] (CPA) 是一种女性化激素治疗中常用的孕激素和抗雄激素。在为女性化激素治疗所用的通常剂量下,CPA 有极强的孕激素效力。因其带来的较强孕激素暴露量,CPA 已被证实可引起 [脑膜瘤][meningioma] (一种罕见的 [良性][benign-tumor] (非癌性) [脑肿瘤][brain-tumor]) 之风险。[脑膜][meninges]包裹着大脑和脊髓,脑膜瘤生成于此。
|
||||
[醋酸环丙孕酮][cpa] (CPA) 是一种女性化激素治疗中常用的孕激素和抗雄激素。在为女性化激素治疗所用的通常剂量下,CPA 有极强的孕激素效力。因其带来的较强孕激素暴露量,CPA 已被证实可引起 [脑膜瘤][meningioma] (一种罕见的 [良性][benign-tumor] (非癌性) [脑肿瘤][brain-tumor]) 之风险。[脑膜][meninges]包裹着大脑和脊髓,脑膜瘤生成于此。
|
||||
尽管脑膜瘤通常并非 [恶性][malignancy] (癌性) 肿瘤,但其仍会引起各种并发症,如视力障碍、头痛和癫痫发作,可能需要对脑部进行手术;甚至已有死亡病例报告。
|
||||
维基百科上有关于 CPA 和脑膜瘤主题的 [更多信息][brain-tumor-side-effect],还有已知 CPA 诱发的脑膜瘤的 [病例报告表][cpa-case-reports]。
|
||||
|
||||
法国近期的一项研究表明 CPA 诱发脑膜瘤的风险比既往认知要高得多 ([ASNM/CNAM][asnm-or-cnam])。本文讨论了这些发现和及其对女性倾向跨性别者使用 CPA 的影响,包括更安全地使用 CPA 的建议。
|
||||
法国近期的一项研究表明 CPA 诱发脑膜瘤的风险比既往认知要高得多 ([ASNM/CNAM][docs-asnm])。本文讨论了这些发现和及其对女性倾向跨性别者使用 CPA 的影响,包括更安全地使用 CPA 的建议。
|
||||
|
||||
[cpa]: https://en.wikipedia.org/wiki/Cyproterone_acetate
|
||||
[meningioma]: https://en.wikipedia.org/wiki/Meningioma
|
||||
[benign-tumor]: https://en.wikipedia.org/wiki/Benign_tumor
|
||||
[brain-tumor]: https://en.wikipedia.org/wiki/Brain_tumor
|
||||
[brain-tumor-side-effect]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Brain_tumors
|
||||
[meninges]: https://en.wikipedia.org/wiki/Meninges
|
||||
[malignancy]: https://en.wikipedia.org/wiki/Malignancy
|
||||
[cpa-case-reports]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_meningioma
|
||||
[asnm-or-cnam]: https://docs.google.com/document/d/1WcHLf7rj4Z0Cg6sqs4sz3JD_GwHFQj3-q0EObc8TJFs/view
|
||||
## 法国近期发现 {#recent-french-findings}
|
||||
|
||||
## 法国近期发现
|
||||
|
||||
CPA 诱发脑膜瘤的病例报告始见于 2007 年,这些报告导致法国政府于 2011 年在 CPA 生产信息中添加了警告,并对 CPA 诱发脑膜瘤的风险进行了大规模的流行病学调查。2018 年,他们公布了其发现并报告如下 ([ASNM/CNAM][asnm-or-cnam]) :
|
||||
CPA 诱发脑膜瘤的病例报告始见于 2007 年,这些报告导致法国政府于 2011 年在 CPA 生产信息中添加了警告,并对 CPA 诱发脑膜瘤的风险进行了大规模的流行病学调查。2018 年,他们公布了其发现并报告如下 ([ASNM/CNAM][docs-asnm]) :
|
||||
|
||||
- 该研究规模非常大,对 290,000 年人次的 CPA 治疗进行随访。
|
||||
- 连续 6 个月使用超过 25 mg/天的 CPA 时,可将诱发脑膜瘤的风险增加 7 倍。\
|
||||
|
|
@ -73,80 +67,39 @@ CPA 诱发脑膜瘤的病例报告始见于 2007 年,这些报告导致法国
|
|||
- 从 2018 年 9 月到 2019 年 9 月,法国 CPA 的销售额下降了 73%。\
|
||||
同期螺内酯的销售额增长小于这个幅度。
|
||||
- 法国也在研究其他高剂量孕激素制剂诱发脑膜瘤的风险,包括 [醋酸诺美孕酮][lutenyl] (Lutenyl) 和 [醋酸氯地孕酮][luteran] (Luteran)。
|
||||
- 法国要求[欧洲药品管理局][ema] (EMA) 对 CPA 和脑膜瘤的关系进行审查。该审查于 2019 年年中开始 <sup>([Chustecka, 2019][medscape-915545])</sup>。\
|
||||
2020 年 2 月,EMA 宣布在欧盟内限制 CPA 的临床使用 <sup>([EMA, 2020][ema-restriction])</sup>。这些限制包括仅在其他治疗手段失效后才能使用 CPA,且以最低有效维持剂量使用 CPA <sup>(EMA, 2020; [Chustecka,][medscape-925271])</sup>。这些限制对 CPA 剂量不小于 10 mg/天 的处方有效 <sup>(EMA, 2020; Chustecka, 2020)</sup>。\
|
||||
英国[药品和保健品监管局][hmra] (MHRA) 于 2020 年 6 月发布了醋酸环丙孕酮的药物安全更新 <sup>([MHRA, 2020][hmra-restriction])</sup>。
|
||||
- 法国要求[欧洲药品管理局][ema] (EMA) 对 CPA 和脑膜瘤的关系进行审查。该审查于 2019 年年中开始 <sup>([Chustecka, 2019][c19])</sup>。\
|
||||
2020 年 2 月,EMA 宣布在欧盟内限制 CPA 的临床使用 <sup>([EMA, 2020][ema20])</sup>。这些限制包括仅在其他治疗手段失效后才能使用 CPA,且以最低有效维持剂量使用 CPA <sup>(EMA, 2020; [Chustecka, 2020][c20])</sup>。这些限制对 CPA 剂量不小于 10 mg/天 的处方有效 <sup>(EMA, 2020; Chustecka, 2020)</sup>。\
|
||||
英国[药品和保健品监管局][hmra] (MHRA) 于 2020 年 6 月发布了醋酸环丙孕酮的药物安全更新 <sup>([MHRA, 2020][mhra20])</sup>。
|
||||
|
||||
[lutenyl]: https://en.wikipedia.org/wiki/Nomegestrol_acetate
|
||||
[luteran]: https://en.wikipedia.org/wiki/Chlormadinone_acetate
|
||||
[ema]: https://en.wikipedia.org/wiki/European_Medicines_Agency
|
||||
[hmra]: https://en.wikipedia.org/wiki/Medicines_and_Healthcare_products_Regulatory_Agency
|
||||
[medscape-915545]: https://www.medscape.com/viewarticle/915545
|
||||
[medscape-925271]: https://www.medscape.com/viewarticle/925271
|
||||
[ema-restriction]: https://www.ema.europa.eu/en/news/restrictions-use-cyproterone-due-meningioma-risk
|
||||
[hmra-restriction]: https://www.gov.uk/drug-safety-update/cyproterone-acetate-new-advice-to-minimise-risk-of-meningioma
|
||||
|
||||
[这篇][french-news] 2018 年的法语新闻文章 (通过 [Google 翻译](https://www-doctissimo-fr.translate.goog/sante/news/androcur-meningiome?_x_tr_sl=fr&_x_tr_tl=en&_x_tr_hl=en) 从法语翻译成英语) 简洁地讨论了一部分进展。一些最近的文献出版物也讨论了这个话题 <sup>([Schmutz, 2018][doi-1016-1]; [Gerson, 2018][jle]; [Coubret et al., 2019][doi-1016-2]; [Plu-Bureau, 2019][doi-1016-3]; [Senofonte, Pallotti, & Lombardo, 2020][doi-1016-4])</sup>。[这里][pharmacovigilance-survey] ([PDF][pharmacovigilance-survey-pdf]; 128 页)
|
||||
和 [这里][pharmacoepidemiology-study] ([PDF][pharmacoepidemiology-study-pdf]; 106 页) 可见与法国政府牵头的流行病学研究的长篇报告有关的更多信息;更简洁的报告亦可[在此查阅][pharmacovigilance-survey] ([PDF][pharmacovigilance-survey-amavea-pdf]; 9 页; [英译文][french-government-reports])。
|
||||
[这篇][french-news] 2018 年的法语新闻文章 (通过 [Google 翻译][french-news-eng] 从法语翻译成英语) 简洁地讨论了一部分进展。一些最近的文献出版物也讨论了这个话题 <sup>([Schmutz, 2018][s18]; [Gerson, 2018][g18]; [Coubret et al., 2019][c19]; [Plu-Bureau, 2019][pb19]; [Senofonte, Pallotti, & Lombardo, 2020][spl20])</sup>。\
|
||||
[这里][ansm1] ([PDF][ansm1-pdf]; 128 页)
|
||||
和 [这里][ansm2] ([PDF][ansm2-pdf]; 106 页) 可见与法国政府牵头的流行病学研究的长篇报告有关的更多信息;更简洁的报告亦可[在此查阅][ansm1] ([PDF][ansm1-amavea-pdf]; 9 页; [英译文][ansm1-eng])。\
|
||||
不过遗憾的是,上述材料有大部分都使用法语或其它非英语语言,且未向英语使用者提供译文(此时 Google 翻译倒是会很有用)。
|
||||
|
||||
[french-news]: https://www.doctissimo.fr/sante/news/androcur-meningiome
|
||||
[doi-1016-1]: https://doi.org/10.1016/j.annder.2018.04.001
|
||||
[doi-1016-2]: https://doi.org/10.1016/j.actpha.2019.09.013
|
||||
[doi-1016-3]: https://doi.org/10.1016/j.actpha.2019.10.006
|
||||
[doi-1016-4]: https://doi.org/10.1007/s40619-020-00746-8
|
||||
[jle]: https://www.jle.com/fr/revues/med/e-docs/androcur_cecite_des_prescripteurs_313193/article.phtml
|
||||
## 对女性倾向跨性别者的影响 {#implications-for-transfeminine-people}
|
||||
|
||||
[pharmacovigilance-survey]: https://ansm.sante.fr/S-informer/Points-d-information-Points-d-information/Acetate-de-cyproterone-Androcur-et-ses-generiques-et-risque-de-meningiome-Resultats-de-l-enquete-de-pharmacovigilance-Point-d-Information
|
||||
[pharmacovigilance-survey-pdf]: https://web.archive.org/web/20210130085742/https://ansm.sante.fr/var/ansm_site/storage/original/application/0a8007f555dd19d99a4b13a425dc8c3b.pdf
|
||||
[pharmacoepidemiology-study]: https://ansm.sante.fr/S-informer/Points-d-information-Points-d-information/Acetate-de-cyproterone-Androcur-et-ses-generiques-et-risque-de-meningiome-publication-du-rapport-complet-de-l-etude-de-pharmaco-epidemiologie-Point-d-information
|
||||
[pharmacoepidemiology-study-pdf]: https://www.ameli.fr/fileadmin/user_upload/documents/rapport_AC_et_meningiomeVFinale.pdf
|
||||
女性倾向跨性别者倾向于使用高剂量 CPA。尽管仅需约 2 至 3 mg/天 的剂量就可提供与妇女整个黄体期相当的孕激素暴露量,但《跨性别护理指南》对女性倾向跨性别者建议的 CPA 剂量通常可达 25 至 100 mg/天。这种孕激素暴露量已经达到甚至高于妇女妊娠期的暴露量(相比黄体期高至 20 倍),因此已高度超出妇女的正常生理水平。\
|
||||
除了脑膜瘤,高剂量的 CPA 还与血凝块、泌乳素瘤和肝毒性存在关联 <sup>([维基百科][brain-tumor-side-effect]; [Aly W., 2019][aw19-cd])</sup>。长期使用 CPA 等孕激素治疗也可能会增加患乳腺癌<sup>([Aly W., 2020][aw20-bc]; [表格][table1]; [乳腺癌激素相关因素合作研究小组(CGHFBC), 2019][cghfbc19]; [de Blok et al., 2019][b19])</sup>和心血管疾病 <sup>([表格][table2]; [Stefanick, 2010][s10])</sup> 的风险。同时还有很多其他的未知安全风险,正如我们近期才发现 CPA 有诱发脑膜瘤的风险这一事实。使用尽可能低剂量的 CPA 很可能会将其各种健康风险降至最低。
|
||||
|
||||
[pharmacovigilance-survey-amavea-pdf]: https://amavea.org/wp-content/uploads/2019/05/rapport-AC-et-meingiome_synthese-longue-v01.pdf
|
||||
[french-government-reports]: https://docs.google.com/document/d/1WcHLf7rj4Z0Cg6sqs4sz3JD_GwHFQj3-q0EObc8TJFs/view
|
||||
女性倾向跨性别者使用的 CPA 的剂量往往远超必要剂量;其仅需 5 至 10 mg/天 的剂量便可在睾酮抑制方面达到最大效力。不妨参阅笔者关于此话题所作[文章][aw19-cd]。\
|
||||
[Meyer 等人 (2020)][m20] 最近证实了低剂量 CPA 的有效性,他们的结果表明,在与雌激素合用时,10 mg/天 与 50 mg/天 的 CPA 剂量对女性倾向跨性别者的睾酮抑制效果没有区别。这应该清楚地证明了女性倾向跨性别者所用 CPA 剂量不应高于 10 或 12.5 mg/天。如使用切药器切割 50 毫克的 CPA 片剂,可以通过每日或每隔一日或服用四分之一片来控制 CPA 剂量在 6.25-12.5 mg/天。\
|
||||
该结果导致了对女性倾向跨性别者推荐的 CPA 剂量在近年有所下降 <sup>([Aly W., 2019][aw19-cd-literature])</sup>。此下降趋势在今后可能会更大。
|
||||
|
||||
|
||||
## 对女性倾向跨性别者的影响
|
||||
|
||||
女性倾向跨性别者倾向于使用高剂量 CPA。尽管仅需约 2 至 3 mg/天 的剂量就可提供与妇女整个黄体期相当的孕激素暴露量,但《跨性别护理指南》对女性倾向跨性别者建议的 CPA 剂量通常可达 25 至 100 mg/天。这种孕激素暴露量已经达到甚至高于妇女妊娠期的暴露量(相比黄体期高至 20 倍),因此已高度超出妇女的正常生理水平。
|
||||
除了脑膜瘤,高剂量的 CPA 还与血凝块、泌乳素瘤和肝毒性存在关联 <sup>([维基百科][brain-tumor-side-effect]; [Aly W., 2019][cpa-dosage])</sup>。长期使用 CPA 等孕激素治疗也可能会增加患乳腺癌<sup>([Aly W., 2020][breast-cancer]; [Wiki-Table][breast-cancer-risk-with-mht]; [乳腺癌激素相关因素合作研究小组(CGHFBC), 2019][doi-1016-5]; [de Blok et al., 2019][doi-1136-1])</sup>和心血管疾病 <sup>([表格][women-health-initiative-mhr-rct]; [Stefanick, 2010][doi-1016-6])</sup> 的风险。同时还有很多其他的未知安全风险,正如我们近期才发现 CPA 有诱发脑膜瘤的风险这一事实。使用尽可能低剂量的 CPA 很可能会将其各种健康风险降至最低。
|
||||
|
||||
[cpa-dosage]: cpa-dosage.md
|
||||
[breast-cancer]: breast-cancer.md
|
||||
[breast-cancer-risk-with-mht]: https://en.wikipedia.org/wiki/Template:Worldwide_epidemiological_evidence_on_breast_cancer_risk_with_menopausal_hormone_therapy
|
||||
[doi-1016-5]: https://doi.org/10.1016/S0140-6736(19)31709-X
|
||||
[doi-1016-6]: https://doi.org/10.1016/j.numecd.2010.02.015
|
||||
[doi-1136-1]: https://doi.org/10.1136/bmj.l1652
|
||||
[women-health-initiative-mhr-rct]: https://en.wikipedia.org/wiki/Template:Results_of_the_Women%27s_Health_Initiative_menopausal_hormone_therapy_randomized_controlled_trials
|
||||
|
||||
女性倾向跨性别者使用的 CPA 的剂量往往远超必要剂量;其仅需 5 至 10 mg/天 的剂量便可在睾酮抑制方面达到最大效力。不妨参阅笔者关于此话题所作[文章][cpa-dosage]。
|
||||
[Meyer 等人 (2020)][doi-1530-1] 最近证实了低剂量 CPA 的有效性,他们的结果表明,
|
||||
在与雌激素合用时,10 mg/天 与 50 mg/天 的 CPA 剂量对女性倾向跨性别者的睾酮抑制效果没有区别。这应该清楚地证明了女性倾向跨性别者所用 CPA 剂量不应高于 10 或 12.5 mg/天。如使用切药器切割 50 毫克的 CPA 片剂,可以通过每日或每隔一日或服用四分之一片来控制 CPA 剂量在 6.25-12.5 mg/天。
|
||||
该结果导致了对女性倾向跨性别者推荐的 CPA 剂量在近年有所下降 <sup>([Aly W., 2019][cpa-dosage-literature])</sup>。此下降趋势在今后可能会更大。
|
||||
|
||||
脑膜瘤表达于孕激素受体 (PRs)以及这些受体的激活被认为会刺激脑膜瘤的发展<sup>([Marosi et al., 2008][doi-1016-7]; [Li et al., 2013][doi-1038-1])</sup>。
|
||||
脑膜瘤表达于孕激素受体 (PRs)以及这些受体的激活被认为会刺激脑膜瘤的发展<sup>([Marosi et al., 2008][m08]; [Li et al., 2013][l13])</sup>。
|
||||
CPA 以外的孕激素和妊娠也被认为与脑膜瘤有关,也曾有过脑膜瘤在怀孕后自发消退的报告<sup>(Li et al., 2013; [维基百科][brain-tumor-side-effect])</sup>。
|
||||
女性脑膜瘤的发病率是男性的 2 至 3 倍,二者的比例最高时在女性生育高峰期<sup>(Marosi et al., 2008; [Wiemels, Wrensch, & Claus, 2010][doi-1007-1]; Li et al., 2013; [Wiki][brain-tumor-side-effect])</sup>。
|
||||
女性脑膜瘤的发病率是男性的 2 至 3 倍,二者的比例最高时在女性生育高峰期<sup>(Marosi et al., 2008; [Wiemels, Wrensch, & Claus, 2010][wwc10]; Li et al., 2013; [维基百科][brain-tumor-side-effect])</sup>。
|
||||
黄体期内孕激素水平上升也与女性脑膜瘤的恶化有关<sup>(Marosi et al., 2008; Wiemels, Wrensch, & Claus, 2010; Li et al., 2013; [维基百科][brain-tumor-side-effect])</sup>。
|
||||
避孕药和更年期激素疗法(雌—孕激素制剂)的使用也与脑膜瘤有关<sup>(Li et al., 2013)</sup>。
|
||||
因此,假设这些关联确实是由于 PR 的激活,那么就脑膜瘤而言,可能没有任何孕激素或 CPA 剂量是完全无风险的。
|
||||
事实上,即使在 5 至 10 mg/天 的 CPA 剂量下,也有诱发脑膜瘤的报告,尽管历史上并不大常用此类剂量 ([表格][brain-tumor-side-effect]) 。
|
||||
事实上,即使在 5 至 10 mg/天 的 CPA 剂量下,也有诱发脑膜瘤的报告,尽管历史上并不大常用此类剂量 ([表格][brain-tumor-side-effect]) 。\
|
||||
无论如何,数据表明风险是与剂量相关的,因此较低的剂量也应具有较小的风险。
|
||||
如连续使用 2 至 3 mg/天 的 CPA 剂量,则其引起的额外脑膜瘤风险应该可达到最小,并与妇女常规生理条件下的一致。
|
||||
|
||||
我们(跨性别)社区内也有 CPA 诱发脑膜瘤的报告。
|
||||
一名女性倾向跨性别者在 [Reddit][reporter-reddit] 上报告了其因 CPA 而罹患脑膜瘤;其所用剂量在第一年仅有 12.5 mg/天,随后更降至 6.25 mg/天。
|
||||
还有一名女性倾向跨性别者也在 [YouTube][reporter-youtuber] 上披露了自己因 CPA 而罹患脑膜瘤。
|
||||
一名女性倾向跨性别者在 [Reddit][reddit1] 上报告了其因 CPA 而罹患脑膜瘤;其所用剂量在第一年仅有 12.5 mg/天,随后更降至 6.25 mg/天。
|
||||
还有一名女性倾向跨性别者也在 [YouTube][youtube1] 上披露了自己因 CPA 而罹患脑膜瘤。
|
||||
|
||||
[doi-1016-7]: https://doi.org/10.1016/j.critrevonc.2008.01.010
|
||||
[doi-1530-1]: https://doi.org/10.1530/EJE-19-0463
|
||||
[doi-1038-1]: https://doi.org/10.1038/pcan.2013.45
|
||||
[doi-1007-1]: https://doi.org/10.1007/s11060-010-0386-3
|
||||
[cpa-dosage-literature]: https://transfemscience.org/articles/cpa-dosage-literature/
|
||||
[reporter-reddit]: https://www.reddit.com/r/AskMtFHRT/comments/g61bts/lovely_tumors_from_cpa_2y_mtf/
|
||||
[reporter-youtuber]: https://www.youtube.com/watch?v=g69cf-FG3o4
|
||||
|
||||
## 对女性倾向跨性别者的建议
|
||||
## 对女性倾向跨性别者的建议 {#recommendations-for-transfeminine-people}
|
||||
|
||||
鉴于 CPA 的风险及其低剂量下也具备的较高睾酮抑制效果,以下关于在女性倾向跨性别者使用 CPA 的建议应该很合适:
|
||||
|
||||
|
|
@ -158,95 +111,137 @@ CPA 以外的孕激素和妊娠也被认为与脑膜瘤有关,也曾有过脑
|
|||
- 尽可能在医生的指导下使用 CPA,服用 CPA 的人应遵循监测指南 (例如像法国一样定期做 MRI 检查) 。
|
||||
|
||||
需要注意的是,CPA 诱发脑膜瘤的绝对发病率较低,对年轻人和 CPA 剂量较低 (如 5 至 12.5 mg/天) 的人群来说风险可能更低。
|
||||
更谨慎和严格地使用 CPA 可能会获得更容易接受的安全性。
|
||||
更谨慎和严格地使用 CPA 可能会获得更容易接受的安全性。
|
||||
无论如何,脑膜瘤和脑部手术都是很严重的状况,因此不应随意使用 CPA。
|
||||
|
||||
---
|
||||
|
||||
-------
|
||||
## 后记 {#updates}
|
||||
|
||||
## 后记
|
||||
|
||||
### 后记一
|
||||
### 后记一 {#update-1}
|
||||
|
||||
2021 年 2 月,上述由法国政府牵头的研究以正式的科学文献发表:
|
||||
|
||||
- Weill, A., Nguyen, P., Labidi, M., Cadier, B., Passeri, T., Duranteau, L., Bernat, A., Yoldjian, I., Fontanel, S., Froelich, S., & Coste, J. (2021).
|
||||
Use of High Dose Cyproterone Acetate and Risk of Intracranial Meningioma in Women: Cohort Study.
|
||||
BMJ, 372, n37. [DOI:[10.1136/bmj.n37][doi-1136-1]]
|
||||
BMJ, 372, n37. [DOI:[10.1136/bmj.n37][b19]]
|
||||
|
||||
[doi-1136-1]: https://doi.org/10.1136/bmj.n37
|
||||
一篇刊载于 Medscape 上的 [文章][medscape1] 提及了这项研究,并讨论了对 CPA 使用的后续限制。
|
||||
|
||||
一篇刊载于 Medscape 上的 [文章][medscape-945218] 涵盖了这项研究,并讨论了对 CPA 使用的后续限制。
|
||||
|
||||
### 后记二
|
||||
### 后记二 {#update-2}
|
||||
|
||||
丹麦的一项全国性研究复现了上文所载发现 (并于 2020 年 12 月在 [medRxiv][medrxiv] 上发布) :
|
||||
|
||||
- Mikkelsen, A. P., Greiber, I. K., Scheller, N. M., Hilden, M., & Lidegaard, Ø.
|
||||
Cyproterone Acetate and Risk of Meningioma.
|
||||
[medRxiv][medrxiv], 2020-12. [DOI:[10.1101/2020.12.29.20248395][doi-1011-1]]
|
||||
|
||||
[medscape-945218]: https://www.medscape.com/viewarticle/945218
|
||||
[medrxiv]: https://www.medrxiv.org
|
||||
[doi-1011-1]: https://doi.org/10.1101/2020.12.29.20248395
|
||||
[medRxiv][medrxiv], 2020-12. [DOI:[10.1101/2020.12.29.20248395][mikk20]]
|
||||
|
||||
论文定稿则于 2021 年 6 月发表:
|
||||
|
||||
- Mikkelsen, A. P., Greiber, I. K., Scheller, N. M., Hilden, M., & Lidegaard, Ø. (2021).
|
||||
Cyproterone acetate and risk of meningioma: a nationwide cohort study. Journal of Neurology, Neurosurgery & Psychiatry.
|
||||
[DOI:[10.1136/jnnp-2021-326138][doi-1136-2]]
|
||||
[DOI:[10.1136/jnnp-2021-326138][m21]]
|
||||
|
||||
[doi-1136-2]: https://doi.org/10.1136/jnnp-2021-326138
|
||||
### 后记三 {#update-3}
|
||||
|
||||
### 后记三
|
||||
|
||||
截至 2020 年 8 月,[阿姆斯特丹自由大学医学中心][vumc] (VUMC) 将所有跨性别者的抗雄激素治疗从醋酸环丙孕酮改为促性腺激素释放激素 (GnRH) 激动剂;这项改变是出于荷兰药品管理局发布的关于 CPA 诱发脑膜瘤的警告<sup>([VUMC, 2020][vumc-report])</sup>。
|
||||
VUMC 是 [性别焦虑专家中心][gd-center] 的所在地,该中心是世界上规模最大的跨性别激素治疗护理和研究机构之一,在该领域具有很高的影响力<sup>([Wiepjes et al.,][doi-1016-8]; [Bakker, 2021][transgender-care])</sup>。据说 VUMC 为荷兰约 95% 的寻求激素治疗的跨性别者提供激素治疗,自 1972 年开设性别诊所以来,已为约一万名跨性别者提供治疗<sup>(Wiepjes et al., 2018; Bakker, 2021)</sup>。
|
||||
|
||||
[vumc]: https://en.wikipedia.org/wiki/VU_University_Medical_Center
|
||||
[vumc-report]: https://www.vumc.nl/zorg/expertisecentra-en-specialismen/kennis-en-zorgcentrum-genderdysforie/informatie-voor-patienten-kennis-en-zorgcentrum-genderdysforie/wijzigingen-medisch-beleid-hormoonbehandeling.htm
|
||||
[gd-center]: https://en.wikipedia.org/wiki/Center_of_Expertise_on_Gender_Dysphoria
|
||||
[doi-1016-8]: https://doi.org/10.1016/j.jsxm.2018.01.016
|
||||
[transgender-care]: https://www.boomgeschiedenis.nl/product/100-9692_Een-halve-eeuw-transgenderzorg-aan-de-VU
|
||||
截至 2020 年 8 月,[阿姆斯特丹自由大学医学中心][vumc] (VUMC) 将所有跨性别者的抗雄激素治疗从醋酸环丙孕酮改为促性腺激素释放激素 (GnRH) 激动剂;这项改变是出于荷兰药品管理局发布的关于 CPA 诱发脑膜瘤的警告<sup>([VUMC, 2020][vumc20])</sup>。
|
||||
VUMC 是 [性别焦虑专家中心][gd-center] 的所在地,该中心是世界上规模最大的跨性别激素治疗护理和研究机构之一,在该领域具有很高的影响力<sup>([Wiepjes et al., 2018][w18]; [Bakker, 2021][b21])</sup>。据说 VUMC 为荷兰约 95% 的寻求激素治疗的跨性别者提供激素治疗,自 1972 年开设性别诊所以来,已为约一万名跨性别者提供治疗<sup>(Wiepjes et al., 2018; Bakker, 2021)</sup>。
|
||||
|
||||
<!-- 以下片段为 2021 年 10 月以来增补的 -->
|
||||
|
||||
### 后记四
|
||||
### 后记四 {#update-4}
|
||||
|
||||
2021 年 10 月,一篇对 CPA 引起的脑膜瘤进行系统性评述的论文公开发表:
|
||||
|
||||
- Millward, C. P., Keshwara, S. M., Islim, A. I., Jenkinson, M. D., Alalade, A. F., & Gilkes, C. E. (2021).
|
||||
Development and Growth of Intracranial Meningiomas in Transgender Women Taking Cyproterone Acetate as Gender-Affirming Progestogen Therapy: A Systematic Review.
|
||||
Transgender Health. [[DOI:10.1089/trgh.2021.0025][M21]]
|
||||
- Millward, C. P., Keshwara, S. M., Islim, A. I., Jenkinson, M. D., Alalade, A. F., & Gilkes, C. E. (2021).
|
||||
Development and Growth of Intracranial Meningiomas in Transgender Women Taking Cyproterone Acetate as Gender-Affirming Progestogen Therapy: A Systematic Review.
|
||||
Transgender Health. \[DOI: <https://doi.org/10.1089/trgh.2021.0025>]
|
||||
|
||||
[M21]: https://doi.org/10.1089/trgh.2021.0025
|
||||
|
||||
|
||||
### 后记五
|
||||
### 后记五 {#update-5}
|
||||
|
||||
2022 年 2 月,一篇对 CPA 引起的脑膜瘤进行系统性荟萃分析及评述的论文公开发表:
|
||||
|
||||
- Lee, K. S., Zhang, J., Kirollos, R., Santarius, T., Nga, V., & Yeo, T. T. (2022).
|
||||
A systematic review and meta-analysis of the association between cyproterone acetate and intracranial meningiomas.
|
||||
Scientific Reports, 12(1), 1942. [[DOI:10.1038/s41598-022-05773-z][L22]]
|
||||
- Lee, K. S., Zhang, J., Kirollos, R., Santarius, T., Nga, V., & Yeo, T. T. (2022).
|
||||
A systematic review and meta-analysis of the association between cyproterone acetate and intracranial meningiomas.
|
||||
Scientific Reports, 12(1), 1942. \[DOI: <https://doi.org/10.1038/s41598-022-05773-z>]
|
||||
|
||||
该论文为《[科学日报][L22-SD]》及《[医学快讯][L22-MX]》的新闻内容所提及。
|
||||
该论文为《[科学日报][l22-sd]》及《[医学快讯][l22-mx]》的新闻内容所提及。
|
||||
|
||||
[L22]: https://doi.org/10.1038/s41598-022-05773-z
|
||||
[L22-SD]: https://www.sciencedaily.com/releases/2022/02/220204113440.htm
|
||||
[L22-MX]: https://medicalxpress.com/news/2022-02-widely-used-hormone-drug-benign-brain.html
|
||||
|
||||
|
||||
### 后记六
|
||||
### 后记六 {#update-6}
|
||||
|
||||
2022 年 9 月,一项在法国进行的、对使用高剂量合成孕酮制剂治疗的人群的脑膜瘤发生率进行系统性筛查的研究,公开发表了其论文:
|
||||
|
||||
- Samoyeau, T., Provost, C., Roux, A., Legrand, L., Dezamis, E., Plu-Bureau, G., Pallud, J., Oppenheim, C., & Benzakoun, J. (2022).
|
||||
Meningioma in patients exposed to progestin drugs: results from a real-life screening program.
|
||||
Journal of Neuro-Oncology, advance online publication. [[DOI:10.1007/s11060-022-04124-2][S22]]
|
||||
- Samoyeau, T., Provost, C., Roux, A., Legrand, L., Dezamis, E., Plu-Bureau, G., Pallud, J., Oppenheim, C., & Benzakoun, J. (2022).
|
||||
Meningioma in patients exposed to progestin drugs: results from a real-life screening program.
|
||||
Journal of Neuro-Oncology, advance online publication. \[DOI: <https://doi.org/10.1007/s11060-022-04124-2>]
|
||||
|
||||
其结果显示,由 103 人组成的该群体,有 13 人因 CPA 而罹患脑膜瘤,发生率达到惊人的 13%。这项数字远比一般人群中约 1-2% 的诱导性脑膜瘤发生率要高。论文作者还提到,在该项目观测到的 13% 发生率很可能还被低估了,因为大多数因 CPA 引起的脑膜瘤病例或许在接受系统性筛查之前便已被确诊。相应地,脑膜瘤年化发生率则为每年每十万人 13.2 例。
|
||||
和其它研究相似,脑膜瘤的发生也被认为和更长的 CPA 使用时间、更高的 CPA 累积剂量与更大的年龄有关。
|
||||
其结果显示,由 103 人组成的该群体,有 13 人因 CPA 而罹患脑膜瘤,发生率达到惊人的 13%。这项数字远比一般人群中约 1-2% 的诱导性脑膜瘤发生率要高。论文作者还提到,在该项目观测到的 13% 发生率很可能还被低估了,因为大多数因 CPA 引起的脑膜瘤病例或许在接受系统性筛查之前便已被确诊。相应地,脑膜瘤年化发生率则为每年每十万人 13.2 例。
|
||||
和其它研究相似,脑膜瘤的发生也被认为和更长的 CPA 使用时间、更高的 CPA 累积剂量与更大的年龄有关。
|
||||
使用醋酸诺美孕酮及醋酸氯地孕酮所引起的脑膜瘤发生率则远低于上值。不过此二者的使用剂量基本上远小于 CPA。
|
||||
|
||||
[S22]: https://doi.org/10.1007/s11060-022-04124-2
|
||||
---
|
||||
|
||||
## 译文修订记录
|
||||
|
||||
- 2021 年 10 月 29 日——首次翻译。
|
||||
- 2022 年 10 月 20 日——第一次修订,梳理全文叙述,增补“后记四~六”内容,整理外链。
|
||||
|
||||
<!-- 维基百科条目 -->
|
||||
[cpa]: https://en.wikipedia.org/wiki/Cyproterone_acetate
|
||||
[meningioma]: https://en.wikipedia.org/wiki/Meningioma
|
||||
[benign-tumor]: https://en.wikipedia.org/wiki/Benign_tumor
|
||||
[brain-tumor]: https://en.wikipedia.org/wiki/Brain_tumor
|
||||
[brain-tumor-side-effect]: https://en.wikipedia.org/wiki/Side_effects_of_cyproterone_acetate#Brain_tumors
|
||||
[meninges]: https://en.wikipedia.org/wiki/Meninges
|
||||
[malignancy]: https://en.wikipedia.org/wiki/Malignancy
|
||||
[cpa-case-reports]: https://en.wikipedia.org/wiki/Template:Published_case_reports_of_cyproterone_acetate-associated_meningioma
|
||||
[lutenyl]: https://en.wikipedia.org/wiki/Nomegestrol_acetate
|
||||
[luteran]: https://en.wikipedia.org/wiki/Chlormadinone_acetate
|
||||
[ema]: https://en.wikipedia.org/wiki/European_Medicines_Agency
|
||||
[hmra]: https://en.wikipedia.org/wiki/Medicines_and_Healthcare_products_Regulatory_Agency
|
||||
[table1]: https://en.wikipedia.org/wiki/Template:Worldwide_epidemiological_evidence_on_breast_cancer_risk_with_menopausal_hormone_therapy
|
||||
[table2]: https://en.wikipedia.org/wiki/Template:Results_of_the_Women%27s_Health_Initiative_menopausal_hormone_therapy_randomized_controlled_trials
|
||||
[vumc]: https://en.wikipedia.org/wiki/VU_University_Medical_Center
|
||||
[gd-center]: https://en.wikipedia.org/wiki/Center_of_Expertise_on_Gender_Dysphoria
|
||||
|
||||
<!-- 引用文献 -->
|
||||
[docs-asnm]: https://docs.google.com/document/d/1WcHLf7rj4Z0Cg6sqs4sz3JD_GwHFQj3-q0EObc8TJFs/view
|
||||
[c19]: https://www.medscape.com/viewarticle/915545
|
||||
[c20]: https://www.medscape.com/viewarticle/925271
|
||||
[ema20]: https://www.ema.europa.eu/en/news/restrictions-use-cyproterone-due-meningioma-risk
|
||||
[mhra20]: https://www.gov.uk/drug-safety-update/cyproterone-acetate-new-advice-to-minimise-risk-of-meningioma
|
||||
[s18]: https://doi.org/10.1016/j.annder.2018.04.001
|
||||
[pb19]: https://doi.org/10.1016/j.actpha.2019.10.006
|
||||
[spl20]: https://doi.org/10.1007/s40619-020-00746-8
|
||||
[g18]: https://www.g18.com/fr/revues/med/e-docs/androcur_cecite_des_prescripteurs_313193/article.phtml
|
||||
[aw19-cd]: https://transfemscience.org/articles/aw19-cd/
|
||||
[aw20-bc]: https://transfemscience.org/articles/aw20-bc/
|
||||
[cghfbc19]: https://doi.org/10.1016/S0140-6736(19)31709-X
|
||||
[s10]: https://doi.org/10.1016/j.numecd.2010.02.015
|
||||
[b19]: https://doi.org/10.1136/bmj.l1652
|
||||
[m08]: https://doi.org/10.1016/j.critrevonc.2008.01.010
|
||||
[m20]: https://doi.org/10.1530/EJE-19-0463
|
||||
[l13]: https://doi.org/10.1038/pcan.2013.45
|
||||
[wwc10]: https://doi.org/10.1007/s11060-010-0386-3
|
||||
[aw19-cd-literature]: https://transfemscience.org/articles/aw19-cd-literature/
|
||||
[mikk20]: https://doi.org/10.1101/2020.12.29.20248395
|
||||
[m21]: https://doi.org/10.1136/jnnp-2021-326138
|
||||
[vumc20]: https://www.vumc.nl/zorg/expertisecentra-en-specialismen/kennis-en-zorgcentrum-genderdysforie/informatie-voor-patienten-kennis-en-zorgcentrum-genderdysforie/wijzigingen-medisch-beleid-hormoonbehandeling.htm
|
||||
[w18]: https://doi.org/10.1016/j.jsxm.2018.01.016
|
||||
[b21]: https://www.boomgeschiedenis.nl/product/100-9692_Een-halve-eeuw-transgenderzorg-aan-de-VU
|
||||
[l22-sd]: https://www.sciencedaily.com/releases/2022/02/220204113440.htm
|
||||
[l22-mx]: https://medicalxpress.com/news/2022-02-widely-used-hormone-drug-benign-brain.html
|
||||
|
||||
<!-- 其它材料 -->
|
||||
[french-news]: https://www.doctissimo.fr/sante/news/androcur-meningiome
|
||||
[french-news-eng]: https://www-doctissimo-fr.translate.goog/sante/news/androcur-meningiome?_x_tr_sl=fr&_x_tr_tl=en&_x_tr_hl=en
|
||||
[ansm1]: https://ansm.sante.fr/S-informer/Points-d-information-Points-d-information/Acetate-de-cyproterone-Androcur-et-ses-generiques-et-risque-de-meningiome-Resultats-de-l-enquete-de-pharmacovigilance-Point-d-Information
|
||||
[ansm1-pdf]: https://web.archive.org/web/20210130085742/https://ansm.sante.fr/var/ansm_site/storage/original/application/0a8007f555dd19d99a4b13a425dc8c3b.pdf
|
||||
[ansm2]: https://ansm.sante.fr/S-informer/Points-d-information-Points-d-information/Acetate-de-cyproterone-Androcur-et-ses-generiques-et-risque-de-meningiome-publication-du-rapport-complet-de-l-etude-de-pharmaco-epidemiologie-Point-d-information
|
||||
[ansm2-pdf]: https://www.ameli.fr/fileadmin/user_upload/documents/rapport_AC_et_meningiomeVFinale.pdf
|
||||
[ansm1-amavea-pdf]: https://amavea.org/wp-content/uploads/2019/05/rapport-AC-et-meingiome_synthese-longue-v01.pdf
|
||||
[ansm1-eng]: https://docs.google.com/document/d/1WcHLf7rj4Z0Cg6sqs4sz3JD_GwHFQj3-q0EObc8TJFs/view
|
||||
[reddit1]: https://reddit.com/r/AskMtFHRT/comments/g61bts
|
||||
[youtube1]: https://www.youtube.com/watch?v=g69cf-FG3o4
|
||||
[medscape1]: https://www.medscape.com/viewarticle/945218
|
||||
[medrxiv]: https://www.medrxiv.org
|
||||
|
|
@ -0,0 +1,363 @@
|
|||
---
|
||||
title: 关于女性倾向跨性别者以阴囊及新阴唇给予透皮雌二醇可极大增强吸收率的简论
|
||||
linkTitle: 阴囊及新阴唇对透皮雌二醇的极高吸收率
|
||||
description: >-
|
||||
外生殖器皮肤(如阴囊、阴茎和阴唇皮肤)对雌二醇的吸收能力似乎要强于其它皮肤区域,而且此处用药并未额外增加癌症风险,相对安全。
|
||||
author: Aly W.
|
||||
published: 2019-03-29
|
||||
updated: 2022-04-27
|
||||
translated: 2022-11-14
|
||||
translators:
|
||||
- 昭心
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 雌激素
|
||||
- 用药途径与剂量
|
||||
trackHash: 707eba7009f219b84a9dcb94eb5c05b8d7400b23
|
||||
---
|
||||
|
||||
## 译者按 {#notice}
|
||||
|
||||
1. **<u>⚠ 免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
---
|
||||
|
||||
## 摘要 {#abstract}
|
||||
|
||||
> 外生殖器皮肤(如阴囊、阴茎和阴唇皮肤)的吸收能力似乎要强于其它皮肤区域。人们通常会将雌二醇、睾酮等透皮激素制剂应用于手臂、臀部和腹部等区域;不过对于外生殖器给药却鲜有研究。\
|
||||
> 通常 100 μg/天剂量的雌二醇透皮贴片可引起平均约 100 pg/ml 的雌二醇水平。在阿根廷,有一项关于前列腺癌患者通过阴囊使用雌二醇贴片的临床研究发现,阴囊给药所提供的雌二醇水平比前臂给药高得多;在此 100 μg/天剂量的雌二醇透皮贴片能引起平均 500 pg/ml 的雌二醇水平。这与以下认知一致:阴囊给药的效率是常规皮肤部位的 5 倍。\
|
||||
> 至于雌二醇透皮凝胶用于外生殖器的用法,至今尚未有文献评估;但有关睾酮凝胶与乳剂用于阴囊的研究已发现,相比于常规皮肤部位,阴囊给药引起的睾酮水平要高出 5-8 倍。由于雌二醇与睾酮的化学性质相似,且通过阴囊给予的雌二醇贴片同样可达到高雌二醇水平,故这项发现应该可推导至雌二醇凝胶。\
|
||||
> 对于女性化激素治疗,外生殖器对雌二醇的高吸收率也许大有可为。如果女性倾向跨性别者通过透皮给药并不能达到理想的雌二醇水平,需要更高水平(例如在高剂量雌激素单药疗法当中)来抑制睾酮;那么可改为外生殖器给药。
|
||||
|
||||
## 前言 {#introduction}
|
||||
|
||||
雌二醇可通过多种[形式][wiki1]与[途径][wiki2]给药<sup>([维基百科][wiki3])</sup>。其中一种途径是[透皮给药][wiki4],其形式包括[雌二醇贴片][wiki3-tp]、[凝胶][wiki3-tg]、[乳剂][wiki3-otf]与[喷雾剂][wiki3-otf];不过,贴片与凝胶是迄今使用最多的。传统上,透皮雌二醇会被应用于手臂、腹部等皮肤部位。\
|
||||
每块 100 μg/天的雌二醇贴片通常可引起 50-100 pg/mL 左右的雌二醇水平;而每 3 mg/天的雌二醇凝胶引起的水平通常约为 100 pg/mL<sup>([Aly W., 2020][aw20-eed]; [维基百科][wiki3])</sup>。不过,雌二醇水平[在个体间差别][wiki4]显著<sup>([维基百科][wiki3-vip])</sup>;在透皮雌二醇的形式与剂量相同的情况下,某些人会有偏高或者偏低的雌二醇水平。对一部分人而言,其雌二醇水平可能低得不足以产生理想的疗效,对睾酮的抑制作用也不充分;如使用高剂量透皮雌二醇单药疗法,其也很难获得抑制睾酮所需的高雌二醇水平。
|
||||
|
||||
1960 年代,一篇有关[氢化可的松][wiki6]用于人皮肤不同部位的透皮[吸收率][wiki7]的临床研究论文公开发表<sup>([Feldmann & Maibach, 1967][fm67]; [相关材料][fm67-suppl])</sup>。(需要指出,氢化可的松——也称[皮质醇][wiki6a]——作为一种[甾体激素][wiki8],在结构上与[雌二醇][wiki9]、[睾酮][wiki10]等[性激素][wiki11]很相似。)此研究将氢化可的松[用放射性同位素标记][wiki12],并将其溶液涂抹于男性的不同皮肤部位,然后对用药后排出的尿液中的放射性物质(氢化可的松及其代谢物)之含量进行测定<sup>(Feldmann & Maibach, 1967)</sup>。\
|
||||
研究者发现,尿液的放射性在不同用药部位之间有很大分别;其中,[阴囊][wiki13]给药后所检出的放射性远远高于前臂及其它部位。不同部位用药后的尿液放射性系数分别为(以前臂为基准,由高到低)<sup>(Feldmann & Maibach, 1967)</sup>:
|
||||
|
||||
- 阴囊(42.0)
|
||||
- 下颌角(13.0)
|
||||
- 前额(6.0)
|
||||
- 腋下(3.6)
|
||||
- 头皮(3.5)
|
||||
- 背部(1.7)
|
||||
- **前臂(1.0)**
|
||||
- 手掌(0.8)
|
||||
- 脚踝(0.4)
|
||||
- 足底(0.1)
|
||||
|
||||
这是第一项表明了外生殖器(如阴囊)皮肤的透皮吸收率可显著高于其它皮肤部位的研究。
|
||||
|
||||
从阴囊对氢化可的松及其它药物吸收更佳的发现,也衍生出了一个问题:雌二醇与睾酮用于外生殖器是否也具有更大的[生物利用度][wiki14]。其中睾酮已在 1980 年代被确认有此特性,此后睾酮的阴囊贴片(品牌 Testoderm)得以研发并于 1993 年在美国批准上市<sup>([Place et al., 1990][p90]; [Mazer et al., 1992][m92]; [Atkinson, Chang, & Snyder, 1998][acs98])</sup>。\
|
||||
与此相反的是,透皮雌二醇似乎从未被研究用于阴囊;这也许是因为雌激素极少用于男性。不过,最近笔者偶然发现了这篇很晦涩的、关于患[前列腺癌][wiki15]的男性在[高剂量雌激素疗法][wiki16]当中通过阴囊使用[雌二醇透皮贴片][wiki17]的研究论文:
|
||||
|
||||
- Premoli, F., Re, I., Asenjo, G., Maximino, G., & Micheletti, L. (2005).
|
||||
Tratamiento del Cáncer de Próstata Avanzado con Estrógenos Transdérmicos Escrotales (ETE).
|
||||
\[阴囊给药的透皮雌激素贴片(TSEP)在晚期前列腺癌治疗当中的应用]
|
||||
_Revista Argentina de Urología, 70_(4), 231–241.
|
||||
[[Google 学术][P05]] [[网页地址][P05-ARCHIVE]] [[PDF 文档][P05-PDF]] [[英译文][P05-ENG]]
|
||||
|
||||
这应该是第一项、也是迄今唯一一项调研阴囊给药的透皮雌二醇的研究。其论文并非以英语撰写,因此早前的文献检索并未发现之。\
|
||||
在讨论该研究的结果之前,下文将会介绍关于阴囊给药的[透皮雌二醇][wiki18]的一些背景和原理。
|
||||
如读者对研究结果更感兴趣,可跳转到“[研究结果]({{< ref "#study-findings" >}})”一章。
|
||||
|
||||
## 背景 {#further-background}
|
||||
|
||||
高剂量的[雌激素][wiki19]有很强的[抗雄激素][wiki20]效力,因此常作为一种[雄激素匮乏疗法][wiki21],用于男性前列腺癌的治疗。具体而言,雌激素可通过其[抗促性腺激素][wiki22]作用来抑制性腺[睾酮][wiki23]的产生;同时,还可增加[性激素结合球蛋白][wiki24] (SHBG) 的产生和血清水平,以降低游离(即具备生物活性)的[雄激素][wiki25]之比例。大剂量雌激素疗法的抗雄效力,与[性腺切除术][wiki26]和[促性腺激素释放激素][wiki27] (GnRH) [激动剂][wiki28]、[拮抗剂][wiki29]相当,不过其具有独特的优缺点。\
|
||||
雌激素疗法的优点包括减少[潮热][wiki30]、保持[骨密度][wiki31]、保留部分[性欲][wiki32]、改善[生活质量][wiki33]、以及低得多的成本。其缺点包括[女性化][wiki34]、[男性乳房发育症][wiki35](对顺性别男性来说乳房发育当然是不受欢迎的)、以及[心血管毒性][wiki36]。\
|
||||
相比于[口服][wiki37]或非生物同质性雌激素(如[己烯雌酚][wiki38]、[炔雌醇][wiki39]和[结合雌激素][wiki40]),使用[非肠胃途径][wiki41]、具[生物同质性][wiki42]的雌二醇是更好的选择——例如[注射用雌二醇酯][wiki43]和透皮雌二醇。这是因为后者的心血管毒性倾向要低得多<sup>([Aly W.,2020][aw20-ecbc])</sup>。
|
||||
|
||||
注射雌二醇酯可以有效对抗前列腺癌,但传统上用于治疗的长效雌二醇酯(如[聚磷酸雌二醇][wiki44]与[十一酸雌二醇][wiki45])皆已停产。至于[戊酸雌二醇][wiki46]、[环戊丙酸雌二醇][wiki47]等短效雌二醇酯,尽管可作为替代,但其注射频率更频繁(例如每周注射一次),而且在全球多个地区的供应有限。此外,注射过程并不方便,且可能引起部分患者的痛苦和焦虑。\
|
||||
透皮雌二醇贴片也较有效,但通常需要 3-4 个 100 μg/天的贴片才能完全抑制睾酮水平<sup>([Ockrim, Lalani, & Abel, 2006][ola06]; [Langley et al., 2008][l08]; [Langley et al., 2021][l21])</sup>。同时使用多个贴片不仅可能带来不适,而且开销会很大。\
|
||||
[透皮雌二醇凝胶][wiki48]也曾被用于治疗前列腺癌,但其所需剂量很高(≥6 mg/天);并且即使如此,也只能有限地提高雌二醇水平,对睾酮的抑制也不完全<sup>([Aly W., 2019][aw19-hdte])</sup>。
|
||||
|
||||
[透皮][wiki4]药剂可经皮肤渗透吸收。不同皮肤部位的[吸收][wiki7]能力有异。早在数十年前,人们便已认识到,阴囊皮肤对药剂的吸收能力远高于其它绝大多数部位<sup>([Feldmann & Maibach, 1967][fm67] [[相关材料][FM67-SUPPL]]; [维基百科][wiki3-ta])</sup>。这里需要指出,最早用于医疗用途的[透皮睾酮贴片][wiki49],是阴囊贴片;这是因为男性所需的睾酮不少。此后,非阴囊给药的睾酮贴片才得以推出,而且为提供基本等量的睾酮,其尺寸必须变得更大<sup>([Behre & Nieschlag, 2012][bn12]; [Khera, 2013][k13])</sup>。\
|
||||
综上,考虑到雌二醇在结构上近似于睾酮,可以认为透皮雌二醇制剂用于阴囊时也有远高于常规部位的吸收率。
|
||||
|
||||
说回上文“[前言]({{< ref "#introduction" >}})”一章提及的 Premoli 等人 (2005) 的研究:其对在前列腺癌治疗中通过阴囊使用单个透皮雌二醇贴片的状况进行了评估。研究者均来自阿根廷;在这个贫困率很高的国家,大部分人口无力承担高昂的药费。因此,除了雌激素疗法相对于常规抗雄激素疗法的优势以外,经济方面的因素也成为他们研究的动机之一。\
|
||||
他们的基本目标是:为了能够完全抑制睾酮水平、并治疗前列腺癌,通过非肠胃给药、毒性更小的途径来达到较高的雌二醇水平,同时维持较小的开销、和较好的便利性。除了治疗前列腺癌之外,这与许多女性倾向跨性别者的治疗目标非常相似。因此,这种疗法或许对女性化激素治疗也很有价值。
|
||||
|
||||
许多女性倾向跨性别者会为了达到更高的雌二醇水平并抑制睾酮,而选择将[口服雌二醇][wiki50]片剂用于[舌下含服][wiki51]。不过,舌下含服存在一些缺点,例如作用时间短、雌二醇水平波动大;同时还有一部分雌二醇会在肝脏内过度暴露,从而可能引起更高的健康风险(如血栓与心血管问题)<sup>([Sam S.,2021][ss21-set];[维基百科][wiki3-sa])</sup>。\
|
||||
因此,如果有一种替代选项能够引起更稳定、持久的雌二醇水平,其应该会很受欢迎。
|
||||
|
||||
## 研究结果 {#study-findings}
|
||||
|
||||
Premoli 等人 (2005) 首先对两名患前列腺癌的男性进行了交叉型概念验证预实验,以评估阴囊对透皮雌二醇的吸收是否优于非阴囊部位。其中一名患者先以前臂使用 50 μg/天的雌二醇贴片,然后再以阴囊给药;另一名患者同样先以前臂、再以阴囊给药,不过使用的是 100 μg/天的雌二醇贴片。\
|
||||
研究者发现,阴囊给药后的最大雌二醇水平远高于前臂:
|
||||
|
||||
<section class="box">
|
||||
|
||||
**表 1**: 在上述预实验中,前臂、阴囊给予雌二醇贴片之后的雌二醇水平:
|
||||
|
||||
```csv
|
||||
患者,雌二醇贴片剂量,给药部位,最大雌二醇水平,差异
|
||||
患者甲,50 μg/天,前臂,55 pg/mL,–
|
||||
,,阴囊,200 pg/mL,3.6 倍
|
||||
患者乙,100 μg/天,前臂,180 pg/mL,–
|
||||
,,阴囊,500 pg/mL,2.8 倍
|
||||
```
|
||||
|
||||
</section>
|
||||
|
||||
下图将这项微型初期预实验的全过程结果可视化(受试者 2 人,交叉对照):
|
||||
|
||||
<section class="box">
|
||||
|
||||
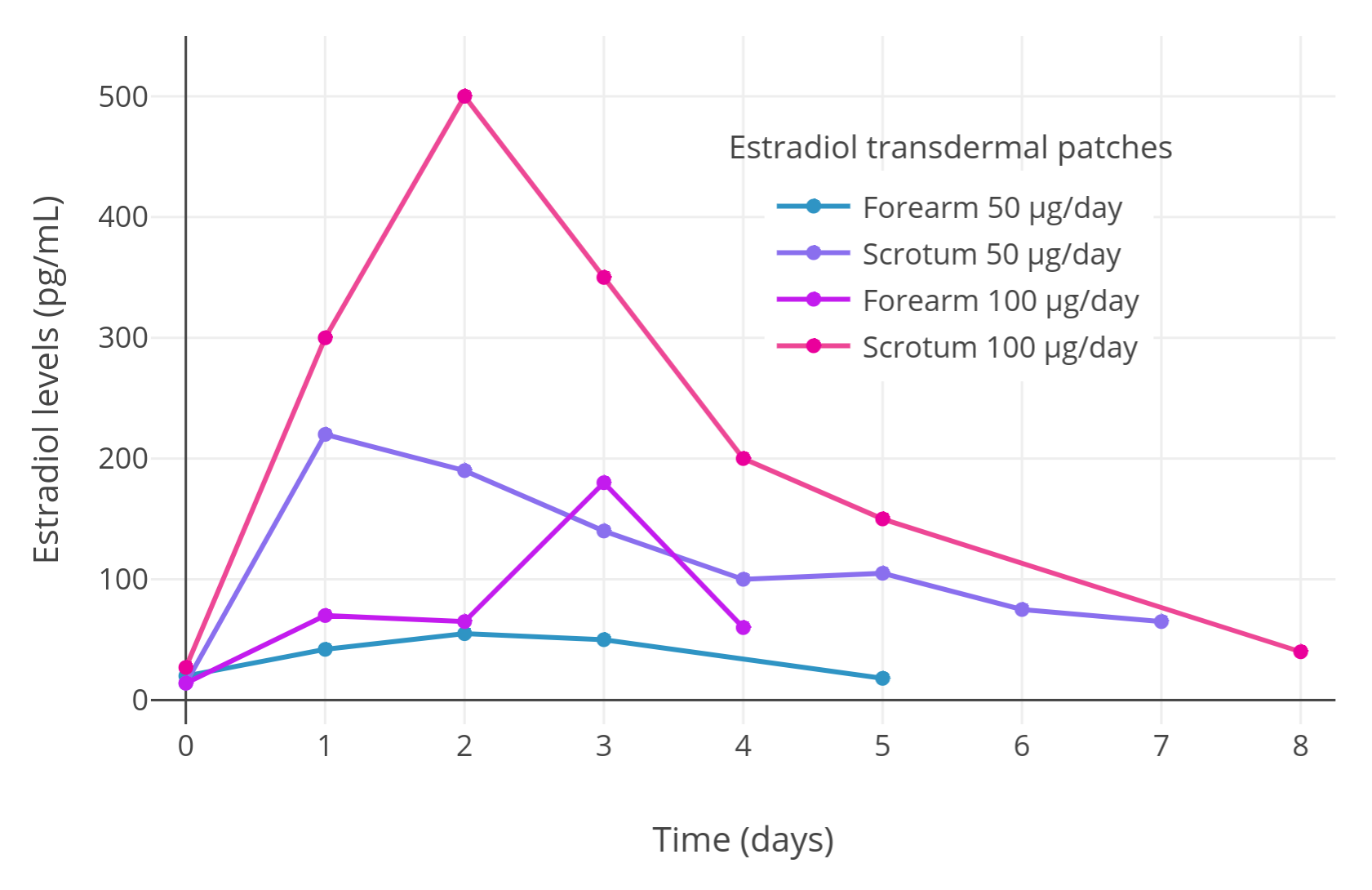
|
||||
|
||||
**图 1**:
|
||||
在交叉对照中,两名男性前列腺癌患者以阴囊给予透皮雌二醇贴片所引起的雌二醇水平<sup>(Premoli et al., 2005)</sup>。\
|
||||
在本项初期预实验之后,研究者对 35 名男性前列腺癌患者以阴囊持续给予 100 μg/天的雌二醇透皮贴片,其观测到的平均雌二醇水平约为 500 pg/mL <sup>(Premoli et al., 2005)</sup>。
|
||||
|
||||
</section>
|
||||
|
||||
这项微型预实验结束之后,Premoli 等人展开了完整的研究,其中包括 35 名前列腺癌患者;每位患者每天经阴囊给予一个 100 μg/天的雌二醇透皮贴片。与预实验结果相似,所有受试者的平均雌二醇水平达 500 pg/ml 左右,范围则在 125 - 1,200 pg/mL 左右。范围幅度之大,恰与透皮途径的雌二醇在个体间可产生雌二醇水平的[巨大差异][wiki5]的认识相吻合<sup>([维基百科][wiki3-ta])</sup>。\
|
||||
如通过常规皮肤部位给药,则单个 100 μg/天 的雌二醇贴片仅可产生平均约 100 pg/mL 的雌二醇水平<sup>([维基百科][wiki3-tp];[图表][graph1])</sup>。\
|
||||
此外,一项研究显示,在使用 2-6 剂雌二醇贴片的情况下,平均雌二醇水平也只能达到 200 - 400 pg/mL<sup>([图表][graph2];[Ockrim, Lalani, & Abel, 2006][ola06])</sup>。\
|
||||
综上,如将雌二醇透皮贴片用于阴囊,则其[生物利用度][wiki14]应该有非阴囊部位的至少约 5 倍之大。此幅度与将口服雌二醇片剂用于舌下含服对生物利用度之提升的幅度(约 2-5 倍)相近<sup>([维基百科][wiki3-sa])</sup>。
|
||||
|
||||
研究中观察到的雌二醇平均水平(即 500 pg/mL)已知足以强烈抑制性腺睾酮的产生、进而抑制血清睾酮水平;已知不小于 200 pg/mL 的雌二醇水平可将睾酮水平平均抑制 ≥90% <sup>([Aly W., 2018][aw18-intro-gs]; [维基百科][wiki52-ae])</sup>。不过遗憾的是,Premoli 及其同行无法获得大多数受试者的睾酮抑制数据;因为几乎所有患者早已在研究开始前接受了常规的雄激素匮乏治疗(如性腺切除术和 GnRH 调节剂),其初始睾酮水平已很低(平均 28 ng/dL,范围 10-90 ng/dL)。\
|
||||
无论如何,据研究者所述,仍有两名患者未事先接受常规的雄激素匮乏治疗,其初始睾酮水平仍在男性范围内;在其接受间歇性治疗期间,以阴囊给予雌二醇贴片时的睾酮水平为 10 - 30 ng/dL,停药时为 200 - 600 ng/dL。这与其它临床研究预期的高雌二醇水平对睾酮水平的强烈抑制是一致的。
|
||||
|
||||
## 对女性倾向跨性别者的意义 {#implications-for-transfeminine-people}
|
||||
|
||||
Premoli 等人 (2005) 的发现很重要,因为他们提供的宝贵信息为在女性化激素治疗中提升雌二醇效力的一种新方法作了有力支持。如女性倾向跨性别者尚未接受[阴道成形术][wiki53],可考虑将雌二醇透皮贴片用于阴囊;对于术后人群,则可用于[新阴唇][wiki54]。如果通过常规皮肤部位仅可达到很低的雌二醇水平,那么这种方式应有助于提升雌二醇水平,从而降低贴片用量和成本;或者,用于高剂量雌二醇单药治疗等,以更高的雌二醇水平,起到抑制睾酮的作用。\
|
||||
而且,如将雌二醇水平的稳定性(或许还有使用的便利性)纳入考虑,则这种方式应比[舌下含服][wiki51]和[直肠给药][wiki55]等其它方案更具优势。
|
||||
|
||||
除贴片之外,凝胶等其它雌二醇透皮制剂用于阴囊时也可大幅提升雌二醇水平。还需要指出,雌二醇凝胶应该无需大面积涂抹;因为根据一项研究的发现,雌二醇凝胶的涂抹面积越小,雌二醇水平就越高<sup>([Järvinen et al., 1997][j97]; [图表][graph3])</sup>。不过,雌二醇凝胶用于阴囊或新阴唇是否更高效尚有待测试和证实;无论如何,如果属实,其将具有相较于贴片的一项显著优势——其仅需每日涂抹一次,而无需时刻往身上贴贴片。\
|
||||
需要指出,有的 100 μg/天雌二醇贴片尺寸很大<sup>([表格][table1])</sup>。阴囊睾酮贴片曾因尺寸过大、刺激性过强而被停用,因此雌二醇贴片的情况便显而易见了。不过,低剂量雌二醇贴片(如 50 或 75 μg/天)的尺寸更小<sup>([表格][table1])</sup>,其用于阴囊时,不仅仍有可能引起高雌二醇水平,而且在实用性与耐受性上应优于高剂量贴片。
|
||||
|
||||
此外,还有个想法很有意思,即[透皮孕酮][wiki56]也有潜在的医疗用途。使用孕酮透皮乳膏之后,可以观察到非常低但仍然显著的血清孕酮水平(~ 0.75 ng/mL)<sup>([维基百科][wiki3-ta])</sup>。目前尚无任何透皮孕酮制剂被批准用于医学用途,因为其引起的孕酮水平很低,其临床效果也不明确。\
|
||||
与雌二醇和睾酮类似,如将透皮孕酮用于阴囊,其可能也会更高效。不过,即使如此,其引起的血清孕酮水平仍将会过低;因此,虽然尚不清楚这是否会让透皮孕酮具备实质疗效,但这也许不大可能。\
|
||||
还有一个问题是:外生殖器皮肤富含 [5α-还原酶][wiki57]——即孕酮的主要[代谢酶][wiki58]。\
|
||||
无论如何,透皮孕酮用于阴囊的途径仍然非常值得探索。
|
||||
|
||||
总而言之,Premoli 等人 (2005) 的研究表明,透皮雌二醇用于阴囊时引起的雌二醇水平,远高于其它皮肤部位。睾酮在这方面已被证实,但对于雌二醇并无任何公开发表的数据佐证——直至此研究发表。
|
||||
|
||||
## 关于经外生殖器给予雌二醇的附加讨论 {#additional-topics-on-genital-application-of-estradiol}
|
||||
|
||||
### 贴片的大小和选择 {#patch-sizes-and-selection}
|
||||
|
||||
透皮雌二醇贴片的品牌众多(例如 Climara、Vivelle、Vivelle-Dot 等),其尺寸、剂量(14 - 100 μg/天)和作用时间(每周一用或两用)也各有不同<sup>([表格][table1])</sup>。\
|
||||
其中,尺寸范围从小于十美分硬币(1.65 cm<sup>2</sup>)到几乎接近于通常的咖啡杯底座(44 cm<sup>2</sup>)不等。差距竟有 25 倍之多!尺寸依剂量也有不同:50 μg/天的贴片有 3.3 - 22 cm<sup>2</sup>不等的尺寸,而 100 μg/天的贴剂尺寸为 6.6 - 44 cm<sup>2</sup> 不等。在阴囊上使用非常大的透皮雌二醇贴片显然很困难,而且不舒适。\
|
||||
前文所载表格链接,可帮助确定适合个人情况的最佳品牌和剂量。当然,贴片本身也可切分。
|
||||
|
||||
### 贴片的切分和粘贴 {#cutting-and-adhesing-patches}
|
||||
|
||||
一部分(但并非所有)的雌二醇透皮贴片可以切成更小的尺寸。有的雌二醇贴片非常大,因此如用于外生殖器,切分贴片可能会很有用。详情见以下文献摘录<sup>([Matthews et al., 2017][m17]; [Klein et al., 2018][k18]; [Norjavaara, Ankarberg-Lindgren, & Kriström, 2016][nak16]; [Rosenfield, Kiess, & Keizer-Schramad, 2006][rkk06])</sup>:
|
||||
|
||||
> 矩阵状的贴片可自粘,每 24 小时释放约 25 µg 的 17β-雌二醇。由于雌二醇均匀分布于整个贴片,故可切分贴片以提供所需的剂量。在实际使用时,贴片大多被切成两份或四份——其它更复杂的切割方式可能不够精确,且不切实际。未使用的部分贴片可放回原包装,并置于冰箱内至多一周。贴剂(或贴剂切片)应放置于清洁干燥的臀部皮肤,如有必要,应使用 Opsite®(透明粘合膜)以确保良好的附着力。[…]\
|
||||
> 贴片切分后可能更难使用,因为它们可能会脱落,从而需要胶带支撑。
|
||||
|
||||
> 目前,市售雌二醇贴片当中最低剂量规格为 14 μg/天,而使用最多的低剂量贴片规格为 25 μg/天。有一种方法可减少贴片剂量,就是将其切为小片。矩阵状的贴片易于切分,但具有储层技术的贴片不应切分。切分贴片的缺点是:切片尺寸较小,可能很难使用,而且亦不为产品说明书所推荐。\
|
||||
> 不过,迄今已有切分贴片的临床案例,尤其是在斯堪的纳维亚——有一个小组在夜间使用贴剂切片(25 微克贴剂四等分后,约等于 6.2 微克甚至更少)来模拟正常的清晨血浆雌二醇峰值;然后撕去贴片,几小时内即回落到基线。
|
||||
|
||||
> 可使用凝胶和贴片进行透皮给药;滴定雌二醇血浆水平显示,贴片切分后给药更为可靠,并且如要模仿自发性青春期早期的生理节律,只需在早晨将贴剂取下即可停止给药。 […]\
|
||||
> 我们目前的建议是,尽可能使用矩阵状的雌二醇贴片。这种贴剂不仅稳定,而且雌二醇分布均匀,可按个人需求切分。然而,即使剂量相同,不同品牌的矩阵状贴剂的尺寸也各有别。贴片面积越大,按目标剂量切分越容易。
|
||||
>
|
||||
> 相比之下,储层式的贴剂则具有单独的药物层,这一层是包含药物溶液或悬浮液的隔室,由粘合层隔开。切开后,隔室将被破坏并导致药液泄漏。
|
||||
|
||||
> 目前尚不清楚如何将雌二醇剂量控制在低于 14 μg/天。欧洲生产的矩阵状贴片可轻松切为四片以便夜间提供雌激素;但美国的制造商建议不要这样做——以我们有限的经验来看,其会导致血浆雌二醇水平不稳定,这表明这些贴片内的雌二醇并未均匀浸透。
|
||||
|
||||
目前几乎所有市售雌二醇贴片,皆为矩阵状。唯一的例外是 Estraderm——一种储层状贴片;其已停止在美国上市,但在英国尚可一用。
|
||||
|
||||
Tegaderm 是一种透明薄膜敷料,可帮助固定贴片<sup>([Reddit 帖子][reddit1])</sup>。
|
||||
|
||||
### 阴茎给药的情况 {#penile-skin-application}
|
||||
|
||||
阴茎皮肤的吸收特性似乎与阴囊皮肤相似,也可提高透皮给药的吸收率。因此,它可以作为阴囊给予透皮雌二醇的补充或替代方式。有关阴茎给药的详情,见以下文献摘录<sup>([Hairston, Becher, & McVary, 2006][hbm06])</sup>:
|
||||
|
||||
> […] 必须考虑到局部阴茎治疗所特有的解剖学和生理学问题。在阴茎皮肤和海绵体之间,有几个解剖/筋膜层;其中,白膜有厚厚的胶原层,故被认为难以穿透。因此,局部治疗试验主要以龟头给药,因为其与海绵体有直接的静脉连通。\
|
||||
> 阴茎皮肤本身具有角质层,故相对不透水。角质层的角质细胞与非常紧密的细胞间矩阵状脂质双层结合,这使得药物渗透很有难度。为克服这一障碍,研究者使用渗透促进剂渗透该层并到达皮下。可喜的是,在所有试验过的解剖部位当中,阴茎和阴囊最为独特:其角质层的可渗透性最强。有的测试药物用于这些局部区域时的吸收率几乎可达 100%(依其分子结构而定);龟头的角质层则更易于药物“突破”。而其它皮肤部位(例如背部和手掌)尤其不透水。\
|
||||
> 另一个可能扰乱药物输送效果的因素是:真皮深层丰富的毛细血管,可能会将药物“偷到”体循环中。
|
||||
|
||||
因此,如需要通过更大的皮肤面积使用雌二醇凝胶或贴片,则阴茎皮肤可能是一个很好的选择。需要指出,大多数已接受阴道成形术(阴茎翻转法)的女性倾向跨性别者的阴道给药情况应也与此有关,因为其新阴道的内壁是阴茎皮瓣再造的。然而,尚未有研究表明经新阴道给药的有效性。
|
||||
|
||||
### 雌二醇凝胶和乳膏用于外生殖器的情况 {#genital-application-of-estradiol-gel-and-cream}
|
||||
|
||||
迄今已有两项关于男性经阴囊使用睾酮凝胶和乳膏的临床研究发表:
|
||||
|
||||
- Iyer, R., Mok, S. F., Savkovic, S., Turner, L., Fraser, G., Desai, R., Jayadev, V., Conway, A. J., & Handelsman, D. J. (2017). Pharmacokinetics of testosterone cream applied to scrotal skin. [睾酮乳剂用于阴囊皮肤时的药代动力学] _Andrology, 5_(4), 725–731. [DOI:[10.1111/andr.12357][i17]]
|
||||
- Kuhnert, B., Byrne, M., Simoni, M., Kopcke, W., Gerss, J., Lemmnitz, G., & Nieschlag, E. (2005). Testosterone substitution with a new transdermal, hydroalcoholic gel applied to scrotal or non-scrotal skin: a multicentre trial. [多中心试验:一种新的透皮水醇凝胶作为睾酮替代品用于阴囊、非阴囊皮肤] _European Journal of Endocrinology, 153_(2), 317–326. [DOI:[10.1530/eje.1.01964][k05]]
|
||||
|
||||
第一篇论文的相关摘录如下(其中也简要描述了第二篇论文的发现):
|
||||
|
||||
> 阴囊皮肤薄、且甾体渗透性高,但关于睾酮用于阴囊皮肤途径的药代动力学尚未得到细致研究。本研究旨在阐明睾酮(乳膏)用于阴囊皮肤时的药代动力学。本研究是一项单中心、三阶段、交叉对照的药代动力学研究;具体为对性腺完好(eugonadal)的健康志愿者先施用癸酸诺龙抑制内源性睾酮,再以随机顺序提供三种不同剂量(12.5、25、50 mg)的睾酮乳膏,每次用药至少间隔 2 天。
|
||||
>
|
||||
> 睾酮用于阴囊皮肤时,其生物利用度显著高于腹部皮肤。本研究使用同种睾酮乳膏,并以液相色谱-质谱联用法(LC-MS)对甾体激素进行测定;发现经阴囊给药时只需最低剂量(12.5 mg)即可提供高达 4.6 ng/mL(16.0 nmol/L)的血药峰值浓度,而经腹部皮肤给药时需要 100mg 的睾酮乳膏方可使血药峰值浓度达到 4.7 ng/mL(16.3 nmol/L)。这表明睾酮用于阴囊时的生物利用度,比用于腹部皮肤高出约 8 倍。
|
||||
>
|
||||
> 一项早前的研究显示,用于阴囊时,睾酮凝胶的药代动力学与睾酮贴片相似;也与用于非阴囊部位、5 倍剂量的睾酮凝胶相似——这与透皮睾酮在阴囊的生物利用度高 5 倍相一致<sup>(Kuhnert et al., 2005)</sup>。\
|
||||
> 其它一些评估了非阴囊给药的透皮睾酮的药代动力学的研究,则观测到峰值浓度时间 (T<sub>max</sub>)为 6-16 小时不等<sup>(Marbury et al., 2003; Miller et al., 2011; Olsson et al., 2014)</sup>,但峰值浓度(C<sub>max</sub>)与经阴囊给药时相似<sup>(Rolf et al., 2002; Bouloux, 2005; Olsson et al., 2014)</sup>。
|
||||
>
|
||||
> 我们总结认为,相比于非阴囊部位,将睾酮乳膏用于阴囊可提高其生物利用度,提高血清睾酮浓度峰值(依剂量而定),而且剂量的大幅减少也提高了其耐受性。
|
||||
|
||||
从上述发现可知,睾酮凝胶或乳膏用于阴囊时的睾酮浓度峰值,相当于非阴囊部位的约 5 - 8 倍。此幅度与睾酮贴片用于阴囊后的水平比非阴囊部位高 5 倍的认识相吻合。
|
||||
|
||||
雌二醇在化学结构和性质(例如亲脂性,可能也包括吸收特性)等方面与睾酮非常相似。因此,尽管目前尚无关于经阴囊/新阴唇使用雌二醇凝胶或乳膏、或者清楚表明其引起的雌二醇水平要高于常规透皮部位的研究;但是,我们可以从睾酮的现象来推断,雌二醇也会有类似性质——在当阴囊给药的透皮雌二醇贴片,被确认可引起远高于非阴囊部位的雌二醇水平之后,我们愈发确信这点。
|
||||
|
||||
因此,与雌二醇贴片类似,经阴囊/新阴唇使用雌二醇凝胶很可能成为一种可提供高雌二醇水平的强力选项。使用雌二醇透皮制剂时,与常规皮肤部位相比,如改为经阴囊/新阴唇给药,则应有更高的效力和明显更低的成本。\
|
||||
此外,凝胶和乳膏每日只需给药一次,干燥得也非常迅速;如果换作贴片,其必须一直贴在身上,此时贴在阴囊/新阴唇就不及贴在常规部位来得舒适和便利了。而且,贴片需要先对阴囊/新阴唇进行脱毛方可使用,还会留下难以去除的粘合剂残留物、并引起局部皮肤反应;而凝胶和软膏则不会有这种问题。
|
||||
综上,雌二醇凝胶或软膏应是更适合用于阴囊/新阴唇的透皮制剂。
|
||||
|
||||
阴囊/新阴唇给药时可能需要注意:透皮雌二醇凝胶由水醇凝胶制成(内含酒精),因而涂抹于外生殖器时,可能会刺激皮肤、引起刺痛或灼伤。为此,可以改用仅含少量或不含酒精的透皮药物——例如乳膏(如复合非处方产品)和乳液(如 Estrasorb),而非水醇凝胶。此外,透皮雌二醇喷雾剂(品牌 Evamist)亦可作为替代方案。
|
||||
|
||||
总之,经阴囊给药的透皮睾酮凝胶或乳膏,相比于常规部位不仅吸收更好,而且睾酮水平高出约 5 - 8 倍。考虑到雌二醇的结构与睾酮相似,且阴囊给药的雌二醇贴片已被证明比常规部位明显吸收得更好,可以认为,透皮雌二醇凝胶和乳膏也有类似的效果。
|
||||
|
||||
### 雌二醇用于外生殖器的安全性 {#safety-of-genital-application-of-estradiol}
|
||||
|
||||
已有人表达了对雌二醇用于外生殖器之安全性的关注。例如,有人询问,雌二醇用于阴囊时是否会因其引起的局部雌二醇水平较高,而提高[睾丸癌][wiki59]或[前列腺癌][wiki15]的风险。\
|
||||
现有的对正接受标准激素治疗的女性倾向跨性别者进行的大型观察性研究,并未发现睾丸癌<sup>([Bensley et al., 2021][b21]; [de Nie et al., 2021][n21])</sup>或前列腺癌<sup>([de Nie et al., 2020][n20])</sup>的风险升高。事实上,这些女性倾向跨性别者的前列腺癌风险反而大幅降低了<sup>(de Nie et al., 2020)</sup>。\
|
||||
此外,对于顺性别男性,雄激素匮乏可降低前列腺癌的风险或发展;而高剂量雌激素疗法在很长时间内都用于治疗前列腺癌,且卓有成效<sup>([Ockrim, Lalani, & Abel, 2006][ola06]; [Norman et al., 2008][n08]; [Langley et al., 2021][l21])</sup>。\
|
||||
因此,对于睾丸或前列腺内的局部超高雌二醇浓度是否会提高患癌风险这个问题,尽管我们尚无相关数据可供回答,但现有的间接临床证据并不予以支持,故大可放心。
|
||||
|
||||
## 参考文献 {#references}
|
||||
|
||||
- Atkinson, L. E., Chang, Y. L., & Snyder, P. J. (1998). Long-term experience with testosterone replacement through scrotal skin. In Nieschlag, E., & Behre, H. M. (Eds.). _Testosterone: Action · Deficiency · Substitution, 2nd Edition_ (pp. 365–388). Berlin/Heidelberg: Springer. \[DOI:[10.1007/978-3-642-72185-4\_13](https://link.springer.com/chapter/10.1007/978-3-642-72185-4_13)\]
|
||||
- Behre, H. M., & Nieschlag, E. (2012). Testosterone preparations for clinical use in males. In Nieschlag, E., Behre, H. M., & Nieschlag, S. (Eds.). _Testosterone: Action · Deficiency · Substitution, 4th Edition_ (pp. 309–335). Cambridge/New York: Cambridge University Press. \[DOI:<https://doi.org/10.1017/CBO9781139003353.016>\]
|
||||
- Bensley, J. G., Cheung, A. S., Grossmann, M., & Papa, N. (2021). Testicular Cancer in Trans People Using Feminising Hormone Therapy– A Brief Review. _Urology_, advance online publication. \[DOI:<https://doi.org/10.1016/j.urology.2021.11.014>\]
|
||||
- de Nie, I., de Blok, C., van der Sluis, T. M., Barbé, E., Pigot, G., Wiepjes, C. M., Nota, N. M., van Mello, N. M., Valkenburg, N. E., Huirne, J., Gooren, L., van Moorselaar, R., Dreijerink, K., & den Heijer, M. (2020). Prostate Cancer Incidence under Androgen Deprivation: Nationwide Cohort Study in Trans Women Receiving Hormone Treatment. _The Journal of Clinical Endocrinology and Metabolism_, _105_(9), e3293–e3299. \[DOI:<https://doi.org/10.1210/clinem/dgaa412>\]
|
||||
- de Nie, I., Wiepjes, C. M., de Blok, C., van Moorselaar, R., Pigot, G., van der Sluis, T. M., Barbé, E., van der Voorn, P., van Mello, N. M., Huirne, J., & den Heijer, M. (2021). Incidence of testicular cancer in trans women using gender‐affirming hormonal treatment: a nationwide cohort study. _BJU International_, advance online publication. \[DOI:<https://doi.org/10.1111/bju.15575>\]
|
||||
- Feldmann, R. J., & Maibach, H. I. (1967). Regional variation in percutaneous penetration of 14C cortisol in man. _The Journal of Investigative Dermatology_, _48_(2), 181–183. \[DOI:<https://doi.org/10.1038/jid.1967.29>\]
|
||||
- Hairston, J. C., Becher, E., & McVary, K. T. (2006). Topical and Intra-Urethral Therapy. In Mulcahy, J. J. (Ed.). _Male Sexual Function: A Guide to Clinical Management, 2nd Edition_ (_Current Clinical Urology_) (pp. 303–321). Totowa: Humana Press. \[DOI:<https://doi.org/10.1007/978-1-59745-155-0_14>\] \[[Google 阅读](https://books.google.com/books?id=3ogNo5qAVJ8C&pg=PA309)\]
|
||||
- Iyer, R., Mok, S. F., Savkovic, S., Turner, L., Fraser, G., Desai, R., Jayadev, V., Conway, A. J., & Handelsman, D. J. (2017). Pharmacokinetics of testosterone cream applied to scrotal skin. _Andrology_, _5_(4), 725–731. \[DOI:<https://doi.org/10.1111/andr.12357>\]
|
||||
- Järvinen, A., Granander, M., Nykänen, S., Laine, T., Geurts, P., & Viitanen, A. (1997). Steady-state pharmacokinetics of oestradiol gel in post-menopausal women: effects of application area and washing. _British Journal of Obstetrics and Gynaecology_, _104_(Suppl 16), 14–18. \[DOI:<https://doi.org/10.1111/j.1471-0528.1997.tb11562.x>\]
|
||||
- Khera, M. (2013). Treatment Options for Testosterone Replacement Therapy. In Hellstrom, W. J. G. (Ed.). _Androgen Deficiency and Testosterone Replacement: Current Controversies and Strategies_ (pp. 129–139). Totowa: Humana Press. \[DOI:<https://doi.org/10.1007/978-1-62703-179-0_10>\]
|
||||
- Klein, K. O., Rosenfield, R. L., Santen, R. J., Gawlik, A. M., Backeljauw, P. F., Gravholt, C. H., Sas, T., & Mauras, N. (2018). Estrogen replacement in Turner syndrome: literature review and practical considerations. _The Journal of Clinical Endocrinology & Metabolism_, _103_(5), 1790–1803. \[DOI:<https://doi.org/10.1210/jc.2017-02183>\]
|
||||
- Kuhnert, B., Byrne, M., Simoni, M., Kopcke, W., Gerss, J., Lemmnitz, G., & Nieschlag, E. (2005). Testosterone substitution with a new transdermal, hydroalcoholic gel applied to scrotal or non-scrotal skin: a multicentre trial. _European Journal of Endocrinology_, _153_(2), 317–326. \[DOI:<https://doi.org/10.1530/eje.1.01964>\]
|
||||
- Langley, R. E., Godsland, I. F., Kynaston, H., Clarke, N. W., Rosen, S. D., Morgan, R. C., Pollock, P., Kockelbergh, R., Lalani, e., Dearnaley, D., Parmar, M., & Abel, P. D. (2008). Early hormonal data from a multicentre phase II trial using transdermal oestrogen patches as first‐line hormonal therapy in patients with locally advanced or metastatic prostate cancer. _BJU International_, _102_(4), 442–445. \[DOI:<https://doi.org/10.1111/j.1464-410X.2008.07583.x>\]
|
||||
- Langley, R. E., Gilbert, D. C., Duong, T., Clarke, N. W., Nankivell, M., Rosen, S. D., Mangar, S., Macnair, A., Sundaram, S. K., Laniado, M. E., Dixit, S., Madaan, S., Manetta, C., Pope, A., Scrase, C. D., Mckay, S., Muazzam, I. A., Collins, G. N., Worlding, J., Williams, S. T., … & Parmar, M. (2021). Transdermal oestradiol for androgen suppression in prostate cancer: long-term cardiovascular outcomes from the randomised Prostate Adenocarcinoma Transcutaneous Hormone (PATCH) trial programme. _The Lancet_, _397_(10274), 581–591. \[DOI:<https://doi.org/10.1016/S0140-6736(21)00100-8>\]
|
||||
- Matthews, D., Bath, L., Högler, W., Mason, A., Smyth, A., & Skae, M. (2017). Hormone supplementation for pubertal induction in girls. _Archives of Disease in Childhood_, _102_(10), 975–980. \[DOI:[10.1136/archdischild-2016-311372](http://dx.doi.org/10.1136/archdischild-2016-311372)\]
|
||||
- Mazer, N. A., Heiber, W. E., Moellmer, J. F., Meikle, A. W., Stringham, J. D., Sanders, S. W., Tolman, K. G., & Odell, W. D. (1992). Enhanced transdermal delivery of testosterone: a new physiological approach for androgen replacement in hypogonadal men. _Journal of Controlled Release_, _19_(1–3), 347–361. \[DOI:<https://doi.org/10.1016/0168-3659(92)90089-A>\]
|
||||
- Norjavaara, E., Ankarberg-Lindgren, C., & Kriström, B. (2016). Sex steroid replacement therapy in female hypogonadism from childhood to young adulthood. In Bourguignon J.-P., Parent A.-S. (Eds.). _Puberty from Bench to Clinic. Lessons for Clinical Management of Pubertal Disorders_ (_Endocrine Development, Volume_ _29_) (pp. 198–213). Basel: Karger. \[DOI:<https://doi.org/10.1159/000438892>\]
|
||||
- Norman, G., Dean, M. E., Langley, R. E., Hodges, Z. C., Ritchie, G., Parmar, M. K., Sydes, M. R., Abel, P., & Eastwood, A. J. (2008). Parenteral oestrogen in the treatment of prostate cancer: a systematic review. _British Journal of Cancer_, _98_(4), 697–707. \[DOI:<https://doi.org/10.1038/sj.bjc.6604230>\]
|
||||
- Ockrim, J., Lalani, E. N., & Abel, P. (2006). Therapy insight: parenteral estrogen treatment for prostate cancer—a new dawn for an old therapy. _Nature clinical practice Oncology_, _3_(10), 552–563. \[DOI:<https://doi.org/10.1038/ncponc0602>\]
|
||||
- Place, V. A., Atkinson, L., Prather, D. A., Trunnell, N., & Yates, F. E. (1990). Transdermal testosterone replacement through genital skin. In Nieschlag, E., & Behre, H. M. (Eds.). _Testosterone: Action · Deficiency · Substitution, 1st Edition_ (pp. 165–181). Berlin/Heidelberg: Springer. \[DOI:<https://doi.org/10.1007/978-3-662-00814-0_9>\]
|
||||
- Premoli, F., Re, I., Asenjo, G., Maximino, G., & Micheletti, L. (2005). Tratamiento del Cáncer de Próstata Avanzado con Estrógenos Transdérmicos Escrotales (ETE). \[Transdermal Scrotal Estrogen Patches (TSEP) in the Treatment of Advanced Prostate Cancer.\] _Revista Argentina de Urología_, _70_(4), 231–241. \[[Google 学术](https://scholar.google.com/scholar?cluster=3203160436559309066)\] \[[URL](https://web.archive.org/web/20201112031803/https://www.sau-net.org/publicaciones/abstracts_70_4.html)\] \[[PDF](https://revistasau.org/index.php/revista/article/viewFile/3224/3168)\] \[[英译文](https://docs.google.com/document/d/1dteNhG9wewvNX5zj0YcXrVAuQFZdtcqWmUWVvgI5uKs/view)\]
|
||||
- Rosenfield, R. L., Kiess, W., & de Muinck Keizer-Schrama, S. (2006). Physiologic induction of puberty in Turner syndrome with very low-dose estradiol. _International Congress Series_, _1298_, 71–79. \[DOI:<https://doi.org/10.1016/j.ics.2006.07.003>\]
|
||||
|
||||
--------
|
||||
|
||||
## 译文修订记录
|
||||
|
||||
- 2021 年 10 月 23 日——首次翻译。
|
||||
- 2022 年 11 月 14 日——第一次修订,梳理全文叙述,增补“用药安全性”一节,整理外链。
|
||||
|
||||
<!-- 图表外链 -->
|
||||
|
||||
[graph1]: https://en.wikipedia.org/wiki/Template:Hormone_levels_with_transdermal_estradiol_patches
|
||||
[graph2]: https://commons.wikimedia.org/wiki/File:Estradiol_and_testosterone_levels_with_high-dose_estradiol_patches_in_men.png
|
||||
[graph3]: https://commons.wikimedia.org/wiki/File:Estradiol_levels_with_1_mg_per_day_transdermal_estradiol_gel_applied_to_different_amounts_of_area_in_postmenopausal_women.png
|
||||
|
||||
<!-- Reddit 外链 -->
|
||||
|
||||
[reddit1]: https://reddit.com/r/TransDIY/comments/b7a0m6
|
||||
|
||||
<!-- 表格外链 -->
|
||||
|
||||
[table1]: https://en.wikipedia.org/wiki/Template:Transdermal_estradiol_patches_marketed_in_the_United_States
|
||||
|
||||
<!-- 维基百科条目 -->
|
||||
|
||||
[wiki1]: https://en.wikipedia.org/wiki/Pharmaceutical_form
|
||||
[wiki2]: https://en.wikipedia.org/wiki/Route_of_administration
|
||||
[wiki3]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol
|
||||
[wiki3-tp]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Transdermal_patches
|
||||
[wiki3-tg]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Transdermal_gel
|
||||
[wiki3-otf]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Other_transdermal_formulations
|
||||
[wiki3-vip]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Variability_in_pharmacokinetics
|
||||
[wiki3-ta]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Transdermal_administration
|
||||
[wiki3-sa]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Sublingual_administration
|
||||
[wiki4]: https://en.wikipedia.org/wiki/Transdermal_administration
|
||||
[wiki5]: https://en.wikipedia.org/wiki/Interindividual_variability
|
||||
[wiki6]: https://en.wikipedia.org/wiki/Hydrocortisone
|
||||
[wiki6a]: https://en.wikipedia.org/wiki/Cortisol
|
||||
[wiki7]: https://en.wikipedia.org/wiki/Absorption_(pharmacology)
|
||||
[wiki8]: https://en.wikipedia.org/wiki/Steroid_hormone
|
||||
[wiki9]: https://en.wikipedia.org/wiki/Estradiol_(medication)
|
||||
[wiki10]: https://en.wikipedia.org/wiki/Testosterone_(medication)
|
||||
[wiki11]: https://en.wikipedia.org/wiki/Sex_hormone
|
||||
[wiki12]: https://en.wikipedia.org/wiki/Radioactive_tracer
|
||||
[wiki13]: https://en.wikipedia.org/wiki/Scrotum
|
||||
[wiki14]: https://en.wikipedia.org/wiki/Bioavailability
|
||||
[wiki15]: https://en.wikipedia.org/wiki/Prostate_cancer
|
||||
[wiki16]: https://en.wikipedia.org/wiki/High-dose_estrogen
|
||||
[wiki17]: https://en.wikipedia.org/wiki/Transdermal_estradiol_patch
|
||||
[wiki18]: https://en.wikipedia.org/wiki/Transdermal_estradiol
|
||||
[wiki19]: https://en.wikipedia.org/wiki/Estrogen_(medication)
|
||||
[wiki20]: https://en.wikipedia.org/wiki/Antiandrogen
|
||||
[wiki21]: https://en.wikipedia.org/wiki/Androgen_deprivation_therapy
|
||||
[wiki22]: https://en.wikipedia.org/wiki/Antigonadotropin
|
||||
[wiki23]: https://en.wikipedia.org/wiki/Testosterone
|
||||
[wiki24]: https://en.wikipedia.org/wiki/Sex%20hormone-binding%20globulin
|
||||
[wiki25]: https://en.wikipedia.org/wiki/Androgen
|
||||
[wiki26]: https://en.wikipedia.org/wiki/Gonadectomy
|
||||
[wiki27]: https://en.wikipedia.org/wiki/Gonadotropin-releasing_hormone
|
||||
[wiki28]: https://en.wikipedia.org/wiki/Gonadotropin-releasing_hormone_agonist
|
||||
[wiki29]: https://en.wikipedia.org/wiki/Gonadotropin-releasing_hormone_antagonist
|
||||
[wiki30]: https://en.wikipedia.org/wiki/Hot_flash
|
||||
[wiki31]: https://en.wikipedia.org/wiki/Bone_density
|
||||
[wiki32]: https://en.wikipedia.org/wiki/Sexual_desire
|
||||
[wiki33]: https://en.wikipedia.org/wiki/Quality_of_life
|
||||
[wiki34]: https://en.wikipedia.org/wiki/Feminization_(biology)
|
||||
[wiki35]: https://en.wikipedia.org/wiki/Gynecomastia
|
||||
[wiki36]: https://en.wikipedia.org/wiki/Cardiovascular_disease
|
||||
[wiki37]: https://en.wikipedia.org/wiki/Oral_administration
|
||||
[wiki38]: https://en.wikipedia.org/wiki/Diethylstilbestrol
|
||||
[wiki39]: https://en.wikipedia.org/wiki/Ethinylestradiol
|
||||
[wiki40]: https://en.wikipedia.org/wiki/Conjugated_estrogens
|
||||
[wiki41]: https://en.wikipedia.org/wiki/Parenteral_administration
|
||||
[wiki42]: https://en.wikipedia.org/wiki/Bioidentical
|
||||
[wiki43]: https://en.wikipedia.org/wiki/Injectable_estradiol_esters
|
||||
[wiki44]: https://en.wikipedia.org/wiki/Polyestradiol_phosphate
|
||||
[wiki45]: https://en.wikipedia.org/wiki/Estradiol_undecylate
|
||||
[wiki46]: https://en.wikipedia.org/wiki/Estradiol_valerate
|
||||
[wiki47]: https://en.wikipedia.org/wiki/Estradiol_cypionate
|
||||
[wiki48]: https://en.wikipedia.org/wiki/Transdermal_estradiol_gel
|
||||
[wiki49]: https://en.wikipedia.org/wiki/Transdermal_testosterone_patch
|
||||
[wiki50]: https://en.wikipedia.org/wiki/Oral_estradiol
|
||||
[wiki51]: https://en.wikipedia.org/wiki/Sublingual_estradiol
|
||||
[wiki52-ae]: https://en.wikipedia.org/wiki/Pharmacodynamics_of_estradiol#Antigonadotropic_effects
|
||||
[wiki53]: https://en.wikipedia.org/wiki/Vaginoplasty
|
||||
[wiki54]: https://en.wikipedia.org/wiki/Neolabia
|
||||
[wiki55]: https://en.wikipedia.org/wiki/Rectal_estradiol
|
||||
[wiki56]: https://en.wikipedia.org/wiki/Transdermal_progesterone
|
||||
[wiki57]: https://en.wikipedia.org/wiki/5%CE%B1-Reductase
|
||||
[wiki58]: https://en.wikipedia.org/wiki/Enzyme
|
||||
[wiki59]: https://en.wikipedia.org/wiki/Testicular_cancer
|
||||
|
||||
<!-- 参考文献外链 -->
|
||||
|
||||
[aw20-eed]: https://transfemscience.org/articles/e2-equivalent-doses/
|
||||
[fm67]: https://doi.org/10.1038/jid.1967.29
|
||||
[fm67-suppl]: https://doi.org/10.1038/jid.1967.29
|
||||
[p90]: https://doi.org/10.1007/978-3-662-00814-0_9
|
||||
[m92]: https://doi.org/10.1016/0168-3659(92)90089-A
|
||||
[acs98]: https://doi.org/10.1007/978-3-642-72185-4_13
|
||||
[p05]: https://scholar.google.com/scholar?cluster=3203160436559309066
|
||||
[p05-archive]: https://web.archive.org/web/20201112031803/https://www.sau-net.org/publicaciones/abstracts_70_4.html
|
||||
[p05-pdf]: https://revistasau.org/index.php/revista/article/viewFile/3224/3168
|
||||
[p05-eng]: https://docs.google.com/document/d/1dteNhG9wewvNX5zj0YcXrVAuQFZdtcqWmUWVvgI5uKs/view
|
||||
[aw20-ecbc]: https://transfemscience.org/articles/estrogens-coagulation-blood-clots/
|
||||
[ola06]: https://doi.org/10.1038/ncponc0602
|
||||
[l08]: https://doi.org/10.1111/j.1464-410X.2008.07583.x
|
||||
[aw19-hdte]: https://transfemscience.org/articles/high-dose-transdermal-e2/
|
||||
[bn12]: https://books.google.com/books?id=MkrAPaQ4wJkC&pg=PA324
|
||||
[k13]: https://doi.org/10.1007/978-1-62703-179-0_10
|
||||
[ss21-set]: https://transfemscience.org/articles/sublingual-e2-transfem/
|
||||
[aw18-intro-gs]: https://transfemscience.org/articles/transfem-intro/#gonadal-suppression
|
||||
[j97]: https://doi.org/10.1111/j.1471-0528.1997.tb11562.x
|
||||
[m17]: https://doi.org/10.1136/archdischild-2016-311372
|
||||
[k18]: https://doi.org/10.1210/jc.2017-02183
|
||||
[nak16]: https://doi.org/10.1159/000438892
|
||||
[rkk06]: https://doi.org/10.1016/j.ics.2006.07.003
|
||||
[hbm06]: https://doi.org/10.1007/978-1-59745-155-0_14
|
||||
[i17]: https://doi.org/10.1111/andr.12357
|
||||
[k05]: https://doi.org/10.1530/eje.1.01964
|
||||
[b21]: https://doi.org/10.1016/j.urology.2021.11.014
|
||||
[n21]: https://doi.org/10.1111/bju.15575
|
||||
[n20]: https://doi.org/10.1210/clinem/dgaa412
|
||||
[n08]: https://doi.org/10.1038/sj.bjc.6604230
|
||||
[l21]: https://doi.org/10.1016/S0140-6736(21)00100-8
|
||||
File diff suppressed because it is too large
Load Diff
|
|
@ -1,51 +1,59 @@
|
|||
# 对非二元女性倾向跨性别者的激素治疗可能性的探索
|
||||
---
|
||||
title: 对非二元女性倾向跨性别者的激素治疗可能性的探索
|
||||
linkTitle: 非二元激素治疗的探索
|
||||
description: 对非二元(女性倾向)激素治疗的需求正日益增多,但目前缺乏相关指引。本文对此作实验性讨论。
|
||||
author: Aly W.
|
||||
published: 2019-06-13
|
||||
updated: 2022-09-26
|
||||
translated: 2022-11-22
|
||||
translators:
|
||||
- yucandy
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 非二元性别
|
||||
- 治疗指南
|
||||
- SERM
|
||||
- 抗雄激素制剂
|
||||
notice: 原文 [最初以 Reddit 帖子的形式发布]({{< ref "announcement" >}}),在迁移至本站之后,其尚未得到适当或全面的修订。
|
||||
trackHash: 7378b09b623aaedc898e8e60a30a5035fb5d10d2
|
||||
---
|
||||
|
||||
> - 作者 [Aly W.][AUTHOR]
|
||||
> + 首次发表于 2019 年 6 月 13 日
|
||||
> + 最后修改于 2022 年 9 月 26 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [yucandy][TRANSLATOR] \| [Bersella AI][REVISOR]
|
||||
> + 翻译于 2022 年 11 月 22 日
|
||||
## 译者按 {#notice}
|
||||
|
||||
[ORIGIN]: https://transfemscience.org/articles/nonbinary-transfem-overview/
|
||||
[AUTHOR]: ../about.md#aly-w
|
||||
[TRANSLATOR]: ../about.md#yucandy
|
||||
[REVISOR]: ../about.md#bersella-ai
|
||||
|
||||
## 译者按
|
||||
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u> 另见“[前言](#前言)”最后一段。**
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u> 另见“[前言]({{< ref "#introduction" >}})”最后一段。**
|
||||
1. **本文讨论的是非二元(女性倾向)激素治疗**,与[常规女性化激素治疗][aw18-intro]有别。全文篇幅较长,需耐心阅读。
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
------
|
||||
---
|
||||
|
||||
**提醒:原文[最初以 Reddit 帖子的形式发布](announcement.md),在迁移至本站之后,其尚未得到适当或全面的修订。**
|
||||
## 摘要 {#abstract}
|
||||
|
||||
## 摘要
|
||||
非二元(女性倾向)跨性别者常盼望着有一种激素疗法,能够区别于常规女性化激素疗法、也有更少的女性化与去男性化效果。例如,非二元(女性倾向)跨性别者会在女性和男性的身体和激素状态之间寻求一种中间态;会期望有除乳房发育之外的实质、或完全的女性化及去男性化效果;会想要有性别中立的外表;会期望在女性化的同时保留更多的男性性欲与性能力。此类需求正日益增多,但相关疗法尚未得到跨性别医学的研究和确立。
|
||||
|
||||
> 非二元(女性倾向)跨性别者常盼望着有一种激素疗法,能够区别于常规女性化激素疗法、也有更少的女性化与去男性化效果。例如,非二元(女性倾向)跨性别者会在女性和男性的身体和激素状态之间寻求一种中间态;会期望有除乳房发育之外的实质、或完全的女性化及去男性化效果;会想要有性别中立的外表;会期望在女性化的同时保留更多的男性性欲与性能力。此类需求正日益增多,但相关疗法尚未得到跨性别医学的研究和确立。
|
||||
> 尽管如此,理论上仍有一批激素调节方案可达成上述目的。例如,去男性化效果可通过使用不同剂量的抗雄激素制剂、孕激素、促性腺激素释放激素调节剂等,达到部分、或完全的睾酮抑制效果来实现。如要产生女性化效果以及其它雌激素效力的同时,仅伴随微弱的、或不伴随乳房发育,则可通过使用选择性雌激素受体调节剂或低剂量雌二醇来实现。
|
||||
> 其它激素类药物也可产生特定的不同效力,例如:5α-还原酶抑制剂可以减缓体毛生长及脱发;局部用于乳房的雄激素可减缓乳房发育;癸酸诺龙(一种雄激素与蛋白同化激素)可作为睾酮的替代物,其对皮肤与毛囊的影响更小。
|
||||
> 如要阻止乳房发育,除激素手段之外,还可接受乳腺切除术。
|
||||
> 此类激素方案也会带来一定健康风险,尤其是与雌激素替代不充分的雄激素缺乏有关的;例如骨质流失——其可通过补充钙与维生素 D、摄入二磷酸盐、做承重运动等来缓解。
|
||||
> 目前此类激素疗法在跨性别健康领域中正日益引起关注;但愿它们将来能够得到更多描述、更好地用于跨性别者。
|
||||
尽管如此,理论上仍有一批激素调节方案可达成上述目的。例如,去男性化效果可通过使用不同剂量的抗雄激素制剂、孕激素、促性腺激素释放激素调节剂等,达到部分、或完全的睾酮抑制效果来实现。如要产生女性化效果以及其它雌激素效力的同时,仅伴随微弱的、或不伴随乳房发育,则可通过使用选择性雌激素受体调节剂或低剂量雌二醇来实现。
|
||||
|
||||
## 前言
|
||||
其它激素类药物也可产生特定的不同效力,例如:5α-还原酶抑制剂可以减缓体毛生长及脱发;局部用于乳房的雄激素可减缓乳房发育;癸酸诺龙(一种雄激素与蛋白同化激素)可作为睾酮的替代物,其对皮肤与毛囊的影响更小。
|
||||
|
||||
“[非二元][wiki1]”跨性别者,意即性别认同不属于[二元性别][wiki2]的人。尽管许多非二元([男性倾向][wiki3]和[女性倾向][wiki4])跨性别者既不认同自己是男性、也不认同是女性,但 ta 们仍希望像跨性别女性、男性一样接受激素治疗。
|
||||
如要阻止乳房发育,除激素手段之外,还可接受乳腺切除术。
|
||||
|
||||
此类激素方案也会带来一定健康风险,尤其是与雌激素替代不充分的雄激素缺乏有关的;例如骨质流失——其可通过补充钙与维生素 D、摄入二磷酸盐、做承重运动等来缓解。
|
||||
|
||||
目前此类激素疗法在跨性别健康领域中正日益引起关注;但愿它们将来能够得到更多描述、更好地用于跨性别者。
|
||||
|
||||
## 前言 {#introduction}
|
||||
|
||||
“[非二元][wiki1]”跨性别者,意即性别认同不属于[二元性别][wiki2]的人。尽管许多非二元([男性倾向][wiki3]和[女性倾向][wiki4])跨性别者既不认同自己是男性、也不认同是女性,但 ta 们仍希望像跨性别女性、男性一样接受激素治疗。
|
||||
有一部分非二元性别人群与大多数认同二元性别的跨性别者一样,接受了完整激素转变;而另一部分更倾向于达到部分的激素转变效果。其效果可能包括:在男性与女性特征之间达到一个[中间态][wiki5];使外观倾向于[性别中立][nih1];或是诱导一部分(但非完全)的[男性化][wiki6]或[女性化][wiki7]效果。
|
||||
|
||||
此外,还有一些不认同自己是跨性别的人,也在寻求通过激素达成女性化/[去男性化][wiki8]。此类自我认同为顺性别的人群常自称“[伪娘][wiki9]”,活跃于 Reddit 等社交平台(如 [r/FemboyTransition][r-femboy] 栏目)。这类有女性化倾向的顺性别者,对激素转变的追求上,常与非二元性别(女性倾向)人群颇为相似——最常见的是,会追求不伴随[乳房发育][wiki10]的女性化。有时,随着时间推移,这类接受激素转变的顺性别人群,会逐渐将自我认同转换为跨性别。
|
||||
此外,还有一些不认同自己是跨性别的人,也在寻求通过激素达成女性化/[去男性化][wiki8]。此类自我认同为顺性别的人群常自称“[伪娘][wiki9]”,活跃于 Reddit 等社交平台(如 <https://reddit.com/r/FemboyTransition> 栏目)。这类有女性化倾向的顺性别者,对激素转变的追求上,常与非二元性别(女性倾向)人群颇为相似——最常见的是,会追求不伴随[乳房发育][wiki10]的女性化。有时,随着时间推移,这类接受激素转变的顺性别人群,会逐渐将自我认同转换为跨性别。
|
||||
|
||||
部分激素转变的手段、甚至是非二元的性别认同,都是近年才逐渐普及的。迄今发表的文献鲜少对这种非常规的激素治疗手段加以描述。此外,目前尚无任何针对这类疗法的[标准或指南][wiki11]发布。不过,近年已有数篇评述开始讨论非二元激素治疗的可能性<sup>([Richards et al., 2016][r16]; [Seal, 2017][s17]; [Bass et al., 2018][b18]; [Cocchetti et al., 2020][c20])</sup>。
|
||||
部分激素转变的手段、甚至是非二元的性别认同,都是近年才逐渐普及的。迄今发表的文献鲜少对这种非常规的激素治疗手段加以描述。此外,目前尚无任何针对这类疗法的[标准或指南][wiki11]发布。不过,近年已有数篇评述开始讨论非二元激素治疗的可能性<sup>([Richards et al., 2016][r16]; [Seal, 2017][s17]; [Bass et al., 2018][b18]; [Cocchetti et al., 2020][c20])</sup>。
|
||||
目前临床上已建立的非常规激素转变手段,尚无法满足日益庞大的需求;因此,有必要从理论角度对各种治疗可能性进行探索——这也是本综述的撰文目的。
|
||||
|
||||
**免责声明:** 本文包含实验性与不成熟的观点。迄今尚无任何有关跨性别者(非二元性别人群)采取部分激素转变目标的研究开展过,也没有任何数据或证据可予以佐证;我们目前只能从对其他群体的理论和研究中来推断——对于非二元(女性倾向)激素治疗,会通过正接受前列腺癌激素治疗、[男性女乳症][wiki12]治疗的顺性别男性,以及正接受激素治疗的跨性别女性等人群来推论。
|
||||
**免责声明:** 本文包含实验性与不成熟的观点。迄今尚无任何有关跨性别者(非二元性别人群)采取部分激素转变目标的研究开展过,也没有任何数据或证据可予以佐证;我们目前只能从对其他群体的理论和研究中来推断——对于非二元(女性倾向)激素治疗,会通过正接受前列腺癌激素治疗、[男性女乳症][wiki12]治疗的顺性别男性,以及正接受激素治疗的跨性别女性等人群来推论。
|
||||
因此,本文仅为探索性讨论,读者不应将本文视为治疗建议。
|
||||
|
||||
|
||||
## 常规女性化激素治疗手段
|
||||
## 常规女性化激素治疗手段 {#conventional-transfeminine-hormone-therapy}
|
||||
|
||||
跨性别女性的常规激素治疗,旨在尽可能最大程度地产生去男性化与女性化效果——包括乳房发育。这需要抑制[睾酮][wiki13]水平并提高[雌二醇][wiki14]水平,使其处于成年女性的正常范围。此外,也可无需完全抑制睾酮,而改为阻断雄激素活性。服用[雌激素][wiki16]、[孕激素][wiki17]、[抗雄激素制剂][wiki18]等[激素类药物][wiki15]皆可引起上述激素变化;其中,雌激素可引起乳房发育等女性化效果,而对睾酮的抑制可引起去男性化、去除对女性化的抑制等效果。雌激素、孕激素和抗雄制剂皆可促进睾酮的抑制。
|
||||
|
||||
|
|
@ -54,7 +62,7 @@
|
|||
- [雌二醇][wiki20]和[雌二醇酯][wiki21],如 [戊酸雌二醇][wiki22];
|
||||
- 抗雄制剂,如[螺内酯][wiki23]、[比卡鲁胺][wiki24]以及[促性腺激素释放激素 (GnRH) 激动剂][wiki25]/[拮抗剂][wiki26];
|
||||
- 孕激素,如[孕酮][wiki27]和[醋酸环丙孕酮][wiki28] (CPA);
|
||||
- [雄激素合成抑制剂][wiki29],如 [5α-还原酶抑制剂][wiki30] (5α-RI)。
|
||||
- [雄激素合成抑制剂][wiki29],如 [5α-还原酶抑制剂][wiki30] (5α-RI)。
|
||||
5α-RI 可抑制某些组织(如皮肤与毛囊)内从睾酮到效力更大的[双氢睾酮][wiki31] (DHT) 的代谢过程,从而有限地发挥抗雄效力。
|
||||
|
||||
有一部分非二元(女性倾向)跨性别者的治疗目标与跨性别女性一致,其效果也与常规女性化激素疗法相当——也即,尽可能最大程度地引起乳房发育等女性化效果、和去男性化效果。如果是这样的话,采取常规女性化激素疗法便可,而无需寻求实验性更强的非常规部分转变手段。
|
||||
|
|
@ -63,12 +71,12 @@
|
|||
|
||||
- [女性倾向跨性别者的激素治疗简介 (中译)][aw18-intro] (Aly W., 2018)
|
||||
|
||||
该文章旨在提供跨性别用药所需要了解的一切内容,以便有一个初步理解。如果刚接触跨性别激素治疗这一话题,强烈建议先阅读该文章,再继续阅读本文。
|
||||
该文章旨在提供跨性别用药所需要了解的一切内容,以便有一个初步理解。如果刚接触跨性别激素治疗这一话题,强烈建议先阅读该文章,再继续阅读本文。
|
||||
该简介涵盖了性激素及其影响,以及为激素治疗所用的激素类药物之具体种类、途径和剂量等。这些信息大部分也适用于非常规的女性化激素治疗手段。
|
||||
|
||||
## 部分女性化的激素治疗手段
|
||||
## 部分女性化的激素治疗手段 {#partial-transfeminine-hormone-therapy}
|
||||
|
||||
有的非二元(女性倾向)跨性别者,以及自我认同为顺性别、但寻求激素女性化的人,只希望部分引起女性化/去男性化效果;此类情况可能比常规的激素治疗更复杂,并需要更多的考量——取决于治疗目的。
|
||||
有的非二元(女性倾向)跨性别者,以及自我认同为顺性别、但寻求激素女性化的人,只希望部分引起女性化/去男性化效果;此类情况可能比常规的激素治疗更复杂,并需要更多的考量——取决于治疗目的。
|
||||
这些部分女性化的激素治疗目的包括:
|
||||
|
||||
1. 在男性和女性的身体和激素状态之间寻求一种中间态;
|
||||
|
|
@ -76,13 +84,13 @@
|
|||
1. 实质性、或最大程度地引起女性化和去男性化,但伴随微弱以至不伴随乳房发育;
|
||||
1. 实质性、或最大程度地引起女性化和去男性化,但基本或完全保留性欲、性能力(如勃起和性高潮能力)、生育能力等。
|
||||
|
||||
其中,第一项很容易达成,其仅需在常规女性化激素治疗当中采取较低剂量;这样一来,既可部分抑制睾酮,也可让雄激素和雌激素同时作为主要性激素存在。
|
||||
第二项需同时去除雄激素和雌激素;尽管可行,但其可能产生一定负面影响,因为性激素在维持某些健康方面上很重要。不过有一些方法可以避免或减轻这种后果。
|
||||
其中,第一项很容易达成,其仅需在常规女性化激素治疗当中采取较低剂量;这样一来,既可部分抑制睾酮,也可让雄激素和雌激素同时作为主要性激素存在。
|
||||
第二项需同时去除雄激素和雌激素;尽管可行,但其可能产生一定负面影响,因为性激素在维持某些健康方面上很重要。不过有一些方法可以避免或减轻这种后果。
|
||||
第三项和第四项在技术上可行,但是更难实现,其需要专门的、可能还很复杂的激素治疗手段。
|
||||
|
||||
## 睾酮的抑制和阻断
|
||||
## 睾酮的抑制和阻断 {#suppression-and-blockade-of-testosterone}
|
||||
|
||||
如果非二元女性化激素治疗的目标仅仅是为了实现性别中立的外观,并且尽量减少或不出现女性化的迹象;那么可采取去除睾酮、但不服用雌激素的方式。
|
||||
如果非二元女性化激素治疗的目标仅仅是为了实现性别中立的外观,并且尽量减少或不出现女性化的迹象;那么可采取去除睾酮、但不服用雌激素的方式。
|
||||
对于出生指派性别为男的人群,有多种方法可以去除雄激素或抑制睾酮,包括:
|
||||
|
||||
- 大剂量孕激素治疗;
|
||||
|
|
@ -92,192 +100,190 @@
|
|||
|
||||
笔者将在本章讨论雄激素去除疗法——其中大多出于疗效的角度。不过,如仅仅去除雄激素,在同时缺乏雌激素的情况下,可能会产生耐受性和安全性等问题;下一章将予以讨论。
|
||||
|
||||
### 大剂量孕激素对雄激素的抑制作用
|
||||
### 大剂量孕激素对雄激素的抑制作用 {#testosterone-suppression-with-high-doses-of-progestogens}
|
||||
|
||||
大剂量的孕激素可起到雄激素去除的作用;其可抑制睾酮水平高达 50% 至 70% <sup>([Aly W., 2019][aw19-cpa])</sup>。此降幅很显著,但不足以落入女性范围。如需要阻断未被抑制的剩余睾酮的作用,还可加入雄激素受体拮抗剂。
|
||||
大剂量的孕激素可起到雄激素去除的作用;其可抑制睾酮水平高达 50% 至 70% <sup>([Aly W., 2019][aw19-cpa])</sup>。此降幅很显著,但不足以落入女性范围。如需要阻断未被抑制的剩余睾酮的作用,还可加入雄激素受体拮抗剂。
|
||||
出于这些目的,也许可以采用低剂量的醋酸环丙孕酮(如 5.0–12.5 mg/天)<sup>([Aly W., 2019][aw19-cpa])</sup>合并比卡鲁胺(如 12.5–50 mg/天)或螺内酯(如 200–400 mg/天)的治疗方案。而大剂量的其它孕激素亦可代替醋酸环丙孕酮使用;例如几乎任意一种合成孕酮制剂,或者直肠给药的孕酮<sup>([Aly W., 2018][aw18-opr])</sup>。
|
||||
|
||||
### 药物或手术去势对雄激素的抑制作用
|
||||
### 药物或手术去势对雄激素的抑制作用 {#testosterone-suppression-with-medical-or-surgical-castration}
|
||||
|
||||
GnRH 激动剂和拮抗剂是抑制睾酮的另一种选择。它们可将睾酮水平抑制约 95%,进入到正常女性范围或已去势的男性范围(<50 ng/dL)。然而,GnRH 激动剂和拮抗剂非常昂贵,尽管可能有一些廉价获取的途径(如某些网上药店)<sup>([Aly W., 2019][aw19-buse])</sup>。
|
||||
|
||||
除 GnRH 激动剂和拮抗剂之外,还有一种永久性手段:切除性腺。不过这需要动刀,而且手术过程开销很大(几千美元),门槛还更高。大多数外科医生在手术前都要求有性别治疗师的书面告知函和[实际生活经历][wiki32];但也有医生仅要求知情同意。该手术过程也不可逆,特别是会造成睾丸和生育能力的永久丧失。
|
||||
除 GnRH 激动剂和拮抗剂之外,还有一种永久性手段:切除性腺。不过这需要动刀,而且手术过程开销很大(几千美元),门槛还更高。大多数外科医生在手术前都要求有性别治疗师的书面告知函和[实际生活经历][wiki32];但也有医生仅要求知情同意。该手术过程也不可逆,特别是会造成睾丸和生育能力的永久丧失。
|
||||
无论如何,从长远来看,性腺切除术的开销要远低于 GnRH 激动剂和拮抗剂,便利性也更高。
|
||||
|
||||
### 抗雄制剂对雄激素的阻断作用
|
||||
### 抗雄制剂对雄激素的阻断作用 {#testosterone-blockade-with-antiandrogens}
|
||||
|
||||
雄激素受体拮抗剂(如比卡鲁胺和螺内酯)可直接与雄激素受体结合,将睾酮和 DHT 等雄激素从受体中置换出来,从而阻止这些雄激素对其的激活。这与通过抑制雄激素的产生和水平而发挥作用的疗法不同。
|
||||
|
||||
高剂量的比卡鲁胺单药治疗(如 150–300 mg/天)可用于雄激素去除治疗<sup>([Aly W., 2019][aw19-bica])</sup>。然而,这种疗法会使睾酮增多,从而使雌二醇水平上升。其中睾酮会被比卡鲁胺阻断,不会产生影响,但雌二醇会升至足以引起明显或完全女性化(包括乳房发育)的浓度区间。此外,如仅使用比卡鲁胺,即使超高剂量下也可能不足以完全阻断处于男性范围的睾酮<sup>([Aly W., 2019][aw19-bica])</sup>。
|
||||
高剂量的比卡鲁胺单药治疗(如 150–300 mg/天)可用于雄激素去除治疗<sup>([Aly W., 2019][aw19-bica])</sup>。然而,这种疗法会使睾酮增多,从而使雌二醇水平上升。其中睾酮会被比卡鲁胺阻断,不会产生影响,但雌二醇会升至足以引起明显或完全女性化(包括乳房发育)的浓度区间。此外,如仅使用比卡鲁胺,即使超高剂量下也可能不足以完全阻断处于男性范围的睾酮<sup>([Aly W., 2019][aw19-bica])</sup>。
|
||||
基于这些考量,比卡鲁胺至少在单药治疗时无法达成完全去男性化、且不伴随女性化(乳房发育)的目标。
|
||||
|
||||
高剂量比卡鲁胺开销很大,有人会因无力承担而排除之。而高剂量螺内酯单药治疗也并非稳妥之选,因为其抗雄效力较弱,可能远不能胜任阻断男性范围内的睾酮水平的任务(似乎需要至少 200 mg/天 才能完全阻断处于女性范围的睾酮水平)<sup>([Aly W., 2018][aw18-spiro]; [维基][wiki33])</sup>。
|
||||
高剂量比卡鲁胺开销很大,有人会因无力承担而排除之。而高剂量螺内酯单药治疗也并非稳妥之选,因为其抗雄效力较弱,可能远不能胜任阻断男性范围内的睾酮水平的任务(似乎需要至少 200 mg/天 才能完全阻断处于女性范围的睾酮水平)<sup>([Aly W., 2018][aw18-spiro]; [维基][wiki33])</sup>。
|
||||
如要同时部分抑制睾酮和雌激素水平,则比起单用拮抗剂,应更适合采用与一种孕激素(如醋酸环丙孕酮)合用的方案。
|
||||
|
||||
与明显或完全抑制睾酮水平相比,采取高剂量比卡鲁胺单药治疗有一些潜在主要优势,即其相当程度地保留了性欲和勃起功能,且应不会导致不孕。
|
||||
|
||||
### 抑制雄激素的其它选项
|
||||
### 抑制雄激素的其它选项 {#other-options-for-testosterone-suppression}
|
||||
|
||||
另一种选择是仅进行部分去男性化,这基本上可以通过使用较低剂量的上述药物(如醋酸环丙孕酮、比卡鲁胺)来实现。需要时还可以加入 5α-还原酶抑制剂,以更大幅度地减缓脱发和体毛生长。需要指出,在睾酮被充分抑制或阻断的情况下,使用 5α-还原酶抑制剂的好处可能会很少或完全没有。
|
||||
|
||||
还有另一种可能,就是加入低剂量的 [癸酸诺龙][wiki34];这是一种雄激素受体激动剂和雄性—蛋白同化激素 (AAS),对皮肤和毛囊的男性化/雄激素效力要小的多<sup>([Aly W., 2020][aw20-nand])</sup>,也可帮助抑制和替代睾酮水平。其也可能有帮助维持性欲和功能的好处。不过,癸酸诺龙最近已停止在美国上市。
|
||||
还有另一种可能,就是加入低剂量的 [癸酸诺龙][wiki34];这是一种雄激素受体激动剂和雄性—蛋白同化激素 (AAS),对皮肤和毛囊的男性化/雄激素效力要小的多<sup>([Aly W., 2020][aw20-nand])</sup>,也可帮助抑制和替代睾酮水平。其也可能有帮助维持性欲和功能的好处。不过,癸酸诺龙最近已停止在美国上市。
|
||||
另一种 AAS:[氧雄龙][wiki35]有类似疗效,但有一定肝脏毒性。
|
||||
|
||||
## 雌激素的去除和替代 {#estrogen-deficiency-and-replacement}
|
||||
|
||||
## 雌激素的去除和替代
|
||||
|
||||
尽管雄激素去除疗法可以有效引起预期变化——即不伴随女性化的去男性化效果;但并不推荐使用。
|
||||
这是因为雌二醇是由睾酮产生的,没有雄激素也就会缺乏雌激素。雌激素对维持男性和女性的[骨密度][wiki36]至关重要;没有雌激素,骨量将快速流失,最终会发展成[骨质疏松症][wiki37],骨折风险也变得很高;还可能会发生骨骼和姿态性损伤<sup>([图片1][fig1]; [图片2][fig2])</sup>。
|
||||
此外,患者还可能出现其它类似[更年期][wiki38]的症状,如[潮热][wiki39]、情绪和睡眠问题、性功能障碍(如性欲低下与勃起功能障碍),以及皮肤加速老化等<sup>([维基][wiki14-skin])</sup>。性激素缺乏也可能与体重增加、II 型糖尿病、冠心病和痴呆症的风险增加存在关联。
|
||||
尽管雄激素去除疗法可以有效引起预期变化——即不伴随女性化的去男性化效果;但并不推荐使用。
|
||||
这是因为雌二醇是由睾酮产生的,没有雄激素也就会缺乏雌激素。雌激素对维持男性和女性的[骨密度][wiki36]至关重要;没有雌激素,骨量将快速流失,最终会发展成[骨质疏松症][wiki37],骨折风险也变得很高;还可能会发生骨骼和姿态性损伤<sup>([图片1][fig1]; [图片2][fig2])</sup>。
|
||||
此外,患者还可能出现其它类似[更年期][wiki38]的症状,如[潮热][wiki39]、情绪和睡眠问题、性功能障碍(如性欲低下与勃起功能障碍),以及皮肤加速老化等<sup>([维基][wiki14-skin])</sup>。性激素缺乏也可能与体重增加、II 型糖尿病、冠心病和痴呆症的风险增加存在关联。
|
||||
综上,长期缺乏雄激素和雌激素且不补充雌激素是不可取的。
|
||||
|
||||
说到这里,有必要作一些澄清。例如,大剂量比卡鲁胺单药疗法可维持一定雌二醇水平,从而具有很小或不具备骨质流失与大多数其它更年期症状的风险。
|
||||
此外,低剂量醋酸环丙孕酮合并低剂量比卡鲁胺的疗法,也具有较低的患更年期症状与骨质疏松症之风险。这是因为,高剂量孕激素(其中“低剂量”醋酸环丙孕酮无疑符合这点)可以帮助治疗潮热(可能还有骨质流失)等特定更年期症状;而且,此疗法亦可维持少量雌二醇存在——睾酮最多被抑制 70-80%,而不再增加。
|
||||
说到这里,有必要作一些澄清。例如,大剂量比卡鲁胺单药疗法可维持一定雌二醇水平,从而具有很小或不具备骨质流失与大多数其它更年期症状的风险。
|
||||
此外,低剂量醋酸环丙孕酮合并低剂量比卡鲁胺的疗法,也具有较低的患更年期症状与骨质疏松症之风险。这是因为,高剂量孕激素(其中“低剂量”醋酸环丙孕酮无疑符合这点)可以帮助治疗潮热(可能还有骨质流失)等特定更年期症状;而且,此疗法亦可维持少量雌二醇存在——睾酮最多被抑制 70-80%,而不再增加。
|
||||
话虽如此,如采取的是后者,可能最好不要冒任何风险。
|
||||
|
||||
### 选择性雌激素受体调节剂 (SERM)
|
||||
### 选择性雌激素受体调节剂 (SERM) {#selective-estrogen-receptor-modulators-serms}
|
||||
|
||||
在去除雄激素和雌激素的同时,可以采用 [选择性雌激素受体调节剂][wiki40] (SERM)——其也被称为“部分雌激素”。这些药物是雌激素受体的[部分激动剂][wiki41] ,依组织不同,可发挥雌激素或[抗雌激素][wiki42]效力。
|
||||
其中一种 SERM 是雷洛昔芬;其在骨骼、脂肪组织和肝脏中发挥雌激素效力,但在乳房中发挥抗雌激素效力。一般而言,SERM 可减缓骨质流失和骨质疏松症的风险,同时不会引起乳房的发育(实际上反而阻止其发育)。
|
||||
SERM 全部种类可于[此处][wiki40-forms]查阅。不过实际上,其中只有[雷洛昔芬][wiki43](“易维特”)、[他莫昔芬][wiki44](Nolvadex)和[托瑞米芬][wiki45](“法乐通”)仍在上市,且相对廉价、使用较多。
|
||||
关于不同 SERM 在各组织之雌激素与抗雌激素效力的概况,可见此[表格][table1]。
|
||||
在去除雄激素和雌激素的同时,可以采用 [选择性雌激素受体调节剂][wiki40] (SERM)——其也被称为“部分雌激素”。这些药物是雌激素受体的[部分激动剂][wiki41] ,依组织不同,可发挥雌激素或[抗雌激素][wiki42]效力。
|
||||
其中一种 SERM 是雷洛昔芬;其在骨骼、脂肪组织和肝脏中发挥雌激素效力,但在乳房中发挥抗雌激素效力。一般而言,SERM 可减缓骨质流失和骨质疏松症的风险,同时不会引起乳房的发育(实际上反而阻止其发育)。
|
||||
SERM 全部种类可于[此处][wiki40-forms]查阅。不过实际上,其中只有[雷洛昔芬][wiki43](“易维特”)、[他莫昔芬][wiki44](Nolvadex)和[托瑞米芬][wiki45](“法乐通”)仍在上市,且相对廉价、使用较多。
|
||||
关于不同 SERM 在各组织之雌激素与抗雌激素效力的概况,可见此[表格][table1]。
|
||||
一般来说,SERM 具有很相似的作用模式。尽管我们对 SERM 在不同组织作用的分别有一些了解,但很多时候并不清楚在特定组织中表现如何。例如,只有一项临床研究表明,SERM——即雷洛昔芬——在脂肪组织中会发挥雌激素效力<sup>([Francucci et al., 2014][f14])</sup>。此外,SERM 在诸如皮肤或大脑多数区域等组织中的作用也不太清楚。
|
||||
|
||||
SERM 也有各种副作用。例如,SERM 通常产生潮热等不良反应。不过,最近推出的 [巴多昔芬/结合雌激素复方药][wiki46] (Duavee) 已知可降低绝经后妇女的潮热发生率<sup>([Duavee 药品说明书][fda1])</sup>;但其仍处于专利期,售价高昂。无论如何,其它类似更年期的症状也可能随 SERM 而生。
|
||||
此外,SERM 在肝脏中表达雌激素效力,因此会影响凝血因子的产生、减少[胰岛素样生长因子-1][wiki47](IGF-1)的产生,还有其它潜在的不良变化。由于增强了凝血功能,SERM 有明显的血栓和心血管并发症(如中风)的风险<sup>([Aly W., 2020][aw20-ecbc])</sup>。
|
||||
某些 SERM(如他莫昔芬)也有独特的[脱靶作用][wiki48]和风险;例如罕见的肝毒性。
|
||||
SERM 也有各种副作用。例如,SERM 通常产生潮热等不良反应。不过,最近推出的 [巴多昔芬/结合雌激素复方药][wiki46] (Duavee) 已知可降低绝经后妇女的潮热发生率<sup>([Duavee 药品说明书][fda1])</sup>;但其仍处于专利期,售价高昂。无论如何,其它类似更年期的症状也可能随 SERM 而生。
|
||||
此外,SERM 在肝脏中表达雌激素效力,因此会影响凝血因子的产生、减少[胰岛素样生长因子-1][wiki47](IGF-1)的产生,还有其它潜在的不良变化。由于增强了凝血功能,SERM 有明显的血栓和心血管并发症(如中风)的风险<sup>([Aly W., 2020][aw20-ecbc])</sup>。
|
||||
某些 SERM(如他莫昔芬)也有独特的[脱靶作用][wiki48]和风险;例如罕见的肝毒性。
|
||||
雷洛昔芬作为[选择性更强][wiki49]的 SERM,可能比他莫昔芬更安全。
|
||||
|
||||
SERM 可有效维持骨密度。不过很遗憾,SERM 在骨骼内仅表达部分雌激素效力,因此其并非该用途的首选——它们虽显著优于不治疗,但不及雌激素有效<sup>([Dane et al., 2007][d07]; [Zirilli et al., 2009][z09]; [Birzniece et al., 2012][b12]; [Vestergaard, 2012][v12])</sup>。
|
||||
事实上,SERM 已知会明显拮抗雌二醇对骨骼的效力——例如雌二醇在维持绝经前妇女的骨密度<sup>([Powles et al., 1996][p66]; [Burshell et al., 1999][b99])</sup>以及促成患[性早熟][wiki50]的顺性别女孩的[骨成熟][wiki51]和[生长板闭合][wiki52]<sup>([Passone et al., 2015][p15])</sup>等方面的效力。
|
||||
一项针对老年男性的研究表明, 60 mg/天的雷洛昔芬对骨密度的影响至多可与 26 pg/mL 的雌二醇水平相当<sup>([Doran et al., 2001][d01]; [Palacios et al., 2020][p20])</sup>。当雌二醇水平低于此值时,雷洛昔芬对骨密度表达雌激素效力;而一旦高于此值,则雷洛昔芬转而表达抗雌激素效力<sup>(Doran et al., 2001; Palacios et al., 2020)</sup>。
|
||||
SERM 可有效维持骨密度。不过很遗憾,SERM 在骨骼内仅表达部分雌激素效力,因此其并非该用途的首选——它们虽显著优于不治疗,但不及雌激素有效<sup>([Dane et al., 2007][d07]; [Zirilli et al., 2009][z09]; [Birzniece et al., 2012][b12]; [Vestergaard, 2012][v12])</sup>。
|
||||
事实上,SERM 已知会明显拮抗雌二醇对骨骼的效力——例如雌二醇在维持绝经前妇女的骨密度<sup>([Powles et al., 1996][p66]; [Burshell et al., 1999][b99])</sup>以及促成患[性早熟][wiki50]的顺性别女孩的[骨成熟][wiki51]和[生长板闭合][wiki52]<sup>([Passone et al., 2015][p15])</sup>等方面的效力。
|
||||
一项针对老年男性的研究表明, 60 mg/天的雷洛昔芬对骨密度的影响至多可与 26 pg/mL 的雌二醇水平相当<sup>([Doran et al., 2001][d01]; [Palacios et al., 2020][p20])</sup>。当雌二醇水平低于此值时,雷洛昔芬对骨密度表达雌激素效力;而一旦高于此值,则雷洛昔芬转而表达抗雌激素效力<sup>(Doran et al., 2001; Palacios et al., 2020)</sup>。
|
||||
因此,尽管 SERM 在低雌二醇水平下会增加骨密度,但在维持骨密度方面,它们不如雌激素有效;如非二元(女性倾向)跨性别者在雄激素去除过程中使用 SERM,其仍可能使骨密度明显下降。
|
||||
|
||||
### 低剂量雌激素补充
|
||||
### 低剂量雌激素补充 {#low-dose-estrogen-supplementation}
|
||||
|
||||
为避免雌激素缺乏,可用低剂量雌激素疗法代替 SERM。仅需约 1 - 2 mg/天的口服雌二醇、或 30 - 50 pg/mL 左右的雌二醇水平(使用透皮贴片等其它途径),即可完全或接近完全地预防骨质流失<sup>([Barbieri, 1992][b92]; [Roux, 1997][r97]; [Hadji, Colli, & Regidor, 2019][hcr19])</sup>。此外,雌二醇的耐受性与安全性优于 SERM,血栓风险也低得多<sup>([Aly W., 2020][aw20-ecbc])</sup>。
|
||||
|
||||
然而,雌激素治疗有一个问题:在缺乏雄激素的情况下,雌激素即使在低水平也会诱发显著的女性化和乳房发育。正常顺性别女孩的雌二醇水平从青春期开始时的 5 至 10 pg/mL 逐渐增加到青春期后期的 50 或 60 pg/mL;如此低水平的雌二醇足以引起女性第二性征的完全发展<sup>([Aly W., 2020][aw20-hlfp])</sup>。类似地,患有[完全性雄激素不敏感综合征][wiki53](CAIS)的顺性别女性仅有平均约 35 pg/mL 的雌二醇水平,但也足以完成女性化,乳房发育也颇为良好<sup>([Aly W., 2020][aw20-cais]; [维基-图表][table2])</sup>。因此,在已去除雄激素的基础上加入低剂量的雌二醇,很可能引起完全的(女性化)转变过程。
|
||||
另外,或许也可采用非常低剂量的雌二醇,其女性化效果也较弱——例如 0.5 mg/天 的口服雌二醇或 14 μg/天的雌二醇贴片,仅会达到 20 pg/mL 的雌二醇水平。如此剂量及水平尽管可维持骨密度<sup>(Dane et al., 2007; Birzniece et al., 2012)</sup>,但不能完全防止骨质流失和其它类似更年期的症状,且仍可能至少引起一部分女性化效果。
|
||||
然而,雌激素治疗有一个问题:在缺乏雄激素的情况下,雌激素即使在低水平也会诱发显著的女性化和乳房发育。正常顺性别女孩的雌二醇水平从青春期开始时的 5 至 10 pg/mL 逐渐增加到青春期后期的 50 或 60 pg/mL;如此低水平的雌二醇足以引起女性第二性征的完全发展<sup>([Aly W., 2020][aw20-hlfp])</sup>。类似地,患有[完全性雄激素不敏感综合征][wiki53](CAIS)的顺性别女性仅有平均约 35 pg/mL 的雌二醇水平,但也足以完成女性化,乳房发育也颇为良好<sup>([Aly W., 2020][aw20-cais]; [维基-图表][table2])</sup>。因此,在已去除雄激素的基础上加入低剂量的雌二醇,很可能引起完全的(女性化)转变过程。
|
||||
另外,或许也可采用非常低剂量的雌二醇,其女性化效果也较弱——例如 0.5 mg/天 的口服雌二醇或 14 μg/天的雌二醇贴片,仅会达到 20 pg/mL 的雌二醇水平。如此剂量及水平尽管可维持骨密度<sup>(Dane et al., 2007; Birzniece et al., 2012)</sup>,但不能完全防止骨质流失和其它类似更年期的症状,且仍可能至少引起一部分女性化效果。
|
||||
需要指出,即使仅接受性腺切除术或仅使用 GnRH 激动剂/拮抗剂,在将雌二醇水平降至 10 pg/mL 左右的情况下,也仍有轻度的乳房发育概率——至多达 15% <sup>([Di Lorenzo et al., 2005][dl05])</sup>。
|
||||
|
||||
### 其它保护骨骼的疗法
|
||||
### 其它保护骨骼的疗法 {#other-therapies-for-bone-maintenance}
|
||||
|
||||
除 SERMs 和雌激素外,还有一些措施可保持骨密度,更好地利于骨骼健康,可以纳入使用。例如:[补充钙质][wiki54]、[补充维生素 D][wiki55] 和[双磷酸盐][wiki56]——如[阿仑膦酸][wiki57](Fosamax)和[唑来膦酸][wiki58](Zometa)<sup>([Chen, Ko, & Chen, 2019][ckc19]; [Rizzoli, 2018][r18])</sup>。不过双磷酸盐有一定不良反应和风险。
|
||||
除 SERMs 和雌激素外,还有一些措施可保持骨密度,更好地利于骨骼健康,可以纳入使用。例如:[补充钙质][wiki54]、[补充维生素 D][wiki55] 和[双磷酸盐][wiki56]——如[阿仑膦酸][wiki57](Fosamax)和[唑来膦酸][wiki58](Zometa)<sup>([Chen, Ko, & Chen, 2019][ckc19]; [Rizzoli, 2018][r18])</sup>。不过双磷酸盐有一定不良反应和风险。
|
||||
[负重][wiki59] [运动][wiki60]也对维持骨密度有益<sup>(Rizzoli, 2018)</sup>。
|
||||
|
||||
有一项小型随机对照试验很有意思:其发现 100 mg/天的螺内酯可以完全防止由 GnRH 激动剂引起的妇女骨质流失<sup>([Moghetti et al., 1999][m99])</sup>。发现此现象的研究者推测,这应出于其[抗盐皮质激素][wiki61]活性的缘故;因为[醛固酮][wiki62](一种来自肾上腺的盐皮质激素——*译者注*)之含量与骨密度呈负相关<sup>(Moghetti et al., 1999)</sup>。
|
||||
有一项小型随机对照试验很有意思:其发现 100 mg/天的螺内酯可以完全防止由 GnRH 激动剂引起的妇女骨质流失<sup>([Moghetti et al., 1999][m99])</sup>。发现此现象的研究者推测,这应出于其[抗盐皮质激素][wiki61]活性的缘故;因为[醛固酮][wiki62](一种来自肾上腺的盐皮质激素——*译者注*)之含量与骨密度呈负相关<sup>(Moghetti et al., 1999)</sup>。
|
||||
然而,在另一项研究中,100 mg/天的螺内酯并不能防止妇女因采用大剂量孕激素(5 mg/天的[炔诺酮][wiki63])而引起的骨质流失<sup>([Preželj & Kocijančič, 1994][pk94]; [Preželj & Kocijančič, 1999][pk99])</sup>。因此,不应依靠螺内酯来维持骨密度。
|
||||
|
||||
### 骨质疏松的萌发和可逆性
|
||||
### 骨质疏松的萌发和可逆性 {#onset-and-reversibility-of-bone-loss}
|
||||
|
||||
有些用于绝经前妇女的药物会抑制性腺性激素的分泌,并与骨质流失有关。这些疗法可以为非二元(女性倾向)跨性别者去除性激素之后的骨质流失风险提供启示。
|
||||
有些用于绝经前妇女的药物会抑制性腺性激素的分泌,并与骨质流失有关。这些疗法可以为非二元(女性倾向)跨性别者去除性激素之后的骨质流失风险提供启示。
|
||||
这些药物包括:
|
||||
|
||||
- 纯孕激素避孕药——其部分抑制雌二醇水平(至大约 20–50 pg/mL)<sup>(Hadji, Colli, & Regidor, 2019)</sup>;
|
||||
- GnRH 激动剂/拮抗剂——其部分或完全抑制雌二醇水平,取决于药物和剂量。
|
||||
- GnRH 激动剂/拮抗剂——其部分或完全抑制雌二醇水平,取决于药物和剂量。
|
||||
|
||||
骨质流失鲜少或完全不会在 30 - 50 pg/mL 的雌二醇水平下发生;但会在 20 - 30 pg/mL 的雌二醇水平下趋于明显<sup>(Hadji, Colli, & Regidor, 2019)</sup>。
|
||||
不过,已知年轻的绝经前妇女停用纯孕激素避孕药之后,其骨密度在数年内便得以大幅或完全恢复;这多少令人欣慰<sup>([Nelson, 2010][n10])</sup>。
|
||||
类似地,绝经前妇女使用[恶拉戈利][wiki64](一种 GnRH 拮抗剂)治疗时,在可部分抑制雌二醇水平(至约 40 pg/mL)的剂量下,两年内都很安全;而在完全抑制雌二醇水平(至约 10 pg/mL)的剂量下,则有至多六个月的安全期<sup>([维基][wiki64-use])</sup>。
|
||||
骨质流失鲜少或完全不会在 30 - 50 pg/mL 的雌二醇水平下发生;但会在 20 - 30 pg/mL 的雌二醇水平下趋于明显<sup>(Hadji, Colli, & Regidor, 2019)</sup>。
|
||||
不过,已知年轻的绝经前妇女停用纯孕激素避孕药之后,其骨密度在数年内便得以大幅或完全恢复;这多少令人欣慰<sup>([Nelson, 2010][n10])</sup>。
|
||||
类似地,绝经前妇女使用[恶拉戈利][wiki64](一种 GnRH 拮抗剂)治疗时,在可部分抑制雌二醇水平(至约 40 pg/mL)的剂量下,两年内都很安全;而在完全抑制雌二醇水平(至约 10 pg/mL)的剂量下,则有至多六个月的安全期<sup>([维基][wiki64-use])</sup>。
|
||||
因此,在保持骨骼健康上,采取较短时长的性激素去除疗法应该比较安全——例如作为非二元(女性倾向)跨性别激素治疗的体验期。而当长期治疗时,需要采取适当的措施来避免骨质流失。
|
||||
|
||||
## 乳房发育的预防 {#prevention-of-breast-development}
|
||||
|
||||
## 乳房发育的预防
|
||||
### 雌激素阻断和抑制 {#estrogen-blockade-and-suppression}
|
||||
|
||||
### 雌激素阻断和抑制
|
||||
|
||||
如需通过药物实现不伴随乳房发育的完全去男性化、与一部分或完全女性化效果,则有许多方法可以实现。
|
||||
例如,在去除雄激素的同时而不补充雌激素,会仅引起去男性化,而无女性化或乳房发育效果(当然比卡鲁胺单疗除外)。不过,如上文所述,此法并不推荐使用,且不会引起女性化。
|
||||
如需通过药物实现不伴随乳房发育的完全去男性化、与一部分或完全女性化效果,则有许多方法可以实现。
|
||||
例如,在去除雄激素的同时而不补充雌激素,会仅引起去男性化,而无女性化或乳房发育效果(当然比卡鲁胺单疗除外)。不过,如上文所述,此法并不推荐使用,且不会引起女性化。
|
||||
另外也可选用 SERM;除了可治疗骨质疏松症,其还可治疗男性女乳症,在足够剂量下可完全阻断雌激素诱发的乳房发育<sup>([Fentiman, 2018][f18])</sup>。然而,SERM 仅可引起部分(而非完全)的女性化效果。与此相反的是[芳香化酶抑制剂][wiki65]:其在此类治疗中没有明显用处,因为它们对预防乳房发育的效果反倒很差<sup>([Fagerlund et al., 2015][f15]; [Bedognetti et al., 2010][b10])</sup>。
|
||||
|
||||
### SERM 导致的睾酮水平升高问题
|
||||
### SERM 导致的睾酮水平升高问题 {#selective-estrogen-receptor-modulators-and-testosterone-elevation}
|
||||
|
||||
如上文所述,可用 SERM 来预防乳房发育。但此法存在一个问题:如用于出生指派性别为男、且性腺完好的人,在睾酮水平未被抑制的情况下,SERM 将诱发性腺睾酮分泌的大幅增加,从而使血清睾酮水平上升。在患有[性腺功能低下][wiki66](睾酮水平低)的男性中,使用两种 SERM:[氯米芬][wiki67](20–50 mg/天)和[恩氯米芬][wiki68](12.5–25 mg/天)可将睾酮水平从平均约 200–300 ng/dL,升高至约 450–600 ng/dL(增长约 2.0 至 2.5 倍,绝对值增加 250–400 ng/dL)<sup>([Bach, Najari, & Kashanian, 2016][bnk16]; [Trost & Khera, 2014][tk14])</sup>。由于 SERM 在提高睾酮水平方面非常有效,因此其作为外源性睾酮的替代品,被用来治疗男性性腺功能减退症。
|
||||
如上文所述,可用 SERM 来预防乳房发育。但此法存在一个问题:如用于出生指派性别为男、且性腺完好的人,在睾酮水平未被抑制的情况下,SERM 将诱发性腺睾酮分泌的大幅增加,从而使血清睾酮水平上升。在患有[性腺功能低下][wiki66](睾酮水平低)的男性中,使用两种 SERM:[氯米芬][wiki67](20–50 mg/天)和[恩氯米芬][wiki68](12.5–25 mg/天)可将睾酮水平从平均约 200–300 ng/dL,升高至约 450–600 ng/dL(增长约 2.0 至 2.5 倍,绝对值增加 250–400 ng/dL)<sup>([Bach, Najari, & Kashanian, 2016][bnk16]; [Trost & Khera, 2014][tk14])</sup>。由于 SERM 在提高睾酮水平方面非常有效,因此其作为外源性睾酮的替代品,被用来治疗男性性腺功能减退症。
|
||||
更糟糕的是,SERM 对于性腺功能未减退的男性,会引起更大幅度的睾酮水平升高。一项研究发现,50 mg/天的氯米芬可将健康的年轻男性的睾酮水平升高约 850 ng/dL;还可使老年男性的睾酮水平升高约 500 ng/dL<sup>(Trost & Khera, 2014)</sup>。同样,在年轻和老年男性中,使用芳香化酶抑制剂抑制一部分雌二醇水平之后,也可见睾酮水平的高度增长<sup>([T’Sjoen et al., 2005][ts05]; [Raven et al., 2006][r06]; [de Ronde et al., 2009][r09])</sup>。
|
||||
|
||||
在睾酮水平已得到抑制的情况下,SERM 提升睾酮水平的能力与睾酮抑制程度呈负相关——例如,在大剂量孕激素治疗下,该能力会大幅减弱;而如经过药物/手术去势,则该能力完全丧失。
|
||||
在睾酮水平已得到抑制的情况下,SERM 提升睾酮水平的能力与睾酮抑制程度呈负相关——例如,在大剂量孕激素治疗下,该能力会大幅减弱;而如经过药物/手术去势,则该能力完全丧失。
|
||||
但是,如将 SERM 与比卡鲁胺合用,情况会变得更差;这是因为比卡鲁胺本身会引起相当程度的睾酮水平增幅,这与 SERM 类似。在患有前列腺癌的老年男性中,比卡鲁胺单疗可使睾酮水平上升 1.5 至 2.0 倍,从约 300–400 ng/dL 升至约 500–600 ng/dL(绝对增加值 150–250 ng/dL)<sup>([维基][wiki69])</sup>。在健康的年轻男性中,比卡鲁胺会使睾酮水平增加到正常男性范围的上限(约可达 900–1,200 ng/dL 的范围内)<sup>([维基][wiki69])</sup>。
|
||||
|
||||
比卡鲁胺作为雄激素受体的竞争性拮抗剂,其疗效从根本上说既依赖于剂量,又依赖于睾酮水平。因此,与 SERM 合用时,睾酮水平可能会变得太高而超出比卡鲁胺的阻断能力。
|
||||
此外,出生指派性别为男的人的[下丘脑-垂体-性腺轴][wiki70](HPG 轴),需要内源性雄激素和雌激素共同维持其负反馈稳态。在 HPG 轴几乎未被抑制的情况下,性腺的性激素分泌以及血清睾酮、雌二醇水平貌似只会继续上升,直至它们盖过比卡鲁胺/SERM 的效力,恢复对 HPG 轴的负反馈。
|
||||
比卡鲁胺作为雄激素受体的竞争性拮抗剂,其疗效从根本上说既依赖于剂量,又依赖于睾酮水平。因此,与 SERM 合用时,睾酮水平可能会变得太高而超出比卡鲁胺的阻断能力。
|
||||
此外,出生指派性别为男的人的[下丘脑-垂体-性腺轴][wiki70](HPG 轴),需要内源性雄激素和雌激素共同维持其负反馈稳态。在 HPG 轴几乎未被抑制的情况下,性腺的性激素分泌以及血清睾酮、雌二醇水平貌似只会继续上升,直至它们盖过比卡鲁胺/SERM 的效力,恢复对 HPG 轴的负反馈。
|
||||
综上,在非常规女性化激素治疗当中仅使用比卡鲁胺和 SERM,也许并不可行。
|
||||
|
||||
不过,尽管如此,已有研究评估了比卡鲁胺和他莫昔芬的组合用于男性前列腺癌患者的情况<sup>([PubMed][pubmed1])</sup>,其中睾酮水平的增加并未造成任何麻烦;这多少令人讶异。从研究结果看,比卡鲁胺与他莫昔芬的确会如预期一般,使总睾酮水平上升;但如此增幅与单用比卡鲁胺的情况没有太大区别。此外,游离睾酮水平要么有一定上升,要么根本没有上升<sup>([Boccardo et al., 2005][b05]; [Saltzstein et al., 2005][s05]; [Fradet et al., 2007][f07])</sup>。目前认为,这种现象是由于 SERM 在肝脏中强烈表达雌激素效力,使得[性激素结合球蛋白][wiki71](SHBG)的产量增加,从而降低了血清游离(即具有生物活性)的睾酮比例。这有助于抵消由总睾酮水平增加带来的生物学影响。
|
||||
不过,尽管如此,已有研究评估了比卡鲁胺和他莫昔芬的组合用于男性前列腺癌患者的情况<sup>([PubMed][pubmed1])</sup>,其中睾酮水平的增加并未造成任何麻烦;这多少令人讶异。从研究结果看,比卡鲁胺与他莫昔芬的确会如预期一般,使总睾酮水平上升;但如此增幅与单用比卡鲁胺的情况没有太大区别。此外,游离睾酮水平要么有一定上升,要么根本没有上升<sup>([Boccardo et al., 2005][b05]; [Saltzstein et al., 2005][s05]; [Fradet et al., 2007][f07])</sup>。目前认为,这种现象是由于 SERM 在肝脏中强烈表达雌激素效力,使得[性激素结合球蛋白][wiki71](SHBG)的产量增加,从而降低了血清游离(即具有生物活性)的睾酮比例。这有助于抵消由总睾酮水平增加带来的生物学影响。
|
||||
因此,相比于单用比卡鲁胺,此类疗法并未被发现会产生雄激素受体信号的不利变化(如[前列腺特异性抗原][wiki72]水平升高);这多少令人欣慰。
|
||||
|
||||
对于比卡鲁胺合并他莫昔芬的疗法、与单用比卡鲁胺的疗法,在总睾酮水平上的提升幅度被观测到差异甚小的缘故,目前仍不大清楚。无论是什么原因,相关研究都已表明,比卡鲁胺和他莫昔芬(或某些其他 SERM)的组合实际上应可用于非常规女性化激素治疗。
|
||||
对于比卡鲁胺合并他莫昔芬的疗法、与单用比卡鲁胺的疗法,在总睾酮水平上的提升幅度被观测到差异甚小的缘故,目前仍不大清楚。无论是什么原因,相关研究都已表明,比卡鲁胺和他莫昔芬(或某些其他 SERM)的组合实际上应可用于非常规女性化激素治疗。
|
||||
不过话虽如此,需要指出,老年男性群体并不同于非二元(女性倾向)跨性别者;与健康的年轻男性相比,老年男性在使用比卡鲁胺和 SERM 时,仅有较小的睾酮水平增幅。相对地,这种组合可能对出生指派性别为男的年轻人不那么有利。
|
||||
|
||||
雷洛昔芬很可能能够代替他莫昔芬,并与比卡鲁胺合用。然而需要注意,不同于他莫昔芬,雷洛昔芬与比卡鲁胺合用的情况尚未得到研究;或者说,至少没有在性腺完整的男性中进行过研究。当下的确已有一项研究描述了比卡鲁胺与雷洛昔芬用于患前列腺癌、且已去势的男性之状况,但其参考性不大<sup>([Ho et al., 2017][h07])</sup>。
|
||||
此外,雷洛昔芬用于预防乳房发育的情况也尚未得到研究。有一项回顾性病例总结指出,其可有效治疗青春期男孩的乳房发育<sup>([Lawrence et al., 2004][l04])</sup>。不过我们目前掌握的数据只有这么多。
|
||||
雷洛昔芬很可能能够代替他莫昔芬,并与比卡鲁胺合用。然而需要注意,不同于他莫昔芬,雷洛昔芬与比卡鲁胺合用的情况尚未得到研究;或者说,至少没有在性腺完整的男性中进行过研究。当下的确已有一项研究描述了比卡鲁胺与雷洛昔芬用于患前列腺癌、且已去势的男性之状况,但其参考性不大<sup>([Ho et al., 2017][h07])</sup>。
|
||||
此外,雷洛昔芬用于预防乳房发育的情况也尚未得到研究。有一项回顾性病例总结指出,其可有效治疗青春期男孩的乳房发育<sup>([Lawrence et al., 2004][l04])</sup>。不过我们目前掌握的数据只有这么多。
|
||||
他莫昔芬的情况与此相反:迄今已有多项有关其用于预防乳房发育的高质量研究,其中也包括与比卡鲁胺合用的情况。
|
||||
|
||||
无论如何,已知雷洛昔芬用于男性时,在睾酮水平上的增幅要低于他莫昔芬或托瑞米芬<sup>([Tsourdi et al., 2009][t09])</sup>。因此,无论是将比卡鲁胺与雷洛昔芬合用,还是与他莫昔芬合用,此二者在睾酮水平上的表现应很相似。不过,这可能只是出于雷洛昔芬作为 SERM 的效力在同等临床剂量下低于他莫昔芬或托瑞米芬的缘故<sup>(Tsourdi et al., 2009)</sup>。
|
||||
|
||||
### 雄激素的局部外用
|
||||
### 雄激素的局部外用 {#topical-androgens}
|
||||
|
||||
还有一种手段可预防乳房发育:就是在乳房上局部外用[双氢睾酮][wiki73](DHT; Andractim);这种雄激素不可[芳香化][wiki74],从而不可转化为雌激素。雄激素可显著阻止雌激素在乳房中的作用;在多项小型研究中,局部和全身用 DHT 可有效治疗男性乳房发育,且与 SERM 相似<sup>([Kuhn et al., 1982][k82]; [Kuhn et al., 1983a][k83a]; [Kuhn et al., 1983b][k83b]; [Eberle & Keenan, 1985][ek85]; [Eberle, Sparrow, & Keenan, 1986][esk86]; [Caron et al., 1987][c87]; [Keenan, Fagan, & Richards, 1989][kfr89]; [De Corrado et al., 1998][dc98]; [Benveniste, Simon, & Herson, 2001][bsh01])</sup>。
|
||||
还有一种手段可预防乳房发育:就是在乳房上局部外用[双氢睾酮][wiki73](DHT; Andractim);这种雄激素不可[芳香化][wiki74],从而不可转化为雌激素。雄激素可显著阻止雌激素在乳房中的作用;在多项小型研究中,局部和全身用 DHT 可有效治疗男性乳房发育,且与 SERM 相似<sup>([Kuhn et al., 1982][k82]; [Kuhn et al., 1983a][k83a]; [Kuhn et al., 1983b][k83b]; [Eberle & Keenan, 1985][ek85]; [Eberle, Sparrow, & Keenan, 1986][esk86]; [Caron et al., 1987][c87]; [Keenan, Fagan, & Richards, 1989][kfr89]; [De Corrado et al., 1998][dc98]; [Benveniste, Simon, & Herson, 2001][bsh01])</sup>。
|
||||
此外,已知其它全身性雄激素在这方面也很有效,例如诺龙<sup>([Heresová et al., 1981][h81]; [Heresová & Vrzanova, 2003][hv03])</sup>和达那唑<sup>([Buckle, 1980][b80]; [Ting, Chow, & Leung, 2000][tcl00])</sup>。
|
||||
|
||||
遗憾的是,目前规模化生产的外用 DHT 仅在法国有售<sup>([Drugs.com][drugs1])</sup>。某些国家的配药房也许可制作外用 DHT 制剂;不过在美国并没有这样的配药房。
|
||||
与 DHT 相反,睾酮很容易经芳香化作用转化为雌二醇,因此会因雌激素暴露过多而诱发一定乳房发育;因此,睾酮应不适合用于此用途。
|
||||
遗憾的是,目前规模化生产的外用 DHT 仅在法国有售<sup>([Drugs.com][drugs1])</sup>。某些国家的配药房也许可制作外用 DHT 制剂;不过在美国并没有这样的配药房。
|
||||
与 DHT 相反,睾酮很容易经芳香化作用转化为雌二醇,因此会因雌激素暴露过多而诱发一定乳房发育;因此,睾酮应不适合用于此用途。
|
||||
外用雄激素基本上只有睾酮和 DHT 可选,因此这类手段可操作性不大。
|
||||
|
||||
与 SERM 相比,外用雄激素也许不能完全有效地防止乳房发育。尽管 SERM 能够抵消雌激素对乳房发育的影响,但只要雌激素暴露量足够高,在雄激素暴露同样较强的情况下,仍可诱导相当程度的乳房发育。
|
||||
此外,在乳房上局部外用雄激素很可能导致局部体毛生长和其它局部雄激素效应(如男性化的皮肤变化、油性皮肤、痤疮等),这对许多女性倾向跨性别者来说可能难以承受。
|
||||
与 SERM 相比,外用雄激素也许不能完全有效地防止乳房发育。尽管 SERM 能够抵消雌激素对乳房发育的影响,但只要雌激素暴露量足够高,在雄激素暴露同样较强的情况下,仍可诱导相当程度的乳房发育。
|
||||
此外,在乳房上局部外用雄激素很可能导致局部体毛生长和其它局部雄激素效应(如男性化的皮肤变化、油性皮肤、痤疮等),这对许多女性倾向跨性别者来说可能难以承受。
|
||||
最后,局部外用的雄激素还有一项风险:其会通过血液向全身分布<sup>([Kuhn et al., 1983a][k83a])</sup>,提高血清雄激素水平,从而对身体其它部位产生雄激素效力。如果与比卡鲁胺这样的雄激素受体拮抗剂合用,这种风险就会减少——不过雄激素受体拮抗剂也可能会同时阻断外用雄激素的局部作用。
|
||||
|
||||
### 乳房切除手术和乳房照射
|
||||
### 乳房切除手术和乳房照射 {#breast-removal-surgery-and-breast-irradiation}
|
||||
|
||||
有两种非药物疗法可预防乳房发育:即预防性乳房切除和预防性乳房照射。
|
||||
|
||||
在没有多余皮肤的情况下,乳房切除术可不留下明显疤痕。[这位][fig3]年轻的跨性别男性就是如此。乳房切除术可非常有效地防止乳房发育,不过当然需要动刀。
|
||||
|
||||
乳房经放射线照射后,其发育会受到抑制<sup>([照片][fig4])</sup>。乳房照射是一种廉价、简单、有效的技术,通常用于接受雌激素或高剂量比卡鲁胺单药治疗的男性前列腺癌患者预防乳房发育<sup>([Viani, da Silva, & Stefano, 2012][vss12])</sup>。然而,其效力不及 SERM,通常只能降低乳房发育的严重程度,而不能完全预防<sup>([Viani, da Silva, & Stefano, 2012][vss12])</sup>。
|
||||
更令人担忧的是,理论上乳房暴露于核辐射会增加乳腺癌的风险<sup>([Aksnessæther et al., 2018][a18])</sup>。研究发现,曾在童年因癌症放疗而使乳房受到辐射的年轻女性,在乳腺癌发生率上,比其他年轻女性要高出 100 倍<sup>([Zacharin, 2010][z10])</sup>。另一方面,目前有限的证据表明,在接受雄激素去除/雌激素治疗的老年男性中,为防止乳房发育而使用乳房照射,仅有极低的乳腺癌发病率<sup>([Aksnessæther et al., 2018][a18]; [Viani, da Silva, & Stefano, 2012][vss12])</sup>。然而,癌症放疗和其它形式的辐射暴露——特别是在年轻时暴露——会增加男性患乳腺癌的风险<sup>([Niewoehner, 2008][n08]; [Giordano, 2005][g05])</sup>。
|
||||
乳房经放射线照射后,其发育会受到抑制<sup>([照片][fig4])</sup>。乳房照射是一种廉价、简单、有效的技术,通常用于接受雌激素或高剂量比卡鲁胺单药治疗的男性前列腺癌患者预防乳房发育<sup>([Viani, da Silva, & Stefano, 2012][vss12])</sup>。然而,其效力不及 SERM,通常只能降低乳房发育的严重程度,而不能完全预防<sup>([Viani, da Silva, & Stefano, 2012][vss12])</sup>。
|
||||
更令人担忧的是,理论上乳房暴露于核辐射会增加乳腺癌的风险<sup>([Aksnessæther et al., 2018][a18])</sup>。研究发现,曾在童年因癌症放疗而使乳房受到辐射的年轻女性,在乳腺癌发生率上,比其他年轻女性要高出 100 倍<sup>([Zacharin, 2010][z10])</sup>。另一方面,目前有限的证据表明,在接受雄激素去除/雌激素治疗的老年男性中,为防止乳房发育而使用乳房照射,仅有极低的乳腺癌发病率<sup>([Aksnessæther et al., 2018][a18]; [Viani, da Silva, & Stefano, 2012][vss12])</sup>。然而,癌症放疗和其它形式的辐射暴露——特别是在年轻时暴露——会增加男性患乳腺癌的风险<sup>([Niewoehner, 2008][n08]; [Giordano, 2005][g05])</sup>。
|
||||
除了理论上的癌症风险外,心脏和肺部问题也与患有前列腺癌的老年男性的乳房照射有关<sup>([Tunio et al., 2012][t12]; [Viani, da Silva, & Stefano, 2012][vss12])</sup>。出于这些健康风险,为预防乳房发育而接受乳房照射是不可取的。
|
||||
|
||||
这两种疗法有一个明显缺点:它们是不可逆的。如果接受上述治疗后转而想要有乳房,或者最终决定完全转变(这种情况并不少见),那么不再有回头路可走。
|
||||
|
||||
### 乳房发育的程度、起始时间和可逆性
|
||||
### 乳房发育的程度、起始时间和可逆性 {#degree-onset-and-reversibility-of-breast-development}
|
||||
|
||||
需要指出,由于不完全清楚的原因,相比于顺性别女性,女性倾向跨性别者的乳房发育往往较差或不理想<sup>([Wierckx, Gooren, & T’Sjoen, 2014][wgt14]; [de Blok et al., 2018][blok18]; [Reisman, Goldstein, & Safer, 2019][rgs19])</sup>。同样,一般在患有前列腺癌的老年男性中,使用大剂量比卡鲁胺单药治疗和大剂量雌激素治疗都会有很大概率引起乳房发育,但其中 90% 的病例中仅产生轻度到中度的乳房发育<sup>([维基百科][wiki75]; [Ockrim et al., 2003][o03])</sup>。(尚不清楚其是否受高年龄影响,但有一定可能。)
|
||||
需要指出,由于不完全清楚的原因,相比于顺性别女性,女性倾向跨性别者的乳房发育往往较差或不理想<sup>([Wierckx, Gooren, & T’Sjoen, 2014][wgt14]; [de Blok et al., 2018][blok18]; [Reisman, Goldstein, & Safer, 2019][rgs19])</sup>。同样,一般在患有前列腺癌的老年男性中,使用大剂量比卡鲁胺单药治疗和大剂量雌激素治疗都会有很大概率引起乳房发育,但其中 90% 的病例中仅产生轻度到中度的乳房发育<sup>([维基百科][wiki75]; [Ockrim et al., 2003][o03])</sup>。(尚不清楚其是否受高年龄影响,但有一定可能。)
|
||||
因此,从普遍或*平均*的角度而言,任何出生指派性别为男的人,不一定会有明显的乳房发育程度;其乳房尺寸的普遍预期应是较小。不过也有例外,有一小部分女性倾向跨性别者会有显著的乳房发育。所以,每个人乳房发育程度如何全凭运气,这点需要留意。
|
||||
|
||||
还有几个方面需要注意:一,乳房发育过程很慢,并非一蹴而就;二,一旦停用激素,发育过程将会中断;三,如在一定时间内(如一年)停药,发育效果似乎还至少部分可逆<sup>([Mancino, Young, & Bland, 2018][myb18]; [Kanakis et al., 2019][k19])</sup>。
|
||||
然而,一项研究发现,在比卡鲁胺单药治疗下,如在引起乳房发育后的一个月内引入他莫昔芬(而非治疗开始时),则疗效会更差<sup>([Serretta et al. 2012][s12])</sup>。
|
||||
还有几个方面需要注意:一,乳房发育过程很慢,并非一蹴而就;二,一旦停用激素,发育过程将会中断;三,如在一定时间内(如一年)停药,发育效果似乎还至少部分可逆<sup>([Mancino, Young, & Bland, 2018][myb18]; [Kanakis et al., 2019][k19])</sup>。
|
||||
然而,一项研究发现,在比卡鲁胺单药治疗下,如在引起乳房发育后的一个月内引入他莫昔芬(而非治疗开始时),则疗效会更差<sup>([Serretta et al. 2012][s12])</sup>。
|
||||
无论如何,出于上述缘故,某些人可以对其乳房发育程度进行监测;如果发育程度超出其可接受范围,则可按需调整用药方案,以防止进一步发育或扭转之。因此,也许无需对乳房发育过分担心。
|
||||
|
||||
## 后记
|
||||
## 后记 {#updates}
|
||||
|
||||
### 后记一
|
||||
### 后记一 {#update-1}
|
||||
|
||||
2021 年六月,一篇关于 SERM 用于非二元(女性倾向)跨性别者的评述公开发表:
|
||||
|
||||
- Xu, J. Y., O’Connell, M. A., Notini, L., Cheung, A. S., Zwickl, S., & Pang, K. C. (2021).
|
||||
**Selective Estrogen Receptor Modulators: A Potential Option For Non-Binary Gender-Affirming Hormonal Care?** [SERM 用于非二元性别人群的性别肯定激素护理的潜在可能性]
|
||||
- Xu, J. Y., O’Connell, M. A., Notini, L., Cheung, A. S., Zwickl, S., & Pang, K. C. (2021).
|
||||
**Selective Estrogen Receptor Modulators: A Potential Option For Non-Binary Gender-Affirming Hormonal Care?** [SERM 用于非二元性别人群的性别肯定激素护理的潜在可能性]
|
||||
_Frontiers in Endocrinology_, _12_, 701364. [DOI:[10.3389/fendo.2021.701364][x21]]
|
||||
|
||||
这是该领域的第一篇正式文献。其指出,由于有关 SERM 用于非二元(女性倾向)激素治疗的有效性和安全性证据匮乏,当下不应推荐 SERM 用于非二元(女性倾向)跨性别者的常规治疗。不过,其慎重允许有需要且签署知情同意书的非二元(女性倾向)跨性别者中使用这些药物。
|
||||
这是该领域的第一篇正式文献。其指出,由于有关 SERM 用于非二元(女性倾向)激素治疗的有效性和安全性证据匮乏,当下不应推荐 SERM 用于非二元(女性倾向)跨性别者的常规治疗。不过,其慎重允许有需要且签署知情同意书的非二元(女性倾向)跨性别者中使用这些药物。
|
||||
该评述总结认为,SERM 是一种理论上对于非二元(女性倾向)跨性别者的激素治疗具有吸引力的潜在选择;其还呼吁针对这些目的对其进行临床研究。
|
||||
|
||||
Ada S. Cheung 是该论文的联名作者之一;其来自澳大利亚墨尔本大学医学院的跨性别健康研究小组([Trans Health Research][thr])。
|
||||
|
||||
在此前文献中,还出现了少量关于 SERM 用于非二元(女性倾向与男性倾向)跨性别者的叙述;不过其提供的资料更为有限<sup>([Carswell & Roberts, 2017][cr17]; [Moser & Devereux, 2019][md19]; [Pang et al., 2020][pang20]; [Naroji et al., 2021][n21])</sup>。
|
||||
|
||||
### 后记二
|
||||
### 后记二 {#update-2}
|
||||
|
||||
在最早的有关为非二元性别人群定制的激素疗法的研究当中,有一项于 2022 年三月公开发表了文献:
|
||||
|
||||
- van Dijken, J. B., Steensma, T. D., Wensing-Kruger, S. A., Heijer, M. D., & Dreijerink, K. M. (2022).
|
||||
**Tailored Gender-Affirming Hormone Treatment in Nonbinary Transgender Individuals: A Retrospective Study in a Referral Center Cohort.** [某治疗转诊中心的一项回顾性研究:为非二元跨性别者定制的性别肯定激素治疗]
|
||||
- van Dijken, J. B., Steensma, T. D., Wensing-Kruger, S. A., Heijer, M. D., & Dreijerink, K. M. (2022).
|
||||
**Tailored Gender-Affirming Hormone Treatment in Nonbinary Transgender Individuals: A Retrospective Study in a Referral Center Cohort.** [某治疗转诊中心的一项回顾性研究:为非二元跨性别者定制的性别肯定激素治疗]
|
||||
*Transgender Health*, 在线发表 (ahead of print). [DOI:[10.1089/trgh.2021.0032][d22]]
|
||||
|
||||
此外,有一篇关于[欧洲性别不一致调查组织网络][wiki76](ENIGI)所做工作的评述,还描述了 ENIGI 在将来针对非二元性别人群之激素治疗的研究计划:
|
||||
|
||||
- Cocchetti, C., Romani, A., Collet, S., Greenman, Y., Schreiner, T., Wiepjes, C., … & Fisher, A. D. (2022).
|
||||
**The ENIGI (European Network for the Investigation of Gender Incongruence) Study: Overview of Acquired Endocrine Knowledge and Future Perspectives.** [对 ENIGI 项目已有的内分泌学认识与未来焦点的综述]
|
||||
- Cocchetti, C., Romani, A., Collet, S., Greenman, Y., Schreiner, T., Wiepjes, C., … & Fisher, A. D. (2022).
|
||||
**The ENIGI (European Network for the Investigation of Gender Incongruence) Study: Overview of Acquired Endocrine Knowledge and Future Perspectives.** [对 ENIGI 项目已有的内分泌学认识与未来焦点的综述]
|
||||
*Journal of Clinical Medicine, 11*(7), 1784. [DOI:[10.3390/jcm11071784][c22]]
|
||||
|
||||
该评述的摘录如下:
|
||||
|
|
@ -288,20 +294,23 @@ Ada S. Cheung 是该论文的联名作者之一;其来自澳大利亚墨尔本
|
|||
|
||||
> 认同仍基于二元性别的、出生指派性别为女的跨性别者,会接受雄激素治疗以促成完全男性化;其原理与性腺功能减退的顺性别男性的激素替代疗法相当。
|
||||
|
||||
> 尽管迄今已有来自更多受试者的数据可以佐证,但当下仍有许多未解之谜。先是,ENIGI 合作项目至今仅评估了用于需要完全男性化/去女性化、或完全女性化/去男性化的跨性别者的标准化 GAHT 之疗效与安全性;不过,据性别诊所所述,前来就诊的非二元跨性别者群体正日益壮大,对非标准化 GAHT 的需求也与日俱增。
|
||||
> 为此,本文部分作者已呼吁制定各种药理学与非药理学对策,以回应来自非二元性别人群的多元化需求。
|
||||
> 尽管迄今已有来自更多受试者的数据可以佐证,但当下仍有许多未解之谜。先是,ENIGI 合作项目至今仅评估了用于需要完全男性化/去女性化、或完全女性化/去男性化的跨性别者的标准化 GAHT 之疗效与安全性;不过,据性别诊所所述,前来就诊的非二元跨性别者群体正日益壮大,对非标准化 GAHT 的需求也与日俱增。
|
||||
> 为此,本文部分作者已呼吁制定各种药理学与非药理学对策,以回应来自非二元性别人群的多元化需求。
|
||||
> 考虑到关于此类疗法的疗效与安全性数据完全缺失,ENIGI 合作项目在近期应更多着眼于此;而考虑到受试者人数众多,今后在激素治疗上采取“一人一方”会更得青睐。
|
||||
|
||||
## 辅助阅读材料
|
||||
## 辅助阅读材料 {#supplementary-material}
|
||||
|
||||
此处附上一份网传[文件][suppl] ([PDF 文档][suppl-pdf]);这是有关一位曾自我认同为伪娘的人使用 50 mg/天比卡鲁胺、12.5 mg/天的醋酸环丙孕酮和 60 mg/天的雷洛昔芬的报告,内容很有意思。
|
||||
|
||||
--------
|
||||
---
|
||||
|
||||
## 译文修订历史
|
||||
## 译文修订历史 {#revise-history}
|
||||
|
||||
- 2021 年 8 月 6 日——首次翻译。
|
||||
- 2022 年 11 月 22 日——第一次修订,优化全文叙述,增补“后记二”内容,跟进移除“结论”一章。
|
||||
```csv
|
||||
时间,备注
|
||||
2021 年 8 月 6 日,首次翻译。
|
||||
2022 年 11 月 22 日,第一次修订,优化全文叙述,增补“后记二”内容,跟进移除“结论”一章。
|
||||
```
|
||||
|
||||
<!-- 维基百科/词典条目 -->
|
||||
[wiki1]: https://en.wikipedia.org/wiki/Non-binary_gender
|
||||
|
|
@ -395,8 +404,8 @@ Ada S. Cheung 是该论文的联名作者之一;其来自澳大利亚墨尔本
|
|||
[table2]: https://en.wikipedia.org/wiki/Template:Hormone_levels_in_gonadally_intact_adolescent_and_adult_females_with_complete_androgen_insensitivity_syndrome
|
||||
|
||||
<!-- 本站其它文章外链 -->
|
||||
[aw18-intro]: transfem-intro.md
|
||||
[aw19-cpa]: cpa-dosage.md
|
||||
[aw18-intro]: https://transfemscience.org/articles/transfem-intro/
|
||||
[aw19-cpa]: https://transfemscience.org/articles/cpa-dosage/
|
||||
|
||||
[aw18-opr]: https://transfemscience.org/articles/oral-p4-rectally/
|
||||
[aw18-spiro]: https://transfemscience.org/articles/spiro-hormone-levels-men-transfem/
|
||||
|
|
@ -485,8 +494,7 @@ Ada S. Cheung 是该论文的联名作者之一;其来自澳大利亚墨尔本
|
|||
|
||||
<!-- 其它外链 -->
|
||||
[nih1]: https://www.ncbi.nlm.nih.gov/mesh?Term=%22Sexual+Infantilism%22%5BMeSH
|
||||
[r-femboy]: https://www.reddit.com/r/femboytransition/
|
||||
[fda1]: https://www.accessdata.fda.gov/drugsatfda_docs/label/2013/022247Orig1s001lbl.pdf
|
||||
[pubmed1]: https://pubmed.ncbi.nlm.nih.gov/?term=bicalutamide[title]+tamoxifen[title]
|
||||
[drugs1]: https://www.drugs.com/international/androstanolone.html
|
||||
[thr]: https://www.transresearch.org.au/
|
||||
[thr]: https://www.transresearch.org.au/
|
||||
|
|
@ -1,65 +1,84 @@
|
|||
# 口服孕酮及其引起的低孕酮水平与较弱效力的简论
|
||||
---
|
||||
title: 口服孕酮及其引起的低孕酮水平与较弱效力的简论
|
||||
description: >-
|
||||
口服孕酮引起的孕酮水平峰值与平均值极低,孕激素效力也较弱,且有类似酒精的副作用。应为此寻求替代。
|
||||
author: Aly W.
|
||||
published: 2018-08-04
|
||||
updated: 2022-11-08
|
||||
translated: 2022-11-18
|
||||
translators:
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 孕激素
|
||||
- 孕酮
|
||||
- 用药途径与剂量
|
||||
trackHash: 707eba7009f219b84a9dcb94eb5c05b8d7400b23
|
||||
---
|
||||
|
||||
> - 作者 [Aly W.][AUTHOR]
|
||||
> + 首次发表于 2018 年 8 月 4 日
|
||||
> + 最后修改于 2022 年 11 月 8 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [Bersella AI][TRANSLATOR]
|
||||
> + 翻译完成于 2022 年 11 月 18 日
|
||||
## 摘要 {#abstract}
|
||||
|
||||
[AUTHOR]: https://transfemscience.org/about/#aly-w
|
||||
[ORIGIN]: https://transfemscience.org/articles/oral-p4-low-levels/
|
||||
[TRANSLATOR]: https://bersella-ai.cc/about-me/
|
||||
在女性化激素疗法当中,口服孕酮是最常用的孕酮形式。早前,通常治疗用剂量的口服孕酮,被认为可达到顺性别妇女在黄体期通常的孕酮水平(约 7-22 ng/mL),这由早年一些未有准确验血结果(即使用了未经充分层析纯化的免疫测定法)的研究项目所支持。然而,新近的研究项目通过更精确的验血方法(经层析纯化的免疫测定法、和质谱测定法等)发现,无论饭前或饭后,每日服用 100 mg 孕酮仅可达到很低的约 2-3 ng/mL 的孕酮水平峰值,以及约 0.1-0.6 ng/mL 的 24 小时内孕酮平均水平。无独有偶,临床研究也发现口服孕酮仅产生较弱的孕酮效力。
|
||||
如为提高孕酮水平而使用更大剂量的孕酮,则作用很有限;这是因为,1) 孕酮水平仍旧很低;2) 肝脏的首过效应产生的神经甾体有显著副作用;3) 个体间会有明显差别。
|
||||
这种孕酮水平对于顺性别妇女,显然足可对子宫内膜起保护作用;但对于女性倾向跨性别者则不大能按预期奏效。
|
||||
因此,如欲起到足够的孕激素效力,女性倾向跨性别者及其医师要避免采用口服孕酮;非口服途径(如经直肠给药,或注射)孕酮的生物利用度更高,可以一用。合成孕酮制剂可替代孕酮使用,其同样具有完全的孕激素效力。
|
||||
|
||||
## 摘要
|
||||
## 口服孕酮引起的孕酮水平 {#progesterone-levels-with-oral-progesterone}
|
||||
|
||||
> 在女性化激素疗法当中,口服孕酮是最常用的孕酮形式。早前,通常治疗用剂量的口服孕酮,被认为可达到顺性别妇女在黄体期通常的孕酮水平(约 7-22 ng/mL),这由早年一些未有准确验血结果(即使用了未经充分层析纯化的免疫测定法)的研究项目所支持。然而,新近的研究项目通过更精确的验血方法(经层析纯化的免疫测定法、和质谱测定法等)发现,无论饭前或饭后,每日服用 100 mg 孕酮仅可达到很低的约 2-3 ng/mL 的孕酮水平峰值,以及约 0.1-0.6 ng/mL 的 24 小时内孕酮平均水平。无独有偶,临床研究也发现口服孕酮仅产生较弱的孕酮效力。
|
||||
> 如为提高孕酮水平而使用更大剂量的孕酮,则作用很有限;这是因为,1) 孕酮水平仍旧很低;2) 肝脏的首过效应产生的神经甾体有显著副作用;3) 个体间会有明显差别。
|
||||
> 这种孕酮水平对于顺性别妇女,显然足可对子宫内膜起保护作用;但对于女性倾向跨性别者则不大能按预期奏效。
|
||||
> 因此,如欲起到足够的孕激素效力,女性倾向跨性别者及其医师要避免采用口服孕酮;非口服途径(如经直肠给药,或注射)孕酮的生物利用度更高,可以一用。合成孕酮制剂可替代孕酮使用,其同样具有完全的孕激素效力。
|
||||
|
||||
## 口服孕酮引起的孕酮水平
|
||||
|
||||
制药厂规模生产的口服(微粉化)孕酮,是一种包含孕酮微晶的油悬浮液胶囊。其上市品牌包括 Prometrium、Utrogestan、Microgest 等等。受肠道及肝脏的[首过效应][wiki-1]影响,口服孕酮的[生物利用度][wiki-2]非常低,不大于 10%——绝大部分孕酮在进入血流前,会被代谢成为[别孕烷醇酮][wiki-3]、[孕烷醇酮][wiki-4]等[神经甾体][wiki-5]<sup>([de Lignieres, Dennerstein, & Backstrom, 1995][LDB95])</sup>。这就是为什么口服孕酮会有镇静等类似于[酒精][wiki-6]的副作用,而经阴道给药或注射的孕酮则无此影响。
|
||||
制药厂规模生产的口服(微粉化)孕酮,是一种包含孕酮微晶的油悬浮液胶囊。其上市品牌包括 Prometrium、Utrogestan、Microgest 等等。受肠道及肝脏的[首过效应][wiki-1]影响,口服孕酮的[生物利用度][wiki-2]非常低,不大于 10%——绝大部分孕酮在进入血流前,会被代谢成为[别孕烷醇酮][wiki-3]、[孕烷醇酮][wiki-4]等[神经甾体][wiki-5]<sup>([de Lignieres, Dennerstein, & Backstrom, 1995][LDB95])</sup>。这就是为什么口服孕酮会有镇静等类似于[酒精][wiki-6]的副作用,而经阴道给药或注射的孕酮则无此影响。
|
||||
不过,在生物利用度低的情况下,临床上口服孕酮的通常剂量(如 100-300 mg/天)已被报告可产生和顺性别妇女[月经周期][wiki-7]当中的[黄体期][wiki-8]相当的孕酮水平(通过[免疫测定法][wiki-9]测得)<sup>([Simon et al., 1993][S93])</sup>。因此,口服孕酮被确信可达到较高的、符合生理所需的孕酮水平。
|
||||
|
||||
> 
|
||||
>
|
||||
> 「图一」正常绝经前妇女的月经周期当中,孕酮水平的变化<sup>([Stricker et al., 2006][S06])</sup>。其中,横向虚线代表各折线的平均水平;纵向虚线区分排卵前后。通常仅当在黄体期内,孕酮水平才会升高。
|
||||
<section class="box">
|
||||
|
||||
> 
|
||||
>
|
||||
> 「图二」已绝经妇女单次口服 100-300 mg 孕酮(微粉化)之后,孕酮水平的变化(通过免疫测定法测得)<sup>([Simon et al., 1993][S93])</sup>。其中,横向虚线代表各折线的 24 小时平均水平。服药达成的孕酮水平似乎与正常黄体期的水平相一致。然而,使用免疫测定法得到的结果其实并不准确<sup>([Nahoul & de Ziegler, 1994][NZ94])</sup>。
|
||||

|
||||
|
||||
目前可以肯定,上述结论并不属实。这是因为,免疫[测定法][wiki-10]年代久远,在准确度和可靠性上存在缺陷;对于孕酮的测定,其暴露出了特异性不足的问题。其中,用于测定孕酮的[免疫蛋白][wiki-11],会跟孕酮的代谢物——[5α-二氢孕酮][wiki-12]、别孕烷醇酮、孕烷醇酮等——产生[交叉反应][wiki-13],最终计入到孕酮总量当中。由于口服孕酮的首过效应所产生的孕酮游离代谢物水平较高,这种交叉反应显然导致采用免疫测定法的研究项目<sup>(正如 [Simon et al., 1993][S93] 等)</sup>,明显高估了孕酮口服后产生的水平<sup>([Nahoul et al., 1993][N93]; [Nahoul & de Ziegler, 1994][NZ94])</sup>。
|
||||
图 1:正常绝经前妇女的月经周期当中,孕酮水平的变化<sup>([Stricker et al., 2006][S06])</sup>。其中,横向虚线代表各折线的平均水平;纵向虚线区分排卵前后。通常仅当在黄体期内,孕酮水平才会升高。
|
||||
|
||||
</section>
|
||||
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 2**:已绝经妇女单次口服 100-300 mg 孕酮(微粉化)之后,孕酮水平的变化(通过免疫测定法测得)<sup>([Simon et al., 1993][S93])</sup>。其中,横向虚线代表各折线的 24 小时平均水平。服药达成的孕酮水平似乎与正常黄体期的水平相一致。然而,使用免疫测定法得到的结果其实并不准确<sup>([Nahoul & de Ziegler, 1994][NZ94])</sup>。
|
||||
|
||||
</section>
|
||||
|
||||
目前可以肯定,上述结论并不属实。这是因为,免疫[测定法][wiki-10]年代久远,在准确度和可靠性上存在缺陷;对于孕酮的测定,其暴露出了特异性不足的问题。其中,用于测定孕酮的[免疫蛋白][wiki-11],会跟孕酮的代谢物——[5α-二氢孕酮][wiki-12]、别孕烷醇酮、孕烷醇酮等——产生[交叉反应][wiki-13],最终计入到孕酮总量当中。由于口服孕酮的首过效应所产生的孕酮游离代谢物水平较高,这种交叉反应显然导致采用免疫测定法的研究项目<sup>(正如 [Simon et al., 1993][S93] 等)</sup>,明显高估了孕酮口服后产生的水平<sup>([Nahoul et al., 1993][N93]; [Nahoul & de Ziegler, 1994][NZ94])</sup>。
|
||||
另外一些采用了特异性更佳的测定方法的研究项目,则发现了口服孕酮所达到的孕酮水平其实非常低<sup>([Nahoul, Dehennin, & Scholler, 1987][NDS87]; [Nahoul & de Ziegler, 1994][NZ94]; [Levine & Watson, 2000][LW00]; [Kuhl, 2011][K11]; [Kuhl & Schneider, 2013][KS13]; [Davey, 2018][D18])</sup>。其测定方法包括:经充分[层析纯化][wiki-14]的免疫测定法,以及[液相色谱—质谱联用法][wiki-15](LC-MS;被认为是临床上测定性激素水平的“黄金标准”)<sup>([Kuhl & Schneider, 2013][KS13]; [Woodward & Rumsby, 2019][WR19]; [Conklin & Knezevic, 2020][CK20])</sup>。
|
||||
|
||||
有一项使用 LC-MS 的研究发现,在单次口服 100 mg 孕酮之后,孕酮水平峰值仅达 2 ng/mL,24 小时内的平均水平仅有 0.14 ng/mL<sup>([Levine & Watson, 2000][LW00]; [Kuhl & Schneider, 2013][KS13])</sup>。另一项更新近、同样采用 LC-MS 的研究则发现,饭后单次口服 100 mg 孕酮之后,孕酮水平峰值约达 2.5-3 ng/mL,24 小时内的平均水平约为 0.6 ng/mL<sup>([Lobo et al., 2019][L19])</sup>——需要提及的是,饭后口服孕酮,可将其生物利用度翻上好几倍<sup>([维基百科][WIKI-CIT-1]; 经 FDA 批准的 [Bijuva 药品说明书][FDA-1]; [Simon et al., 1993][S93]; [FDA 对 Prometrium 药品的评述, 1996][FDA-2]; [Pickar et al., 2015][P15])</sup>。这样的孕酮水平明显低于正常黄体期的孕酮水平——后者经 LC-MS 测定,介乎 7-22 ng/mL<sup>([Nakamoto, 2016][N16])</sup>。
|
||||
一些研究项目将以免疫测定法与其它更可靠方法测定的孕酮结果进行直接比较,发现免疫测定法下,孕酮水平会被高估 5-8 倍<sup>([Nahoul, Dehennin, & Scholler, 1987][NDS87]; [Nahoul & de Ziegler, 1994][NZ94]; [Levine & Watson, 2000][LW00]; [Kuhl, 2011][K11]; [Kuhl & Schneider, 2013][KS13]; [Davey, 2018][D18])</sup>。有一项包含几名受试者的小型研究,采用了多种已商业化的免疫测定法,其高估程度在 2 倍到 40 倍之间<sup>([Sapin et al., 2000][S00])</sup>。
|
||||
有一项使用 LC-MS 的研究发现,在单次口服 100 mg 孕酮之后,孕酮水平峰值仅达 2 ng/mL,24 小时内的平均水平仅有 0.14 ng/mL<sup>([Levine & Watson, 2000][LW00]; [Kuhl & Schneider, 2013][KS13])</sup>。另一项更新近、同样采用 LC-MS 的研究则发现,饭后单次口服 100 mg 孕酮之后,孕酮水平峰值约达 2.5-3 ng/mL,24 小时内的平均水平约为 0.6 ng/mL<sup>([Lobo et al., 2019][L19])</sup>——需要提及的是,饭后口服孕酮,可将其生物利用度翻上好几倍<sup>([维基百科][WIKI-CIT-1]; 经 FDA 批准的 [Bijuva 药品说明书][FDA-1]; [Simon et al., 1993][S93]; [FDA 对 Prometrium 药品的评述, 1996][FDA-2]; [Pickar et al., 2015][P15])</sup>。这样的孕酮水平明显低于正常黄体期的孕酮水平——后者经 LC-MS 测定,介乎 7-22 ng/mL<sup>([Nakamoto, 2016][N16])</sup>。
|
||||
一些研究项目将以免疫测定法与其它更可靠方法测定的孕酮结果进行直接比较,发现免疫测定法下,孕酮水平会被高估 5-8 倍<sup>([Nahoul, Dehennin, & Scholler, 1987][NDS87]; [Nahoul & de Ziegler, 1994][NZ94]; [Levine & Watson, 2000][LW00]; [Kuhl, 2011][K11]; [Kuhl & Schneider, 2013][KS13]; [Davey, 2018][D18])</sup>。有一项包含几名受试者的小型研究,采用了多种已商业化的免疫测定法,其高估程度在 2 倍到 40 倍之间<sup>([Sapin et al., 2000][S00])</sup>。
|
||||
这些发现相当偏僻,在科研及医学界至今尚鲜为人知。但无论如何,可以肯定的是,口服孕酮所达到的孕酮水平远低于早年一度认为的那样,亦低于黄体期的水平——后者是女性倾向跨性别者在治疗过程中应该要达到的。
|
||||
|
||||
> 
|
||||
>
|
||||
> 「图三」已绝经妇女单次口服或经阴道给予孕酮(微粉化)之后,孕酮水平的变化(通过免疫测定法或 LC-MS 测得)<sup>([Levine & Watson, 2000][LW00]; [Kuhl & Schneider, 2013][KS13])</sup>。其中,口服孕酮后使用免疫测定法的结果受交叉反应影响,错误地偏高了。而以 LC-MS 测定的结果,和经阴道给药后的测定结果,可认为较准确。
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
> 
|
||||
>
|
||||
> 「图四」已绝经妇女饭后口服 100 mg/天的孕酮(微粉化)之后,孕酮水平的变化(通过 LC-MS 测得)<sup>([Lobo et al., 2019][L19])</sup>。其中,横向虚线表示 24 小时内的平均水平。饭后口服孕酮可将孕酮水平提升约 2-3 倍<sup>([Bijuva 药品说明书][FDA-1]; [Simon et al., 1993][S93])</sup>。本项目结果使用 LC-MS 测定,可认为较准确。
|
||||
**图 3**:已绝经妇女单次口服或经阴道给予孕酮(微粉化)之后,孕酮水平的变化(通过免疫测定法或 LC-MS 测得)<sup>([Levine & Watson, 2000][LW00]; [Kuhl & Schneider, 2013][KS13])</sup>。其中,口服孕酮后使用免疫测定法的结果受交叉反应影响,错误地偏高了。而以 LC-MS 测定的结果,和经阴道给药后的测定结果,可认为较准确。
|
||||
|
||||
## 临床表现
|
||||
</section>
|
||||
|
||||
### 孕激素效力与效应
|
||||
<section class="box">
|
||||
|
||||
数十年间,有一系列关于口服孕酮引起的孕激素临床效应的发现涌现了出来,其在当时令人费解;而今有了以更精确的测定方法得到的有关口服孕酮的数据,它们变得顺理成章了。临床医学上,口服孕酮多被用于更年期妇女,保护子宫内膜免受雌激素的不受控制的刺激,从而可避免雌激素引起的子宫内膜增生——即便是在临床上的通常剂量所达到孕酮水平较低的情况下<sup>([维基百科][WIKI-CIT-2])</sup>。不过,根据一项大型观察性研究,口服孕酮并不足以抑制由雌激素促成的子宫内膜癌之风险<sup>([Davey, 2018][D18])</sup>。即便采用超高剂量,口服孕酮仍无法促成子宫内膜的完全转化(黄体期内高孕酮水平所带来的正常效应);而经阴道给药或注射的孕酮则可有效促成转化<sup>([de Ziegler et al., 2013][Z13])</sup>。因此,和胃肠外给药不同,口服孕酮被认为不适合用于辅助生育<sup>([de Ziegler et al., 2013][Z13])</sup>。
|
||||
此外,对于顺性别男性,即便使用超高剂量(400 mg/天)的口服孕酮,亦未能压制其睾酮水平<sup>([Trollan et al., 1993][T93]; [维基百科][WIKI-CIT-3])</sup>。与此相反,顺性别男性使用直肠给药的孕酮、注射用孕酮与合成孕酮制剂,皆可实实在在地压制其睾酮水平<sup>([维基百科][WIKI-CIT-3]; [Aly W., 2019][AW19-CPA])</sup>。
|
||||

|
||||
|
||||
**图 4**:已绝经妇女饭后口服 100 mg/天的孕酮(微粉化)之后,孕酮水平的变化(通过 LC-MS 测得)<sup>([Lobo et al., 2019][L19])</sup>。其中,横向虚线表示 24 小时内的平均水平。饭后口服孕酮可将孕酮水平提升约 2-3 倍<sup>([Bijuva 药品说明书][FDA-1]; [Simon et al., 1993][S93])</sup>。本项目结果使用 LC-MS 测定,可认为较准确。
|
||||
|
||||
</section>
|
||||
|
||||
## 临床表现 {#therapeutic-implications}
|
||||
|
||||
### 孕激素效力与效应 {#progestogenic-potency-and-effects}
|
||||
|
||||
数十年间,有一系列关于口服孕酮引起的孕激素临床效应的发现涌现了出来,其在当时令人费解;而今有了以更精确的测定方法得到的有关口服孕酮的数据,它们变得顺理成章了。临床医学上,口服孕酮多被用于更年期妇女,保护子宫内膜免受雌激素的不受控制的刺激,从而可避免雌激素引起的子宫内膜增生——即便是在临床上的通常剂量所达到孕酮水平较低的情况下<sup>([维基百科][WIKI-CIT-2])</sup>。不过,根据一项大型观察性研究,口服孕酮并不足以抑制由雌激素促成的子宫内膜癌之风险<sup>([Davey, 2018][D18])</sup>。即便采用超高剂量,口服孕酮仍无法促成子宫内膜的完全转化(黄体期内高孕酮水平所带来的正常效应);而经阴道给药或注射的孕酮则可有效促成转化<sup>([de Ziegler et al., 2013][Z13])</sup>。因此,和胃肠外给药不同,口服孕酮被认为不适合用于辅助生育<sup>([de Ziegler et al., 2013][Z13])</sup>。
|
||||
此外,对于顺性别男性,即便使用超高剂量(400 mg/天)的口服孕酮,亦未能压制其睾酮水平<sup>([Trollan et al., 1993][T93]; [维基百科][WIKI-CIT-3])</sup>。与此相反,顺性别男性使用直肠给药的孕酮、注射用孕酮与合成孕酮制剂,皆可实实在在地压制其睾酮水平<sup>([维基百科][WIKI-CIT-3]; [Aly W., 2019][AW19-CPA])</sup>。
|
||||
对于更年期顺性别妇女,口服孕酮同样仅表现出了些微、以至无明显的抗促性腺激素效应,这亦和合成孕酮制剂的表现大相迥异<sup>([Holst, 1983][H83]; [Holst et al., 1983][H83-ET]; [Ottosson, 1984][O84]; [Maxson & Hargrove, 1985][MH85]; [Saarikoski, Yliskosk, & Penttilä, 1990][SYP90])</sup>。
|
||||
|
||||
目前认为,更年期妇女使用雌激素疗法时加入口服孕酮,并不会额外提高患[静脉血栓栓塞][wiki-16](VTE)的风险,这与其它临床上使用的孕酮情况不同<sup>([维基百科][WIKI-CIT-4])</sup>;其在短期(小于 5 年)的疗程内,也不会增加[乳腺癌][wiki-17]风险<sup>([维基百科][WIKI-CIT-5])</sup>。然而,在长期治疗(不小于 5 年)的情况下,使用雌激素与孕酮(口服)合并疗法的乳腺癌风险将显著高于单雌激素疗法——这与其它孕激素形式相似<sup>([Aly W., 2020][AW20]; [Sam S., 2020][SS20]; [维基百科][WIKI-CIT-6]; [表格][TABLE-1])</sup>。
|
||||
已有人评论道,由于口服孕酮对乳腺的增生作用很弱,其对乳腺癌风险之增长的作用需要更长的暴露时间方可显现,这与上述相一致<sup>([Kuhl & Schneider, 2013][KS13]; [Davey, 2018][D18])</sup>。有临床前研究也表明了孕酮及其受体的激活在乳腺当中有致癌性作用<sup>([Kuhl & Schneider, 2013][KS13]; [Trabert et al., 2020][T20])</sup>。
|
||||
目前认为,更年期妇女使用雌激素疗法时加入口服孕酮,并不会额外提高患[静脉血栓栓塞][wiki-16](VTE)的风险,这与其它临床上使用的孕酮情况不同<sup>([维基百科][WIKI-CIT-4])</sup>;其在短期(小于 5 年)的疗程内,也不会增加[乳腺癌][wiki-17]风险<sup>([维基百科][WIKI-CIT-5])</sup>。然而,在长期治疗(不小于 5 年)的情况下,使用雌激素与孕酮(口服)合并疗法的乳腺癌风险将显著高于单雌激素疗法——这与其它孕激素形式相似<sup>([Aly W., 2020][AW20]; [Sam S., 2020][SS20]; [维基百科][WIKI-CIT-6]; [表格][TABLE-1])</sup>。
|
||||
已有人评论道,由于口服孕酮对乳腺的增生作用很弱,其对乳腺癌风险之增长的作用需要更长的暴露时间方可显现,这与上述相一致<sup>([Kuhl & Schneider, 2013][KS13]; [Davey, 2018][D18])</sup>。有临床前研究也表明了孕酮及其受体的激活在乳腺当中有致癌性作用<sup>([Kuhl & Schneider, 2013][KS13]; [Trabert et al., 2020][T20])</sup>。
|
||||
以上有关口服孕酮对子宫内膜之效力、对睾酮与促性腺激素之压制、对静脉血栓与乳腺癌风险之影响的临床发现,和有关其它几乎所有临床使用的合成孕酮制剂的情况皆大相径庭(但表现类似于口服孕酮的制剂:[地屈孕酮][wiki-18]除外)。这种差别在早年曾令人费解,但如今发现口服孕酮所达成的孕酮水平相当低之后,一切都变得顺理成章。
|
||||
|
||||
### 生物利用度、半衰期与持续时间
|
||||
### 生物利用度、半衰期与持续时间 {#bioavailability-half-life-and-duration}
|
||||
|
||||
在一些采用更精确的测定方法的研究项目观察到口服孕酮所达到的水平远低于早年资料之后,有必要重新评估口服孕酮的生物利用度。在(早年)采用免疫测定法的研究当中,口服孕酮的生物利用度被报告大致为 10%<sup>([维基百科][WIKI-CIT-1])</sup>。至于其真实的生物利用度,由于迄今尚未有采用更可靠的测定方法的项目进行过(测量),故并未可知;无论如何,基于免疫测定法会将孕酮水平高估 5-8 倍的发现,可以估计其应接近于 1-2%。
|
||||
|
||||
|
|
@ -67,51 +86,59 @@
|
|||
|
||||
一些采用 LC-MS 等更可靠的测定方法的研究发现,口服孕酮的半衰期为 5-10 小时,而较高孕酮水平的维持时长仅有约 4-8 小时<sup>([维基百科][WIKI-CIT-7]; [图表][GRAPH-1])</sup>。这些发现也表明,口服孕酮的作用时长远小于早前所认为的那样。因此,如要使用口服孕酮,应建议每日分多次服用以维持稳定的孕酮暴露量。
|
||||
|
||||
### 高剂量口服孕酮与神经甾体副作用的关系
|
||||
### 高剂量口服孕酮与神经甾体副作用的关系 {#higher-oral-progesterone-doses-and-neurosteroid-side-effects}
|
||||
|
||||
使用高于常规剂量的口服孕酮,似乎会相应提高孕酮水平<sup>([表格][TABLE-2])</sup>。然而,既然已经从较可靠的测定方法知道了口服孕酮引起的孕酮水平有多低,那么可以确信,在大多数情况下,即便用超高剂量也不会有多高的孕酮水平。另外,使用高剂量口服孕酮会导致体内其神经甾体代谢物的水平变得很高,而这被发现会大大增强类似于酒精的副作用(即[对神经中枢的抑制][wiki-21]及其衍生效应)<sup>([维基百科1][WIKI-CIT-9]; [维基百科2][WIKI-CIT-10])</sup>。这些限制因素会让高剂量的口服孕酮变得不大可行。
|
||||
|
||||
> 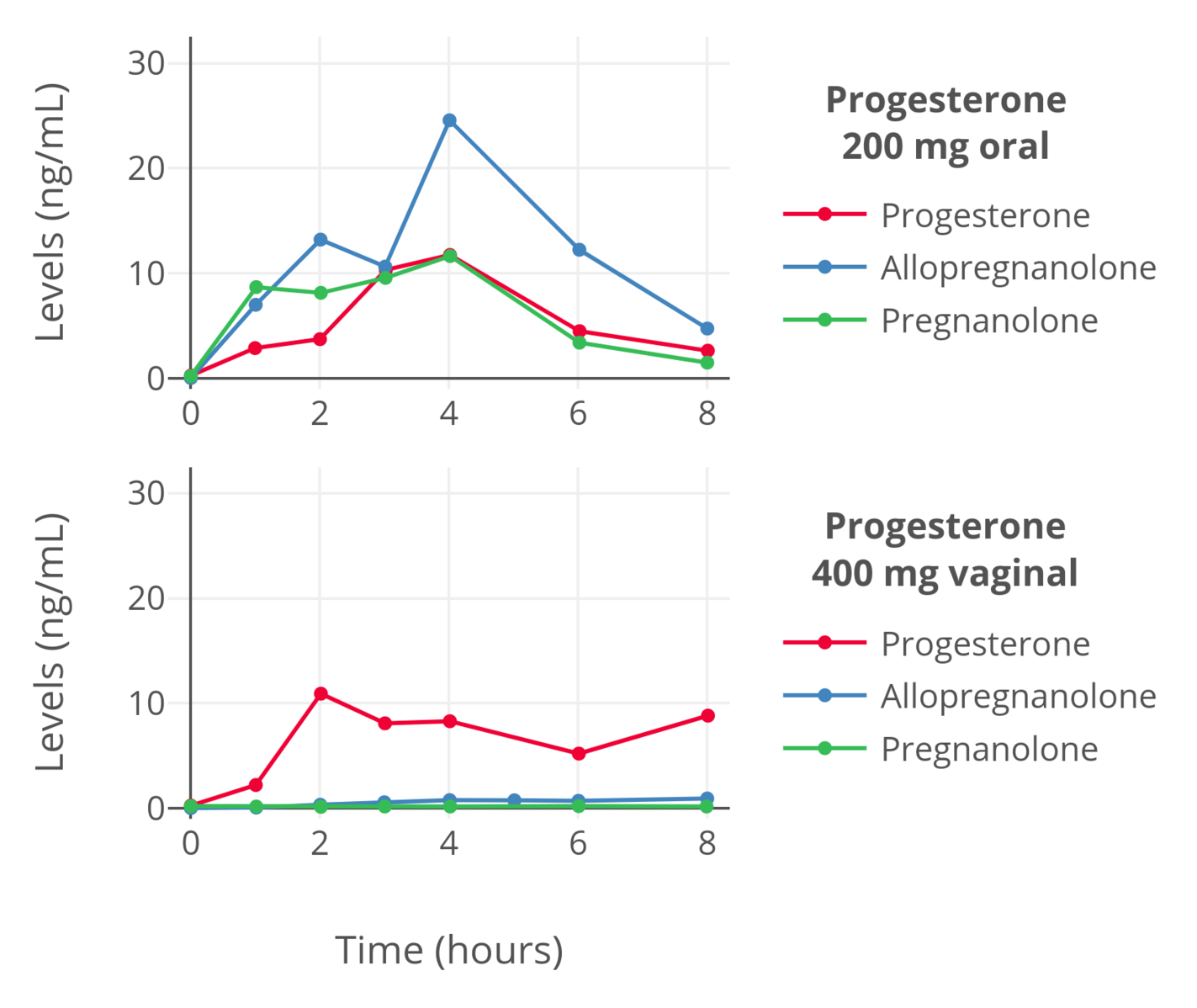
|
||||
>
|
||||
> 「图五」绝经前妇女单次口服(或经阴道给予栓剂)孕酮之后,体内孕酮、别孕烷醇酮和孕烷醇酮水平的变化<sup>([de Lignieres, Dennerstein, & Backstrom, 1995][LDB95])</sup>。其中,别孕烷醇酮和孕烷醇酮以质谱分析法测定,而孕酮则以经层析纯化的免疫测定法测定;故此,以上数据应当可靠。
|
||||
<section class="box">
|
||||
|
||||
## 关于口服孕酮之代谢物的补充
|
||||

|
||||
|
||||
口服孕酮在首过效应之后,孕酮水平之低与孕酮代谢物数量之高显得不成比例<sup>([Sitruk-Ware et al., 1987][SW87]; [de Lignieres, Dennerstein, & Backstrom, 1995][LDB95]; [de Lignieres, 1999][L99]; [de Ziegler & Fanchin, 2000][ZF00]; [Lobo, 2000][L00]; [Kuhl, 2005][K05])</sup>。此外,有一部分孕酮代谢物尽管在效力上远弱于孕酮,但其孕激素活性被发现和孕酮本身相当<sup>(例如 [Besch et al., 1965][B65]; [Junkermann, Runnebaum, & Lisboa, 1977][JRL77]; [Lobo, 2000][L00])</sup>。其活性来源有两方面:其本身固有的孕激素活性;或者其又被转化成孕酮或其它孕酮代谢物(这属于某些组织的[胞内][wiki-22]活动的一部分,例如子宫)。这些代谢物包括:[20α-二氢孕酮][wiki-23]、[20β-二氢孕酮][wiki-24]、[5α-二氢孕酮][wiki-12]、[3β-二氢孕酮][wiki-25]、[别孕烷醇酮][wiki-3]和 [11-去氧皮质酮][wiki-26]等等。
|
||||
如果口服孕酮可以通过代谢物产生大部分孕激素活性,那么其孕激素作用强度会大于其在孕酮水平上所体现的那样;然而,这仅仅存在理论可能,而且迄今罕有文献对此加以讨论。尚需更多研究来确定口服孕酮之代谢物是否真的会在口服孕酮效力上发挥一定作用。
|
||||
**图 5**:绝经前妇女单次口服(或经阴道给予栓剂)孕酮之后,体内孕酮、别孕烷醇酮和孕烷醇酮水平的变化<sup>([de Lignieres, Dennerstein, & Backstrom, 1995][LDB95])</sup>。其中,别孕烷醇酮和孕烷醇酮以质谱分析法测定,而孕酮则以经层析纯化的免疫测定法测定;故此,以上数据应当可靠。
|
||||
|
||||
</section>
|
||||
|
||||
## 关于口服孕酮之代谢物的补充 {#a-note-on-oral-progesterones-metabolites}
|
||||
|
||||
口服孕酮在首过效应之后,孕酮水平之低与孕酮代谢物数量之高显得不成比例<sup>([Sitruk-Ware et al., 1987][SW87]; [de Lignieres, Dennerstein, & Backstrom, 1995][LDB95]; [de Lignieres, 1999][L99]; [de Ziegler & Fanchin, 2000][ZF00]; [Lobo, 2000][L00]; [Kuhl, 2005][K05])</sup>。此外,有一部分孕酮代谢物尽管在效力上远弱于孕酮,但其孕激素活性被发现和孕酮本身相当<sup>(例如 [Besch et al., 1965][B65]; [Junkermann, Runnebaum, & Lisboa, 1977][JRL77]; [Lobo, 2000][L00])</sup>。其活性来源有两方面:其本身固有的孕激素活性;或者其又被转化成孕酮或其它孕酮代谢物(这属于某些组织的[胞内][wiki-22]活动的一部分,例如子宫)。这些代谢物包括:[20α-二氢孕酮][wiki-23]、[20β-二氢孕酮][wiki-24]、[5α-二氢孕酮][wiki-12]、[3β-二氢孕酮][wiki-25]、[别孕烷醇酮][wiki-3]和 [11-去氧皮质酮][wiki-26]等等。
|
||||
如果口服孕酮可以通过代谢物产生大部分孕激素活性,那么其孕激素作用强度会大于其在孕酮水平上所体现的那样;然而,这仅仅存在理论可能,而且迄今罕有文献对此加以讨论。尚需更多研究来确定口服孕酮之代谢物是否真的会在口服孕酮效力上发挥一定作用。
|
||||
无论如何,基于临床对口服孕酮的孕激素效应之研究,其依旧是效力相对较弱的一种孕激素形式。
|
||||
|
||||
## 口服孕酮的替代选项
|
||||
## 口服孕酮的替代选项 {#alternative-options-to-oral-progesterone}
|
||||
|
||||
### 非口服形式的孕酮
|
||||
### 非口服形式的孕酮 {#non-oral-forms-of-progesterone}
|
||||
|
||||
诸如[阴道栓剂][wiki-27]、[直肠栓剂][wiki-28]、[舌下含服制剂][WIKI-CIT-13]以及[注射剂][WIKI-CIT-16]等非口服形式的孕酮,已知可达到远高于口服的孕酮水平<sup>([维基百科][WIKI-CIT-11])</sup>。它们可取代口服孕酮使用,以达到更高、更合适的孕酮水平。然而很遗憾,它们尽管有更高效力,但也有各自的限制因素。
|
||||
|
||||
首先是[孕酮阴道栓剂][wiki-27]:对于女性倾向跨性别者,如未进行[阴道成形术][wiki-29],其显然无法使用之;即便经过手术,其[新阴道][wiki-30]的内壁亦并非正常的阴道粘膜,而是皮瓣([阴茎翻转法][wiki-29-piv])或肠壁([乙状结肠移植法][wiki-31])。因此,经新阴道给药的吸收特征可能和(原生)阴道的情况不同<sup>([Aly W., 2018][AW18-INTRO])</sup>。需要指出,[透皮给予孕酮][WIKI-CIT-12]所达到的孕酮水平,和口服同样低,故而其并非孕酮治疗的一个好选项<sup>([维基百科][WIKI-CIT-12]; [Hermann et al., 2005][H05]; [图表][GRAPH-2])</sup>。如以阴茎翻转法再造阴道,当使用孕酮阴道栓剂时,应该仅可达到很低的孕酮水平。
|
||||
|
||||
其次是[孕酮直肠栓剂][wiki-28]:其可达到和正常黄体期一样高的孕酮水平,是一种不错的给药途径。不过,其给药后作用时长稍短,可能需要一日使用两次以维持孕酮水平稳定。
|
||||
更大的问题在于,目前世界上由制药厂出品的孕酮直肠栓剂供应有限,在大部分国家均未上市<sup>([维基百科][WIKI-CIT-15])</sup>。不过,一些国家的[配药房][wiki-32]可制作此类栓剂。
|
||||
另外,可以轻松获得的孕酮口服胶囊,在用于阴道给药时取得了成功<sup>([Miles et al., 1994][M94]; [Wang et al., 2019][W19])</sup>。孕酮口服胶囊用于直肠给药的形式显然卓有成效,也可达到远高于口服的孕酮水平,颇似直肠栓剂<sup>([Aly W., 2019][AW19-RECT])</sup>。然而,这种应用形式尚未经过正式研究,而一些女性倾向跨性别者亦报告了以此法仅可获得很低的孕酮水平。
|
||||
其次是[孕酮直肠栓剂][wiki-28]:其可达到和正常黄体期一样高的孕酮水平,是一种不错的给药途径。不过,其给药后作用时长稍短,可能需要一日使用两次以维持孕酮水平稳定。
|
||||
更大的问题在于,目前世界上由制药厂出品的孕酮直肠栓剂供应有限,在大部分国家均未上市<sup>([维基百科][WIKI-CIT-15])</sup>。不过,一些国家的[配药房][wiki-32]可制作此类栓剂。
|
||||
另外,可以轻松获得的孕酮口服胶囊,在用于阴道给药时取得了成功<sup>([Miles et al., 1994][M94]; [Wang et al., 2019][W19])</sup>。孕酮口服胶囊用于直肠给药的形式显然卓有成效,也可达到远高于口服的孕酮水平,颇似直肠栓剂<sup>([Aly W., 2019][AW19-RECT])</sup>。然而,这种应用形式尚未经过正式研究,而一些女性倾向跨性别者亦报告了以此法仅可获得很低的孕酮水平。
|
||||
直肠栓剂尽管很高效,但使用(尤其是长期使用)则较为不便。不过无论如何,在非口服途径的孕酮形式当中,直肠栓剂或为最优之选。
|
||||
|
||||
> 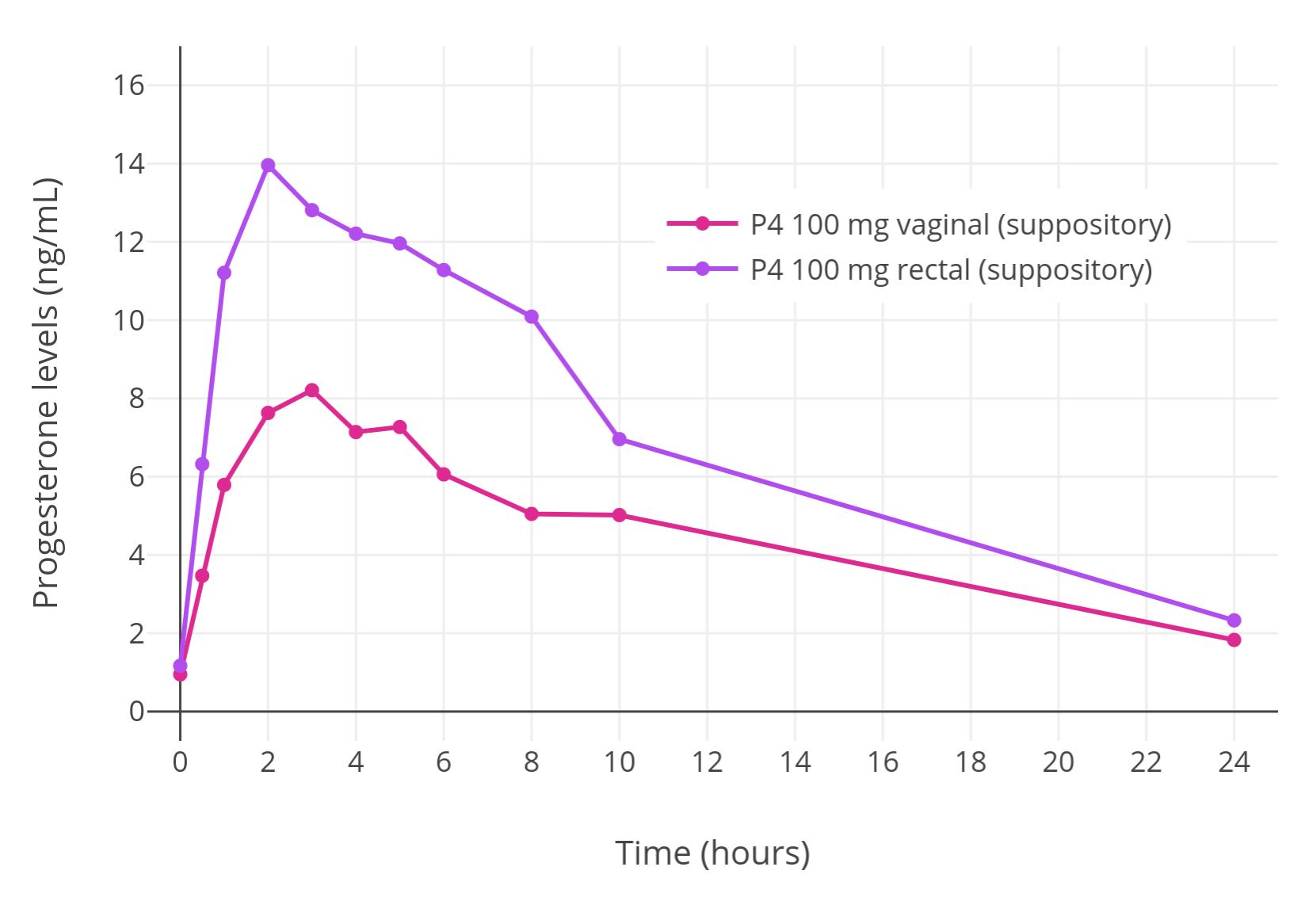
|
||||
>
|
||||
> 「图六」绝经前妇女单次经直肠或阴道给予 100 mg 孕酮栓剂之后,孕酮水平的变化<sup>([Chakmakjian & Zachariah, 1987][CZ87])</sup>。
|
||||
<section class="box">
|
||||
|
||||
再次是[舌下含服的孕酮][WIKI-CIT-13]:其可达到较高的、比口服更接近生理的孕酮水平,但维持高水平的时长也较短,每日需分多次服用<sup>([维基百科][WIKI-CIT-13]; [图表][GRAPH-3])</sup>。另外,早年其曾于全球广泛上市<sup>([维基百科][WIKI-CIT-14])</sup>,而今仅在一些东欧国家可用<sup>([维基百科][WIKI-CIT-15])</sup>。不过,某些国家的药店可能亦有售。
|
||||

|
||||
|
||||
**图 6**:绝经前妇女单次经直肠或阴道给予 100 mg 孕酮栓剂之后,孕酮水平的变化<sup>([Chakmakjian & Zachariah, 1987][CZ87])</sup>。
|
||||
|
||||
</section>
|
||||
|
||||
再次是[舌下含服的孕酮][WIKI-CIT-13]:其可达到较高的、比口服更接近生理的孕酮水平,但维持高水平的时长也较短,每日需分多次服用<sup>([维基百科][WIKI-CIT-13]; [图表][GRAPH-3])</sup>。另外,早年其曾于全球广泛上市<sup>([维基百科][WIKI-CIT-14])</sup>,而今仅在一些东欧国家可用<sup>([维基百科][WIKI-CIT-15])</sup>。不过,某些国家的药店可能亦有售。
|
||||
迄今已有人描述了口服(微粉化)孕酮用于舌下含服的经过,而此用法尚未被正式研究过;不过,考虑到口服孕酮的剂型是油悬浮液胶囊,其用于舌下含服并不容易。因此,舌下含服口服用(微粉化)孕酮看来有难度,可能也不大舒适。
|
||||
|
||||
最后是孕酮注射剂([肌注][WIKI-CIT-16]或[皮下注射][WIKI-CIT-17]):其可轻松达到相当高的孕酮水平<sup>([维基百科1][WIKI-CIT-16]; [多图表1][GRAPH-4]; [维基百科2][WIKI-CIT-17]; [图表2][GRAPH-4])</sup>,但孕酮维持时间在诸性激素注射剂当中较短,每 1-3 日便需注射一次。对多数人而言(尤其是长期用药者),如此注射间隔显然过于频繁。此外,相较肌注更为方便的、用于皮下注射的孕酮,供应很有限,目前基本仅在欧洲上市<sup>([维基百科][WIKI-CIT-15])</sup>。
|
||||
最后是孕酮注射剂([肌注][WIKI-CIT-16]或[皮下注射][WIKI-CIT-17]):其可轻松达到相当高的孕酮水平<sup>([维基百科1][WIKI-CIT-16]; [多图表1][GRAPH-4]; [维基百科2][WIKI-CIT-17]; [图表2][GRAPH-4])</sup>,但孕酮维持时间在诸性激素注射剂当中较短,每 1-3 日便需注射一次。对多数人而言(尤其是长期用药者),如此注射间隔显然过于频繁。此外,相较肌注更为方便的、用于皮下注射的孕酮,供应很有限,目前基本仅在欧洲上市<sup>([维基百科][WIKI-CIT-15])</sup>。
|
||||
由于孕酮无任何可供结合为酯的羟基团,因此也不可能合成[孕酮酯][wiki-33],这种酯本应具有更佳的脂溶性、并在注射后延长孕酮维持时间;此性质与雌二醇、睾酮等其它性激素截然不同。除此之外,孕酮水悬浮液注射剂曾因其维持时长远甚于当下正在使用的油溶液、水溶液注射剂,而上市了一段时间<sup>([维基百科1][WIKI-CIT-18]; [维基百科2][WIKI-CIT-19]; [Aly W., 2019][AW19-AQU])</sup>;但其代价是注射位点会引起疼痛等不适,从而导致其退市。不过,当下在一些东欧国家,似乎尚可见到孕酮水悬浮液注射剂在使用<sup>([Aly W., 2019][AW19-AQU])</sup>。
|
||||
|
||||
### 合成孕酮制剂
|
||||
### 合成孕酮制剂 {#progestins-as-alternative-progestogens}
|
||||
|
||||
[合成孕酮制剂][wiki-34]可代替孕酮使用<sup>([Aly W., 2018][AW18-INTRO])</sup>。其中一些存在[脱靶效应][wiki-35](例如较弱的[雄激素][wiki-36]/[糖皮质激素][wiki-37]活性),从而不适合用于女性化激素疗法;这些制剂包括[醋酸甲羟孕酮][wiki-38]和大多数 [19-去甲睾酮][wiki-39]类似物(如[炔诺酮][wiki-40]、[左炔诺孕酮][wiki-41])等<sup>([Kuhl, 2005][K05]; [Aly W., 2018][AW18-INTRO])</sup>。
|
||||
不过,有许多其它合成孕酮具备更适合用于该疗法的特性,问题也更少;例如[醋酸环丙孕酮][wiki-42](低剂量)<sup>([Aly W., 2019][AW19-CPA])</sup>、[屈螺酮][wiki-43]、[地诺孕素][wiki-44]、[醋酸诺美孕酮][wiki-45]、[己酸羟孕酮][wiki-46]和[苯乙酮缩二羟孕酮][wiki-47]等<sup>([Kuhl, 2005][K05])</sup>。上述制剂均不表现除孕激素之外的任何不良生理活性<sup>([Kuhl, 2005][K05])</sup>。
|
||||
另外,还有一种叫[地屈孕酮][wiki-18]的合成制剂,其虽无任何不利的生理活性,但却表现出不寻常的孕激素特性,无法确保能够提供和非口服途径的孕酮、或其它类型孕激素相当的完全孕激素效力<sup>([维基百科][WIKI-CIT-20])</sup>。
|
||||
[合成孕酮制剂][wiki-34]可代替孕酮使用<sup>([Aly W., 2018][AW18-INTRO])</sup>。其中一些存在[脱靶效应][wiki-35](例如较弱的[雄激素][wiki-36]/[糖皮质激素][wiki-37]活性),从而不适合用于女性化激素疗法;这些制剂包括[醋酸甲羟孕酮][wiki-38]和大多数 [19-去甲睾酮][wiki-39]类似物(如[炔诺酮][wiki-40]、[左炔诺孕酮][wiki-41])等<sup>([Kuhl, 2005][K05]; [Aly W., 2018][AW18-INTRO])</sup>。
|
||||
不过,有许多其它合成孕酮具备更适合用于该疗法的特性,问题也更少;例如[醋酸环丙孕酮][wiki-42](低剂量)<sup>([Aly W., 2019][AW19-CPA])</sup>、[屈螺酮][wiki-43]、[地诺孕素][wiki-44]、[醋酸诺美孕酮][wiki-45]、[己酸羟孕酮][wiki-46]和[苯乙酮缩二羟孕酮][wiki-47]等<sup>([Kuhl, 2005][K05])</sup>。上述制剂均不表现除孕激素之外的任何不良生理活性<sup>([Kuhl, 2005][K05])</sup>。
|
||||
另外,还有一种叫[地屈孕酮][wiki-18]的合成制剂,其虽无任何不利的生理活性,但却表现出不寻常的孕激素特性,无法确保能够提供和非口服途径的孕酮、或其它类型孕激素相当的完全孕激素效力<sup>([维基百科][WIKI-CIT-20])</sup>。
|
||||
目前尚无任何合成孕酮会产生神经甾体代谢物及其衍生反应,这点与孕酮相反<sup>([Kuhl, 2005][K05])</sup>。
|
||||
|
||||
## 总结
|
||||
## 总结 {#summary-and-conclusions}
|
||||
|
||||
总的而言,临床剂量下的口服孕酮仅可达到很低的孕酮水平,其孕激素效力也远弱于生理所需的水平。尽管加大其剂量似乎能提高体内孕酮水平,但事实上孕酮水平仍维持低值,而且伴随而来的神经甾体之副作用会更大、更难以承受,从而使此法变得不可行。
|
||||
|
||||
|
|
@ -119,27 +146,66 @@
|
|||
|
||||
准确来说,口服孕酮大体上应该归类为一种具有较弱孕激素效力的强效神经甾体前体药。与此相反,非口服途径的孕酮、以及合成孕酮制剂,皆可视为强效孕激素——前者具有生理强度的神经甾体效力,后者则无。
|
||||
|
||||
## 扩展阅读材料
|
||||
## 扩展阅读材料 {#additional-reading}
|
||||
|
||||
### 相关文献
|
||||
### 相关文献 {#literature}
|
||||
|
||||
本文所引用资料来源、文献等,已汇总于[此处][APPENDIX];其中,某些文献被本文引用,以讨论有关测量问题、以及口服孕酮后体内水平之低的话题,此处将其引用片段列出。
|
||||
|
||||
### 外部链接
|
||||
### 外部链接 {#external-links}
|
||||
|
||||
- [孕酮的药代动力学:口服孕酮 - 维基百科(英文)][WIKI-CIT-21]
|
||||
- [图集:使用口服孕酮之后的激素水平变化 - 维基百科(英文)][GRAPH-1]
|
||||
|
||||
## 参考文献
|
||||
## 参考文献 {#references}
|
||||
|
||||
略
|
||||
- Besch, P. K., Barry, R. D., Vorys, N., Stevens, V., & Ullery, J. C. (1965). A review of some aspects of the metabolism of progestational agents. _Metabolism_, _14_(3), 432–443. \[DOI:<https://doi.org/10.1016/0026-0495(65)90031-4>\]
|
||||
- _Bijuva Estradiol/Progesterone Label._ U.S. Food and Drug Administration. \[[URL](http://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&varApplNo=210132)\] \[[PDF](https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/210132s000lbl.pdf)\]
|
||||
- Chakmakjian, Z. H., & Zachariah, N. Y. (1987). Bioavailability of progesterone with different modes of administration. _The Journal of Reproductive Medicine_, _32_(6), 443–448. \[[Google Scholar](https://scholar.google.com/scholar?cluster=12162342847012788095)\] \[[PubMed](https://pubmed.ncbi.nlm.nih.gov/3612635/)\] \[[PDF](https://files.transfemscience.org/pdfs/Chakmakjian%20&%20Zachariah%20(1987)%20-%20Bioavailability%20of%20Progesterone%20with%20Different%20Modes%20of%20Administration.pdf)\]
|
||||
- Conklin, S. E., & Knezevic, C. E. (2020). Advancements in the gold standard: Measuring steroid sex hormones by mass spectrometry. _Clinical Biochemistry_, _82_, 21–32. \[DOI:<https://doi.org/10.1016/j.clinbiochem.2020.03.008>\]
|
||||
- Davey, D. A. (2018). Menopausal hormone therapy: a better and safer future. _Climacteric_, _21_(5), 454–461. \[DOI:<https://doi.org/10.1080/13697137.2018.1439915>\]
|
||||
- de Lignières, B., Dennerstein, L., & Backstrom, T. (1995). Influence of route of administration on progesterone metabolism. _Maturitas_, _21_(3), 251–257. \[DOI:<https://doi.org/10.1016/0378-5122(94)00882-8>\]
|
||||
- de Lignières, B. (1999). Oral micronized progesterone. _Clinical Therapeutics_, _21_(1), 41–60. \[DOI:<https://doi.org/10.1016/S0149-2918(00)88267-3>\]
|
||||
- de Ziegler, D., & Fanchin, R. (2000). Progesterone and progestins: applications in gynecology. _Steroids_, _65_(10–11), 671–679. \[DOI:<https://doi.org/10.1016/S0039-128X(00)00123-9>\]
|
||||
- de Ziegler, D., Streuli, I., Marszalek, A., Gayet, V., & Chapron, C. (2013). Preparing the Endometrium to Maximize Success: The Dynamics of Artificial Cycles. In Sauer, M. V. (Ed.). _Principles of Oocyte and Embryo Donation, 2nd Edition_ (pp. 109–127). London: Springer. \[DOI:<https://doi.org/10.1007/978-1-4471-2392-7_9>\]
|
||||
- Hermann, A. C., Nafziger, A. N., Victory, J., Kulawy, R., Rocci Jr, M. L., & Bertino Jr, J. S. (2005). Over‐the‐Counter Progesterone Cream Produces Significant Drug Exposure Compared to a Food and Drug Administration‐Approved Oral Progesterone Product. _The Journal of Clinical Pharmacology_, _45_(6), 614–619. \[DOI:<https://doi.org/10.1177/0091270005276621>\]
|
||||
- Holst, J. (1983). Percutaneous estrogen therapy: Endometrial response and metabolic effects. _Acta Obstetricia et Gynecologica Scandinavica_, _62_(Suppl 115), 4–30. \[DOI:<https://doi.org/10.3109/00016348309155363>\]
|
||||
- Holst, J., Cajander, S., Carlström, K., Damber, M. G., & von Schoultz, B. (1983). Percutaneous oestrogen therapy opposed by lynestrenol or natural progesterone-effects on circulating oestrogens, FSH, sex hormone binding globulin and pregnancy zone protein. _Maturitas_, _5_(1), 1–8. \[DOI:<https://doi.org/10.1016/0378-5122(83)90015-4>\]
|
||||
- Junkermann, H., Runnebaum, B., & Lisboa, B. P. (1977). New progesterone metabolites in human myometrium. _Steroids_, _30_(1), 1–14. \[DOI:<https://doi.org/10.1016/0039-128X(77)90131-3>\]
|
||||
- Kuhl, H. (2005). Pharmacology of Estrogens and Progestogens: Influence of Different Routes of Administration. _Climacteric_, _8_(Suppl 1), 3–63. \[DOI:<http://doi.org/10.1080/13697130500148875>\] \[[PDF](http://hormonebalance.org/images/documents/Kuhl%2005%20%20Pharm%20Estro%20Progest%20Climacteric_1311166827.pdf)\]
|
||||
- Kuhl, H. (2011). Pharmacology of progestogens. _Journal für Reproduktionsmedizin und Endokrinologie_ \[_Journal of Reproductive Medicine and Endocrinology_\], _8_(1), 157–177. \[[URL](https://www.kup.at/journals/summary/10168.html)\]
|
||||
- Kuhl, H., & Schneider, H. P. G. (2013). Progesterone–promoter or inhibitor of breast cancer. _Climacteric_, _16_(Suppl 1), 54–68. \[DOI:<https://doi.org/10.3109/13697137.2013.768806>\]
|
||||
- Lobo, R. A. (2000). Progestogens. In Lobo, R. A., Kelsey, J., & Marcus, R. (Eds.). _Menopause: Biology and Pathobiology_ (pp. 429–444). Burlington: Academic Press. \[[Google Books](https://books.google.com/books?id=i9HXKhjvNVAC&pg=PA433)\]
|
||||
- Lobo, R. A., Liu, J., Stanczyk, F. Z., Constantine, G. D., Pickar, J. H., Shadiack, A. M., Bernick, B., & Mirkin, S. (2019). Estradiol and progesterone bioavailability for moderate to severe vasomotor symptom treatment and endometrial protection with the continuous-combined regimen of TX-001HR (oral estradiol and progesterone capsules). _Menopause (New York, NY)_, _26_(7), 720–727.\[DOI:<http://doi.org/10.1097/GME.0000000000001306>\]
|
||||
- Levine, H., & Watson, N. (2000). Comparison of the pharmacokinetics of Crinone 8% administered vaginally versus Prometrium administered orally in postmenopausal women. _Fertility and Sterility_, _73_(3), 516–521. \[DOI:<https://doi.org/10.1016/S0015-0282(99)00553-1>\]
|
||||
- Maxson, W. S., & Hargrove, J. T. (1985). Bioavailability of oral micronized progesterone. _Fertility and Sterility_, _44_(5), 622–626. \[DOI:<https://doi.org/10.1016/S0015-0282(16)48977-6>\]
|
||||
- Miles, R. A., Paulson, R. J., Lobo, R. A., Press, M. F., Dahmoush, L., & Sauer, M. V. (1994). Pharmacokinetics and endometrial tissue levels of progesterone after administration by intramuscular and vaginal routes: a comparative study. _Fertility and Sterility_, _62_(3), 485–490. \[DOI:<https://doi.org/10.1016/S0015-0282(16)56935-0>\]
|
||||
- Nahoul, K., Dehennin, L., & Scholler, R. (1987). Radioimmunoassay of plasma progesterone after oral administration of micronized progesterone. _Journal of Steroid Biochemistry_, _26_(2), 241–249. \[DOI:<https://doi.org/10.1016/0022-4731(87)90078-1>\]
|
||||
- Nahoul, K., Dehennin, L., Jondet, M., & Roger, M. (1993). Profiles of plasma estrogens, progesterone and their metabolites after oral or vaginal administration of estradiol or progesterone. _Maturitas_, _16_(3), 185–202. \[DOI:<https://doi.org/10.1016/0378-5122(93)90064-O>\]
|
||||
- Nahoul, K., & de Ziegler, D. (1994). “ Validity” of serum progesterone levels after oral progesterone. _Fertility and Sterility_, _61_(4), 790–792. \[DOI:<https://doi.org/10.1016/S0015-0282(16)56666-7>\]
|
||||
- Nakamoto, J. (2016). Endocrine Testing. In Jameson, J. L., & De Groot, L. J. (Eds.). _Endocrinology: Adult and Pediatric, 7th Edition_ (pp. 2655–2688.e1). Philadelphia: Saunders/Elsevier. \[DOI:<https://doi.org/10.1016/B978-0-323-18907-1.00154-2>\]
|
||||
- Ottosson, U. B. (1984). Oral progesterone and estrogen/progestogen therapy: effects of natural and synthetic hormones on subfractions of HDL cholesterol and liver proteins. _Acta Obstetricia et Gynecologica Scandinavica_, _63_(Suppl 127), 1–37. \[DOI:<https://doi.org/10.3109/00016348409157016>\]
|
||||
- Pickar, J. H., Bon, C., Amadio, J. M., Mirkin, S., & Bernick, B. (2015). Pharmacokinetics of the first combination 17β-estradiol/progesterone capsule in clinical development for menopausal hormone therapy. _Menopause (New York, NY)_, _22_(12), 1308–1316. \[DOI:[10.1097/GME.0000000000000467](https://dx.doi.org/10.1097%2FGME.0000000000000467)\]
|
||||
- Prometrium FDA Review 1996. _Application Number: NDA 19-781. Clinical Pharmacology and Biopharmaceutics Review(s) \[Prometrium\]._ Center for Drug Evaluation and Research, U.S. Food and Drug Administration. \[[PDF](https://www.accessdata.fda.gov/drugsatfda_docs/nda/98/19781-clinpharm.pdf)\]
|
||||
- Saarikoski, S., Yliskosk, M., & Penttilä, I. (1990). Sequential use of norethisterone and natural progesterone in pre-menopausal bleeding disorders. _Maturitas_, _12_(2), 89–97. \[DOI:<https://doi.org/10.1016/0378-5122(90)90086-L>\]
|
||||
- Sapin, R., Neamtu, D., Gasser, F., Ohl, J., Grunenberger, F., & Grucker, D. (2000). De la prudence lors de l’utilisation des dosages directs de progestérone. \[Caution when using direct progesterone assays.\] _Immuno-analyse et Biologie Spécialisée_, _3_(15), 203–204. \[DOI:<https://doi.org/10.1016/S0923-2532(00)80010-1>\] \[[Translation](https://docs.google.com/document/d/1Udo41d1uu2ezjsHIl7v3eIelxZCuhMJofLbeN63yEvM/view)\]
|
||||
- Simon, J. A., Robinson, D. E., Andrews, M. C., Hildebrand III, J. R., Rocci Jr, M. L., Blake, R. E., & Hodgen, G. D. (1993). The absorption of oral micronized progesterone: the effect of food, dose proportionality, and comparison with intramuscular progesterone. _Fertility and Sterility_, _60_(1), 26–33. \[DOI:<https://doi.org/10.1016/S0015-0282(16)56031-2>\]
|
||||
- Sitruk-Ware, R., Bricaire, C., De Lignieres, B., Yaneva, H., & Mauvais-Jarvis, P. (1987). Oral micronized progesterone: Bioavailability pharmacokinetics, pharmacological and therapeutic implications—A review. _Contraception_, _36_(4), 373–402. \[DOI:<https://doi.org/10.1016/0010-7824(87)90088-6>\]
|
||||
- Stricker, R., Eberhart, R., Chevailler, M. C., Quinn, F. A., Bischof, P., & Stricker, R. (2006). Establishment of detailed reference values for luteinizing hormone, follicle stimulating hormone, estradiol, and progesterone during different phases of the menstrual cycle on the Abbott ARCHITECT® analyzer. _Clinical Chemistry and Laboratory Medicine (CCLM)_, _44_(7), 883–887. \[DOI:<https://doi.org/10.1515/CCLM.2006.160>\]
|
||||
- Tollan, A., Øian, P., Kjeldsen, S. E., Eide, I., & Maltau, J. M. (1993). Progesterone reduces sympathetic tone without changing blood pressure or fluid balance in men. _Gynecologic and Obstetric Investigation_, _36_(4), 234–238. \[DOI:<https://doi.org/10.1159/000292636>\]
|
||||
- Trabert, B., Sherman, M. E., Kannan, N., & Stanczyk, F. Z. (2020). Progesterone and breast cancer. _Endocrine Reviews_, _41_(2), 320–344. \[DOI:<https://doi.org/10.1210/endrev/bnz001>\]
|
||||
- Wang, H., Liu, M., Fu, Q., & Deng, C. (2019). Pharmacokinetics of hard micronized progesterone capsules via vaginal or oral route compared with soft micronized capsules in healthy postmenopausal women: a randomized open-label clinical study. _Drug Design, Development and Therapy_, _13_, 2475–2482. \[DOI:<https://doi.org/10.2147/dddt.s204624>\]
|
||||
- Woodward, G. M., & Rumsby, G. (2019). Steroid Profiling: Analytical Perspectives. In Rumsby, G., Woodward, G. M. (Eds.). _Disorders of Steroidogenesis: Guide to Steroid Profiling and Biochemical Diagnosis_ (pp. 27–40). Cham: Springer. \[DOI:<https://doi.org/10.1007/978-3-319-96364-8_3>\]
|
||||
|
||||
--------
|
||||
|
||||
## 译文修订历史
|
||||
## 译文修订历史 {#revise-history}
|
||||
|
||||
- 2022 年 10 月 11 日——首次翻译。
|
||||
- 2022 年 11 月 18 日——**更正 progesterone(孕酮)的名称**,增补一条新引用的文献(Wang et al., 2019),加入若干指向维基百科的链接。
|
||||
```csv
|
||||
时间,备注
|
||||
2022 年 10 月 11 日,首次翻译。
|
||||
2022 年 11 月 18 日,"**更正 progesterone(孕酮)的名称**,增补一条新引用的文献(Wang et al., 2019),加入若干指向维基百科的链接。"
|
||||
```
|
||||
|
||||
[LDB95]: https://doi.org/10.1016/0378-5122(94)00882-8
|
||||
[S93]: https://doi.org/10.1016/S0015-0282(16)56031-2
|
||||
|
|
@ -165,7 +231,7 @@
|
|||
[Z13]: https://doi.org/10.1007/978-1-4471-2392-7_9
|
||||
[T93]: https://doi.org/10.1159/000292636
|
||||
[WIKI-CIT-3]: https://en.wikipedia.org/wiki/Pharmacodynamics_of_progesterone#Antigonadotropic_effects
|
||||
[AW19-CPA]: cpa-dosage.md
|
||||
[AW19-CPA]: https://transfemscience.org/articles/cpa-dosage/
|
||||
[H83]: https://doi.org/10.3109/00016348309155363
|
||||
[H83-ET]: https://doi.org/10.1016/0378-5122(83)90015-4
|
||||
[O84]: https://doi.org/10.3109/00016348409157016
|
||||
|
|
@ -173,7 +239,7 @@
|
|||
[SYP90]: https://doi.org/10.1016/0378-5122(90)90086-L
|
||||
[WIKI-CIT-4]: https://en.wikipedia.org/wiki/Progestogen_(medication)#Blood_clots
|
||||
[WIKI-CIT-5]: https://en.wikipedia.org/wiki/Progestogen_(medication)#Breast_cancer_2
|
||||
[AW20]: breast-cancer.md
|
||||
[AW20]: https://transfemscience.org/articles/breast-cancer/
|
||||
[SS20]: https://transfemscience.org/articles/progestogens-breast-cancer/
|
||||
[WIKI-CIT-6]: https://en.wikipedia.org/wiki/Progesterone_(medication)#Breast_cancer
|
||||
[TABLE-1]: https://en.wikipedia.org/wiki/Template:Worldwide_epidemiological_evidence_on_breast_cancer_risk_with_menopausal_hormone_therapy
|
||||
|
|
@ -210,18 +276,16 @@
|
|||
[WIKI-CIT-16]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_progesterone#Intramuscular_injection
|
||||
[GRAPH-4]: https://en.wikipedia.org/wiki/Template:Hormone_levels_with_progesterone_by_intramuscular_injection
|
||||
[WIKI-CIT-17]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_progesterone#Subcutaneous_injection
|
||||
[GRAPH-5]: https://commons.wikimedia.org/wiki/File:Progesterone_levels_after_a_single_subcutaneous_injection_of_different_doses_of_an_aqueous_solution_of_progesterone_complexed_with_%CE%B2-cyclodextrin_in_postmenopausal_women.png
|
||||
[WIKI-CIT-18]: https://en.wikipedia.org/wiki/Progesterone_(medication)#Injections_and_implants
|
||||
[WIKI-CIT-19]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_progesterone#Aqueous_suspensions
|
||||
[AW19-AQU]: https://transfemscience.org/articles/aqueous-suspensions/
|
||||
|
||||
[AW18-INTRO]: transfem-intro.md#孕激素介绍
|
||||
[AW18-INTRO]: https://transfemscience.org/articles/transfem-intro/#progestogens
|
||||
[WIKI-CIT-20]: https://en.wikipedia.org/wiki/Dydrogesterone#Atypical_progestogenic_profile
|
||||
|
||||
[APPENDIX]: https://transfemscience.org/articles/oral-p4-low-levels-literature/
|
||||
[WIKI-CIT-21]: https://en.wikipedia.org/wiki/Pharmacokinetics_of_progesterone#Oral_administration
|
||||
|
||||
|
||||
<!-- 正文内的维基百科/词典条目链接,非引用 -->
|
||||
[wiki-1]: https://en.wikipedia.org/wiki/First_pass_effect
|
||||
[wiki-2]: https://en.wikipedia.org/wiki/Bioavailability
|
||||
|
|
@ -270,4 +334,4 @@
|
|||
[wiki-44]: https://en.wikipedia.org/wiki/Dienogest
|
||||
[wiki-45]: http://en.wikipedia.org/wiki/Nomegestrol_acetate
|
||||
[wiki-46]: https://en.wikipedia.org/wiki/Hydroxyprogesterone_caproate
|
||||
[wiki-47]: https://en.wikipedia.org/wiki/Algestone_acetophenide
|
||||
[wiki-47]: https://en.wikipedia.org/wiki/Algestone_acetophenide
|
||||
|
|
@ -1,20 +1,32 @@
|
|||
# 性激素与性激素结合球蛋白及其对女性化激素治疗的意义
|
||||
---
|
||||
title: 性激素与性激素结合球蛋白及其对女性化激素治疗的意义
|
||||
description: 在女性化激素治疗的典型雌二醇水平下,SHBG 对游离雌二醇的限制作用很小。
|
||||
author: Aly W.
|
||||
published: 2020-07-10
|
||||
updated: 2021-10-24
|
||||
translated: 2021-11-26
|
||||
translators:
|
||||
- Sue-e89893
|
||||
original: https://transfemscience.org/articles/shbg
|
||||
hidden: true
|
||||
---
|
||||
|
||||
作者 [Aly W.](https://transfemscience.org/articles-by-author/aly-w/)
|
||||
## 摘要 / TL;DR {#abstract}
|
||||
|
||||
首次发表于 2020 年 7 月 10 日
|
||||
性激素(如睾酮,雌二醇)与血蛋白(如白蛋白, SHBG)结合。
|
||||
这减少了其游离部分,从而限制了其生物活性。
|
||||
雄激素减少 SHBG 的产生,而雌二醇增加 SHBG 的产生,因此睾酮和雌二醇可以影响到各自的游离部分。
|
||||
由于肝脏的强烈灭活作用,正常情况下,睾酮和雌二醇对 SHBG 的影响相当小。
|
||||
但在很高水平时,它们能显著地影响 SHBG 的水平。
|
||||
怀孕时雌二醇的水平极大地增加(例如,100 倍),SHBG 水平最高可提高 5 ~ 10 倍。
|
||||
尽管大量增加的 SHBG 水平能强烈地抑制睾酮的生物活性,但对雌二醇却有所不同。
|
||||
在怀孕后期,游离雌二醇的百分比似乎只降到非妊娠时的一半左右。
|
||||
怀孕初期—雌二醇水平低一些—游离雌二醇却减少到更少的程度。
|
||||
在女性化激素治疗的典型雌二醇水平下,SHBG 对游离雌二醇的限制作用很小。
|
||||
口服雌二醇对 SHBG 产生的影响大于非口服雌二醇,这或许会使口服与非口服雌二醇出现不同的效果,但口服雌二醇最终的活性较低只是理论上的,现有的临床研究未曾报道与非口服雌二醇有关的重要治疗差异。
|
||||
总而言之,尽管 SHBG 的增加会减少游离雌二醇的百分比,女性倾向跨性别者不必太担心 SHBG 对雌二醇的有效性的影响。
|
||||
|
||||
最后修改于 2021 年 10 月 24 日
|
||||
|
||||
译者 [Sue-e89893](https://github.com/Sue-e89893)
|
||||
|
||||
翻译于 2021 年 11 月 26 日
|
||||
|
||||
## 摘要 / TL;DR
|
||||
|
||||
性激素(如睾酮,雌二醇)与血蛋白(如白蛋白, SHBG )结合。这减少了其游离部分,从而限制了其生物活性。雄激素减少 SHBG 的产生,而雌二醇增加 SHBG 的产生,因此睾酮和雌二醇可以影响到各自的游离部分。由于肝脏的强烈灭活作用,正常情况下,睾酮和雌二醇对 SHBG 的影响相当小。但在很高水平时,它们能显著地影响 SHBG 的水平。怀孕时雌二醇的水平极大地增加(例如, 100 倍), SHBG 水平最高可提高 5 ~ 10 倍。尽管大量增加的 SHBG 水平能强烈地抑制睾酮的生物活性,但对雌二醇却有所不同。在怀孕后期,游离雌二醇的百分比似乎只降到非妊娠时的一半左右。怀孕初期—雌二醇水平低一些—游离雌二醇却减少到更少的程度。在女性化激素治疗的典型雌二醇水平下,SHBG 对游离雌二醇的限制作用很小。口服雌二醇对 SHBG 产生的影响大于非口服雌二醇,这或许会使口服与非口服雌二醇出现不同的效果,但口服雌二醇最终的活性较低只是理论上的,现有的临床研究未曾报道与非口服雌二醇有关的重要治疗差异。总而言之,尽管 SHBG 的增加会减少游离雌二醇的百分比,女性倾向跨性别者不必太担心 SHBG 对雌二醇的有效性的影响。
|
||||
|
||||
## 性激素对血蛋白的结合
|
||||
## 性激素对血蛋白的结合 {#binding-of-sex-hormones-to-blood-proteins}
|
||||
|
||||
[性激素][2]与血液中名为[血浆蛋白][3]的蛋白结合。这一现象被称为[血浆蛋白结合][4]。至于雄激素和雌激素,它们主要与[白蛋白][5]和[性激素结合球蛋白][6]( SHBG )。血浆蛋白结合起到防止性激素与其靶细胞相互作用,从而防止结合和激活其受体结( [Hammond, 2016][7] )。这是因为血浆蛋白太大又[不溶于脂][8]而不能穿过富脂的[细胞膜][9]。结果,它们不能穿透[毛细血管][10]退出血液循环或进入组织或被细胞吸收。当性激素与血浆蛋白结合,它也不能进入靶细胞。因此,血浆蛋白结合限制了性激素的生物活性( Hammond, 2016 )。与血浆蛋白结合也起到延长性激素的[生物半衰期][11],因为与蛋白质结合的性激素同样地不能被代谢,也无法进行依赖于细胞吸收的清除。
|
||||
|
||||
|
|
@ -72,7 +84,7 @@
|
|||
[23]: https://doi.org/10.1210/er.2017-00171
|
||||
[24]: https://doi.org/10.1016/j.jsbmb.2019.04.008
|
||||
|
||||
## 性激素对 SHBG 产生的影响
|
||||
## 性激素对 SHBG 产生的影响 {#effects-of-sex-hormones-on-shbg-production}
|
||||
|
||||
血浆蛋白(如白蛋白,SHBG )在肝脏中合成并分泌到血液中。除了与 SHBG 结合,性激素还调节肝脏产生 SHBG ,从而影响到它们各自的血浆蛋白结合。雄激素减少 SHBG 的产生,而雌激素增加 SHBG 的产生( Anderson, 1974; Moore & Bulbrook, 1988 )。服用合成代谢类固醇 stanozolol (一种合成 DHT 衍生物)几天就可抑制达 63% 的 SHBG 水平( [Krause et al., 2004][25] )。持续使用极大剂量的睾酮和其他合成代谢类固醇能降低 90% 的 SHBG 水平( [Ruokonen et al., 1985][26]; Moore & Bulbrook, 1988 )。类似地,弱雄激素性孕激素,如[醋酸甲羟孕酮][27]( MPA ),[炔诺酮][28]( NET )和[左炔诺孕酮][29]( LNG ),会降低 SHBG 产生( [Kuhl, 2005][30] ),非常高剂量的醋酸甲羟孕酮和 [醋酸甲地孕酮][31]( MGA )被报道会降低高达约 50 ~ 90% 的 SHBG 水平( [Heubner et al., 1987][32]; [Lundgren et al., 1990][33]; [Lundgren & Lønning, 1990][34] )。与此相反,含有合成雌激素炔雌醇(及少许雄激素性或抗雄激素性孕激素)的避孕药增加约 4 倍的 SHBG 水平( [Odlind et al., 2002][35] )。高剂量的口服合成雌激素曾加 SHBG 水平高达 5 ~ 10 倍( [von Schoultz et al., 1989][36] )。
|
||||
|
||||
|
|
@ -149,21 +161,29 @@
|
|||
[66]: https://doi.org/10.1111/j.1365-2265.1994.tb02478.x
|
||||
[67]: https://doi.org/10.1007/978-3-642-60107-1_18
|
||||
|
||||
| 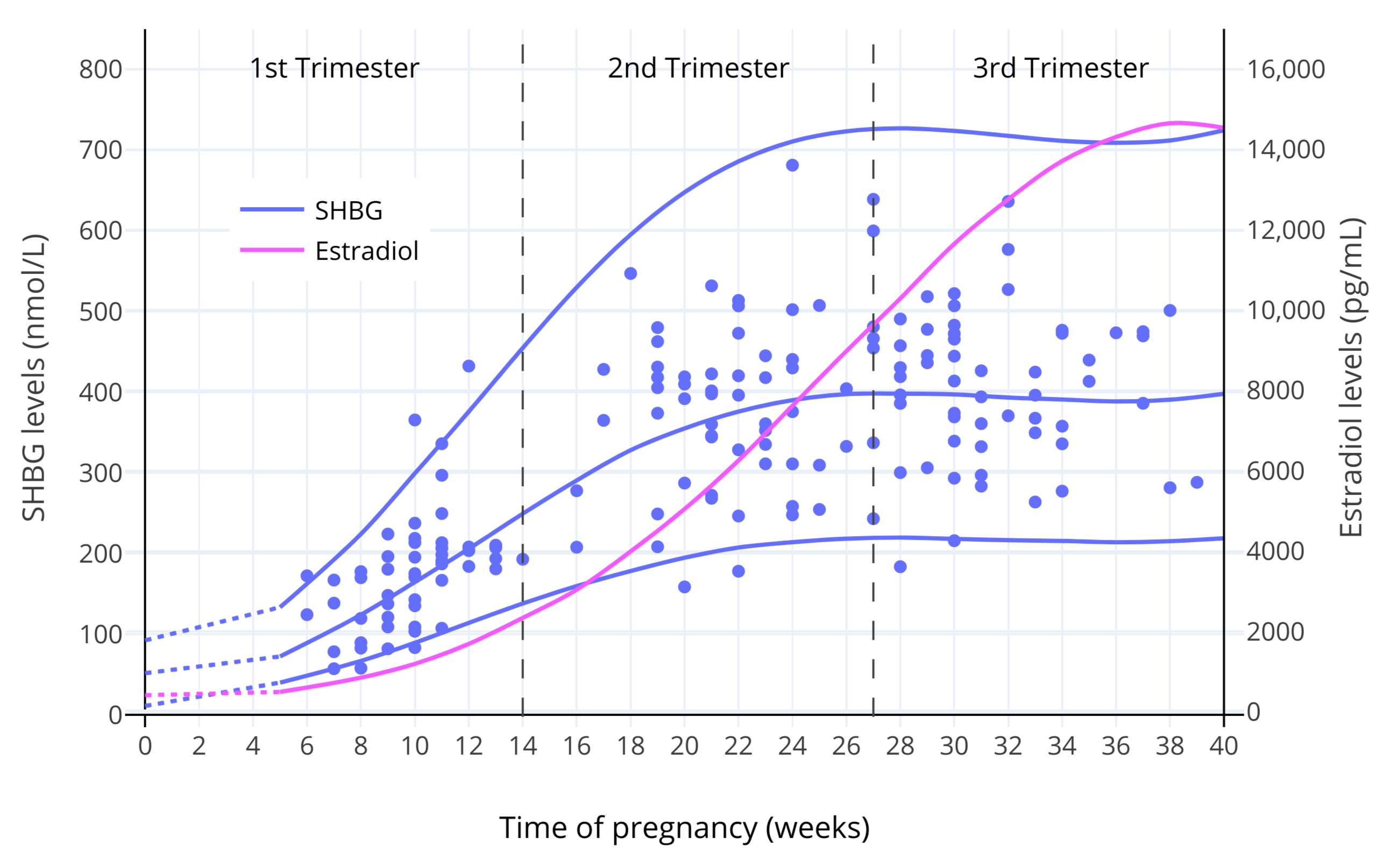 |
|
||||
| ---------------------------------------------------------------------------------------------------------------------------- |
|
||||
| **图 1**:妊娠期间,SHBG 和总雌二醇的水平( O’Leary et al., 1991 )。线代表平均值和/或第 95 百分位数,而点表示单独的测量值。 |
|
||||
<section class="box">
|
||||
|
||||
| 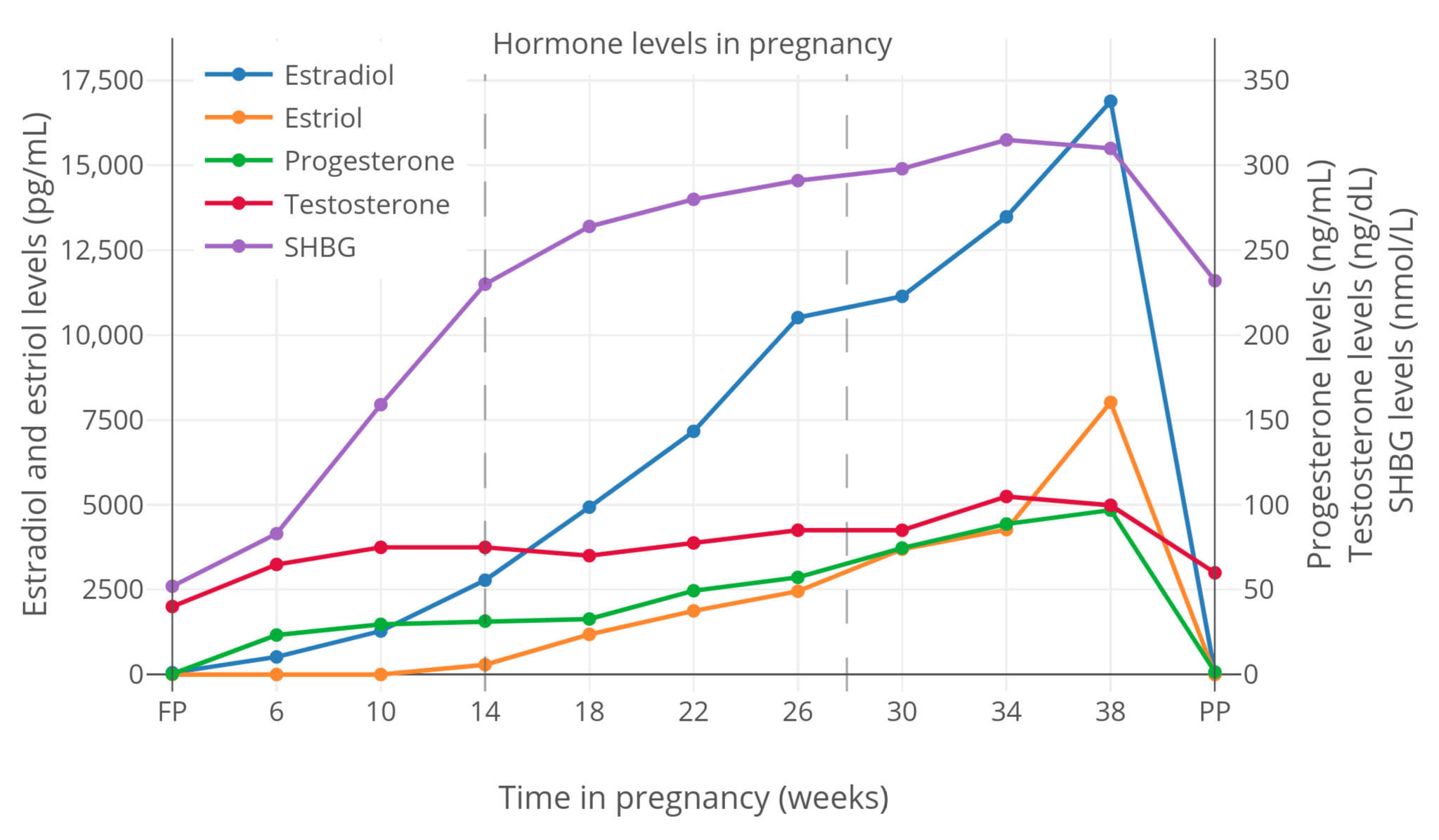 |
|
||||
| ----------------------------------------------------------------------- |
|
||||
| **图 2**:女性妊娠期间,总性激素和 SHBG 水平( Kerlan et al., 1994 )。 |
|
||||

|
||||
|
||||
## SHBG 增加对游离性激素水平的影响
|
||||
**图 1**:妊娠期间,SHBG 和总雌二醇的水平(O’Leary et al., 1991)。线代表平均值和/或第 95 百分位数,而点表示单独的测量值。
|
||||
|
||||
</section>
|
||||
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 2**:女性妊娠期间,总性激素和 SHBG 水平(Kerlan et al., 1994)。
|
||||
|
||||
</section>
|
||||
|
||||
## SHBG 增加对游离性激素水平的影响 {#effects-of-shbg-increase-on-free-sex-hormone-levels}
|
||||
|
||||
SHBG 水平的变化导致了与 SHBG 结合的性激素水平和游离性激素的改变。除了 DHT 外,雌二醇和睾酮是在这一方面有最大关系的性激素。
|
||||
|
||||
### SHBG 增加与游离睾酮
|
||||
### SHBG 增加与游离睾酮 {#shbg-increase-and-free-testosterone}
|
||||
|
||||
含有 EE 的避孕药,会使 SHBG 水平增长 4 倍,能显著地降低游离睾酮的百分比( [Graham et al., 2007][68]; [Zimmerman et al., 2014][69] )。在一项研究中,一片含有 EE 的避孕药使游离睾酮的百分比从 2.45% 降至 0.78% (降低 3.2 倍或降至基线的 32% )( Graham et al., 2007 )。由于同时抑制了睾酮的产生,从而降低了总睾酮水平,游离睾酮水平从 0.89 pg/mL 降至 0.18 pg/mL (降低 5 倍,至基线的 20% )( Graham et al., 2007 )。含有 EE 的避孕药对 SHBG 水平的影响显著地增强了其抗雄作用,这被用来治疗女性痤疮和多毛症。
|
||||
含有 EE 的避孕药,会使 SHBG 水平增长 4 倍,能显著地降低游离睾酮的百分比([Graham et al., 2007][68]; [Zimmerman et al., 2014][69])。在一项研究中,一片含有 EE 的避孕药使游离睾酮的百分比从 2.45% 降至 0.78% (降低 3.2 倍或降至基线的 32%)(Graham et al., 2007)。由于同时抑制了睾酮的产生,从而降低了总睾酮水平,游离睾酮水平从 0.89 pg/mL 降至 0.18 pg/mL (降低 5 倍,至基线的 20%)(Graham et al., 2007)。含有 EE 的避孕药对 SHBG 水平的影响显著地增强了其抗雄作用,这被用来治疗女性痤疮和多毛症。
|
||||
|
||||
[68]: https://doi.org/10.1016/j.psyneuen.2006.12.011
|
||||
[69]: https://doi.org/10.1093/humupd/dmt038
|
||||
|
|
@ -175,9 +195,9 @@ SHBG 水平的变化导致了与 SHBG 结合的性激素水平和游离性激素
|
|||
[72]: https://doi.org/10.1530/EC-19-0110
|
||||
[73]: https://doi.org/10.1172/JCI14060
|
||||
|
||||
### SHBG 增加和游离雌二醇
|
||||
### SHBG 增加和游离雌二醇 {#shbg-increase-and-free-estradiol}
|
||||
|
||||
#### 内源和非口服雌二醇
|
||||
#### 内源和非口服雌二醇 {#endogenous-and-non-oral-estradiol}
|
||||
|
||||
研究表明,生理水平下的雌二醇(如 <200 pg/mL )受 SHBG 水平增加而降低游离雌二醇的影响甚微。只要是非口服途径,无论内源的还是外源的雌二醇都是这样。这样的结论是由计算出的和测量出的游离雌二醇的研究两者得出的。( e.g., Freymann et al., 1977b )。
|
||||
|
||||
|
|
@ -240,22 +260,30 @@ SHBG 水平的变化导致了与 SHBG 结合的性激素水平和游离性激素
|
|||
[85]: https://doi.org/10.1016/0002-9378(87)90126-8
|
||||
[86]: https://doi.org/10.1038/bjc.1988.223
|
||||
|
||||
| 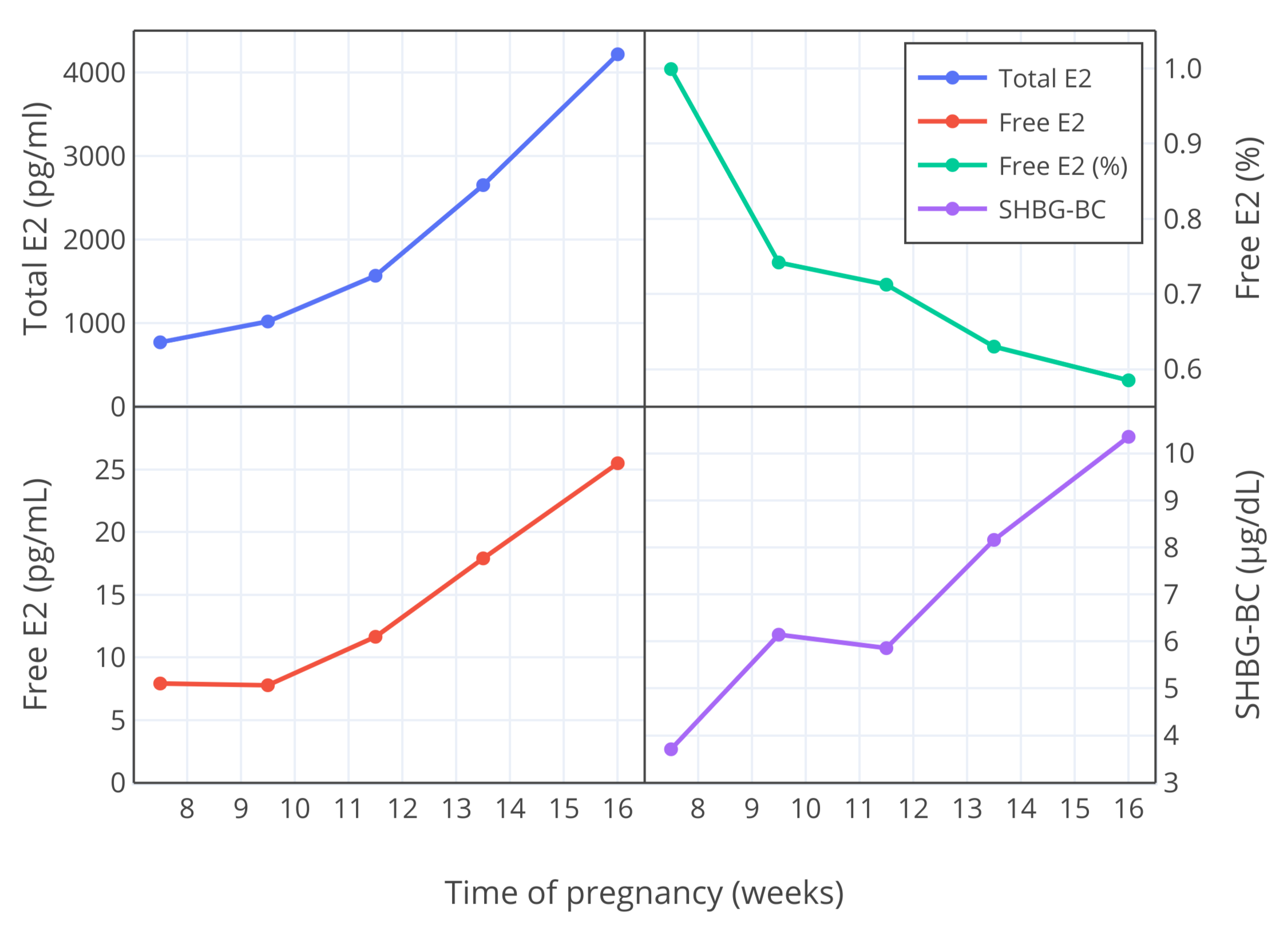 |
|
||||
| ----------------------------------------------------------------------------------------------------------------------------------------------------------- |
|
||||
| **图 3**:女性妊娠 7 到 16 周时,总雌二醇水平和游离雌二醇水平变化 (pg/mL),游离雌二醇百分比变化 (%) 和 SHBG 总量的变化 (μg/dL) ( Bernstein et al., 1986 ) |
|
||||
<section class="box">
|
||||
|
||||
妊娠期间,游离雌二醇可以用总雌二醇水平和 SHBG 水平计算。我粗略地算出了妊娠时游离雌二醇的百分比(使用了 O’Leary et al. (1991) 的数据和已出版的 [Mazer (2009)][87] 的电子表格计算器( [Aly W., 2020][88] )。结果见下。
|
||||

|
||||
|
||||
**图 3**:女性妊娠 7 到 16 周时,总雌二醇水平和游离雌二醇水平变化 (pg/mL),游离雌二醇百分比变化 (%) 和 SHBG 总量的变化 (μg/dL)(Bernstein et al., 1986)
|
||||
|
||||
</section>
|
||||
|
||||
妊娠期间,游离雌二醇可以用总雌二醇水平和 SHBG 水平计算。我粗略地算出了妊娠时游离雌二醇的百分比(使用了 O’Leary et al. (1991) 的数据和已出版的 [Mazer (2009)][87] 的电子表格计算器([Aly W., 2020][88])。结果见下。
|
||||
|
||||
[87]: https://doi.org/10.1016/j.steroids.2009.01.008
|
||||
[88]: https://transfemscience.org/articles/shbg-suppl/
|
||||
|
||||
| 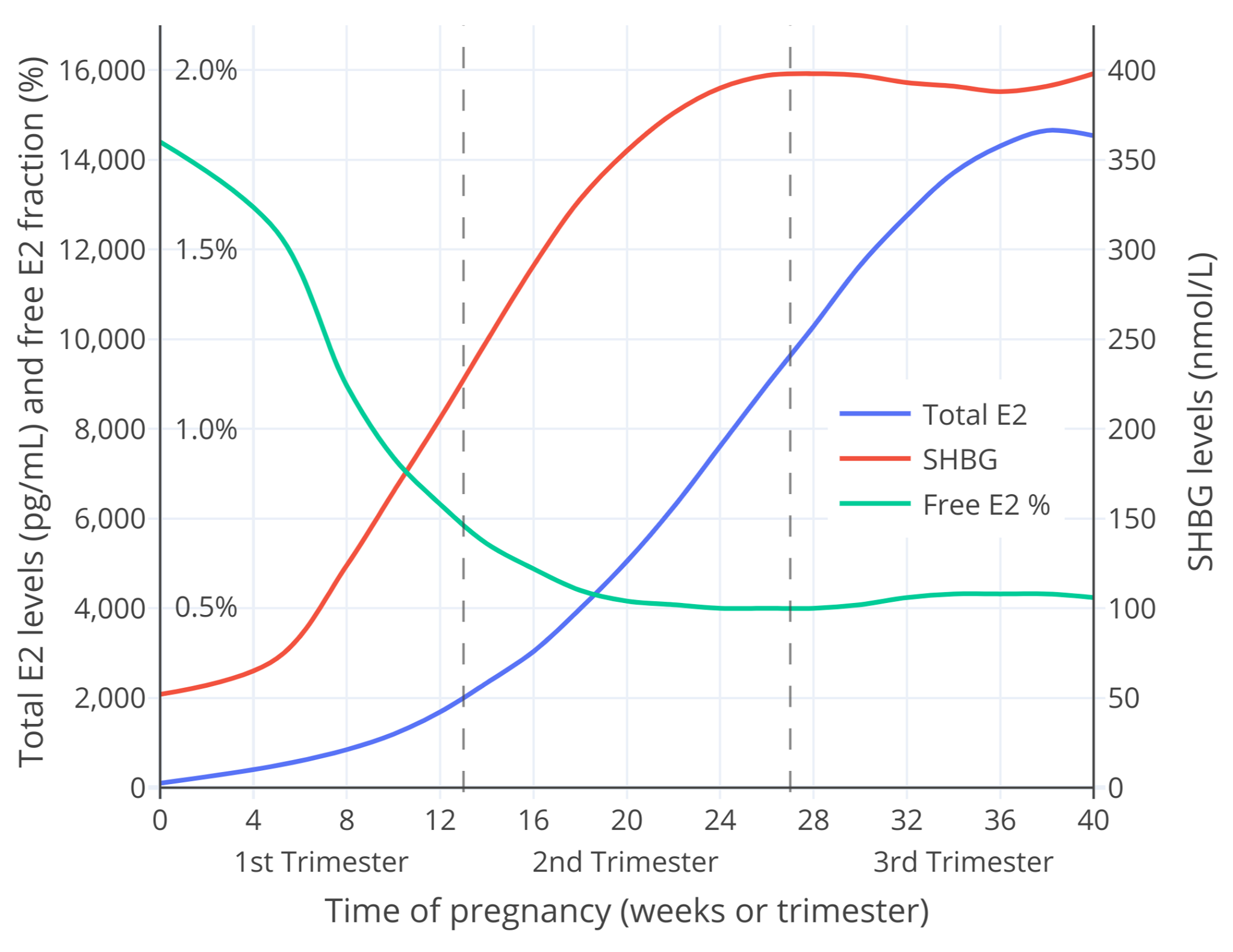 |
|
||||
| --------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------- |
|
||||
| **图 4**:女性整个妊娠期测出的平均总雌二醇和总 SHBG 水平( O’Leary et al., 1991 )和计算出的游离雌二醇百分比( Mazer, 2009 )。这幅图还有另一个缩放到第一孕期的版本(雌二醇水平通常 ≤2,000 pg/mL )([图][89]) |
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 4**:女性整个妊娠期测出的平均总雌二醇和总 SHBG 水平( O’Leary et al., 1991 )和计算出的游离雌二醇百分比( Mazer, 2009 )。这幅图还有另一个缩放到第一孕期的版本(雌二醇水平通常 ≤2,000 pg/mL )([图][89])
|
||||
|
||||
[89]: https://transfemscience.org/assets/images/fdd36yplqia51.png
|
||||
|
||||
图中的游离雌二醇百分比仅仅是粗略的估计值,因此,应当保守考虑。不管怎么说,它们近似于现有的关于妊娠早期测量的游离雌二醇,如在数量级(相较于 Bernstein et al. )和整个孕期的变化方式(相较与 Bernstein et al. 和 Freymann et al. 两者)。由此,这些算出的值提供了一个可信的,重要的模型。
|
||||
</section>
|
||||
|
||||
图中的游离雌二醇百分比仅仅是粗略的估计值,因此,应当保守考虑。不管怎么说,它们近似于现有的关于妊娠早期测量的游离雌二醇,如在数量级(相较于 Bernstein et al.)和整个孕期的变化方式(相较与 Bernstein et al. 和 Freymann et al. 两者)。由此,这些算出的值提供了一个可信的,重要的模型。
|
||||
|
||||
总的来讲,妊娠期间,总雌二醇水平极大地增加,与之相称地,SHBG 的增长虽相对较低但仍巨大。由于大量增长的 SHBG 水平,游离雌二醇的百分比在整个孕期逐步降低。现有的研究就游离雌二醇的百分比降至何种程度有所矛盾。不管怎样,妊娠后期游离雌二醇的可能百分比的范围约是 0.5 到 1.5% 。这些数值可与非孕期的游离雌二醇百分比 1.5 至 2.1% 进行比较。这相当于妊娠后期的游离雌二醇百分比最多降低到非孕期的 60% 左右。极端情况下,可能只降到非孕期时的 25% 左右。相反地,妊娠早期时,游离雌二醇相对较低,游离雌二醇的百分比更高。
|
||||
|
||||
|
|
@ -263,7 +291,7 @@ SHBG 水平的变化导致了与 SHBG 结合的性激素水平和游离性激素
|
|||
|
||||
在妊娠期间,SHBG 并不像影响睾酮那样影响雌二醇,因为与之相称的雌二醇水平增长远大于 SHBG 水平的增长,雌二醇对 SHBG 的亲和力又相对较弱。一般而言,由于缺少大量的 SHBG 来面对更高的雌二醇水平这一内在要求,SHBG 不可能像限制睾酮那样限制雌二醇的活性。
|
||||
|
||||
#### 口服雌二醇
|
||||
#### 口服雌二醇 {#oral-estradiol}
|
||||
|
||||
当涉及到游离雌二醇时,口服雌二醇可能与非口服雌二醇不同。这是因为口服雌二醇要经历首过——这会使在肝脏中的雌二醇水平高于血液中的雌二醇水平。结果,口服雌二醇导致不相称的肝影响,使 SHBG 水平升至与其相称的比非口服雌二醇高的程度。因此,口服雌二醇带来的更高的 SHBG 水平可能会使游离雌二醇百分比比非口服的低。
|
||||
|
||||
|
|
@ -280,7 +308,7 @@ SHBG 水平的变化导致了与 SHBG 结合的性激素水平和游离性激素
|
|||
[95]: https://doi.org/10.1016/j.fct.2018.12.013
|
||||
[96]: https://imgur.com/a/VItjDNS
|
||||
|
||||
## 对女性化激素治疗的意义
|
||||
## 对女性化激素治疗的意义 {#relevance-for-transfeminine-hormone-therapy}
|
||||
|
||||
一些女性倾向跨性别者担心 SHBG 可能会很大地限制雌二醇生效,从而妨碍女性化和/或乳房发育。一些人甚至声称,由于 SHBG 在较高的雌二醇水平时增加,高水平的雌二醇可能没有较低水平的有效。但是,这些观念很可能都是被误导的,都没有深入了解 SHBG 。这是因为就女性化和乳房发育而言,低雌二醇水平( <50 pg/mL )就足以完全起效—被顺性别女孩正常的和诱导的青春期( [Aly W., 2020][97] )及第二性征发育良好的患完全雄激素不敏症女性证实( CAIS )( [Aly W., 2020][98]; [Wiki][99] )。现时,没有证据表明较高的雌二醇水平对女性化或乳房发育有益或不可或缺( [Nolan & Cheung, 2020][100] )。事实上,现有的研究表明,女性倾向跨性别者在典型治疗水平的雌二醇下( 如 50–200 pg/mL ),雌二醇水平与乳房发育没有关联( [de Blok et al., 2018][101]; [Meyer et al., 2020][102]; [de Blok et al., 2020][103] )。这与在较低雌二醇水平时就已确立雌二醇在女性化和乳房发育方面能起到的最大效果的概念相一致。因此,除了女性倾向跨性别者使用较高水平的雌二醇抑制睾酮外,对于缺乏雌激素暴露而致使不完全的女性化效果的担忧是站不住脚的。
|
||||
|
||||
|
|
@ -304,8 +332,8 @@ SHBG 水平的变化导致了与 SHBG 结合的性激素水平和游离性激素
|
|||
|
||||
总之,女性倾向跨性别者不应该太担心因升高的 SHBG 水平而降低的游离雌二醇,不论非口服还是口服雌二醇。
|
||||
|
||||
## 附加素材
|
||||
## 附加素材 {#supplementary-material}
|
||||
|
||||
这篇文章的附加素材,见[此处][107],包含一份电子表格和其他能估计游离激素的计算器(如 Mazer, 2009 )。
|
||||
这篇文章的附加素材,见[此处][107],包含一份电子表格和其他能估计游离激素的计算器(如 Mazer, 2009)。
|
||||
|
||||
[107]: https://transfemscience.org/articles/shbg-suppl/
|
||||
|
|
@ -1,122 +1,138 @@
|
|||
# 性激素与性激素结合球蛋白的相互作用及其对女性化激素疗法的意义
|
||||
---
|
||||
title: 性激素与性激素结合球蛋白的相互作用及其对女性化激素疗法的意义
|
||||
linkTitle: 性激素结合球蛋白与性激素的相互作用及其意义
|
||||
description: 性激素结合球蛋白尽管会降低血清游离雌二醇比例,但总体不影响雌二醇的效力。
|
||||
author: Aly W.
|
||||
published: 2020-07-10
|
||||
updated: 2021-10-24
|
||||
translated: 2022-10-19
|
||||
translators:
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 性激素结合球蛋白
|
||||
- 雌激素
|
||||
trackHash: 6d4f2b59cba164b995402e394d0353d681f4b0e1
|
||||
---
|
||||
|
||||
> - 作者 [Aly W.][AUTHOR]
|
||||
> + 首次发表于 2020 年 7 月 10 日
|
||||
> + 最后修改于 2021 年 10 月 24 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [Bersella AI][TRANSLATOR]
|
||||
> + 翻译完成于 2022 年 10 月 19 日
|
||||
## 译者按 {#notice}
|
||||
|
||||
[AUTHOR]: https://transfemscience.org/about/#aly-w
|
||||
[ORIGIN]: https://transfemscience.org/articles/shbg/
|
||||
[TRANSLATOR]: https://bersella-ai.cc/about-me/
|
||||
|
||||
## 译者按
|
||||
|
||||
1. 本次翻译系对[早前译文](shbg-old.md)的完全重制。在此感谢 Sue-e89893 早前的贡献。
|
||||
1. 本次翻译系对[早前译文]({{< ref "shbg-2021-11-26" >}})的完全重制。在此感谢 Sue-e89893 早前的贡献。
|
||||
1. 因译者能力所限,部分术语及段落之翻译或有纰漏,烦请指正。(个别句子在中文语境中稍显冗余或有语病,亦略去。)
|
||||
|
||||
---------
|
||||
---
|
||||
|
||||
## 摘要
|
||||
## 摘要 {#abstract}
|
||||
|
||||
> 诸如睾酮、雌二醇等性激素,会与一些血蛋白结合,如白蛋白和性激素结合球蛋白(SHBG)。该结合过程会降低性激素的游离比例,从而使其生物活性减弱。因此,睾酮、雌二醇可影响到其自身的游离比例。
|
||||
> 在通常情况下,由于睾酮、雌二醇会在肝脏内被大量灭活,故其对 SHBG 水平的影响较小;而一旦其水平变得很高,其将对 SHBG 水平产生明显影响。例如,妊娠期间,随着雌二醇水平的大幅升高(可达 100 倍),SHBG 水平的增幅也会高达 5-10 倍。SHBG 水平的大幅增加会显著抑制睾酮的生物活性,但对雌二醇的情况则不同。在妊娠后期,游离雌二醇比例仅有非孕期的约一半;而在雌二醇水平更低的妊娠早期,游离雌二醇比例的降幅则更小。
|
||||
> 在女性化激素疗法当中,临床上常规的雌二醇水平只会使得 SHBG 对其游离比例的限制作用相当微弱。不过,口服雌二醇的情况比较特殊,其对 SHBG 之生成的作用要大于非口服形式,从而减弱其活性;但上述仅存于理论可能,迄今尚未有临床研究报告其相对于非口服形式的重大疗效差异。
|
||||
> 综上所述,女性倾向跨性别者无需过分担心 SHBG 对雌二醇效力的影响——尽管其会降低游离雌二醇比例。
|
||||
诸如睾酮、雌二醇等性激素,会与一些血蛋白结合,如白蛋白和性激素结合球蛋白(SHBG)。该结合过程会降低性激素的游离比例,从而使其生物活性减弱。因此,睾酮、雌二醇可影响到其自身的游离比例。
|
||||
在通常情况下,由于睾酮、雌二醇会在肝脏内被大量灭活,故其对 SHBG 水平的影响较小;而一旦其水平变得很高,其将对 SHBG 水平产生明显影响。例如,妊娠期间,随着雌二醇水平的大幅升高(可达 100 倍),SHBG 水平的增幅也会高达 5-10 倍。SHBG 水平的大幅增加会显著抑制睾酮的生物活性,但对雌二醇的情况则不同。在妊娠后期,游离雌二醇比例仅有非孕期的约一半;而在雌二醇水平更低的妊娠早期,游离雌二醇比例的降幅则更小。
|
||||
在女性化激素疗法当中,临床上常规的雌二醇水平只会使得 SHBG 对其游离比例的限制作用相当微弱。不过,口服雌二醇的情况比较特殊,其对 SHBG 之生成的作用要大于非口服形式,从而减弱其活性;但上述仅存于理论可能,迄今尚未有临床研究报告其相对于非口服形式的重大疗效差异。
|
||||
综上所述,女性倾向跨性别者无需过分担心 SHBG 对雌二醇效力的影响——尽管其会降低游离雌二醇比例。
|
||||
|
||||
## 性激素与血蛋白的结合
|
||||
## 性激素与血蛋白的结合 {#binding-of-sex-hormones-to-blood-proteins}
|
||||
|
||||
[性激素][SH]会与血液中的[血浆蛋白结合][PPB]。对于雄激素与雌激素,其主要与[白蛋白][ALB]、[性激素结合球蛋白][SHBG](SHBG)进行结合。该结合过程会使得性激素无法与其靶细胞相互作用,即结合并激活靶细胞之受体<sup>([Hammond, 2016][H16])</sup>。这是因为,血浆蛋白体积过大,亲脂性也很弱,无法穿过主要由脂质构成的细胞膜。故此,它们不可能离开血液循环而从毛细血管扩散出来,从而渗透到各组织或被细胞吸收;与其结合的性激素自然也不能接触到对应的靶细胞。综上,血浆蛋白结合过程会限制性激素的生物活性<sup>(Hammond, 2016)</sup>。
|
||||
[性激素][SH]会与血液中的[血浆蛋白结合][PPB]。对于雄激素与雌激素,其主要与[白蛋白][ALB]、[性激素结合球蛋白][SHBG](SHBG)进行结合。该结合过程会使得性激素无法与其靶细胞相互作用,即结合并激活靶细胞之受体<sup>([Hammond, 2016][H16])</sup>。这是因为,血浆蛋白体积过大,亲脂性也很弱,无法穿过主要由脂质构成的细胞膜。故此,它们不可能离开血液循环而从毛细血管扩散出来,从而渗透到各组织或被细胞吸收;与其结合的性激素自然也不能接触到对应的靶细胞。综上,血浆蛋白结合过程会限制性激素的生物活性<sup>(Hammond, 2016)</sup>。
|
||||
该结合过程也会使得性激素的生物半衰期延长,因为性激素的代谢及消除过程同样需要被细胞摄入,而其结合蛋白无法被摄入。
|
||||
|
||||
每个 SHBG 分子仅有一个性激素结合位点<sup>([Moore & Bulbrook, 1988][MB88])</sup>,而白蛋白有六个可结合不同基质的位点<sup>([Pardridge, 1988][P88])</sup>。雄激素与雌二醇对 SHBG 的亲和力较强,而对白蛋白的亲和力较弱<sup>(Moore & Bulbrook, 1988; Hammond, 2016)</sup>;不过,白蛋白的水平相较 SHBG 要高几个数量级[微摩尔浓度(μM)单位对纳摩尔浓度(nM)单位],从而使得性激素对两种蛋白的结合比例相近<sup>(Hammond, 2016)</sup>。
|
||||
每个 SHBG 分子仅有一个性激素结合位点<sup>([Moore & Bulbrook, 1988][MB88])</sup>,而白蛋白有六个可结合不同基质的位点<sup>([Pardridge, 1988][P88])</sup>。雄激素与雌二醇对 SHBG 的亲和力较强,而对白蛋白的亲和力较弱<sup>(Moore & Bulbrook, 1988; Hammond, 2016)</sup>;不过,白蛋白的水平相较 SHBG 要高几个数量级[微摩尔浓度(μM)单位对纳摩尔浓度(nM)单位],从而使得性激素对两种蛋白的结合比例相近<sup>(Hammond, 2016)</sup>。
|
||||
雄激素对 SHBG 的亲和力要高于雌二醇等雌激素;雌二醇的亲和力仅有二氢睾酮(DHT)的约 10-20%、睾酮的约 33-50%<sup>([Anderson, 1974][A74]; [Ojasoo & Raynaud, 1978][OR78]; [Pugeat, Dunn, Nisula, 1981][PDN81])</sup>。
|
||||
|
||||
血液中的性激素绝大部分皆与血浆蛋白结合;无论任何时候,都有超过 97% 的睾酮、雌二醇与孕激素被结合<sup>([Strauss & FitzGerald, 2019][SF19])</sup>。*未结合* 的部分性激素(也被称为*游离* 性激素),可扩散到细胞当中,从而被认为具有生物活性<sup>([Hammond, 2016][H16])</sup>。
|
||||
血液中的性激素绝大部分皆与血浆蛋白结合;无论任何时候,都有超过 97% 的睾酮、雌二醇与孕激素被结合<sup>([Strauss & FitzGerald, 2019][SF19])</sup>。*未结合* 的部分性激素(也被称为*游离* 性激素),可扩散到细胞当中,从而被认为具有生物活性<sup>([Hammond, 2016][H16])</sup>。
|
||||
激素的*总和* 水平包括了已结合与未结合(游离)之激素;激素的*可利用* 水平则包括游离激素与已结合于白蛋白的激素——由于性激素对白蛋白的亲和力较弱,其与之结合时可能仍具备一定的生物活性,也即“可被利用”<sup>([Nguyen et al., 2008][N08])</sup>。不过,尚需更多研究来充分阐明与白蛋白结合的性激素之生物活性。
|
||||
|
||||
下表列出了经大致计算得到的,雌二醇、睾酮和 DHT 对白蛋白、SHBG 及皮质类固醇结合球蛋白(CBG)的结合比例——其中 CBG 仅与一小部分的雄激素结合,而不与雌二醇结合。
|
||||
|
||||
> 【表一】各性激素与血浆蛋白的结合比例(计算值)<sup>([Dunn, Nisula, & Rodbard, 1981][DNR81])</sup>:
|
||||
>
|
||||
> | 性激素 | 组别 | 白蛋白 (%) | SHBG (%) | CBG (%) | 游离 (%) |
|
||||
> |-|-|-|-|-|-|
|
||||
> | **雌二醇** | 妇女(卵泡期) | 60.8 | 37.3 | <0.1 | 1.81 |
|
||||
> | | 妇女(黄体期) | 61.1 | 37.0 | <0.1 | 1.82 |
|
||||
> | | 妇女(妊娠期) | 11.7 | 87.8 | <0.1 | 0.49 |
|
||||
> | | 男性 | 78.0 | 19.6 | <0.1 | 2.32 |
|
||||
> | **睾酮** | 妇女(卵泡期) | 30.4 | 66.0 | 2.26 | 1.36 |
|
||||
> | | 妇女(黄体期) | 30.7 | 65.7 | 2.20 | 1.37 |
|
||||
> | | 妇女(妊娠期) | 3.60 | 95.4 | 0.82 | 0.23 |
|
||||
> | | 男性 | 49.9 | 44.3 | 3.56 | 2.23 |
|
||||
> | **DHT** | 妇女(卵泡期) | 21.0 | 78.4 | 0.12 | 0.47 |
|
||||
> | | 妇女(黄体期) | 21.3 | 78.1 | 0.12 | 0.48 |
|
||||
> | | 妇女(妊娠期) | 2.15 | 97.8 | 0.04 | 0.07 |
|
||||
> | | 男性 | 39.2 | 59.7 | 0.22 | 0.88 |
|
||||
<section class="box">
|
||||
|
||||
**表 1**:各性激素与血浆蛋白的结合比例(计算值)<sup>([Dunn, Nisula, & Rodbard, 1981][DNR81])</sup>:
|
||||
|
||||
| 性激素 | 组别 | 白蛋白 (%) | SHBG (%) | CBG (%) | 游离 (%) |
|
||||
|-|-|-|-|-|-|
|
||||
| **雌二醇** | 妇女(卵泡期) | 60.8 | 37.3 | <0.1 | 1.81 |
|
||||
| | 妇女(黄体期) | 61.1 | 37.0 | <0.1 | 1.82 |
|
||||
| | 妇女(妊娠期) | 11.7 | 87.8 | <0.1 | 0.49 |
|
||||
| | 男性 | 78.0 | 19.6 | <0.1 | 2.32 |
|
||||
| **睾酮** | 妇女(卵泡期) | 30.4 | 66.0 | 2.26 | 1.36 |
|
||||
| | 妇女(黄体期) | 30.7 | 65.7 | 2.20 | 1.37 |
|
||||
| | 妇女(妊娠期) | 3.60 | 95.4 | 0.82 | 0.23 |
|
||||
| | 男性 | 49.9 | 44.3 | 3.56 | 2.23 |
|
||||
| **DHT** | 妇女(卵泡期) | 21.0 | 78.4 | 0.12 | 0.47 |
|
||||
| | 妇女(黄体期) | 21.3 | 78.1 | 0.12 | 0.48 |
|
||||
| | 妇女(妊娠期) | 2.15 | 97.8 | 0.04 | 0.07 |
|
||||
| | 男性 | 39.2 | 59.7 | 0.22 | 0.88 |
|
||||
|
||||
</section>
|
||||
|
||||
游离性激素水平及比例,多通过依据多项已发表研究的数据所构建、确立的数学模型,从性激素总和水平及白蛋白、SHBG、CBG 水平算得。这是因为,游离性激素水平通常很低[仅在皮摩尔浓度级(pM)范围],难以被常规验血手段检出。该计算结果并非完全准确,尽管与实际值基本相当<sup>([Rosner, 2015][R15]; [Goldman et al., 2017][G17]; [Handelsman, 2017][H17]; [Keevil & Adaway, 2019][KA19])</sup>。因此,如果可能的话,直接测量的结果会更佳。
|
||||
|
||||
## 性激素对 SHBG 之生成的影响 {#effects-of-sex-hormones-on-shbg-production}
|
||||
|
||||
## 性激素对 SHBG 之生成的影响
|
||||
|
||||
血浆蛋白(如白蛋白与 SHBG)在肝脏合成并分泌至血液中。除了与 SHBG 结合,性激素还调节肝脏生成 SHBG,从而影响其结合特性。雄激素会减少 SHBG 的生成,而雌激素则增加之<sup>(Anderson, 1974; Moore & Bulbrook, 1988)</sup>。
|
||||
例如,服用[蛋白同化激素][AS]:司坦唑醇(一种人工合成的 DHT 衍生物),几天内便可将 SHBG 水平抑制达 63%<sup>([Krause et al., 2004][K04])</sup>。如持续服用超大剂量的睾酮及其它蛋白同化激素,可将 SHBG 水平降低 90%<sup>([Ruokonen et al., 1985][R85]; Moore & Bulbrook, 1988)</sup>。
|
||||
与此类似,一些具有较弱雄激素效力的合成孕酮制剂(如醋酸甲羟孕酮、炔诺酮和左炔诺孕酮),会减少 SHBG 的产生<sup>([Kuhl, 2005][K05]; Moore & Bulbrook, 1988)</sup>;而超高剂量下的醋酸甲羟孕酮及醋酸甲地孕酮,已被报告可将 SHBG 水平降低至多约 50-90%<sup>([Heubner et al., 1987][H87]; [Lundgren et al., 1990][L90]; [Lundgren & Lønning, 1990][LL90])</sup>。
|
||||
血浆蛋白(如白蛋白与 SHBG)在肝脏合成并分泌至血液中。除了与 SHBG 结合,性激素还调节肝脏生成 SHBG,从而影响其结合特性。雄激素会减少 SHBG 的生成,而雌激素则增加之<sup>(Anderson, 1974; Moore & Bulbrook, 1988)</sup>。
|
||||
例如,服用[蛋白同化激素][AS]:司坦唑醇(一种人工合成的 DHT 衍生物),几天内便可将 SHBG 水平抑制达 63%<sup>([Krause et al., 2004][K04])</sup>。如持续服用超大剂量的睾酮及其它蛋白同化激素,可将 SHBG 水平降低 90%<sup>([Ruokonen et al., 1985][R85]; Moore & Bulbrook, 1988)</sup>。
|
||||
与此类似,一些具有较弱雄激素效力的合成孕酮制剂(如醋酸甲羟孕酮、炔诺酮和左炔诺孕酮),会减少 SHBG 的产生<sup>([Kuhl, 2005][K05]; Moore & Bulbrook, 1988)</sup>;而超高剂量下的醋酸甲羟孕酮及醋酸甲地孕酮,已被报告可将 SHBG 水平降低至多约 50-90%<sup>([Heubner et al., 1987][H87]; [Lundgren et al., 1990][L90]; [Lundgren & Lønning, 1990][LL90])</sup>。
|
||||
与上述相反的是,服用包含炔雌醇(一种合成雌激素)与一种合成孕酮(有极低雄激素效力或抗雄激素效力)的复方避孕药,会使 SHBG 水平升高约 4 倍<sup>([Odlind et al., 2002][O02])</sup>。高剂量的合成雌激素可将 SHBG 水平升高至多 5-10 倍<sup>([von Schoultz et al., 1989][S89])</sup>。
|
||||
|
||||
通常情况下,睾酮、DHT 与雌二醇会被肝脏大量灭活,其在该部位的效力也较弱。因此,其对 SHBG 之生成的影响,要远弱于合成激素药物。与此对应,在妇女的整个月经周期当中,即便在雌二醇水平大幅波动的情况下,SHBG 水平亦仅有小幅变化<sup>([Freymann et al., 1977b][F77b]; [Plymate et al., 1985][P85]; [Schijf et al., 1993][S93]; [Braunstein et al., 2011][B11]; [Rothman et al., 2011][R11]; [Fanelli et al., 2013][F13]; [Rezaii et al., 2017][R17])</sup>。在一项研究中,从卵泡期过渡到黄体期时,SHBG 水平增加了约 6-13%(即 2.9–5.3 nmol/L)。此外,在更年期,即使雌二醇水平急剧降低,SHBG 水平也仅降低少许<sup>([Burger et al., 2000][B00]; [Guthrie et al., 2004][G04])</sup>。还有,接受雌二醇治疗时,在特定情形下还会显著地影响 SHBG 及其它肝蛋白的生成<sup>([Kuhl, 1998][K98])</sup>。这是因为:1) 口服雌二醇的使用,因肝脏的首过效应,其对雌激素相关的肝脏分泌活动造成的影响相较非口服形式会更大;2) 高剂量雌二醇的使用,例如使用注射剂时的通常剂量。
|
||||
通常情况下,睾酮、DHT 与雌二醇会被肝脏大量灭活,其在该部位的效力也较弱。因此,其对 SHBG 之生成的影响,要远弱于合成激素药物。与此对应,在妇女的整个月经周期当中,即便在雌二醇水平大幅波动的情况下,SHBG 水平亦仅有小幅变化<sup>([Freymann et al., 1977b][F77b]; [Plymate et al., 1985][P85]; [Schijf et al., 1993][S93]; [Braunstein et al., 2011][B11]; [Rothman et al., 2011][R11]; [Fanelli et al., 2013][F13]; [Rezaii et al., 2017][R17])</sup>。在一项研究中,从卵泡期过渡到黄体期时,SHBG 水平增加了约 6-13%(即 2.9–5.3 nmol/L)。此外,在更年期,即使雌二醇水平急剧降低,SHBG 水平也仅降低少许<sup>([Burger et al., 2000][B00]; [Guthrie et al., 2004][G04])</sup>。还有,接受雌二醇治疗时,在特定情形下还会显著地影响 SHBG 及其它肝蛋白的生成<sup>([Kuhl, 1998][K98])</sup>。这是因为:1) 口服雌二醇的使用,因肝脏的首过效应,其对雌激素相关的肝脏分泌活动造成的影响相较非口服形式会更大;2) 高剂量雌二醇的使用,例如使用注射剂时的通常剂量。
|
||||
下表展示了来自各研究项目的,不同雌激素给药途径、剂量及类型下的 SHBG 增幅。
|
||||
|
||||
> 【表二】不同雌激素暴露量下的 SHBG 增幅:
|
||||
>
|
||||
> | 雌激素形式 | 剂量 | 通常的雌二醇水平<sup>(1)</sup> | SHBG 倍数 | 数据来源 |
|
||||
> |-|-|-|-|-|
|
||||
> | 口服雌二醇 | 1 mg/天 | \~25 pg/mL | 1.6x | Kuhl (1998) |
|
||||
> | | 2 mg/天 | \~50 pg/mL | 2.2x | Kuhl (1998) |
|
||||
> | | 4 mg/天 | \~100 pg/mL | 1.9-3.2x | [Fåhraeus & Larsson-Cohn (1982)][FL82];<br/>[Gibney et al. (2005)][G05];<br/>[Ropponen et al. (2005)][R05] |
|
||||
> | 口服戊酸雌二醇<sup>(2)</sup> | 6 mg/天 | \~112.5 pg/mL | 3.0x | [Dittrich et al. (2005)][D05] |
|
||||
> | 雌二醇贴片 | 50 μg/天 | \~50 pg/mL | 1.1x | Kuhl (2005) |
|
||||
> | | 100 μg/天 | \~100 pg/mL | 1.2x | Shifren et al. (2008) |
|
||||
> | | 200 μg/天 | \~200 pg/mL | \~1.5x | [Smith et al. (2019)][S19] |
|
||||
> | | 300 μg/天 | \~300 pg/mL | \~1.7x | Smith et al. (2019) |
|
||||
> | | 600 μg/天 | \~600 pg/mL | 2.3x | [Bland et al. (2005)][B05] |
|
||||
> | 十一酸雌二醇注射剂 | 100 mg/月 | \~550 pg/mL | 2.0x | [Derra (1981)][D81] |
|
||||
> | 聚磷酸雌二醇注射剂 | 320 mg/月 | \~700 pg/mL | 1.7x | [Stege et al. (1988)][S88] |
|
||||
> | 戊酸雌二醇注射剂 | 10 mg/十天 | 不定(较高) | 3.2x | [Mueller et al. (2011)][M11] |
|
||||
> | 口服炔雌醇 | 10 μg/天 | - | 3.0x | Kuhl (1998) |
|
||||
> | | 50 μg/天 | - | 4.0x | [Kuhl (1997)][K97] |
|
||||
> | 合成雌激素 | 很高 | - | 5-10x | von Schoultz et al. (1989) |
|
||||
>
|
||||
> (1) 依据多个来源的估计值<sup>(例如[维基百科][WIKI-1]; [Aly W., 2020][AW20-E2])</sup>。
|
||||
> (2) 由于分子质量的不同,戊酸雌二醇所含雌二醇,相当于同等质量雌二醇的约 75%;因此,6 mg/天剂量的戊酸雌二醇相当于摄入 4.5 mg/天的雌二醇。
|
||||
<section class="box">
|
||||
|
||||
雌二醇对 SHBG 水平的影响与妊娠联系最密切,妊娠时雌二醇水平远高于正常值。在妊娠后期,雌二醇平均水平通常可达约 15000-25000 pg/mL<sup>([图表][GRAPH-1]; [Troisi et al., 2003][T03]; [Adamcová et al., 2018][A18])</sup>;该值相当于正常月经周期内之水平的 100 倍左右。妊娠后期,在雌二醇水平大幅上升的同时,SHBG 水平也升高约 5-10 倍<sup>(Anderson, 1974; [Hammond, 2017][HAM17])</sup>。
|
||||
**表 2**:不同雌激素暴露量下的 SHBG 增幅:
|
||||
|
||||
| 雌激素形式 | 剂量 | 通常的雌二醇水平<sup>(1)</sup> | SHBG 倍数 | 数据来源 |
|
||||
|-|-|-|-|-|
|
||||
| 口服雌二醇 | 1 mg/天 | \~25 pg/mL | 1.6x | Kuhl (1998) |
|
||||
| | 2 mg/天 | \~50 pg/mL | 2.2x | Kuhl (1998) |
|
||||
| | 4 mg/天 | \~100 pg/mL | 1.9-3.2x | [Fåhraeus & Larsson-Cohn (1982)][FL82];<br/>[Gibney et al. (2005)][G05];<br/>[Ropponen et al. (2005)][R05] |
|
||||
| 口服戊酸雌二醇<sup>(2)</sup> | 6 mg/天 | \~112.5 pg/mL | 3.0x | [Dittrich et al. (2005)][D05] |
|
||||
| 雌二醇贴片 | 50 μg/天 | \~50 pg/mL | 1.1x | Kuhl (2005) |
|
||||
| | 100 μg/天 | \~100 pg/mL | 1.2x | Shifren et al. (2008) |
|
||||
| | 200 μg/天 | \~200 pg/mL | \~1.5x | [Smith et al. (2019)][S19] |
|
||||
| | 300 μg/天 | \~300 pg/mL | \~1.7x | Smith et al. (2019) |
|
||||
| | 600 μg/天 | \~600 pg/mL | 2.3x | [Bland et al. (2005)][B05] |
|
||||
| 十一酸雌二醇注射剂 | 100 mg/月 | \~550 pg/mL | 2.0x | [Derra (1981)][D81] |
|
||||
| 聚磷酸雌二醇注射剂 | 320 mg/月 | \~700 pg/mL | 1.7x | [Stege et al. (1988)][S88] |
|
||||
| 戊酸雌二醇注射剂 | 10 mg/十天 | 不定(较高) | 3.2x | [Mueller et al. (2011)][M11] |
|
||||
| 口服炔雌醇 | 10 μg/天 | - | 3.0x | Kuhl (1998) |
|
||||
| | 50 μg/天 | - | 4.0x | [Kuhl (1997)][K97] |
|
||||
| 合成雌激素 | 很高 | - | 5-10x | von Schoultz et al. (1989) |
|
||||
|
||||
(1) 依据多个来源的估计值<sup>(例如[维基百科][WIKI-1]; [Aly W., 2020][AW20-E2])</sup>。
|
||||
(2) 由于分子质量的不同,戊酸雌二醇所含雌二醇,相当于同等质量雌二醇的约 75%;因此,6 mg/天剂量的戊酸雌二醇相当于摄入 4.5 mg/天的雌二醇。
|
||||
|
||||
</section>
|
||||
|
||||
雌二醇对 SHBG 水平的影响与妊娠联系最密切,妊娠时雌二醇水平远高于正常值。在妊娠后期,雌二醇平均水平通常可达约 15000-25000 pg/mL<sup>([图表][GRAPH-1]; [Troisi et al., 2003][T03]; [Adamcová et al., 2018][A18])</sup>;该值相当于正常月经周期内之水平的 100 倍左右。妊娠后期,在雌二醇水平大幅上升的同时,SHBG 水平也升高约 5-10 倍<sup>(Anderson, 1974; [Hammond, 2017][HAM17])</sup>。
|
||||
雌激素对 SHBG 之生成的剂量—反应曲线,显示了(SHBG 存在)饱和状态,表现在 SHBG 水平的升高多发生在雌二醇水平较低的区间、以及 SHBG 水平存在上限<sup>([Mean, Pellaton, & Magrini, 1977][MPM77]; [O’Leary et al., 1991][O91]; [Kerlan et al., 1994][K94]; [Kuhl, 1999][K99])</sup>。下图展示了妊娠期间 SHBG 水平的变化。
|
||||
|
||||
> 
|
||||
>
|
||||
> 【图一】妊娠期间,SHBG 及总和雌二醇水平的变化<sup>(O’Leary et al., 1991)</sup>。其中,实线表示平均值/第 95 百分位数,而散点表示对各受试个体的测量值。
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
> 
|
||||
>
|
||||
> 【图二】妊娠期间,SHBG 与性激素总和水平的变化<sup>(Kerlan et al., 1994)</sup>。
|
||||
**图 1**:妊娠期间,SHBG 及总和雌二醇水平的变化<sup>(O’Leary et al., 1991)</sup>。其中,实线表示平均值/第 95 百分位数,而散点表示对各受试个体的测量值。
|
||||
|
||||
</section>
|
||||
|
||||
## SHBG 水平之升高对游离性激素水平的影响
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 2**:妊娠期间,SHBG 与性激素总和水平的变化<sup>(Kerlan et al., 1994)</sup>。
|
||||
|
||||
</section>
|
||||
|
||||
## SHBG 水平之升高对游离性激素水平的影响 {#effects-of-shbg-increase-on-free-sex-hormone-levels}
|
||||
|
||||
SHBG 水平的变化会引起与 SHBG 结合的性激素与游离性激素水平的改变。在这方面,除了 DHT 之外,雌二醇与睾酮是与之关联性最大的激素。
|
||||
|
||||
### SHBG 水平之升高与游离睾酮的关系
|
||||
### SHBG 水平之升高与游离睾酮的关系 {#shbg-increase-and-free-testosterone}
|
||||
|
||||
含炔雌醇(EE)的避孕药,在将 SHBG 水平提升 4 倍的同时,会显著降低游离睾酮比例<sup>([Graham et al., 2007][G07]; [Zimmerman et al., 2014][Z14])</sup>。在一项研究中,服用一片含 EE 的避孕药,可将游离睾酮比例从 2.45% 降至 0.78%(仅为前者的 32% 之多)<sup>(Graham et al., 2007)</sup>。由于其还可抑制睾酮生成、从而降低睾酮总和水平,故游离睾酮水平从 0.89 pg/mL 降至 0.18 pg/mL(仅为前者的 20% 之多)<sup>(Graham et al., 2007)</sup>。EE 对 SHBG 水平的影响,显著地增强了含 EE 的避孕药之抗雄效力,这也使得其被用于治疗女性痤疮及多毛症。
|
||||
|
||||
妊娠期间,睾酮水平可高达 150 ng/dL(约 5 倍于非孕期水平)<sup>([McClamrock, 2007][M07])</sup>。妊娠期间 SHBG 生成的增多,在其对高水平的睾酮生物活性之中和上起到了重要作用<sup>(Hammond, 2017)</sup>。在一项研究中,妊娠后期的游离睾酮比例(0.23%)降至非孕期(1.36%)的 17%<sup>(Dunn, Nisula, & Rodbard, 1981)</sup>。因此,妊娠期间尽管有睾酮总和水平的大幅上升,但游离睾酮水平——或者说,体内雄激素作用——几乎不变<sup>([Barini, Liberale, & Menini, 1993][BLM93]; Schuijt et al., 2019)</sup>。一例由 SHBG 严重不足引起高雄激素血症的孕妇病例,证实了妊娠期 SHBG 对睾酮的雄激素活性之抑制作用<sup>([Hogeveen et al., 2002][H02]; Hammond, 2017)</sup>。
|
||||
|
||||
### SHBG 水平之升高与游离雌二醇的关系
|
||||
### SHBG 水平之升高与游离雌二醇的关系 {#shbg-increase-and-free-estradiol}
|
||||
|
||||
#### 内源性与非口服形式的雌二醇
|
||||
#### 内源性与非口服形式的雌二醇 {#endogenous-and-non-oral-estradiol}
|
||||
|
||||
研究表明,在生理水平的雌二醇(如 <200 pg/mL)之下,SHBG 水平的增幅、以及游离雌二醇比例的降幅皆甚微。只要雌二醇来源并非口服,无论内源还是外源皆如此。这是由诸研究项目的游离雌二醇数据(通过计算或测量而得)所得出的结论<sup>(例如 Freymann et al., 1977b)</sup>。
|
||||
|
||||
|
|
@ -124,92 +140,106 @@ SHBG 水平的变化会引起与 SHBG 结合的性激素与游离性激素水平
|
|||
|
||||
妊娠期间,尽管游离雌二醇比例确实降低了,但增加的雌二醇远比被 SHBG 中和的要多;因此,游离雌二醇的情况与游离睾酮大相径庭。以下是一篇摘录对此的叙述<sup>([Rubinow et al., 2002][R02])</sup>:
|
||||
|
||||
> 血浆中许多甾体与多肽激素之水平随妊娠而缓慢、但持续地增长,而分娩后的几日内则骤降。当妊娠进入后三个月时,血浆孕激素水平平均在 150 ng/mL 左右,而雌二醇水平则达 10-15 ng/mL;其分别相当于月经周期内最大值的 10 倍和 50 倍<sup>(Tulchinsky et al., 1972)</sup>。妊娠期间,尽管这些甾体激素只有一小部分未被结合,但“游离”(即具备生物活性)的孕激素与雌激素总量仍大幅增加<sup>(Heidrich et al., 1994)</sup>。
|
||||
血浆中许多甾体与多肽激素之水平随妊娠而缓慢、但持续地增长,而分娩后的几日内则骤降。当妊娠进入后三个月时,血浆孕激素水平平均在 150 ng/mL 左右,而雌二醇水平则达 10-15 ng/mL;其分别相当于月经周期内最大值的 10 倍和 50 倍<sup>(Tulchinsky et al., 1972)</sup>。妊娠期间,尽管这些甾体激素只有一小部分未被结合,但“游离”(即具备生物活性)的孕激素与雌激素总量仍大幅增加<sup>(Heidrich et al., 1994)</sup>。
|
||||
|
||||
该摘录引用了一项由 Heidrich 及其同行进行的研究,后者发现在分娩时,雌二醇总和水平达 21500 pg/mL,游离雌二醇水平则测得 232 pg/mL(占比约 1.08%)<sup>([Heidrich et al., 1994][H94])</sup>。相比之下,非孕期妇女的游离雌二醇比例为 1.5-2.1%[经免疫测定法(RIA)测定];而其游离雌二醇水平则达 0.30-4.1 pg/mL(经 RIA 测定),或 0.40-5.9 pg/mL[经质谱测定法(MS)或液相色谱-质谱联用法(LC-MS)测定]<sup>([Jameson & De Groot, 2015][JG15])</sup>。因此,在此研究中的妊娠后期游离雌二醇水平,约为非孕期水平最大值的 50 倍。
|
||||
|
||||
因检测方法不同,来自单一研究的发现可能不具备代表性;故于下表列出取自多个项目的、妊娠后期游离雌二醇比例的测量值。
|
||||
|
||||
> 【表三】妊娠后期游离雌二醇比例的测量值(平均值 ± 标准差)<sup>([Perry et al., 1987][P87])</sup>:
|
||||
>
|
||||
> | 研究项目 | 测量方法 | 采样次数 | 游离雌二醇 (%) |
|
||||
> |-|-|-|-|
|
||||
> | Perry et al. (1987) | 离心超滤法 | 25 | 1.27 ± 0.23 |
|
||||
> | [Hammond et al. (1980)][H80] | 离心超滤法 | 5 | 0.96 ± 0.12 |
|
||||
> | Heidrich et al. (1994) | 离心超滤法 | 26 | 1.08 |
|
||||
> | [Tulchinsky et al. (1973)][T73] | 平衡透析法 | 5 | 0.67 ± 0.18 |
|
||||
> | [Freymann et al. (1977a)][F77a] | 平衡透析法 | 17 | 1.15 |
|
||||
> | [Anderson et al. (1986)][A86] | 稳态凝胶过滤法 | 12 | 1.48 ± 0.55 |
|
||||
<section class="box">
|
||||
|
||||
如上表所示,妊娠后期游离雌二醇比例约在 0.7-1.5% 之间。而经计算(而非测量)得出的结果,与测量值相近,不过有的显得略低(如 0.5%)<sup>(Dunn, Nisula, & Rodbard, 1981; [Campino et al., 2001][C01])</sup>。
|
||||
**表 3**:妊娠后期游离雌二醇比例的测量值(平均值 ± 标准差)<sup>([Perry et al., 1987][P87])</sup>:
|
||||
|
||||
| 研究项目 | 测量方法 | 采样次数 | 游离雌二醇 (%) |
|
||||
|-|-|-|-|
|
||||
| Perry et al. (1987) | 离心超滤法 | 25 | 1.27 ± 0.23 |
|
||||
| [Hammond et al. (1980)][H80] | 离心超滤法 | 5 | 0.96 ± 0.12 |
|
||||
| Heidrich et al. (1994) | 离心超滤法 | 26 | 1.08 |
|
||||
| [Tulchinsky et al. (1973)][T73] | 平衡透析法 | 5 | 0.67 ± 0.18 |
|
||||
| [Freymann et al. (1977a)][F77a] | 平衡透析法 | 17 | 1.15 |
|
||||
| [Anderson et al. (1986)][A86] | 稳态凝胶过滤法 | 12 | 1.48 ± 0.55 |
|
||||
|
||||
</section>
|
||||
|
||||
如上表所示,妊娠后期游离雌二醇比例约在 0.7-1.5% 之间。而经计算(而非测量)得出的结果,与测量值相近,不过有的显得略低(如 0.5%)<sup>(Dunn, Nisula, & Rodbard, 1981; [Campino et al., 2001][C01])</sup>。
|
||||
这些测量值可与非孕期妇女的 1.5-2.1% 做审慎比较。如分别取中位数,则妊娠后期的游离雌二醇比例应大致为非孕期的 60%。此估计值与一项研究测量的实际结果(相比非孕期降至 55%)相当接近<sup>(Freymann et al., 1977a; Freymann et al., 1977b)</sup>。
|
||||
|
||||
雌酮、雌三醇的情况与雌二醇相反:其游离比例在妊娠后期与非孕期时并无区别。
|
||||
雌酮、雌三醇的情况与雌二醇相反:其游离比例在妊娠后期与非孕期时并无区别。
|
||||
一些研究也测定了妊娠早期游离雌二醇比例——理论上妊娠早期的情况应与后期有异。下表列出了一项研究中对整个妊娠期内游离雌二醇测定的结果。
|
||||
|
||||
> 【表四】妊娠期间雌二醇(E2)总和水平及游离水平的变化(平均值 ± 标准差)<sup>(Freymann et al., 1977a/b)</sup>:
|
||||
>
|
||||
> | 时间段 | 采样次数 | E2 (ng/mL) | 倍数 | 游离E2 (%) | 增幅 | 游离E2 (pg/mL) | 倍数 |
|
||||
> |-|-|-|-|-|-|-|-|
|
||||
> | 非孕期 | 35 | 0.16 ± 0.10 | 1.0× | 2.2 ± 0.4 | –0% | 3.5 ± 2.0 | 1.0× |
|
||||
> | 妊娠 6-20 周 | 9 | 2.0 ± 1.1 | 13× | 1.6 ± 0.4 | –27% | 32 ± 21 | 9.1× |
|
||||
> | 妊娠 12–20 周 | 10 | 5.5 ± 2.2 | 34× | 1.3 ± 0.3 | –41% | 72 ± 39 | 21× |
|
||||
> | 妊娠 20–30 周 | 12 | 10.8 ± 4.6 | 68× | 1.2 ± 0.3 | –45% | 130 ± 74 | 37× |
|
||||
> | 妊娠 30–38 周 | 17 | 16.0 ± 7.0 | 100× | 1.2 ± 0.2 | –45% | 184 ± 103 | 53× |
|
||||
<section class="box">
|
||||
|
||||
**图 4**:妊娠期间雌二醇(E2)总和水平及游离水平的变化(平均值 ± 标准差)<sup>(Freymann et al., 1977a/b)</sup>:
|
||||
|
||||
| 时间段 | 采样次数 | E2 (ng/mL) | 倍数 | 游离E2 (%) | 增幅 | 游离E2 (pg/mL) | 倍数 |
|
||||
|-|-|-|-|-|-|-|-|
|
||||
| 非孕期 | 35 | 0.16 ± 0.10 | 1.0× | 2.2 ± 0.4 | –0% | 3.5 ± 2.0 | 1.0× |
|
||||
| 妊娠 6-20 周 | 9 | 2.0 ± 1.1 | 13× | 1.6 ± 0.4 | –27% | 32 ± 21 | 9.1× |
|
||||
| 妊娠 12–20 周 | 10 | 5.5 ± 2.2 | 34× | 1.3 ± 0.3 | –41% | 72 ± 39 | 21× |
|
||||
| 妊娠 20–30 周 | 12 | 10.8 ± 4.6 | 68× | 1.2 ± 0.3 | –45% | 130 ± 74 | 37× |
|
||||
| 妊娠 30–38 周 | 17 | 16.0 ± 7.0 | 100× | 1.2 ± 0.2 | –45% | 184 ± 103 | 53× |
|
||||
|
||||
</section>
|
||||
|
||||
由另一研究者群体进行的研究,也测定了妊娠早期(7-16 周)的游离雌二醇比例,结果发现其低于 Freymann 及其同行的测量值;第 10 周的测量值约为 0.9-1.0%,到第 12 周则测得约 0.7%<sup>([Bernstein et al., 1986][B86]; [Depue et al., 1987][D87]; [Bernstein et al., 1988][B88])</sup>。因此,与 Freymann 及其同行的结果相似,游离雌二醇比例随妊娠进行而降低。下图以可视化方式展示其发现。
|
||||
|
||||
> 
|
||||
>
|
||||
> 【图三】妊娠第 7-16 周,雌二醇总和与游离水平 (pg/mL)、游离雌二醇比例 (%) 以及 SHBG 结合能力 (μg/dL) 的变化<sup>(Bernstein et al., 1986)</sup>。
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 3**:妊娠第 7-16 周,雌二醇总和与游离水平 (pg/mL)、游离雌二醇比例 (%) 以及 SHBG 结合能力 (μg/dL) 的变化<sup>(Bernstein et al., 1986)</sup>。
|
||||
|
||||
</section>
|
||||
|
||||
妊娠期游离雌二醇亦可通过雌二醇总和水平及 SHBG 水平计算得出。笔者使用 O’Leary 等人 (1991) 发表的数据与 [Mazer (2009)][M09] 公开的电子表格计算器,粗略计算了妊娠期的游离雌二醇比例<sup>([Aly W., 2020][SUPPL])</sup>。结果见下。
|
||||
|
||||
> 
|
||||
>
|
||||
> 【图四】整个妊娠期当中的 SHBG 与雌二醇总和水平测量值,以及游离雌二醇比例计算值。
|
||||
> 本图的[另一个版本](https://transfemscience.org/assets/images/fdd36yplqia51.png)仅显示妊娠早期的变化(此时雌二醇水平通常不大于 2000 pg/mL)。
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 4**:整个妊娠期当中的 SHBG 与雌二醇总和水平测量值,以及游离雌二醇比例计算值。
|
||||
本图的[另一个版本](https://transfemscience.org/assets/images/fdd36yplqia51.png)仅显示妊娠早期的变化(此时雌二醇水平通常不大于 2000 pg/mL)。
|
||||
|
||||
</section>
|
||||
|
||||
图中的游离雌二醇比例仅为粗略估计,对此应有所保留。无论如何,其很接近于上文所讨论的研究项目对妊娠早期游离雌二醇的测量值——在数值上与 Bernstein 等人的相似,而在整个孕期的变化模式上则与 Bernstein 等人、Freymann 等人的相似。综上,此计算值所展现的模型不仅合理,也具有意义。
|
||||
|
||||
总的而言,妊娠期间雌二醇总和水平大幅上升,而 SHBG 水平也有较大提升(不过幅度相对较小);相应地,游离雌二醇比例随妊娠进行而逐渐降低。现有的研究就游离雌二醇比例降至何种程度尚有所矛盾;但无论如何,到妊娠后期,该比例应该介于 0.5-1.5% 左右。该比例可与非孕期的游离雌二醇比例(1.5-2.1%)做比较,前者约为后者的 60%;极端情况下,该数字可达 25%。
|
||||
总的而言,妊娠期间雌二醇总和水平大幅上升,而 SHBG 水平也有较大提升(不过幅度相对较小);相应地,游离雌二醇比例随妊娠进行而逐渐降低。现有的研究就游离雌二醇比例降至何种程度尚有所矛盾;但无论如何,到妊娠后期,该比例应该介于 0.5-1.5% 左右。该比例可与非孕期的游离雌二醇比例(1.5-2.1%)做比较,前者约为后者的 60%;极端情况下,该数字可达 25%。
|
||||
与妊娠后期相反,在雌二醇水平更低的妊娠早期,游离雌二醇比例会更高。
|
||||
|
||||
妊娠期间,尽管游离雌二醇比例降低了,但游离雌二醇水平随着总和雌二醇的大幅增加也有不小增长。由此可见,雌二醇水平的升高明显突破了与之一同上升的 SHBG 水平对其的限制作用。故此,妊娠会让人处于一种雌激素效力极高的状态。
|
||||
|
||||
妊娠期间,SHBG 对雌二醇的影响并不及对睾酮的那样,因为雌二醇水平的增长远大于 SHBG 的增长,而且雌二醇对 SHBG 的亲和力也不及睾酮。一般来说,与抑制睾酮的情况不同,要抑制随雌二醇水平大幅提高的雌二醇活性,则无疑需要极大提高 SHBG 的产量,而这是不可能的。
|
||||
|
||||
|
||||
#### 口服雌二醇
|
||||
#### 口服雌二醇 {#oral-estradiol}
|
||||
|
||||
在游离雌二醇方面,口服雌二醇的表现或与非口服形式有所不同。这是因为,肝脏的首过效应会使其在肝脏中产生的雌二醇水平要高于血液中的水平,从而使得其对肝脏的效力与非口服形式不相称、SHBG 水平的增幅也更高。故此,口服雌二醇所引起的更高 SHBG 水平会导致游离雌二醇比例相较非口服形式更低。
|
||||
|
||||
如果要比较口服和非口服形式的雌二醇在游离雌二醇方面之差异,会发现测量其准确值愈发困难——不过这确实是可能的,迄今也有一些相关数据发表。一些有关更年期顺性别妇女使用低剂量口服雌二醇的临床研究称,SHBG 增加后对游离雌二醇(计算值)的限制作用较小<sup>([Nilsson, Holst, & von Schoultz, 1984][NHS84]; [Nachtigall et al., 2000][N00])</sup>。类似地,口服雌二醇对更年期症状显现的效果与非口服形式相近<sup>([维基百科][WIKI-2]; 见第二段)</sup>。
|
||||
迄今罕有研究项目提供关于更高剂量的口服雌二醇所引起的 SHBG 或游离雌二醇水平数据;不过有这么一项研究,其发现跨性别女性使用 6 mg/天剂量的口服戊酸雌二醇(大致相当于 4.5 mg/天口服雌二醇),可将 SHBG 水平升高约 3.0 倍<sup>(Dittrich et al., 2005)</sup>。依据该项目有关总和雌二醇与 SHBG 水平的数据,可以粗略计算<sup>(Mazer, 2009)</sup>,其游离雌二醇比例应该从 2.1% 左右降至 1.2%(降幅达 43%)。与此类似,有一项研究使用了口服结合雌激素(“倍美力”),将 SHBG 水平升高 2.3 倍;其也报告相较于同等剂量(即总和雌二醇水平相当)的透皮雌二醇,游离雌二醇比例(计算值)要低出 40%<sup>([Shifren et al., 2007][S07])</sup>。
|
||||
如果要比较口服和非口服形式的雌二醇在游离雌二醇方面之差异,会发现测量其准确值愈发困难——不过这确实是可能的,迄今也有一些相关数据发表。一些有关更年期顺性别妇女使用低剂量口服雌二醇的临床研究称,SHBG 增加后对游离雌二醇(计算值)的限制作用较小<sup>([Nilsson, Holst, & von Schoultz, 1984][NHS84]; [Nachtigall et al., 2000][N00])</sup>。类似地,口服雌二醇对更年期症状显现的效果与非口服形式相近<sup>([维基百科][WIKI-2]; 见第二段)</sup>。
|
||||
迄今罕有研究项目提供关于更高剂量的口服雌二醇所引起的 SHBG 或游离雌二醇水平数据;不过有这么一项研究,其发现跨性别女性使用 6 mg/天剂量的口服戊酸雌二醇(大致相当于 4.5 mg/天口服雌二醇),可将 SHBG 水平升高约 3.0 倍<sup>(Dittrich et al., 2005)</sup>。依据该项目有关总和雌二醇与 SHBG 水平的数据,可以粗略计算<sup>(Mazer, 2009)</sup>,其游离雌二醇比例应该从 2.1% 左右降至 1.2%(降幅达 43%)。与此类似,有一项研究使用了口服结合雌激素(“倍美力”),将 SHBG 水平升高 2.3 倍;其也报告相较于同等剂量(即总和雌二醇水平相当)的透皮雌二醇,游离雌二醇比例(计算值)要低出 40%<sup>([Shifren et al., 2007][S07])</sup>。
|
||||
以上发现表明,在女性倾向跨性别者通常使用的剂量下,口服雌二醇会降低游离雌二醇比例,而这不容忽视。所以,即使总和雌二醇水平相当,口服雌二醇的效力可能也在某种程度上不及非口服形式。
|
||||
|
||||
不过需要明白,这一点尚未完全确定。在雌酮水平上,口服雌二醇要远高于非口服形式(约 5 倍)<sup>(Kuhl, 2005)</sup>,而雌酮尽管在效力上弱于雌二醇,但也有不小的、类似雌二醇的固有雌激素活性<sup>([Aly W., 2019][AW19])</sup>。目前尚不明确雌酮会在多大程度上增强雌二醇的雌激素活性(如果有的话);不过,大幅增强的可能性很高<sup>([Pande et al., 2019][P19]; [表格][TABLE-1])</sup>。这样的话,额外的雌激素暴露量可能会弥补由口服雌二醇引起的高 SHBG 水平及较低游离雌二醇比例所造成的影响。然而,尚需更多研究来评估这一可能性。
|
||||
不过需要明白,这一点尚未完全确定。在雌酮水平上,口服雌二醇要远高于非口服形式(约 5 倍)<sup>(Kuhl, 2005)</sup>,而雌酮尽管在效力上弱于雌二醇,但也有不小的、类似雌二醇的固有雌激素活性<sup>([Aly W., 2019][AW19])</sup>。目前尚不明确雌酮会在多大程度上增强雌二醇的雌激素活性(如果有的话);不过,大幅增强的可能性很高<sup>([Pande et al., 2019][P19]; [表格][TABLE-1])</sup>。这样的话,额外的雌激素暴露量可能会弥补由口服雌二醇引起的高 SHBG 水平及较低游离雌二醇比例所造成的影响。然而,尚需更多研究来评估这一可能性。
|
||||
此外,还需要考虑到,除游离雌二醇之外,口服雌二醇引起的高 SHBG 水平应该还会降低游离睾酮比例(而且降幅会更大)。这一点尤为重要,因为对于女性倾向跨性别者,对睾酮的压制是雌二醇疗效的关键一环,也是保持较高雌二醇水平的首要正当理由。基于上述可能性,以及激素游离水平仅可代表其理论生物活性的事实,不应想当然地认为口服雌二醇不及非口服形式有效。这个问题只能让对口服和非口服雌二醇做进一步比较的临床研究来解释了。
|
||||
|
||||
## 对女性化激素疗法的意义
|
||||
## 对女性化激素疗法的意义 {#relevance-for-transfeminine-hormone-therapy}
|
||||
|
||||
有些女性倾向跨性别者担心,SHBG 会相当程度地限制雌二醇效力,从而对其女性化/乳房发育过程造成阻碍。还有人声称,较高的雌二醇水平会引起 SHBG 的升高,从而会让其效力低于较低雌二醇水平。然而,即使不考虑 SHBG 的情况,这些观点也很可能有误;这是因为,较低雌二醇水平(不足 50 pg/mL)已知足以在女性化、及乳房发育方面产生完全效力——这点在经历正常或诱发的青春期的顺性别女孩<sup>([Aly W., 2020][AW20-HLFP])</sup>以及患有完全性雄激素不敏感综合征(CAIS)的、第二性征发育良好的女性身上被证实<sup>([Aly W., 2020][AW20-CAIS]; [维基百科][WIKI-3])</sup>。目前尚无证据表明,需要较高雌二醇水平以更好地促进女性化或乳房发育<sup>([Nolan & Cheung, 2020][NC20])</sup>。事实上,现有研究认为,临床上通常水平下的雌二醇(如 50-200 pg/mL)与女性倾向跨性别者的乳房发育不存在关联性<sup>([de Blok et al., 2018][B18]; [Meyer et al., 2020][M20]; [de Blok et al., 2020][B20])</sup>。这与一项观点相契合:较低的雌二醇水平便已能够确保女性化及乳房发育效果最大化。因此,因为对雌激素暴露量不足、从而使女性化效果不完全的担忧,而使用高剂量雌二醇,是没有道理的;只当在需要压制睾酮的情况下才合乎情理。
|
||||
|
||||
不过,即使要深入探究 SHBG,从现有研究表明的 SHBG 在限制游离雌二醇——很可能也在限制雌二醇的生物活性——方面的作用也只能说有那么一些。在非孕期雌二醇的生理水平下,由内源性及非口服形式的雌二醇引起的 SHBG 水平及游离雌二醇比例之变化相当微小。然而,当雌二醇水平相当高时,对 SHBG 之生成的影响才会更大。妊娠期内,随着大量增多的雌二醇而上升多达 5-10 倍的 SHBG 水平,会使游离雌二醇比例降低至非孕期的 60%;但同时游离雌二醇的实际水平也会大幅上扬。而且,妊娠早期 SHBG 水平的增幅、以及游离雌二醇比例的降幅都要小于妊娠后期。
|
||||
不过,即使要深入探究 SHBG,从现有研究表明的 SHBG 在限制游离雌二醇——很可能也在限制雌二醇的生物活性——方面的作用也只能说有那么一些。在非孕期雌二醇的生理水平下,由内源性及非口服形式的雌二醇引起的 SHBG 水平及游离雌二醇比例之变化相当微小。然而,当雌二醇水平相当高时,对 SHBG 之生成的影响才会更大。妊娠期内,随着大量增多的雌二醇而上升多达 5-10 倍的 SHBG 水平,会使游离雌二醇比例降低至非孕期的 60%;但同时游离雌二醇的实际水平也会大幅上扬。而且,妊娠早期 SHBG 水平的增幅、以及游离雌二醇比例的降幅都要小于妊娠后期。
|
||||
即使在非口服形式的雌二醇疗法所能达到的雌二醇水平最高位之下,由 SHBG 引起的游离雌二醇比例之降幅应该也很有限;仅需略为提高雌二醇剂量,便可覆盖其影响。
|
||||
|
||||
至于口服雌二醇,其情况则与上文不同:其对 SHBG 之生成的影响较非口服形式更大,SHBG 水平也更高,从而对游离雌二醇的限制作用更大。不过,目前有关这种游离雌二醇的降低会导致口服雌二醇的活性或效力减弱的说法仅存于理论可能。从疗效而言,口服雌二醇已经证明其自身非常有效;在低剂量下,游离雌二醇比例似乎降得并不多。此外,高剂量口服雌二醇对睾酮的压制作用,似乎与非口服形式相当——尽管尚无任何直接比较以佐证<sup>([维基百科][WIKI-4]; [图表][GRAPH-2])</sup>。除压制睾酮的效果外,现有研究并未发现口服与非口服形式雌二醇在女性化、乳房发育效果等方面有任何差异<sup>([Sam S., 2020][SS20])</sup>。
|
||||
至于口服雌二醇,其情况则与上文不同:其对 SHBG 之生成的影响较非口服形式更大,SHBG 水平也更高,从而对游离雌二醇的限制作用更大。不过,目前有关这种游离雌二醇的降低会导致口服雌二醇的活性或效力减弱的说法仅存于理论可能。从疗效而言,口服雌二醇已经证明其自身非常有效;在低剂量下,游离雌二醇比例似乎降得并不多。此外,高剂量口服雌二醇对睾酮的压制作用,似乎与非口服形式相当——尽管尚无任何直接比较以佐证<sup>([维基百科][WIKI-4]; [图表][GRAPH-2])</sup>。除压制睾酮的效果外,现有研究并未发现口服与非口服形式雌二醇在女性化、乳房发育效果等方面有任何差异<sup>([Sam S., 2020][SS20])</sup>。
|
||||
综上,在 SHBG 水平及游离雌二醇比例方面,口服与非口服形式的雌二醇应该基本不存在值得关注的疗效差别。
|
||||
|
||||
SHBG 水平的升高除了会降低游离雌二醇比例之外,还会降低游离睾酮比例,降幅亦更大。这点对女性倾向跨性别者很有利。
|
||||
|
||||
总而言之,女性倾向跨性别者无需过分担心因 SHBG 升高引起的游离雌二醇比例降低的影响——无论使用口服还是非口服形式的雌二醇。
|
||||
|
||||
## 辅助阅读材料
|
||||
## 辅助阅读材料 {#supplementary-material}
|
||||
|
||||
本文的辅助阅读材料[见此][SUPPL],其中有便于估算游离雌二醇水平的电子表格及其它计算器<sup>(如 Mazer, 2009)</sup>。
|
||||
|
||||
|
||||
[SH]: https://zh.wikipedia.org/wiki/%E6%80%A7%E7%B1%BB%E5%9B%BA%E9%86%87
|
||||
[PPB]: https://zh.wikipedia.org/wiki/%E8%A1%80%E6%B5%86%E8%9B%8B%E7%99%BD%E7%BB%93%E5%90%88
|
||||
[ALB]: https://zh.wikipedia.org/wiki/%E7%99%BD%E8%9B%8B%E7%99%BD
|
||||
|
|
@ -251,7 +281,6 @@ SHBG 水平的升高除了会降低游离雌二醇比例之外,还会降低游
|
|||
[G05]: https://doi.org/10.1210/jc.2005-0173
|
||||
[R05]: https://doi.org/10.1210/jc.2005-0352
|
||||
[D05]: http://doi.org/10.1055/s-2005-865900
|
||||
[S08]: https://doi.org/10.1210/jc.2007-2193
|
||||
[S19]: https://doi.org/10.1016/j.clgc.2019.09.019
|
||||
[B05]: https://doi.org/10.1002/cncr.20857
|
||||
[D81]: https://scholar.google.com/scholar?cluster=13814186946311677814
|
||||
|
|
@ -273,7 +302,6 @@ SHBG 水平的升高除了会降低游离雌二醇比例之外,还会降低游
|
|||
[Z14]: https://doi.org/10.1093/humupd/dmt038
|
||||
[M07]: https://books.google.com/books?id=Ch-BsGAOtucC&pg=PA108
|
||||
[BLM93]: https://doi.org/10.1093/clinchem/39.6.936
|
||||
[S19]: https://doi.org/10.1530/EC-19-0110
|
||||
[H02]: https://doi.org/10.1172/JCI14060
|
||||
|
||||
[R02]: https://books.google.com/books?id=6GgHpQdk8vYC&pg=PA54
|
||||
|
|
@ -309,4 +337,4 @@ SHBG 水平的升高除了会降低游离雌二醇比例之外,还会降低游
|
|||
[GRAPH-2]: https://en.wikipedia.org/wiki/Template:Antigonadotropic_effects_of_estradiol
|
||||
[SS20]: https://transfemscience.org/articles/oral-vs-transdermal-e2/
|
||||
|
||||
[SUPPL]: https://transfemscience.org/articles/shbg-suppl/
|
||||
[SUPPL]: https://transfemscience.org/articles/shbg-suppl/
|
||||
|
|
@ -1,143 +1,152 @@
|
|||
# 对女性倾向跨性别者舌下含服雌二醇以取代口服雌二醇的探索
|
||||
---
|
||||
title: 对女性倾向跨性别者舌下含服雌二醇以取代口服雌二醇的探索
|
||||
linkTitle: 替代口服:舌下含服雌二醇的有效性
|
||||
description: 雌二醇的舌下含服途径尽管研究较少,也有一定不足,但已在实践中行之有效,可作为口服途径的替代。
|
||||
author: Sam S.
|
||||
published: 2021-06-11
|
||||
updated: 2021-09-06
|
||||
translated: 2022-10-25
|
||||
translators:
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 雌激素
|
||||
- 用药途径与剂量
|
||||
trackHash: 7378b09b623aaedc898e8e60a30a5035fb5d10d2
|
||||
---
|
||||
|
||||
> - 作者 [Sam S.][AUTHOR]
|
||||
> + 首次发表于 2021 年 6 月 11 日
|
||||
> + 最后修改于 2021 年 9 月 6 日
|
||||
> + [原文出处][ORIGIN]
|
||||
> - 译者 [Bersella AI][TRANSLATOR]
|
||||
> + 翻译于 2022 年 10 月 25 日
|
||||
|
||||
[AUTHOR]: https://transfemscience.org/about/#sam-s
|
||||
[ORIGIN]: https://transfemscience.org/articles/sublingual-e2-transfem/
|
||||
[TRANSLATOR]: https://bersella-ai.cc/about-me/
|
||||
|
||||
## 译者按
|
||||
## 译者按 {#notice}
|
||||
|
||||
1. **<u>⚠免责声明:本文不构成任何医疗、处方建议。如有医疗需要,应于专业医师指导下进行。</u>**
|
||||
1. 本文系基于 Aly W. 所作《[舌下含服雌二醇及口服醋酸甲羟孕酮在女性倾向跨性别者中的应用][AW19-SUB]》的一次充分拓展的讨论,显然已取而代之。其译文仍可[于此][AW19-SUB-CN]查阅,以资参考。
|
||||
1. 本文系基于 Aly W. 所作《[舌下含服雌二醇及口服醋酸甲羟孕酮在女性倾向跨性别者中的应用][AW19-SUB]》的一次充分拓展的讨论,显然已取而代之。
|
||||
1. 因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
[AW19-SUB]: https://transfemscience.org/articles/sublingual-e2-mpa-jain-2019/
|
||||
[AW19-SUB-CN]: sublingual-e2-mpa-jain-2019.md
|
||||
|
||||
--------
|
||||
---
|
||||
|
||||
## 摘要
|
||||
## 摘要 {#abstract}
|
||||
|
||||
> 目前为止,全球已有数家性别诊所成功应用了雌二醇的舌下含服途径——尽管尚鲜有医学文献对其加以描述。舌下含服途径尽管可能存在一些实际不足之处,但在适当剂量下,其有效性与经济性应该能为临床经验与权威评价所证明。对于部分女性倾向跨性别者,舌下含服雌二醇应当可以代替口服,用于女性化激素疗法。
|
||||
|
||||
## 前言
|
||||
## 前言 {#introduction}
|
||||
|
||||
口服雌二醇片剂的最常用途径是口服,不过也可通过舌下、面颊含服<sup>([Kuhl, 2005][K05])</sup>。所谓舌下含服是指,将片剂置于舌头下方,使其溶解并被吸收,进入血液循环。而面颊含服与此类似,其需将片剂置于嘴唇与牙龈之间,片剂在此也会快速溶解并被吸收<sup>([Gass et al., 2004][G04]; [Bartlett & Maarschalk, 2012][BM12])</sup>。
|
||||
|
||||
许多女性倾向跨性别者会想知道有关舌下含服雌二醇的详情;在网上询问最多的问题有“我应该使用多大剂量的含服雌二醇?”“我应该隔多久含服一次?”“舌下含服比口服要好吗?”等等。
|
||||
|
||||
在早前,笔者曾对有关口服与舌下含服雌二醇之间之比较的文献作了评述<sup>([Sam S., 2020a][SS20a])</sup>。尽管不少女性倾向跨性别者已有舌下含服雌二醇的经验,对于自行用药者亦然,但笔者未在该评述当中提及舌下/面颊含服。其中部分原因包括,对此类不同于传统上更常用的途径的雌二醇用法给予关注的研究特别少;这貌似也是许多临床实践指南未囊括舌下含服雌二醇的原因所在<sup>([Aly W., 2020a][AW20-GUIDE])</sup>。而且,当时笔者希望只专注于口服雌二醇。
|
||||
在早前,笔者曾对有关口服与舌下含服雌二醇之间之比较的文献作了评述<sup>([Sam S., 2020a][SS20a])</sup>。尽管不少女性倾向跨性别者已有舌下含服雌二醇的经验,对于自行用药者亦然,但笔者未在该评述当中提及舌下/面颊含服。其中部分原因包括,对此类不同于传统上更常用的途径的雌二醇用法给予关注的研究特别少;这貌似也是许多临床实践指南未囊括舌下含服雌二醇的原因所在<sup>([Aly W., 2020a][AW20-GUIDE])</sup>。而且,当时笔者希望只专注于口服雌二醇。
|
||||
不过,在该评述发表之后,有好几篇关于女性倾向跨性别者舌下含服雌二醇的研究论文都发表了。有了这些新资料,笔者觉得有必要针对女性倾向跨性别者常见的问题,来深入剖析此类用法;于是便有了本文。本文对已发表的有关舌下含服雌二醇——尤其是其在跨性别护理方面的应用——的医学文献进行概述,以期为上述问题进行释疑。
|
||||
|
||||
需要指出,尽管舌下含服与面颊含服完全是两回事,但其作用机理与药理学特性非常相似<sup>([Perloff, 1950][P50]; [Chandrasekhara et al., 2002][C02])</sup>。因此,虽然笔者在此主要讨论的是舌下含服,但其中许多内容同样适用于面颊含服途径。
|
||||
|
||||
|
||||
## 舌下含服雌二醇的药理学特性
|
||||
## 舌下含服雌二醇的药理学特性 {#pharmacology-of-sublingual-estradiol}
|
||||
|
||||
目前舌下含服雌二醇在临床实践当中的使用,并不及口服或其它形式的雌二醇要普遍;不过,迄今已有一批研究项目对这种形式的药理学特性做了考察。这些项目的受试者包括已绝经顺性别妇女、女性倾向跨性别者及其他患者群体<sup>([Casper & Yen, 1981][CY81]; [Serhal & Craft, 1989][SC89]; [Deutsch, Bhakri & Kubicek, 2015][DBK15]; [Cirrincione et al., 2021][C21])</sup>。口服雌二醇、戊酸雌二醇片剂均可用于舌下含服<sup>([Serhal, 1990][S90])</sup>。
|
||||
|
||||
口服雌二醇之后,片剂成分会被肝脏大量代谢并失活,成为雌激素结合物<sup>([Kuhl, 2005][K05])</sup>。这些代谢物反过来会逐渐转换成雌二醇,使得雌二醇半衰期延长(约为 13-20 小时)<sup>([Stanczyk, Archer & Bhavnani, 2013][SAB13])</sup>。舌下含服雌二醇则与此相反:其不会大量经过肝脏,也不会因肝脏代谢而大幅失活;其很快就被吸收并直接进入血液循环。因此,舌下含服雌二醇的生物利用度要高于口服;这意味着只用较低剂量,便可达到相近的雌二醇累积水平<sup>([Kuhl, 2005][K05])</sup>(见下图)。这是舌下含服相较于口服的一项优势,其对剂量需求更小、药费也更少。
|
||||
|
||||
> 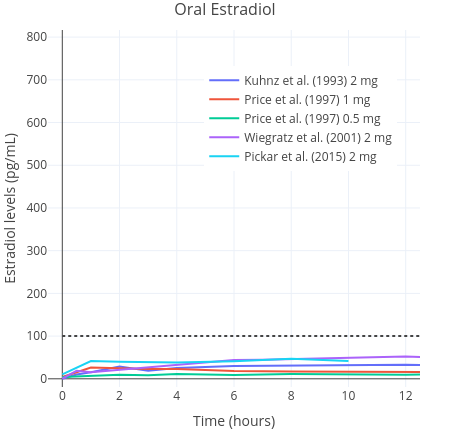
|
||||
> 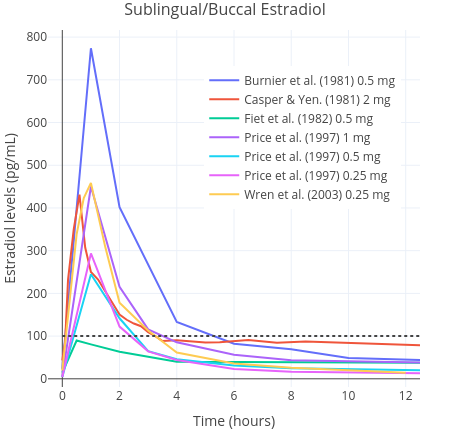
|
||||
>
|
||||
> ---
|
||||
>
|
||||
> 【多图表】口服(上)与舌下/面颊含服(下)的途径下,单次服用 0.25-2 mg 雌二醇(已微粉化)之后的药代动力学特性。数据来自多项研究<sup>([Burnier et al., 1981][B81]; [Casper & Yen, 1981][CY81]; [Fiet et al., 1982][F82]; [Kuhnz, Gansau & Mahler, 1993][KGM93]; [Price et al., 1997][P97]; [Wiegratz et al., 2001][W01]; [Wren et al., 2003][W03]; [Pickar et al., 2015][P15])</sup>。
|
||||
> 其中,横向虚线表示绝经前妇女大致的雌二醇综合平均水平<sup>([Verdonk et al., 2019][V19])</sup>。
|
||||
<section class="box">
|
||||
|
||||
由于在舌下含服过程中可能会不慎吞服部分雌二醇,故舌下含服途径很可能囊括了含服与口服给药的情况<sup>([Lobo, 1987][L87]; [Kuhl, 2005][K05])</sup>。一项正在进行的有关女性倾向跨性别者的研究在其初期报告里写道,单次舌下含服 1 mg 雌二醇之后的 1-2 小时内,雌二醇水平皆有所上升,最高达 179 pg/mL 以上;与此相反,口服 1 mg 雌二醇仅可达到 36 pg/mL 的水平峰值<sup>([Doll et al., 2020][D20])</sup>;此后雌二醇水平快速下降。另一些针对已绝经妇女的研究,同样观测到了类似的大幅上升的浓度峰值<sup>([Burnier et al., 1981][B81]; [Price et al., 1997][P97]; [Wren et al., 2003][W03])</sup>。雌二醇水平上升时,增幅被发现可达口服的十倍左右,随后快速下降,而消除半衰期仅有几个小时<sup>([Kuhl, 2005][K05])</sup>。在这方面,舌下含服雌二醇与静脉注射途径较为相似,后者在注射后也引起雌二醇水平的快速上升、消除半衰期则非常短<sup>([Kuhnz, Gansau & Mahler, 1993][KGM93])</sup>。同样类似的是经鼻腔给药途径<sup>([Devissaguet et al., 1999][D99])</sup>。
|
||||

|
||||

|
||||
|
||||
**多图表**:口服(上)与舌下/面颊含服(下)的途径下,单次服用 0.25-2 mg 雌二醇(已微粉化)之后的药代动力学特性。数据来自多项研究<sup>([Burnier et al., 1981][B81]; [Casper & Yen, 1981][CY81]; [Fiet et al., 1982][F82]; [Kuhnz, Gansau & Mahler, 1993][KGM93]; [Price et al., 1997][P97]; [Wiegratz et al., 2001][W01]; [Wren et al., 2003][W03]; [Pickar et al., 2015][P15])</sup>。
|
||||
其中,横向虚线表示绝经前妇女大致的雌二醇综合平均水平<sup>([Verdonk et al., 2019][V19])</sup>。
|
||||
</sup>。
|
||||
|
||||
</section>
|
||||
|
||||
由于在舌下含服过程中可能会不慎吞服部分雌二醇,故舌下含服途径很可能囊括了含服与口服给药的情况<sup>([Lobo, 1987][L87]; [Kuhl, 2005][K05])</sup>。一项正在进行的有关女性倾向跨性别者的研究在其初期报告里写道,单次舌下含服 1 mg 雌二醇之后的 1-2 小时内,雌二醇水平皆有所上升,最高达 179 pg/mL 以上;与此相反,口服 1 mg 雌二醇仅可达到 36 pg/mL 的水平峰值<sup>([Doll et al., 2020][D20])</sup>;此后雌二醇水平快速下降。另一些针对已绝经妇女的研究,同样观测到了类似的大幅上升的浓度峰值<sup>([Burnier et al., 1981][B81]; [Price et al., 1997][P97]; [Wren et al., 2003][W03])</sup>。雌二醇水平上升时,增幅被发现可达口服的十倍左右,随后快速下降,而消除半衰期仅有几个小时<sup>([Kuhl, 2005][K05])</sup>。在这方面,舌下含服雌二醇与静脉注射途径较为相似,后者在注射后也引起雌二醇水平的快速上升、消除半衰期则非常短<sup>([Kuhnz, Gansau & Mahler, 1993][KGM93])</sup>。同样类似的是经鼻腔给药途径<sup>([Devissaguet et al., 1999][D99])</sup>。
|
||||
由于尖峰较大、作用时间短,舌下含服雌二醇在浓度上的表现并不如其它剂型那样稳定。因此,这是和其它剂型的明显不同之处——像口服雌二醇在一天里就很少有激素水平上的波动。
|
||||
|
||||
已有研究报告了对舌下含服雌二醇之生物利用度的估计范围。其中一项针对已绝经妇女的小型随机性研究发现,在同等剂量下,舌下含服雌二醇引起的雌二醇累积水平较口服高出约 2.5 倍<sup>([Price et al., 1997][P97])</sup>。另一些研究则报告,舌下含服雌二醇的生物利用度估计值相对口服可达 5 倍之多<sup>([Pines et al., 1999][P99])</sup>。一项以绒猴进行试验的研究发现,舌下含服雌二醇的绝对生物利用度为 10%;此数字约为传统上对口服雌二醇的生物利用度的估计值(5%)的两倍(不过范围可达 0.1-12%)<sup>([Kuhnz, Blode & Zimmermann, 1993][KBZ93])</sup>。因此,在雌二醇累积水平上,舌下含服途径应相当于口服的 2-5 倍。
|
||||
已有研究报告了对舌下含服雌二醇之生物利用度的估计范围。其中一项针对已绝经妇女的小型随机性研究发现,在同等剂量下,舌下含服雌二醇引起的雌二醇累积水平较口服高出约 2.5 倍<sup>([Price et al., 1997][P97])</sup>。另一些研究则报告,舌下含服雌二醇的生物利用度估计值相对口服可达 5 倍之多<sup>([Pines et al., 1999][P99])</sup>。一项以绒猴进行试验的研究发现,舌下含服雌二醇的绝对生物利用度为 10%;此数字约为传统上对口服雌二醇的生物利用度的估计值(5%)的两倍(不过范围可达 0.1-12%)<sup>([Kuhnz, Blode & Zimmermann, 1993][KBZ93])</sup>。因此,在雌二醇累积水平上,舌下含服途径应相当于口服的 2-5 倍。
|
||||
基于上述发现,可以得出用于女性化激素疗法的舌下含服雌二醇剂量(见下表)。需要指出,因缺乏相关研究,舌下含服雌二醇的相对效力尚未被准确描述。
|
||||
|
||||
> 【表一】在总雌二醇暴露量上大致相当的口服或舌下含服雌二醇(E2)、戊酸雌二醇(EV)之剂量<sup>([Price et al., 1997][P97]; [Pines et al., 1999][P99])</sup>:
|
||||
>
|
||||
> | | 低剂量 | 中等剂量 | 高剂量 | 超高剂量 |
|
||||
> |-|-|-|-|-|
|
||||
> | **口服 E2** | 2 mg/天 | 4 mg/天 | 8 mg/天 | 10 mg/天 |
|
||||
> | **舌下含服 E2**<sup>(1)</sup> | 0.5-1 mg/天 | 1-2 mg/天 | 2-4 mg/天 | 2.5-5 mg/天 |
|
||||
> | **口服 EV** | 3 mg/天 | 6 mg/天 | 10 mg/天 | 12 mg/天 |
|
||||
> | **舌下含服 EV**<sup>(1)</sup> | 0.75-1.5 mg/天 | 1.5-3 mg/天 | 2.5-5 mg/天 | 3-6 mg/天 |
|
||||
>
|
||||
> (1) 按口服剂量的 25-50% 计,以反映在绝对生物利用度上的差异;按 0.5 mg 取整。
|
||||
> (另注) 雌二醇的生物利用度因人而异,和剂量有关的效应也在个体间相差显著。EV 的分子质量更大,在同样剂量下的有效成分也更少。需要指出,EV 的相对生物利用度系从无戊酸基团的 E2 推断而来。
|
||||
<section class="box">
|
||||
|
||||
### 舌下含服雌二醇与女性化效果
|
||||
**表 1**:在总雌二醇暴露量上大致相当的口服或舌下含服雌二醇(E2)、戊酸雌二醇(EV)之剂量<sup>([Price et al., 1997][P97]; [Pines et al., 1999][P99])</sup>:
|
||||
|
||||
```csv
|
||||
,低剂量,中等剂量,高剂量,超高剂量
|
||||
**口服 E2**,2 mg/天,4 mg/天,8 mg/天,10 mg/天
|
||||
**舌下含服 E2**<sup>a</sup>,0.5–1 mg/天,1–2 mg/天,2–4 mg/天,2.5–5 mg/天
|
||||
**口服 EV**,3 mg/天,6 mg/天,10 mg/天,12 mg/天
|
||||
**舌下含服 EV**<sup>a</sup>,0.75–1.5 mg/天,1.5–3 mg/天,2.5–5 mg/天,3–6 mg/天
|
||||
```
|
||||
|
||||
(1) 按口服剂量的 25-50% 计,以反映在绝对生物利用度上的差异;按 0.5 mg 取整。
|
||||
(另注) 雌二醇的生物利用度因人而异,和剂量有关的效应也在个体间相差显著。
|
||||
EV 的分子质量更大,在同样剂量下的有效成分也更少。
|
||||
需要指出,EV 的相对生物利用度系从无戊酸基团的 E2 推断而来。
|
||||
|
||||
</section>
|
||||
|
||||
### 舌下含服雌二醇与女性化效果 {#sublingually-administered-estradiol-and-feminisation}
|
||||
|
||||
由于舌下/面颊含服雌二醇的半衰期很短,一些与在女性化激素疗法使用之有关的问题浮出了水面。在网络论坛上,有一个最常见的问题是:哪种性别肯定激素治疗的处方是最“有利于”雌激素产生女性化效果的——其中包括(而不限于)乳房发育和脂肪分布的效果。
|
||||
|
||||
目前尚无任何数据描述舌下含服雌二醇引起的女性化程度;相比之下,口服及透皮雌二醇已有所描述<sup>([Sam S., 2020a][SS20a])</sup>。不过,如上文所述,在女性倾向跨性别者及性腺发育不良的顺性别女孩的乳房发育及其它女性化效果上,口服与非口服形式的雌二醇并未被发现有任何差别<sup>([Rosenfield et al., 2005][R05]; [Shah et al., 2014][S14]; [Klaver et al., 2018][K18]; [de Blok et al., 2021][B21])</sup>。因此,对于舌下含服的雌二醇,应该也不会在效力上有别于之。
|
||||
目前尚无任何数据描述舌下含服雌二醇引起的女性化程度;相比之下,口服及透皮雌二醇已有所描述<sup>([Sam S., 2020a][SS20a])</sup>。不过,如上文所述,在女性倾向跨性别者及性腺发育不良的顺性别女孩的乳房发育及其它女性化效果上,口服与非口服形式的雌二醇并未被发现有任何差别<sup>([Rosenfield et al., 2005][R05]; [Shah et al., 2014][S14]; [Klaver et al., 2018][K18]; [de Blok et al., 2021][B21])</sup>。因此,对于舌下含服的雌二醇,应该也不会在效力上有别于之。
|
||||
迄今已有多家性别诊所使用舌下含服雌二醇;这一事实令人振奋,其表明舌下含服雌二醇可有效促进女性化<sup>([Deutsch, Bhakri & Kubicek, 2015][DBK15]; [Lim et al., 2019][L19]; [Cirrincione et al., 2021][C21])</sup>。而且,鉴于迄今尚无任何对比并客观评价舌下含服雌二醇之女性化效力的研究,目前根本说不准口服与舌下含服雌二醇在女性化效果上到底有任何差别。但愿将来会有更多研究聚焦于此。
|
||||
|
||||
### 舌下含服雌二醇对睾酮的压制效力
|
||||
### 舌下含服雌二醇对睾酮的压制效力 {#testosterone-suppressing-efficacy-of-sublingually-administered-estradiol}
|
||||
|
||||
因为舌下含服雌二醇的半衰期很短,还催生了另一个问题:在对睾酮及其它雄激素的压制能力上,舌下含服途径和其它传统途径的对比如何。
|
||||
|
||||
最早在 1940 年代,雌激素首次被描述为具有抗促性腺激素作用的抗雄激素制剂;其以口服合成雌激素(即己烯雌酚)的形式,用于治疗男性的前列腺癌<sup>([Huggins & Hodges, 1941][HH41])</sup>。而口服炔雌醇、一些长效雌二醇酯(如聚磷酸雌二醇)以及雌二醇透皮贴片,也曾有相关研究;其抗雄效力已确认无疑<sup>([Stege et al., 1996][S96]; [Kohli, 2006][K06]; [Sciarra et al., 2015][S15])</sup>。由于有关女性倾向跨性别者使用雌激素压制睾酮的数据稀缺,上述数据对女性化激素疗法会很有启发。
|
||||
最早在 1940 年代,雌激素首次被描述为具有抗促性腺激素作用的抗雄激素制剂;其以口服合成雌激素(即己烯雌酚)的形式,用于治疗男性的前列腺癌<sup>([Huggins & Hodges, 1941][HH41])</sup>。而口服炔雌醇、一些长效雌二醇酯(如聚磷酸雌二醇)以及雌二醇透皮贴片,也曾有相关研究;其抗雄效力已确认无疑<sup>([Stege et al., 1996][S96]; [Kohli, 2006][K06]; [Sciarra et al., 2015][S15])</sup>。由于有关女性倾向跨性别者使用雌激素压制睾酮的数据稀缺,上述数据对女性化激素疗法会很有启发。
|
||||
而另一方面,舌下含服雌二醇从未被用于治疗前列腺癌,因此尚无任何数据表明其抗雄效力如何。
|
||||
|
||||
近期一些研究发现,在许多女性倾向跨性别者身上,仅由非舌下含服形式达到生理水平(即 100-200 pg/mL)的雌二醇,足以快速且接近完全地将睾酮水平压制到女性范围<sup>([Leinung, Feustel & Joseph, 2018][LFJ18]; [Pappas et al., 2020][P20])</sup>。另外,有一项正于英国进行的多中心随机对照试验研究,对约 900 名男性使用前列腺癌透皮激素疗法(PATCH);其提供的新数据显示,通过透皮贴片维持雌二醇水平中位数在 215-250 pg/mL 之间,可将睾酮水平压制到阉割范围(<50 ng/dL),降幅约 95%,效力与促性腺激素释放激素(GnRH)类似物相当<sup>([Langley et al., 2021][L21])</sup>。
|
||||
近期一些研究发现,在许多女性倾向跨性别者身上,仅由非舌下含服形式达到生理水平(即 100-200 pg/mL)的雌二醇,足以快速且接近完全地将睾酮水平压制到女性范围<sup>([Leinung, Feustel & Joseph, 2018][LFJ18]; [Pappas et al., 2020][P20])</sup>。另外,有一项正于英国进行的多中心随机对照试验研究,对约 900 名男性使用前列腺癌透皮激素疗法(PATCH);其提供的新数据显示,通过透皮贴片维持雌二醇水平中位数在 215-250 pg/mL 之间,可将睾酮水平压制到阉割范围(<50 ng/dL),降幅约 95%,效力与促性腺激素释放激素(GnRH)类似物相当<sup>([Langley et al., 2021][L21])</sup>。
|
||||
然而,考虑到舌下含服雌二醇在药代动力学上的显著差异,可以认为,在雌二醇累积水平相当的剂量下,舌下含服雌二醇对睾酮的压制作用可能低于其它途径的平均水平。换句话说,在睾酮压制作用上,舌下含服之后波动很大、且作用时间更短的雌二醇水平,可能不及更稳定的雌二醇水平那样有效。
|
||||
|
||||
对此有一些药理学研究可略为佐证。其中一项证据是:一些关于妇女使用舌下含服与静脉注射雌二醇的研究报告,尽管雌二醇水平在数个小时内充分升高,也能较快产生对促性腺激素(即促卵泡激素与促黄体激素)的压制作用,但该作用相对有限<sup>([Tsai & Yen, 1971][TY71]; [Burnier et al., 1981][B81]; [Casper & Yen, 1981][CY81]; [Hoon et al., 1993][H93])</sup>。这些研究质量较差,而且由于未测量睾酮压制作用几何、受试者也仅有顺性别妇女,其证据也不够明了。另一个问题在于,这些研究均仅安排单次用药,其结果不大能代表多次用药的情况。有这样一种可能:重复以生理剂量使用舌下含服雌二醇,便可使促性腺激素压制效果最大化。
|
||||
对此有一些药理学研究可略为佐证。其中一项证据是:一些关于妇女使用舌下含服与静脉注射雌二醇的研究报告,尽管雌二醇水平在数个小时内充分升高,也能较快产生对促性腺激素(即促卵泡激素与促黄体激素)的压制作用,但该作用相对有限<sup>([Tsai & Yen, 1971][TY71]; [Burnier et al., 1981][B81]; [Casper & Yen, 1981][CY81]; [Hoon et al., 1993][H93])</sup>。这些研究质量较差,而且由于未测量睾酮压制作用几何、受试者也仅有顺性别妇女,其证据也不够明了。另一个问题在于,这些研究均仅安排单次用药,其结果不大能代表多次用药的情况。有这样一种可能:重复以生理剂量使用舌下含服雌二醇,便可使促性腺激素压制效果最大化。
|
||||
然而,这些研究可能表明:对于女性倾向跨性别者,如果舌下含服雌二醇的剂量不够大、且不使用其它抗雄制剂,则不足以最大程度地压制性腺功能;而大剂量又会带来更高的健康风险。
|
||||
|
||||
还有一种可能:在与有关前列腺癌的研究所采用的剂量(如 2-4 片 100 μg/24小时的透皮贴片)相当的情况下,舌下含服的单雌二醇疗法可能不及前者有效。因此,对于单雌激素疗法的处方,使用雌二醇透皮贴片、凝胶,或者非肠道途径的雌二醇酯(如戊酸雌二醇注射剂),可能更为可靠。
|
||||
还有一种可能:在与有关前列腺癌的研究所采用的剂量(如 2-4 片 100 μg/24小时的透皮贴片)相当的情况下,舌下含服的单雌二醇疗法可能不及前者有效。因此,对于单雌激素疗法的处方,使用雌二醇透皮贴片、凝胶,或者非肠道途径的雌二醇酯(如戊酸雌二醇注射剂),可能更为可靠。
|
||||
另一方面,已有研究者对女性倾向跨性别者使用舌下含服雌二醇(合并或不合并低剂量醋酸甲羟孕酮,即 MPA——一种合成孕酮制剂)进行了研究<sup>([Jain, Kwan & Forcier, 2019][JKF19])</sup>。研究显示,当女性倾向跨性别者同时使用舌下含服雌二醇与 MPA 时,睾酮水平均至少有相当程度的下降,并降至女性范围(<50 ng/dL);这表明如果合并其它抗雄制剂(如 10 mg/天的醋酸环丙孕酮)使用,舌下含服雌二醇很可能足以有效地压制睾酮<sup>([Aly W., 2019][AW19-CPA])</sup>。
|
||||
|
||||
### 对舌下含服引起的雌二醇水平的监测
|
||||
### 对舌下含服引起的雌二醇水平的监测 {#monitoring-of-estradiol-levels-with-sublingual-administration}
|
||||
|
||||
由于舌下含服雌二醇引起的雌二醇水平的大幅波动,也进一步产生了是否通过验血来监视雌二醇水平的考虑。截至目前,所有《指南》均未对用药后何时进行验血作出建议<sup>([Deutsch, 2016][D16]; [Cheung et al., 2019][C19]; [T’Sjoen et al., 2020][T20])</sup>。这可能和实际需求有一定关系;或者是因为目前尚未有来自任何随机性对照试验的、可供指引女性化激素疗法所用剂量的可靠数据。而且,也由于舌下含服后的雌二醇水平波动很大,有必要知道用药后何时进行采血,以更准确地解读来自实验室的结果。
|
||||
|
||||
例如,如果刚用药便去测定激素水平,则很可能会引起误解,因为此时测得的雌二醇水平会特别高,从而促使用药者为控制雌二醇于合理水平而减小其剂量。事实上,这是由舌下含服雌二醇的药理学特性引起的误解:因为这个采样时间点几乎正值雌二醇水平最高之时。如此雌二醇水平无法代表其平均暴露量——后者才能更准确地衡量总雌激素效力。
|
||||
例如,如果刚用药便去测定激素水平,则很可能会引起误解,因为此时测得的雌二醇水平会特别高,从而促使用药者为控制雌二醇于合理水平而减小其剂量。事实上,这是由舌下含服雌二醇的药理学特性引起的误解:因为这个采样时间点几乎正值雌二醇水平最高之时。如此雌二醇水平无法代表其平均暴露量——后者才能更准确地衡量总雌激素效力。
|
||||
类似地,如果在时间轴的另一端——即即将用药时——进行采血,也可能会引起“雌激素水平过低”的误解,从而过量服用雌激素。此类误解在不熟悉舌下含服雌二醇的药理学特性的人群当中更为常见:因为雌二醇水平仅在用药后最初几个小时内维持高值,此后快速下降。
|
||||
|
||||
有关舌下含服雌二醇的研究也存在这种疏忽的迹象。例如,在上文提到的对性别肯定激素疗法使用舌下含服雌二醇进行的分析结果当中,并未说明其用药频率与用药之后何时进行测定<sup>([Jain, Kwan & Forcier, 2019][JKF19])</sup>。尽管其数据非常宝贵、并且对在这方面持续进行的研究具备参考价值,但是并没有解答用药后何时测定雌二醇水平这个关键问题。当下很难再对该研究所记录的雌二醇水平作任何评述;而且,无法利用其数据来得出口服与舌下含服雌二醇在何种剂量下(效力)相当。
|
||||
|
||||
为了解决因舌下含服后雌二醇水平快速波动而导致的上述问题,或许只需选择在雌二醇水平大概最接近于平均值的时间点进行测定。相关研究发现,对于舌下含服雌二醇,这个时间点一般在服药后四小时左右——不过个体之间差异可能会很大<sup>([Kuhl, 2005][K05])</sup>。而且,通过这种方式,可以获得最能代表总雌激素暴露量的“大致印象”,也能够帮助使用舌下含服雌二醇的人避免对实验室(测定)数据产生误解。
|
||||
|
||||
### 关于每日分多次含服的说明
|
||||
### 关于每日分多次含服的说明 {#administration-of-multiple-sublingual-doses-per-day}
|
||||
|
||||
为补偿舌下含服雌二醇的较短半衰期,可以每日以小剂量分多次服用,以维持稍为更稳定的激素水平<sup>([Ahokas, Kaukoranta & Aito, 1999][AKA99])</sup>。
|
||||
|
||||
在一项研究当中,在高剂量雌激素疗法下,每日舌下含服 3-4 次 2 mg 雌二醇(总剂量 6-8 mg/天)的绝经前妇女的激素水平,相比每日服一次者显著稳定得多<sup>([Serhal & Craft, 1989][SC89])</sup>。另一项研究安排每日服用 3-8 次,也复现了上述结果<sup>([Ahokas et al., 2001][A01])</sup>。
|
||||
与此相反,在有关低剂量面颊含服雌二醇的研究中,有三分之一都使用每日含服 1-2 次 0.25 mg 雌二醇;在 12 小时观察时段内,其发现无论含服 1 次还是 2 次,其雌二醇浓度“稳态”都没有明显差别<sup>([Wren et al., 2003][W03])</sup>。
|
||||
在一项研究当中,在高剂量雌激素疗法下,每日舌下含服 3-4 次 2 mg 雌二醇(总剂量 6-8 mg/天)的绝经前妇女的激素水平,相比每日服一次者显著稳定得多<sup>([Serhal & Craft, 1989][SC89])</sup>。另一项研究安排每日服用 3-8 次,也复现了上述结果<sup>([Ahokas et al., 2001][A01])</sup>。
|
||||
与此相反,在有关低剂量面颊含服雌二醇的研究中,有三分之一都使用每日含服 1-2 次 0.25 mg 雌二醇;在 12 小时观察时段内,其发现无论含服 1 次还是 2 次,其雌二醇浓度“稳态”都没有明显差别<sup>([Wren et al., 2003][W03])</sup>。
|
||||
上述发现表明,舌下/面颊含服雌二醇可能要每日分至少三次服用,以使雌二醇水平更为稳定。
|
||||
|
||||
基于上述理由,如果女性倾向跨性别者要使用舌下含服雌二醇,一日内分多次服用的方式会更适合;或许最好每日至少分 3-4 次。例如,比起一次性服用 2 mg,如在 24 小时内分四次服用 0.5 mg,应该会更佳(在可行范围内尽量让间隔均等)。虽然每日分多次含服可能会带来一定不便,但至少雌二醇水平会因此更加均衡、睾酮压制作用也可能更好。
|
||||
基于上述理由,如果女性倾向跨性别者要使用舌下含服雌二醇,一日内分多次服用的方式会更适合;或许最好每日至少分 3-4 次。例如,比起一次性服用 2 mg,如在 24 小时内分四次服用 0.5 mg,应该会更佳(在可行范围内尽量让间隔均等)。虽然每日分多次含服可能会带来一定不便,但至少雌二醇水平会因此更加均衡、睾酮压制作用也可能更好。
|
||||
每日分多次服用的方式应视为舌下含服雌二醇的最佳用法。
|
||||
|
||||
|
||||
## 安全性与耐受性
|
||||
## 安全性与耐受性 {#safety-and-tolerability}
|
||||
|
||||
遗憾的是,在与舌下/面颊含服雌二醇的药代动力学有关的安全性与耐受性方面,现有的医学文献尚显不足。不同于口服及透皮雌二醇(已在围绝经期妇女身上进行严谨研究),当下尚无任何有关舌下含服雌二醇的长期安全性数据<sup>([Rovinski et al., 2018][R18]; [乳腺癌激素相关因素合作研究小组, CGHFBC, 2019][CGHFBC19])</sup>。
|
||||
|
||||
### 雌激素的不良健康影响
|
||||
### 雌激素的不良健康影响 {#adverse-health-effects-of-estrogens}
|
||||
|
||||
由于对肝脏的一系列影响,雌激素在暴露量足够的条件下,会引起血栓风险的上升<sup>([Kuhl, 2005][K05]; [Aly W., 2020b][AW20-CLOT])</sup>。此外,雌激素在特定条件下还会引起其它心血管并发症<sup>([Anderson et al., 2004][A04]; [Mikkola et al., 2005][M05])</sup>。这些是跟性别肯定激素疗法相关的最大的健康顾虑——尽管其绝对风险在短期内很低。
|
||||
|
||||
仅有少量研究评估了舌下含服雌二醇对肝脏的影响<sup>([Pines et al., 1999][P99]; [Lim et al., 2019][L19])</sup>。数据发现其在脂质与胆固醇上的作用与其它形式的雌激素相似。有一项证据表明舌下含服雌二醇对肝脏的作用要强于透皮雌二醇等其它形式;那就是其引起的雌酮与硫酸雌酮含量显著更高——也即,其在肝脏内引起的雌激素暴露量更大<sup>([Burnier et al., 1981][B81]; [Cirrincione et al., 2021][C21])</sup>。非口服形式的雌二醇在高剂量下可引起高凝状态,从而在肝脏引起强烈的雌激素活动。
|
||||
|
||||
有相当一部分的研究对雌激素的短期与长期健康影响有所关注,不过无一研讨过舌下/面颊含服的情况<sup>([Oliver-Williams et al., 2019][OW19]; [Mishra et al., 2021][M21])</sup>。由于口服雌二醇的风险比非口服形式更高、且舌下含服只是部分(而非完全)避免了肝脏首过效应的代谢作用,可以认为,舌下含服雌二醇的风险应不高于口服、但也不低于其它非口服途径。
|
||||
一项在美国进行的回顾性群体研究发现,修正干扰因子后,在血栓栓塞发生率上,正服用平均 4 mg/天的口服雌二醇的女性倾向跨性别者约为对照组(未服用激素的顺性别妇女)的两倍;相对对照组的风险比率为 2.0(95% 可信区间:1.4-2.8)<sup>([Getahun et al., 2018][G18])</sup>。此类风险之增幅已经远比早年女性倾向跨性别者所用处方(含高剂量合成雌激素)的要小;但同时需要注意,即便是此等增幅也会大幅增加发病率和死亡率<sup>([Morimont, Dogné & Douxfils, 2020][MDD20])</sup>。
|
||||
有相当一部分的研究对雌激素的短期与长期健康影响有所关注,不过无一研讨过舌下/面颊含服的情况<sup>([Oliver-Williams et al., 2019][OW19]; [Mishra et al., 2021][M21])</sup>。由于口服雌二醇的风险比非口服形式更高、且舌下含服只是部分(而非完全)避免了肝脏首过效应的代谢作用,可以认为,舌下含服雌二醇的风险应不高于口服、但也不低于其它非口服途径。
|
||||
一项在美国进行的回顾性群体研究发现,修正干扰因子后,在血栓栓塞发生率上,正服用平均 4 mg/天的口服雌二醇的女性倾向跨性别者约为对照组(未服用激素的顺性别妇女)的两倍;相对对照组的风险比率为 2.0(95% 可信区间:1.4-2.8)<sup>([Getahun et al., 2018][G18])</sup>。此类风险之增幅已经远比早年女性倾向跨性别者所用处方(含高剂量合成雌激素)的要小;但同时需要注意,即便是此等增幅也会大幅增加发病率和死亡率<sup>([Morimont, Dogné & Douxfils, 2020][MDD20])</sup>。
|
||||
在此建议限制舌下/面颊含服雌二醇的剂量(如小于 6 mg/天),这样它们不至于产生过多有害作用,并可令性别肯定激素治疗的益处与风险处于平衡。
|
||||
|
||||
### 用药者的不配合行为
|
||||
### 用药者的不配合行为 {#non-compliance}
|
||||
|
||||
对于女性倾向跨性别者,舌下含服有一项很现实的阻碍:即每日需含服三次、四次乃至更多,会带来相当程度的不便。一些观察性研究发现,一般而言,为患者开出的药量与每日剂量,和患者的不配合行为及漏服次数呈正关联<sup>([Jin et al., 2008][J08]; [Toh et al., 2014][T14])</sup>。这些发现尤其跟女性倾向跨性别者有关,因为一般情况下,我们需要在数十年间一直服用激素。如果一段时间里仅漏服一次,倒无伤大雅;但连续多次漏服的话,问题就大了。
|
||||
|
||||
与舌下含服相反的是,口服雌二醇及其透皮凝胶的半衰期长至足以仅需每日用药一次<sup>([Wiegratz et al., 2001][W01]; [Potts & Lobo, 2005][PL05])</sup>。至于透皮贴片和非肠道给药(如注射剂——译者注)形式的雌二醇,其补充间隔可长达数日、以至更长<sup>([Thurman et al., 2013][T13]; [Wisner et al., 2015][W15])</sup>。因此,如果女性倾向跨性别者准备使用舌下含服而非其它途径,也应当格外留意,每日都要多次含服是否符合实际、足够方便;如否,则其它剂型应更适合使用。如要长期用药,那就更应该考虑这点了。
|
||||
|
||||
|
||||
## 总结
|
||||
## 总结 {#summary-and-conclusions}
|
||||
|
||||
相比于其它雌激素形式,当下对于舌下/面颊含服雌二醇的研究还很少。历史上,诸如口服、透皮雌激素等形式,常用于缓解围绝经期症状及其它用途;因此,在女性化激素疗法当中,这些形式得到了远甚于舌下含服形式的关注度与特性描述。不过,近期数项研究填补了我们对舌下含服雌二醇的认知空白。如果有跨性别健康临床实践指南未曾讨论舌下含服雌二醇之使用的话,其应当考虑在相关信息愈发完善之后修订其内容。
|
||||
|
||||
|
|
@ -145,18 +154,74 @@
|
|||
|
||||
> \* 译者注:原文为“(比口服)低 2-4 倍的剂量”。
|
||||
|
||||
目前尚无任何证据显示或表明,在女性化效果上,舌下含服雌二醇是比其它途径更好还是更差;不过可以确信的是,在同等雌二醇总暴露量下,舌下含服雌二醇对睾酮的压制作用可能稍弱。尽管如此,当合并服用其它抗雄制剂时,舌下含服雌二醇还是能够有效压制睾酮。
|
||||
目前尚无任何证据显示或表明,在女性化效果上,舌下含服雌二醇是比其它途径更好还是更差;不过可以确信的是,在同等雌二醇总暴露量下,舌下含服雌二醇对睾酮的压制作用可能稍弱。尽管如此,当合并服用其它抗雄制剂时,舌下含服雌二醇还是能够有效压制睾酮。
|
||||
使用舌下含服雌二醇时,如要监测雌二醇水平,需要留意(检测时机)以确保其结果可被准确解读。为尽量让上述潜在问题变得最小,可以每日分多次含服。
|
||||
|
||||
迄今尚无任何大型观察性或随机性研究对舌下含服雌二醇带来的健康风险进行测定。因此,其引起心血管问题的风险尚未可知——尽管其一部分引起的肝脏首过效应在这方面而言是安全的。
|
||||
迄今尚无任何大型观察性或随机性研究对舌下含服雌二醇带来的健康风险进行测定。因此,其引起心血管问题的风险尚未可知——尽管其一部分引起的肝脏首过效应在这方面而言是安全的。
|
||||
舌下含服雌二醇的使用(尤其是长期使用)可能不大方便,这时可以考虑换用其它剂型。
|
||||
|
||||
总而言之,舌下含服雌二醇应具有许多优良特性,可代替口服雌二醇用于女性化激素治疗——尽管其显然尚需更多研究来得到更准确的描述。
|
||||
|
||||
## 参考文献 {#references}
|
||||
|
||||
## 参考文献
|
||||
|
||||
略
|
||||
- Ahokas, A., Kaukoranta, J., & Aito, M. (1999). Effect of oestradiol on postpartum depression. _Psychopharmacology_, _146_(1), 108–110. \[DOI:<https://doi.org/10.1007/s002130051095>\]
|
||||
- Ahokas, A., Kaukoranta, J., Wahlbeck, K., & Aito, M. (2001). Estrogen deficiency in severe postpartum depression: successful treatment with sublingual physiologic 17β-estradiol: a preliminary study. _Journal of Clinical Psychiatry_, _62_(5), 332–336. \[DOI:<https://doi.org/10.4088/jcp.v62n0504>\] \[[PDF](https://files.transfemscience.org/pdfs/Ahokas%20(2001)%20-%20Estrogen%20Deficiency%20in%20Severe%20Postpartum%20Depression_%20Successful%20Treatment%20With%20Sublingual%20Physiologic%2017%CE%B2-Estradiol_%20A%20Preliminary%20Study.pdf)\]
|
||||
- Anderson, G. L., Limacher, M., Assaf, A. R., Bassford, T., Beresford, S. A., Black, H., Bonds, D., Brunner, R., Brzyski, R., Caan, B., Chlebowski, R., Curb, D., Gass, M., Hays, J., Heiss, G., Hendrix, S., Howard, B. V., Hsia, J., Hubbell, A., Jackson, R., … & Women’s Health Initiative Steering Committee (2004). Effects of conjugated equine estrogen in postmenopausal women with hysterectomy: the Women’s Health Initiative randomized controlled trial. _JAMA_, _291_(14), 1701–1712. \[DOI:<https://doi.org/10.1001/jama.291.14.1701>\]
|
||||
- Bartlett, J. A., & van der Voort Maarschalk, K. (2012). Understanding the oral mucosal absorption and resulting clinical pharmacokinetics of asenapine. _AAPS Pharmscitech_, _13_(4), 1110–1115. \[DOI:<https://doi.org/10.1208/s12249-012-9839-7>\]
|
||||
- Burnier, A. M., Martin, P. L., Yen, S. S., & Brooks, P. (1981). Sublingual absorption of micronized 17β-estradiol. _American Journal of Obstetrics and Gynecology_, _140_(2), 146–150. \[DOI:<https://doi.org/10.1016/0002-9378(81)90101-0>\]
|
||||
- Casper, R. F., & Yen, S. S. (1981). Rapid absorption of micronized estradiol-17β following sublingual administration. _Obstetrics and Gynecology_, _57_(1), 62–64. \[[PubMed](https://pubmed.ncbi.nlm.nih.gov/7454177/])\] \[[URL](https://journals.lww.com/greenjournal/Abstract/1981/01000/Rapid_Absorption_of_Micronized_Estradiol_17_.14.aspx)\]
|
||||
- Chandrasekhara, D. S., Ali, V., Prost, H. M., & Nader-Estekhari, S. (2002). Buccal estrogen in toothpaste study: systemic absorption of estradiol in postmenopausal or surgically menopausal women when administered as a component in toothpaste. _Fertility and Sterility_, _78_(Suppl 1), S98–S98 (O-258). \[DOI:<https://doi.org/10.1016/S0015-0282(02)03639-7>\]
|
||||
- Cheung, A. S., Wynne, K., Erasmus, J., Murray, S., & Zajac, J. D. (2019). Position statement on the hormonal management of adult transgender and gender diverse individuals. _Medical Journal of Australia_, _211_(3), 127–133. \[DOI:<https://doi.org/10.5694/mja2.50259>\]
|
||||
- Cirrincione, L. R., Winston McPherson, G., Rongitsch, J., Sadilkova, K., Drees, J. C., Krasowski, M. D., Dickerson, J. A., & Greene, D. N. (2021). Sublingual Estradiol Is Associated with Higher Estrone Concentrations than Transdermal or Injectable Preparations in Transgender Women and Gender Nonbinary Adults. _LGBT Health_, _8_(2), 125–132. \[DOI:<https://doi.org/10.1089/lgbt.2020.0249>\]
|
||||
- Collaborative Group on Hormonal Factors in Breast Cancer. (2019). Type and timing of menopausal hormone therapy and breast cancer risk: individual participant meta-analysis of the worldwide epidemiological evidence. _The Lancet_, _394_(10204), 1159–1168. \[DOI:<https://doi.org/10.1016/S0140-6736(19)31709-X>\]
|
||||
- de Blok, C., Dijkman, B., Wiepjes, C. M., Staphorsius, A. S., Timmermans, F. W., Smit, J. M., Dreijerink, K., & den Heijer, M. (2021). Sustained Breast Development and Breast Anthropometric Changes in 3 Years of Gender-Affirming Hormone Treatment. _The Journal of Clinical Endocrinology & Metabolism_, _106_(2), e782–e790. \[DOI:<https://doi.org/10.1210/clinem/dgaa841>\]
|
||||
- Deutsch, M. B., Bhakri, V., & Kubicek, K. (2015). Effects of cross-sex hormone treatment on transgender women and men. _Obstetrics and Gynecology_, _125_(3), 605–610. \[DOI:<https://doi.org/10.1097/AOG.0000000000000692>\]
|
||||
- Deutsch, M. B. (Ed.). (2016). _Guidelines for the Primary and Gender-Affirming Care of Transgender and Gender Nonbinary People, 2nd Edition._ San Francisco: University of California, San Francisco/UCSF Transgender Care. \[[URL](https://transcare.ucsf.edu/guidelines)\] \[[PDF](https://transcare.ucsf.edu/sites/transcare.ucsf.edu/files/Transgender-PGACG-6-17-16.pdf)\]
|
||||
- Devissaguet, J. P., Brion, N., Lhote, O., & Deloffre, P. (1999). Pulsed estrogen therapy: pharmacokinetics of intranasal 17-beta-estradiol (S21400) in postmenopausal women and comparison with oral and transdermal formulations. _European Journal of Drug Metabolism and Pharmacokinetics_, _24_(3), 265–271. \[DOI:<https://doi.org/10.1007/BF03190030>\]
|
||||
- Doll, E. E., Gunsolus, I., Lamberton, N., Tangpricha, V., & Sarvaideo, J. L. (2020). Pharmacokinetics of Sublingual Versus Oral Estradiol in Transgender Women. _Journal of the Endocrine Society_, _4_(Suppl 1), A1128–A1128 (SUN-LB9). \[DOI:<https://doi.org/10.1210/jendso/bvaa046.2237>\]
|
||||
- Fiet, J., Hermano, M., Witte, J., Villette, J. M., Haimart, M., Gourmel, B., Tabuteau, F., Rouffy, J., & Dreux, C. (1982). Post-menopausal concentrations of plasma oestradiol, oestrone, FSH and LH and of total urinary oestradiol and oestrone after a single sublingual dose of oestradiol-17β. _Acta Endocrinologica_, _101_(1), 93–97. \[DOI:<https://doi.org/10.1530/acta.0.1010093>\]
|
||||
- Gass, M. S., Rebar, R. W., Cuffie-Jackson, C., Cedars, M. I., Lobo, R. A., Shoupe, D., Judd, H. L., Buyalos, R. P., & Clisham, P. R. (2004). A short study in the treatment of hot flashes with buccal administration of 17-β estradiol. _Maturitas_, _49_(2), 140–147. \[DOI:<https://doi.org/10.1016/j.maturitas.2003.12.004>\]
|
||||
- Getahun, D., Nash, R., Flanders, W. D., Baird, T. C., Becerra-Culqui, T. A., Cromwell, L., Hunkeler, E., Lash, T. L., Millman, A., Quinn, V. P., Robinson, B., Roblin, D., Silverberg, M. J., Safer, J., Slovis, J., Tangpricha, V., & Goodman, M. (2018). Cross-sex hormones and acute cardiovascular events in transgender persons: a cohort study. _Annals of Internal Medicine_, _169_(4), 205–213. \[DOI:<https://doi.org/10.7326/M17-2785>\]
|
||||
- Haupt, C., Henke, M., Kutschmar, A., Hauser, B., Baldinger, S., Saenz, S. R., & Schreiber, G. (2020). Antiandrogen or estradiol treatment or both during hormone therapy in transitioning transgender women. _Cochrane Database of Systematic Reviews_, _11_(11), CD013138. \[DOI:<https://doi.org/10.1002/14651858.CD013138.pub2>\]
|
||||
- Hoon, T. J., Dawood, M. Y., Khan‐Dawood, F. S., Ramos, J., & Batenhorst, R. L. (1993). Bioequivalence of a 17β‐Estradiol Hydroxypropyl‐β‐Cyclodextrin Complex in Postmenopausal Women. _The Journal of Clinical Pharmacology_, _33_(11), 1116–1121. \[DOI:<https://doi.org/10.1002/j.1552-4604.1993.tb01949.x>\]
|
||||
- Huggins, C., & Hodges, C. V. (1941). Studies on prostatic cancer. I. The effect of castration, of estrogen and of androgen injection on serum phosphatases in metastatic carcinoma of the prostate. _Cancer Research_, _1_(4), 293–297. \[DOI:<https://doi.org/10.3322/canjclin.22.4.232>\]
|
||||
- Jain, J., Kwan, D., & Forcier, M. (2019). Medroxyprogesterone acetate in Gender-Affirming therapy for Transwomen: results from a retrospective study. _The Journal of Clinical Endocrinology & Metabolism_, _104_(11), 5148–5156. \[DOI:<https://doi.org/10.1210/jc.2018-02253>\]
|
||||
- Jin, J., Sklar, G. E., Oh, V. M. S., & Li, S. C. (2008). Factors affecting therapeutic compliance: A review from the patient’s perspective. _Therapeutics and Clinical Risk Management_, _4_(1), 269–286. \[DOI:<https://doi.org/10.2147/TCRM.S1458>\]
|
||||
- Klaver, M., de Blok, C. J. M., Wiepjes, C. M., Nota, N. M., Dekker, M. J., de Mutsert, R., Schreiner, T., Fisher, A. D., T’Sjoen, G., & den Heijer, M. (2018). Changes in regional body fat, lean body mass and body shape in trans persons using cross-sex hormonal therapy: results from a multicenter prospective study. _European Journal of Endocrinology_, _178_(2), 163–171. \[DOI:<https://doi.org/10.1530/EJE-17-0496>\]
|
||||
- Kohli, M. (2006). Phase II study of transdermal estradiol in androgen‐independent prostate carcinoma. _Cancer_, _106_(1), 234–235. \[DOI:<https://doi.org/10.1002/cncr.21528>\]
|
||||
- Kuhl, H. (2005). Pharmacology of estrogens and progestogens: influence of different routes of administration. _Climacteric_, _8_(Suppl 1), 3–63. \[DOI:<https://doi.org/10.1080/13697130500148875>\] \[[PDF](https://hormonebalance.org/images/documents/Kuhl%2005%20%20Pharm%20Estro%20Progest%20Climacteric_1311166827.pdf)\]
|
||||
- Kuhnz, W., Blode, H., & Zimmermann, H. (1993). Pharmacokinetics of exogenous natural and synthetic estrogens and antiestrogens. In Oettel, M., & Schillinger, E. (Eds.). _Estrogens and Antiestrogens II: Pharmacology and Clinical Application of Estrogens and Antiestrogen_ (_Handbook of Experimental Pharmacology, Volume 135/II_) (pp. 261–322). Berlin/Heidelberg: Springer. \[DOI:<https://doi.org/10.1007/978-3-642-60107-1_15>\]
|
||||
- Kuhnz, W., Gansau, C., & Mahler, M. (1993). Pharmacokinetics of estradiol, free and total estrone, in young women following single intravenous and oral administration of 17β-estradiol. _Arzneimittelforschung_, _43_(9), 966–973. \[[Google Scholar](https://scholar.google.com/scholar?cluster=3536999842749234957)\] \[[PubMed](https://pubmed.ncbi.nlm.nih.gov/8240460/])\] \[[PDF](https://files.transfemscience.org/pdfs/Kuhnz,%20Gansau,%20&%20Mahler%20(1993)%20-%20Pharmacokinetics%20of%20Estradiol,%20Free%20and%20Total%20Estrone,%20in%20Young%20Women%20Following%20Single%20Intravenous%20and%20Oral%20Administration%20of%2017%CE%B2-Estradiol.pdf)\]
|
||||
- Langley, R. E., Gilbert, D. C., Duong, T., Clarke, N. W., Nankivell, M., Rosen, S. D., Mangar, S., Macnair, A., Sundaram, S. K., Laniado, M. E., Dixit, S., Madaan, S., Manetta, C., Pope, A., Scrase, C. D., Mckay, S., Muazzam, I. A., Collins, G. N., Worlding, J., Williams, S. T., … & Parmar, M. (2021). Transdermal oestradiol for androgen suppression in prostate cancer: long-term cardiovascular outcomes from the randomised Prostate Adenocarcinoma Transcutaneous Hormone (PATCH) trial programme. _The Lancet_, _397_(10274), 581–591. \[DOI:<https://doi.org/10.1016/S0140-6736(21)00100-8>\]
|
||||
- Leinung, M. C., Feustel, P. J., & Joseph, J. (2018). Hormonal treatment of transgender women with oral estradiol. _Transgender Health_, _3_(1), 74–81. \[DOI:<https://doi.org/10.1089/trgh.2017.0035>\]
|
||||
- Lim, H. H., Jang, Y. H., Choi, G. Y., Lee, J. J., & Lee, E. S. (2019). Gender affirmative care of transgender people: a single center’s experience in Korea. _Obstetrics & Gynecology Science_, _62_(1), 46–55. \[DOI:<https://doi.org/10.5468/ogs.2019.62.1.46>\]
|
||||
- Lobo, R. A. (1987). Absorption and metabolic effects of different types of estrogens and progestogens. _Obstetrics and Gynecology Clinics of North America_, _14_(1), 143–167. \[[PubMed](https://pubmed.ncbi.nlm.nih.gov/3306517/])\] \[DOI:<https://doi.org/10.1016/S0889-8545(21)00577-5>\] \[[URL](https://www.obgyn.theclinics.com/article/S0889-8545(21)00577-5/fulltext)\] \[[PDF](https://files.transfemscience.org/pdfs/Lobo%20(1987)%20-%20Absorption%20and%20metabolic%20effects%20of%20different%20types%20of%20estrogens%20and%20progestogens.pdf)\]
|
||||
- Mikkola, A., Aro, J., Rannikko, S., Oksanen, H., Ruutu, M., & Finnprostate Group. (2005). Cardiovascular complications in patients with advanced prostatic cancer treated by means of orchiectomy or polyestradiol phosphate. _Scandinavian Journal of Urology and Nephrology_, _39_(4), 294–300. \[DOI:<https://doi.org/10.1080/00365590510031228>\]
|
||||
- Mishra, S. R., Chung, H. F., Waller, M., & Mishra, G. D. (2021). Duration of estrogen exposure during reproductive years, age at menarche and age at Menopause, and risk of cardiovascular disease events, all‐cause and cardiovascular mortality: a systematic review and meta‐analysis. _BJOG: An International Journal of Obstetrics & Gynaecology_, _128_(5), 809–821. \[DOI:<https://doi.org/10.1111/1471-0528.16524>\]
|
||||
- Morimont, L., Dogné, J. M., & Douxfils, J. (2020). Letter to the Editors-in-Chief in response to the article of Abou-Ismail, et al. entitled _“Estrogen and thrombosis: A bench to bedside review”_ (Thrombosis Research 192 (2020) 40–51). _Thrombosis Research_, _193_, 221–223. \[DOI:<https://doi.org/10.1016/j.thromres.2020.08.006>\]
|
||||
- Oliver-Williams, C., Glisic, M., Shahzad, S., Brown, E., Pellegrino Baena, C., Chadni, M., Chowdhury, R., Franco, O. H., & Muka, T. (2019). The route of administration, timing, duration and dose of postmenopausal hormone therapy and cardiovascular outcomes in women: a systematic review. _Human Reproduction Update_, _25_(2), 257–271. \[DOI:<https://doi.org/10.1093/humupd/dmy039>\]
|
||||
- Pappas, I. I., Craig, W. Y., Spratt, L. V., & Spratt, D. I. (2021). Efficacy of Sex Steroid Therapy Without Progestin or GnRH Agonist for Gonadal Suppression in Adult Transgender Patients. _The Journal of Clinical Endocrinology & Metabolism_, _106_(3), e1290–e1300. \[DOI:<https://doi.org/10.1210/clinem/dgaa884>\]
|
||||
- Perloff, W. H. (1950). Estradiol buccal tablets in the treatment of the menopause. _American Journal of Obstetrics and Gynecology_, _59_(1), 223–225. \[DOI:<https://doi.org/10.1016/0002-9378(50)90390-5>\]
|
||||
- Pickar, J. H., Bon, C., Amadio, J. M., Mirkin, S., & Bernick, B. (2015). Pharmacokinetics of the first combination 17β-estradiol/progesterone capsule in clinical development for menopausal hormone therapy. _Menopause_, _22_(12), 1308–1316. \[DOI:<https://doi.org/10.1097/GME.0000000000000467>\]
|
||||
- Pines, A., Averbuch, M., Fisman, E. Z., & Rosano, G. M. (1999). The acute effects of sublingual 17β-estradiol on the cardiovascular system. _Maturitas_, _33_(1), 81–85. \[DOI:<https://doi.org/10.1016/S0378-5122(99)00036-5>\]
|
||||
- Potts, R. O., & Lobo, R. A. (2005). Transdermal drug delivery: clinical considerations for the obstetrician–gynecologist. _Obstetrics & Gynecology_, _105_(5), 953–961. \[DOI:<https://doi.org/10.1097/01.AOG.0000161958.70059.db>\]
|
||||
- Price, T. M., Blauer, K. L., Hansen, M., Stanczyk, F., Lobo, R., & Bates, G. W. (1997). Single-dose pharmacokinetics of sublingual versus oral administration of micronized 17β-estradiol. _Obstetrics & Gynecology_, _89_(3), 340–345. \[DOI:<https://doi.org/10.1016/S0029-7844(96)00513-3>\]
|
||||
- Rosenfield, R. L., Devine, N., Hunold, J. J., Mauras, N., Moshang Jr, T., & Root, A. W. (2005). Salutary effects of combining early very low-dose systemic estradiol with growth hormone therapy in girls with Turner syndrome. _The Journal of Clinical Endocrinology & Metabolism_, _90_(12), 6424–6430. \[DOI:<https://doi.org/10.1210/jc.2005-1081>\]
|
||||
- Rovinski, D., Ramos, R. B., Fighera, T. M., Casanova, G. K., & Spritzer, P. M. (2018). Risk of venous thromboembolism events in postmenopausal women using oral versus non-oral hormone therapy: a systematic review and meta-analysis. _Thrombosis Research_, _168_, 83–95. \[DOI:<https://doi.org/10.1016/j.thromres.2018.06.014>\]
|
||||
- Sciarra, A., Gentile, V., Cattarino, S., Gentilucci, A., Alfarone, A., D’Eramo, G., & Salciccia, S. (2015). Oral ethinylestradiol in castration‐resistant prostate cancer: a 10‐year experience. _International Journal of Urology_, _22_(1), 98–103. \[DOI:<https://doi.org/10.1111/iju.12613>\]
|
||||
- Serhal, P., & Craft, I. (1989). Oocyte donation in 61 patients. _The Lancet_, _333_(8648), 1185–1187. \[DOI:<https://doi.org/10.1016/S0140-6736(89)92762-1>\]
|
||||
- Serhal, P. (1990). Oocyte donation and surrogacy. _British Medical Bulletin_, _46_(3), 796–812. \[DOI:<https://doi.org/10.1093/oxfordjournals.bmb.a072432>\]
|
||||
- Shah, S., Forghani, N., Durham, E., & Neely, E. K. (2014). A randomized trial of transdermal and oral estrogen therapy in adolescent girls with hypogonadism. _International Journal of Pediatric Endocrinology_, _2014_(1), 12. \[DOI:<https://doi.org/10.1186/1687-9856-2014-12>\]
|
||||
- Stanczyk, F. Z., Archer, D. F., & Bhavnani, B. R. (2013). Ethinyl estradiol and 17β-estradiol in combined oral contraceptives: pharmacokinetics, pharmacodynamics and risk assessment. _Contraception_, _87_(6), 706–727. \[DOI:<https://doi.org/10.1016/j.contraception.2012.12.011>\]
|
||||
- Stege, R., Gunnarsson, P. O., Johansson, C. J., Olsson, P., Pousette, Å., & Carlström, K. (1996). Pharmacokinetics and testosterone suppression of a single dose of polyestradiol phosphate (Estradurin®) in prostatic cancer patients. _The Prostate_, _28_(5), 307–310. \[DOI:[10.1002/(SICI)1097-0045(199605)28:5<307::AID-PROS6>3.0.CO;2-8](https://doi.org/10.1002/(SICI)1097-0045(199605)28:5%3C307::AID-PROS6%3E3.0.CO;2-8)\]
|
||||
- T’Sjoen, G., Arcelus, J., De Vries, A. L., Fisher, A. D., Nieder, T. O., Özer, M., & Motmans, J. (2020). European Society for Sexual Medicine position statement “assessment and hormonal management in adolescent and adult trans people, with attention for sexual function and satisfaction”. _The Journal of Sexual Medicine_, _17_(4), 570–584. \[DOI:<https://doi.org/10.1016/j.jsxm.2020.01.012>\]
|
||||
- Thurman, A., Kimble, T., Hall, P., Schwartz, J. L., & Archer, D. F. (2013). Medroxyprogesterone acetate and estradiol cypionate injectable suspension (Cyclofem) monthly contraceptive injection: steady-state pharmacokinetics. _Contraception_, _87_(6), 738–743. \[DOI:<https://doi.org/10.1016/j.contraception.2012.11.010>\]
|
||||
- Toh, M. R., Teo, V., Kwan, Y. H., Raaj, S., Tan, S. Y. D., & Tan, J. Z. Y. (2014). Association between number of doses per day, number of medications and patient’s non-compliance, and frequency of readmissions in a multi-ethnic Asian population. _Preventive Medicine Reports_, _1_, 43–47. \[DOI:<https://doi.org/10.1016/j.pmedr.2014.10.001>\]
|
||||
- Tsai, C. C., & Yen, S. S. C. (1971). Acute effects of intravenous infusion of 17β-estradiol on gonadotropin release in pre-and post-menopausal women. _The Journal of Clinical Endocrinology & Metabolism_, _32_(6), 766–771. \[DOI:<https://doi.org/10.1210/jcem-32-6-766>\]
|
||||
- Verdonk, S. J., Vesper, H. W., Martens, F., Sluss, P. M., Hillebrand, J. J., & Heijboer, A. C. (2019). Estradiol reference intervals in women during the menstrual cycle, postmenopausal women and men using an LC-MS/MS method. _Clinica Chimica Acta_, _495_, 198–204. \[DOI:<https://doi.org/10.1016/j.cca.2019.04.062>\]
|
||||
- Wiegratz, I., Fink, T., Rohr, U. D., Lang, E., Leukel, P., & Kuhl, H. (2001). Überkreuz-Vergleich der Pharmakokinetik von Estradiol unter der Hormonsubstitution mit Estradiolvalerat oder mikronisiertem Estradiol. \[Cross-over comparison of the pharmacokinetics of estradiol during hormone replacement therapy with estradiol valerate or micronized estradiol.\] _Zentralblatt für Gynäkologie_, _123_(9), 505–512. \[[PubMed](https://pubmed.ncbi.nlm.nih.gov/11709743/)\] \[DOI:<https://doi.org/10.1055/s-2001-18223>\]
|
||||
- Wisner, K. L., Sit, D. K., Moses-Kolko, E. L., Driscoll, K. E., Prairie, B. A., Stika, C. S., Eng, H. F., Dills, J. L., Luther, J. F., & Wisniewski, S. R. (2015). Transdermal estradiol treatment for postpartum depression: a pilot randomized trial. _Journal of Clinical Psychopharmacology_, _35_(4), 389–395. \[DOI:<https://doi.org/10.1097/JCP.0000000000000351>\]
|
||||
- Wren, B. G., Day, R. O., McLachlan, A. J., & Williams, K. M. (2003). Pharmacokinetics of estradiol, progesterone, testosterone and dehydroepiandrosterone after transbuccal administration to postmenopausal women. _Climacteric_, _6_(2), 104–111. \[DOI:<https://doi.org/10.1080/cmt.6.2.104.111>\]
|
||||
|
||||
[K05]: https://www.tandfonline.com/doi/abs/10.1080/13697130500148875
|
||||
[SAB13]: https://www.contraceptionjournal.org/article/S0010-7824(12)01079-7/fulltext
|
||||
|
|
@ -202,7 +267,7 @@
|
|||
[TY71]: https://academic.oup.com/jcem/article-abstract/32/6/766/2716339
|
||||
[H93]: https://accp1.onlinelibrary.wiley.com/doi/abs/10.1002/j.1552-4604.1993.tb01949.x
|
||||
[JKF19]: https://academic.oup.com/jcem/article/104/11/5148/5479358
|
||||
[AW19-CPA]: cpa-dosage.md
|
||||
[AW19-CPA]: https://transfemscience.org/articles/cpa-dosage/
|
||||
|
||||
[D16]: https://transcare.ucsf.edu/guidelines
|
||||
[C19]: https://onlinelibrary.wiley.com/doi/abs/10.5694/mja2.50259
|
||||
|
|
@ -225,4 +290,4 @@
|
|||
[T14]: https://www.sciencedirect.com/science/article/pii/S2211335514000102
|
||||
[PL05]: https://journals.lww.com/greenjournal/Abstract/2005/05000/Transdermal_Drug_Delivery__Clinical_Considerations.7.aspx
|
||||
[T13]: https://linkinghub.elsevier.com/retrieve/pii/S0010782412009808
|
||||
[W15]: https://journals.lww.com/psychopharmacology/Abstract/2015/08000/Transdermal_Estradiol_Treatment_for_Postpartum.7.aspx
|
||||
[W15]: https://journals.lww.com/psychopharmacology/Abstract/2015/08000/Transdermal_Estradiol_Treatment_for_Postpartum.7.aspx
|
||||
|
|
@ -1,34 +1,45 @@
|
|||
# 关于女性倾向跨性别者舌下含服戊酸雌二醇片剂的简介
|
||||
---
|
||||
title: 关于女性倾向跨性别者舌下含服戊酸雌二醇片剂的简介
|
||||
linkTitle: 舌下含服戊酸雌二醇的可行性
|
||||
description: 戊酸雌二醇的舌下含服途径尽管鲜有研究,但其与含服雌二醇同样有效,也可作为口服途径的替代。
|
||||
author: Aly W.
|
||||
published: 2019-01-05
|
||||
updated: 2021-09-07
|
||||
translated: 2022-02-18
|
||||
translators:
|
||||
- Bersella AI
|
||||
tags:
|
||||
- 雌激素
|
||||
- 用药途径与剂量
|
||||
trackHash: 707eba7009f219b84a9dcb94eb5c05b8d7400b23
|
||||
---
|
||||
|
||||
作者 [Aly W.](https://transfemscience.org/articles-by-author/aly-w/)
|
||||
|
||||
首次出版于 2019 年 1 月 5 日
|
||||
|
||||
最后修改于 2021 年 9 月 7 日
|
||||
|
||||
译者 [Bersella AI](https://bersella-ai.cc)
|
||||
|
||||
翻译于 2022 年 2 月 18 日
|
||||
|
||||
## 免责声明
|
||||
## 免责声明 {#notice}
|
||||
|
||||
**本文不构成任何医疗、处方建议。** 如有医疗需要,应于专业医师指导下进行。
|
||||
因译者能力所限,部分术语之翻译或有纰漏,烦请指正。
|
||||
|
||||
---
|
||||
|
||||
## 摘要
|
||||
## 摘要 {#abstract}
|
||||
|
||||
> 口服用雌二醇片可经舌下含服,此举相较口服可达到更高的生物利用度,以及雌二醇水平。因此,舌下含服雌二醇在女性倾向跨性别者当中被广泛采用。在世界部分地区也有口服用的戊酸雌二醇(EV)片,常有女性倾向跨性别者咨询其被舌下含服时是否也能高效利用。
|
||||
> 这方面的研究很有限,尚无二者的直接对比;不过至少,已有一项在顺性别女性当中进行的研究表明,EV 片舌下含服时可引起较高的雌二醇水平,以及和雌二醇片类似的对睾酮之抑制。此外,已有至少一座性别肯定激素治疗(GAHT)诊所报告了女性倾向跨性别者使用舌下含服的 EV。因此,舌下含服 EV 似乎是跟舌下含服雌二醇相似的一种高效给药途径。
|
||||
> 二者之间有一处不同:EV 的雌二醇含量更少,故所需摄入量也略多。此外,雌二醇片与 EV 片并非为舌下含服而准备与设计(尽管很有效),其剂型亦有不同。在临床特性上,*(不同剂型)*可能的影响尚未可知。不过显然,不同剂型的片剂舌下含服所需吸收时间会有明显差别。这些剂型的一些性状,例如微粉化、亲油性等,对其药代动力学的影响也会有异,而这尚未得到研究。
|
||||
> 那么,选择舌下含服雌二醇,而非 EV,应是明智之举,因为有关前者的描述更丰富,不确定性更少。不过显然,经舌下含服的 EV 对于女性倾向跨性别者也会很有效。
|
||||
口服用雌二醇片可经舌下含服,此举相较口服可达到更高的生物利用度,以及雌二醇水平。因此,舌下含服雌二醇在女性倾向跨性别者当中被广泛采用。在世界部分地区也有口服用的戊酸雌二醇(EV)片,常有女性倾向跨性别者咨询其被舌下含服时是否也能高效利用。
|
||||
|
||||
## 介绍
|
||||
这方面的研究很有限,尚无二者的直接对比;不过至少,已有一项在顺性别女性当中进行的研究表明,EV 片舌下含服时可引起较高的雌二醇水平,以及和雌二醇片类似的对睾酮之抑制。此外,已有至少一座性别肯定激素治疗(GAHT)诊所报告了女性倾向跨性别者使用舌下含服的 EV。因此,舌下含服 EV 似乎是跟舌下含服雌二醇相似的一种高效给药途径。
|
||||
|
||||
雌二醇片[如诺坤复(Estrofem)、Estrace 等]口服后,通常会被吞服。然而,作为通常的吞服途径之替代,雌二醇片也被用于舌下含服,或含于面颊或嘴唇、牙龈处。舌下、面颊含服雌二醇片相较口服,可达到更高的生物利用度,以及雌二醇水平 ([Sam S., 2021](sublingual-e2-transfem.md))。女性倾向跨性别者在激素治疗当中,常采用舌下含服雌二醇。在一些国家(例如在欧洲),口服用雌二醇会以戊酸雌二醇[EV,如补佳乐(Progynova)]片的形式提供。经常有女性倾向跨性别者咨询,**EV 片是否也能像雌二醇片那样被舌下含服,以及二者是否会有差异**。本文旨在探讨并聚焦于这些问题。
|
||||
二者之间有一处不同:EV 的雌二醇含量更少,故所需摄入量也略多。此外,雌二醇片与 EV 片并非为舌下含服而准备与设计(尽管很有效),其剂型亦有不同。在临床特性上,*(不同剂型)*可能的影响尚未可知。不过显然,不同剂型的片剂舌下含服所需吸收时间会有明显差别。这些剂型的一些性状,例如微粉化、亲油性等,对其药代动力学的影响也会有异,而这尚未得到研究。
|
||||
|
||||
## EV 舌下含服之有效性
|
||||
那么,选择舌下含服雌二醇,而非 EV,应是明智之举,因为有关前者的描述更丰富,不确定性更少。不过显然,经舌下含服的 EV 对于女性倾向跨性别者也会很有效。
|
||||
|
||||
## 介绍 {#introduction}
|
||||
|
||||
雌二醇片[如诺坤复(Estrofem)、Estrace 等]口服后,通常会被吞服。然而,作为通常的吞服途径之替代,雌二醇片也被用于舌下含服,或含于面颊或嘴唇、牙龈处。舌下、面颊含服雌二醇片相较口服,可达到更高的生物利用度,以及雌二醇水平 ([Sam S., 2021](https://transfemscience.org/articles/sublingual-e2-transfem/))。
|
||||
|
||||
女性倾向跨性别者在激素治疗当中,常采用舌下含服雌二醇。在一些国家(例如在欧洲),口服用雌二醇会以戊酸雌二醇[EV,如补佳乐(Progynova)]片的形式提供。经常有女性倾向跨性别者咨询,**EV 片是否也能像雌二醇片那样被舌下含服,以及二者是否会有差异**。
|
||||
|
||||
本文旨在探讨并聚焦于这些问题。
|
||||
|
||||
## EV 舌下含服之有效性 {#effectiveness-of-sublingual-estradiol-valerate}
|
||||
|
||||
EV 是一种雌二醇酯,是雌二醇的前体。雌二醇酯本身在被转换成雌二醇前,并不具备药理活性。EV 及其它雌二醇酯,会被各种酯酶裂解为雌二醇。这些酯酶遍布全身;从雌二醇酯到雌二醇的代谢过程,除肝脏外,也见于血液和其它组织中 ([维基百科](https://en.wikipedia.org/wiki/Estradiol_valerate#Pharmacokinetics))。因此,形如 EV 的雌二醇酯,可以不经过肝脏的首过效应(口服后转换为雌二醇时会发生)。综上,对于非口服方式(如舌下含服,以及肌注)的 EV,其之转换不会成为一种障碍。
|
||||
|
||||
|
|
@ -36,21 +47,26 @@ EV 是一种雌二醇酯,是雌二醇的前体。雌二醇酯本身在被转
|
|||
|
||||
只有一项研究调查并描述了 EV 片的舌下含服。这项研究对一组每日以口服用 EV 片(“补佳乐”品牌)进行 3\~4 次舌下含服的,绝经前的顺性别妇女进行了评估。研究发现在以下两篇论文被发表:
|
||||
|
||||
- Serhal, P., & Craft, I. (1989). Oocyte donation in 61 patients. The Lancet, 333(8648), 1185–1187. [DOI:10.1016/S0140-6736(89)92762-1]
|
||||
- Serhal, P. (1990). Oocyte donation and surrogacy. British Medical Bulletin, 46(3), 796–812. [DOI:10.1093/oxfordjournals.bmb.a072432]
|
||||
- Serhal, P., & Craft, I. (1989). Oocyte donation in 61 patients. The Lancet, 333(8648), 1185–1187. \[DOI: <https://doi.org/10.1016/S0140-6736(89)92762-1>]
|
||||
- Serhal, P. (1990). Oocyte donation and surrogacy. British Medical Bulletin, 46(3), 796–812. \[DOI: <https://doi.org/10.1093/oxfordjournals.bmb.a072432>]
|
||||
|
||||
以下是舌下含服 EV 时,激素水平的结果(上图表示参照组的一个月经周期;下图为含服 EV 组的一个周期):
|
||||
|
||||
> 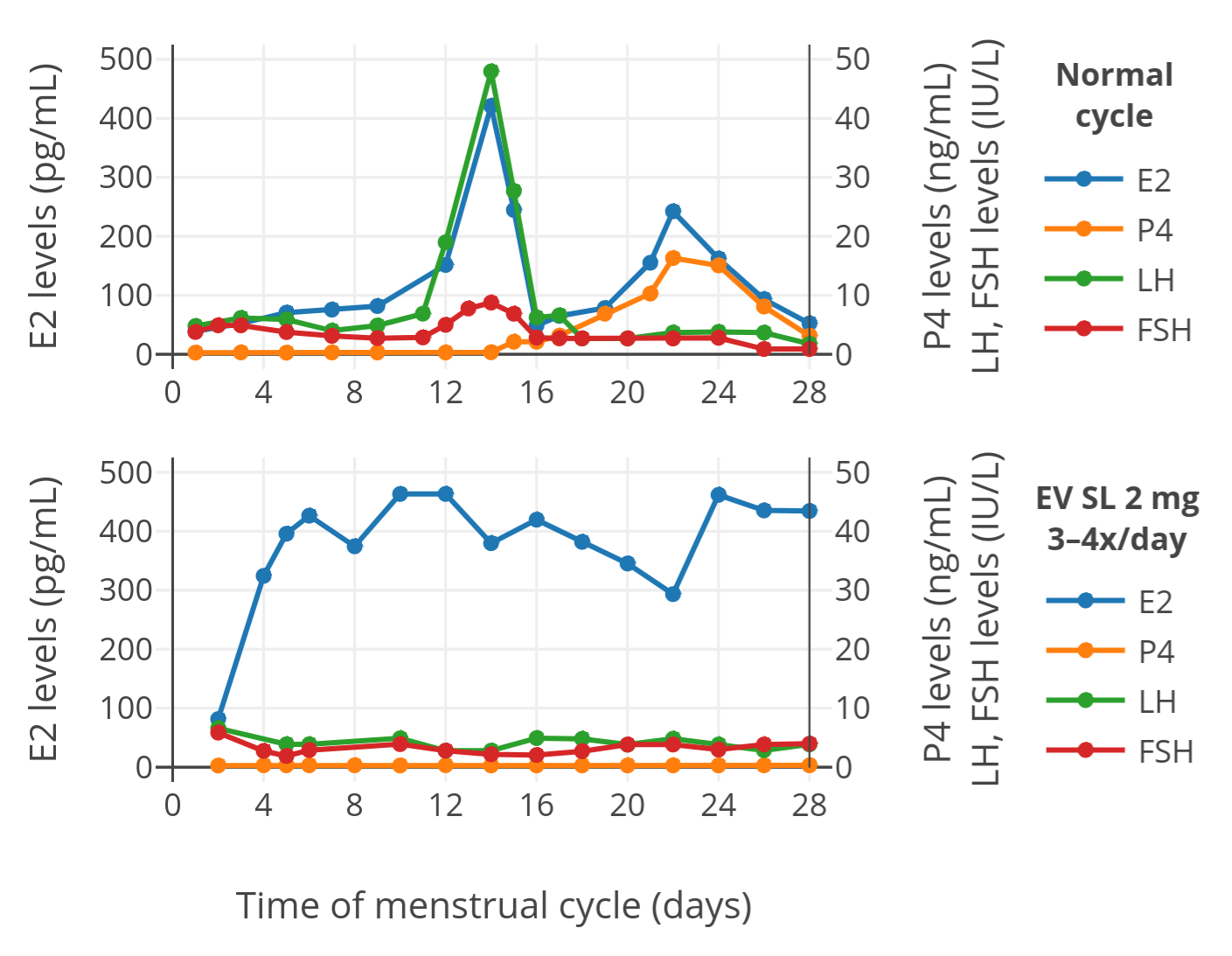
|
||||
> 【图一】每日舌下含服 3\~4 次 2mg EV 片(补佳乐,已微粉化)的绝经前妇女之激素水平(下图),包括雌二醇 (E2)、孕酮 (P4)、促黄体生成素 (LH) 与促卵泡激素 (FSH)。上图为参照组的正常月经周期。服药后在何时采血并未明确说明。
|
||||
<section class="box">
|
||||
|
||||

|
||||
|
||||
**图 1**:每日舌下含服 3\~4 次 2mg EV 片(补佳乐,已微粉化)的绝经前妇女之激素水平(下图),包括雌二醇 (E2)、孕酮 (P4)、促黄体生成素 (LH) 与促卵泡激素 (FSH)。上图为参照组的正常月经周期。服药后在何时采血并未明确说明。
|
||||
|
||||
</section>
|
||||
|
||||
如上图所示,舌下含服 EV 组妇女的雌二醇水平,显著高于处于正常周期的参照组。此外,其它激素的水平也被抑制;这是高水平的雌二醇对下丘脑-垂体-性腺轴之负反馈,并对激素产生之抑制所致。该发现表明,舌下含服的 EV 被很好地吸收了,并可达到和含服雌二醇相似的高雌二醇水平。换句话说,尽管尚无直接对比,但显然,经舌下含服 EV 是一种和含服雌二醇类似的高效的给药方式。
|
||||
|
||||
值得一提的是,在韩国,已有至少一座性别肯定激素治疗(GAHT)诊所报告了女性倾向跨性别者使用舌下含服的 EV。当地医师在近期一份论文里 ([Lim et al., 2019](https://doi.org/10.5468/ogs.2019.62.1.46)) 简要描述了使用舌下含服 EV 的经验,以及未使用口服雌二醇而选择它的理论依据。尽管他们并未提供实际的药代动力学数据,但基于其经验,显然舌下含服是一种行之有效的服用 EV 之途径。
|
||||
|
||||
## 雌二醇片与 EV 片的剂型,及其舌下含服之障碍
|
||||
## 雌二醇片与 EV 片的剂型,及其舌下含服之障碍 {#formulation-of-estradiol-and-estradiol-valerate-tablets-and-implications-for-sublingual-use}
|
||||
|
||||
### 口服用 EV 片的微粉化
|
||||
### 口服用 EV 片的微粉化 {#physicochemical-properties-of-estradiol-versus-estradiol-valerate}
|
||||
|
||||
微粉化是一种将固体颗粒变得更小的生产过程。微粉化可修改药物的吸收速率,从而改变其药代动力学特性。口服用的雌二醇片原先并未被微粉化,其雌激素效力相较今日也更低;但到了 1970 年代,微粉化的雌二醇片开始推出,并取代了早前的剂型。事实表明,将雌二醇晶体微粉化为特定大小之颗粒,使得雌二醇片的吸收率及生物利用度翻了几番 ([维基百科](https://en.wikipedia.org/wiki/Pharmacokinetics_of_estradiol#Absorption_and_bioavailability))。现今市面上所有雌二醇片皆可视为已经过微粉化。
|
||||
|
||||
|
|
@ -62,24 +78,34 @@ EV 是一种雌二醇酯,是雌二醇的前体。雌二醇酯本身在被转
|
|||
|
||||
加州大学旧金山分校 (UCSF) 的《跨性别护理指南》指出,只有经微粉化的雌二醇片可被用于舌下含服,暗示并非所有雌二醇片皆已微粉化 ([Deutsch, 2016](https://transcare.ucsf.edu/sites/transcare.ucsf.edu/files/Transgender-PGACG-6-17-16.pdf#page=26))。该观点可能也适用于 EV 片。然而,正如本文所述,目前这些观点尚缺乏依据。
|
||||
|
||||
### 雌二醇与 EV 的物化特性
|
||||
### 雌二醇与 EV 的物化特性 {#physicochemical-properties-of-estradiol-versus-estradiol-valerate}
|
||||
|
||||
作为含有脂肪酸(也即戊酸)的酯,EV 的脂溶性较雌二醇更高。脂溶性已知可改变药物舌下、面颊含服时的吸收率 ([Smart, 2005](https://doi.org/10.1517/17425247.2.3.507); [Batheja, Thakur, & Michniak, 2006](https://doi.org/10.1201/9781420004816-17))。关于雌二醇与 EV 在脂溶性之差异如何影响其舌下含服时的药代动力学,迄今尚未得到研究。因此,其带来的疗效如何也不清楚。不过,已知在口腔黏膜及唾液内,存在可以将 EV 之类的有机酸酯分解为结合前之形态的酯酶。这也许能够缩小通过舌下、面颊含服的雌二醇与 EV 在物化特性上的差异。
|
||||
|
||||
雌二醇与 EV 的另一项差别在于,作为一种酯,后者的摩尔质量更大,因此相同用量下后者提供的雌二醇更少。EV 的摩尔质量是雌二醇的 131%;这意味着,EV 内雌二醇约占其质量的 76%。这项差异在对口服雌二醇与 EV 的药代动力学研究上已有体现,在相同用量下,口服 EV 在雌二醇水平上要低 25%。这或许也适用于通过其它途径的给药,包括舌下含服。因此,为达到和服用雌二醇相同的雌二醇水平、与雌激素效力,使用 EV 可能需要稍微提高用量(例如 2mg 对应 1.5mg 雌二醇)。
|
||||
|
||||
### EV 片的剂型与溶解
|
||||
### EV 片的剂型与溶解 {#formulation-and-dissolution-of-oral-estradiol-valerate-tablets}
|
||||
|
||||
口服用雌二醇片与 EV 片被设计用于口服,而非舌下含服。其中一些片剂舌下含服的表现尚佳;不过在剂型上,例如包衣、成分与辅料,皆有所区别。一篇文献摘录 ([Sayeed & Ashraf, 2014](https://web.archive.org/web/20201111205841/https://www.pharmtech.com/view/considerations-developing-sublingual-tablets-overview)) 认为,这种差异有可能会影响剂型舌下含服时的特性:
|
||||
|
||||
> 通常,舌下含服的片剂在口腔内分裂并溶解的情况,是有别于口服片剂的。其它一些特制的口服片剂,诸如缓释片、肠溶片等,也可能会在胃中释放部分药剂。与此相反,舌下含服的片剂被设计为可在口腔、舌下完全分裂并溶解。
|
||||
|
||||
有一种特殊情况是:雌二醇、EV 的不同口服片剂,溶解速率或有明显差异。一项关于舌下含服口服用雌二醇片的研究,报告了其在 1\~2 分钟内溶解了 ([Burnier, 1981](<https://doi.org/10.1016/0002-9378(81)90101-0>))。传闻在美国有一种仿制的糖包衣的雌二醇口服片 ([照片](https://img.medscapestatic.com/pi/features/drugdirectory/octupdate/BRR08870.jpg)),情况与此类似,舌下含服时在数分钟内即溶解以至消失。不过,一些女性倾向跨性别者在 Reddit 等社交平台上披露,她们的片剂在舌下、或面颊内溶解用了更长时间。例如,有人报告其服用的 EV 片(“补佳乐”)用了约一小时的时间才完全溶解 (Reddit [来源一](https://www.reddit.com/r/MtFHRT/comments/ad0uhp/hormone_levels_with_2_mg_oral_estradiol_valerate/eg5oyks/); [来源二](https://www.reddit.com/r/MtFHRT/comments/9h8s04/so_whats_the_consensus_on_buccalsublingual/e8mz1bk/))。尽管如此,她们仍报告了采用单服 EV(面颊含服)疗法时达到了高水平的雌二醇浓度,以及对睾酮的强力压制。总之,基于其剂型,雌二醇片与 EV 片的溶解速率会有差异;而且其中部分剂型相对会更适合舌下含服。如果 _(某品牌)_ 片剂舌下含服时溶解得更慢,也许可以考虑换用其它品牌。
|
||||
有一种特殊情况是:雌二醇、EV 的不同口服片剂,溶解速率或有明显差异。一项关于舌下含服口服用雌二醇片的研究,报告了其在 1\~2 分钟内溶解了 ([Burnier, 1981](https://doi.org/10.1016/0002-9378(81)90101-0))。传闻在美国有一种仿制的糖包衣的雌二醇口服片 ([照片](https://img.medscapestatic.com/pi/features/drugdirectory/octupdate/BRR08870.jpg)),情况与此类似,舌下含服时在数分钟内即溶解以至消失。不过,一些女性倾向跨性别者在 Reddit 等社交平台上披露,她们的片剂在舌下、或面颊内溶解用了更长时间。例如,有人报告其服用的 EV 片(“补佳乐”)用了约一小时的时间才完全溶解 (Reddit [来源一](https://reddit.com/r/MtFHRT/comments/ad0uhp/comment/eg5oyks/); [来源二](https://reddit.com/r/MtFHRT/comments/9h8s04/comment/e8mz1bk/))。尽管如此,她们仍报告了采用单服 EV(面颊含服)疗法时达到了高水平的雌二醇浓度,以及对睾酮的强力压制。总之,基于其剂型,雌二醇片与 EV 片的溶解速率会有差异;而且其中部分剂型相对会更适合舌下含服。如果 _(某品牌)_ 片剂舌下含服时溶解得更慢,也许可以考虑换用其它品牌。
|
||||
|
||||
## 应该选择含服雌二醇片,还是 EV 片?
|
||||
## 应该选择含服雌二醇片,还是 EV 片? {#estradiol-or-estradiol-valerate-for-sublingual-use}
|
||||
|
||||
相较 EV 片而言,对于雌二醇片的舌下含服,相关调查与描述丰富得多。因此,选择含服不确定性更少的雌二醇片,而非 EV 片,不失为明智之举。不过,在某些市场上,并不一定会有雌二醇片,而 EV 片则会被作为处方开出;雌二醇片也可能出于其它原因而不大适合选用。就这点而言,基于已有文献,显然舌下含服 EV 片是一种和舌下含服雌二醇相似的、高效的雌二醇给药方式,有需要时不妨一用。
|
||||
|
||||
## 参考文献
|
||||
## 参考文献 {#references}
|
||||
|
||||
略
|
||||
- Batheja, P., Thakur, R., & Michniak, B. (2006). Basic Biopharmaceutics of Buccal and Sublingual Absorption. In Touitou, E., & Barry, B. W. (Eds.). _Enhancement in Drug Delivery_ (pp. 175–202). Boca Raton/London/New York: CRC Press. \[[Google Scholar](https://scholar.google.com/scholar?cluster=8652202749142820648)\] \[[Google Books](https://books.google.com/books?id=t0L_zFoXmjkC&pg=PA175)\] \[DOI:<https://doi.org/10.1201/9781420004816-17>\] \[[PDF](https://files.transfemscience.org/pdfs/Batheja,%20Thakur,%20&%20Michniak%20(2006)%20-%20Basic%20Biopharmaceutics%20of%20Buccal%20and%20Sublingual%20Absorption%20%5BIn%20Touitou%20&%20Barry%20-%20Enhancement%20in%20Drug%20Delivery%20(pp.%20175%E2%80%93202)%5D.pdf)\]
|
||||
- Burnier, A. M., Martin, P. L., Yen, S. S., & Brooks, P. (1981). Sublingual absorption of micronized 17β-estradiol. _American Journal of Obstetrics and Gynecology_, _140_(2), 146–150. \[DOI:<https://doi.org/10.1016/0002-9378(81)90101-0>\]
|
||||
- Deutsch, M. B. (2016). Overview of feminizing hormone therapy. In Deutsch, M. B. (Ed.). _Guidelines for the Primary and Gender-Affirming Care of Transgender and Gender Nonbinary People, 2nd Edition_ (pp. 26–48). San Francisco: University of California, San Francisco/UCSF Transgender Care. \[[Google Scholar](https://scholar.google.com/scholar?cluster=14884919836847089083)\] \[[URL](https://transcare.ucsf.edu/guidelines/feminizing-hormone-therapy)\] \[[PDF](https://transcare.ucsf.edu/sites/transcare.ucsf.edu/files/Transgender-PGACG-6-17-16.pdf#page=26)\]
|
||||
- Devroey, P., & Pados, G. (1998). Preparation of endometrium for egg donation. _Human Reproduction Update_, _4_(6), 856–861. \[DOI:<https://doi.org/10.1093/humupd/4.6.856>\]
|
||||
- Lim, H. H., Jang, Y. H., Choi, G. Y., Lee, J. J., & Lee, E. S. (2019). Gender affirmative care of transgender people: a single center’s experience in Korea. _Obstetrics & Gynecology Science_, _62_(1), 46–55. \[DOI:<https://doi.org/10.5468/ogs.2019.62.1.46>\]
|
||||
- Rathbone, M. J., Drummond, B. K., & Tucker, I. G. (1994). The oral cavity as a site for systemic drug delivery. _Advanced Drug Delivery Reviews_, _13_(1–2), 1–22. \[DOI:<https://doi.org/10.1016/0169-409X(94)90024-8>\]
|
||||
- Sayeed, V. A., & Ashraf, M. (2014). Considerations in Developing Sublingual Tablets—An Overview. _Pharmaceutical Technology_, _38_(11), 34–72. \[[Google Scholar](https://scholar.google.com/scholar?cluster=1357039233409295184)\] \[[URL](https://web.archive.org/web/20201111205841/https://www.pharmtech.com/view/considerations-developing-sublingual-tablets-overview)\] \[[PDF](https://files.transfemscience.org/pdfs/Sayeed%20&%20Ashraf%20(2014)%20-%20Considerations%20in%20Developing%20Sublingual%20Tablets%E2%80%94An%20Overview%20-%20Pharmaceutical%20Technology.pdf)\]
|
||||
- Serhal, P., & Craft, I. (1989). Oocyte donation in 61 patients. _The Lancet_, _333_(8648), 1185–1187. \[DOI:<https://doi.org/10.1016/S0140-6736(89)92762-1>\]
|
||||
- Serhal, P. (1990). Oocyte donation and surrogacy. _British Medical Bulletin_, _46_(3), 796–812. \[DOI:<https://doi.org/10.1093/oxfordjournals.bmb.a072432>\]
|
||||
- Smart, J. D. (2005). Buccal drug delivery. _Expert Opinion on Drug Delivery_, _2_(3), 507–517. \[DOI:<https://doi.org/10.1517/17425247.2.3.507>\]
|
||||
- Yamahara, H., & Lee, V. H. (1993). Drug metabolism in the oral cavity. _Advanced Drug Delivery Reviews_, _12_(1–2), 25–39. \[DOI:<https://doi.org/10.1016/0169-409X(93)90039-7>\]
|
||||
File diff suppressed because it is too large
Load Diff
|
|
@ -0,0 +1,18 @@
|
|||
---
|
||||
title: Transfeminine Science License
|
||||
description: Transfeminine Science is Copyright of Aly W. and the other authors of Transfeminine Science.
|
||||
hidden: true
|
||||
---
|
||||
|
||||
Transfeminine Science is [Copyright](https://en.wikipedia.org/wiki/Copyright) of [Aly W][aly-w].
|
||||
and the other authors of Transfeminine Science.
|
||||
|
||||
[All rights are reserved](https://en.wikipedia.org/wiki/All_rights_reserved).
|
||||
Please do not reproduce content from Transfeminine Science unless given direct permission from [Aly W][aly-w].
|
||||
(e.g., for [translation projects](https://transfemscience.org/misc/#transfeminine-science-translations)).
|
||||
|
||||
If permission to reproduce content is granted, the content should be properly attributed and linked back to the original page(s) on Transfeminine Science.
|
||||
|
||||
see <https://transfemscience.org/about/#license>
|
||||
|
||||
[aly-w]: https://transfemscience.org/articles-by-author/aly-w/
|
||||
|
|
@ -0,0 +1,5 @@
|
|||
---
|
||||
title: 杂项
|
||||
description: 杂项
|
||||
weight: 3
|
||||
---
|
||||
|
|
@ -0,0 +1,19 @@
|
|||
---
|
||||
title: 未确定的特殊名词翻译一览表
|
||||
description: 若不同文章间出现了相同的未确定翻译,则以其按照顺序中第一次出现的文章计入本表。
|
||||
---
|
||||
|
||||
若不同文章间出现了相同的未确定翻译,则以其按照顺序中第一次出现的文章计入本表。
|
||||
|
||||
## 女性倾向跨性别者的激素治疗简介 {#transfem-intro}
|
||||
|
||||
see [女性倾向跨性别者的激素治疗简介]({{< ref "transfem-intro" >}})
|
||||
|
||||
```csv
|
||||
英文原词,中文待定翻译
|
||||
GAH therapy,性别肯定激素治疗
|
||||
Gender-Affirming Hormone therapy,
|
||||
Hormonal profile,激素状况
|
||||
Transfeminine hormone therapy,女性化激素治疗
|
||||
Transfeminine people,女性倾向跨性别者
|
||||
```
|
||||
|
|
@ -0,0 +1,84 @@
|
|||
FHT:
|
||||
origin: Feminizing Hormone Therapy
|
||||
title: 女性化激素疗法
|
||||
href: https://en.wikipedia.org/wiki/Feminizing_hormone_therapy
|
||||
MtF:
|
||||
origin: Male to Female
|
||||
title: 跨性别女性
|
||||
href: https://en.wikipedia.org/wiki/MtF
|
||||
HRT:
|
||||
origin: Hormone Replacement Therapy
|
||||
title: 激素替代疗法
|
||||
href: https://en.wikipedia.org/wiki/Transgender_hormone_therapy
|
||||
GaHT:
|
||||
origin: Gender-affirming Hormone Therapy
|
||||
title: 性别肯定激素疗法
|
||||
href: https://en.wikipedia.org/wiki/Transgender_hormone_therapy
|
||||
E:
|
||||
origin: Estrogen
|
||||
title: 雌激素
|
||||
href: https://en.wikipedia.org/wiki/Estrogen
|
||||
P:
|
||||
origin: Progestogen
|
||||
title: 孕激素
|
||||
href: https://en.wikipedia.org/wiki/Progestogen
|
||||
E2:
|
||||
origin: Estradiol
|
||||
title: 雌二醇
|
||||
href: https://en.wikipedia.org/wiki/Estradiol
|
||||
P4:
|
||||
origin: Progesterone
|
||||
title: 孕酮
|
||||
href: https://en.wikipedia.org/wiki/Progesterone
|
||||
T:
|
||||
origin: Testosterone
|
||||
title: 睾酮
|
||||
href: https://en.wikipedia.org/wiki/Testosterone
|
||||
DHT:
|
||||
origin: Dihydrotestosterone
|
||||
title: 双氢睾酮
|
||||
href: https://en.wikipedia.org/wiki/Dihydrotestosterone
|
||||
AR:
|
||||
origin: Androgen Receptor
|
||||
title: 雄激素受体
|
||||
href: https://en.wikipedia.org/wiki/Androgen_receptor
|
||||
ER:
|
||||
origin: Estrogen Receptor
|
||||
title: 雌激素受体
|
||||
href: https://en.wikipedia.org/wiki/Estrogen_receptor
|
||||
PR:
|
||||
origin: Progesterone Receptor
|
||||
title: 孕激素受体
|
||||
href: https://en.wikipedia.org/wiki/Progesterone_receptor
|
||||
PO:
|
||||
origin: Oral administration
|
||||
title: 口服给药
|
||||
href: https://en.wikipedia.org/wiki/Oral_administration
|
||||
SL:
|
||||
origin: Sublingual administration
|
||||
title: 舌下给药
|
||||
href: https://en.wikipedia.org/wiki/Sublingual_administration
|
||||
BUC:
|
||||
origin: Buccal administration
|
||||
title: 颊部给药
|
||||
href: https://en.wikipedia.org/wiki/Buccal_administration
|
||||
TD:
|
||||
origin: Transdermal
|
||||
title: 透皮给药
|
||||
href: https://en.wikipedia.org/wiki/Transdermal
|
||||
REC:
|
||||
origin: Rectal administration
|
||||
title: 直肠给药
|
||||
href: https://en.wikipedia.org/wiki/Rectal_administration
|
||||
IM:
|
||||
origin: Intramuscular injection
|
||||
title: 肌肉注射
|
||||
href: https://en.wikipedia.org/wiki/Intramuscular_injection
|
||||
SC:
|
||||
origin: Subcutaneous injection
|
||||
title: 皮下注射
|
||||
href: https://en.wikipedia.org/wiki/Subcutaneous_injection
|
||||
SCi:
|
||||
origin: Subcutaneous implant
|
||||
title: 皮下植入
|
||||
href: https://en.wikipedia.org/wiki/Subcutaneous_implant
|
||||
|
|
@ -0,0 +1,69 @@
|
|||
{
|
||||
"name": "@mtf-wiki/tfsci",
|
||||
"version": "0.0.0",
|
||||
"lockfileVersion": 2,
|
||||
"requires": true,
|
||||
"packages": {
|
||||
"": {
|
||||
"name": "@mtf-wiki/tfsci",
|
||||
"version": "0.0.0",
|
||||
"dependencies": {
|
||||
"bulma": "^0.9.4",
|
||||
"throttle-debounce-ts": "^1.1.1",
|
||||
"tippy.js": "^6.3.7"
|
||||
}
|
||||
},
|
||||
"node_modules/@popperjs/core": {
|
||||
"version": "2.11.6",
|
||||
"resolved": "https://registry.npmjs.org/@popperjs/core/-/core-2.11.6.tgz",
|
||||
"integrity": "sha512-50/17A98tWUfQ176raKiOGXuYpLyyVMkxxG6oylzL3BPOlA6ADGdK7EYunSa4I064xerltq9TGXs8HmOk5E+vw==",
|
||||
"funding": {
|
||||
"type": "opencollective",
|
||||
"url": "https://opencollective.com/popperjs"
|
||||
}
|
||||
},
|
||||
"node_modules/bulma": {
|
||||
"version": "0.9.4",
|
||||
"resolved": "https://registry.npmjs.org/bulma/-/bulma-0.9.4.tgz",
|
||||
"integrity": "sha512-86FlT5+1GrsgKbPLRRY7cGDg8fsJiP/jzTqXXVqiUZZ2aZT8uemEOHlU1CDU+TxklPEZ11HZNNWclRBBecP4CQ=="
|
||||
},
|
||||
"node_modules/throttle-debounce-ts": {
|
||||
"version": "1.1.1",
|
||||
"resolved": "https://registry.npmjs.org/throttle-debounce-ts/-/throttle-debounce-ts-1.1.1.tgz",
|
||||
"integrity": "sha512-GUz8pRapqadMqXhQcQPwN/Cvmt0QqFtvr/aVle4yyigqhsC+aCtS3dSnsQwmxAeeB6D8ww6xsl2GRsWWad9/4w=="
|
||||
},
|
||||
"node_modules/tippy.js": {
|
||||
"version": "6.3.7",
|
||||
"resolved": "https://registry.npmjs.org/tippy.js/-/tippy.js-6.3.7.tgz",
|
||||
"integrity": "sha512-E1d3oP2emgJ9dRQZdf3Kkn0qJgI6ZLpyS5z6ZkY1DF3kaQaBsGZsndEpHwx+eC+tYM41HaSNvNtLx8tU57FzTQ==",
|
||||
"dependencies": {
|
||||
"@popperjs/core": "^2.9.0"
|
||||
}
|
||||
}
|
||||
},
|
||||
"dependencies": {
|
||||
"@popperjs/core": {
|
||||
"version": "2.11.6",
|
||||
"resolved": "https://registry.npmjs.org/@popperjs/core/-/core-2.11.6.tgz",
|
||||
"integrity": "sha512-50/17A98tWUfQ176raKiOGXuYpLyyVMkxxG6oylzL3BPOlA6ADGdK7EYunSa4I064xerltq9TGXs8HmOk5E+vw=="
|
||||
},
|
||||
"bulma": {
|
||||
"version": "0.9.4",
|
||||
"resolved": "https://registry.npmjs.org/bulma/-/bulma-0.9.4.tgz",
|
||||
"integrity": "sha512-86FlT5+1GrsgKbPLRRY7cGDg8fsJiP/jzTqXXVqiUZZ2aZT8uemEOHlU1CDU+TxklPEZ11HZNNWclRBBecP4CQ=="
|
||||
},
|
||||
"throttle-debounce-ts": {
|
||||
"version": "1.1.1",
|
||||
"resolved": "https://registry.npmjs.org/throttle-debounce-ts/-/throttle-debounce-ts-1.1.1.tgz",
|
||||
"integrity": "sha512-GUz8pRapqadMqXhQcQPwN/Cvmt0QqFtvr/aVle4yyigqhsC+aCtS3dSnsQwmxAeeB6D8ww6xsl2GRsWWad9/4w=="
|
||||
},
|
||||
"tippy.js": {
|
||||
"version": "6.3.7",
|
||||
"resolved": "https://registry.npmjs.org/tippy.js/-/tippy.js-6.3.7.tgz",
|
||||
"integrity": "sha512-E1d3oP2emgJ9dRQZdf3Kkn0qJgI6ZLpyS5z6ZkY1DF3kaQaBsGZsndEpHwx+eC+tYM41HaSNvNtLx8tU57FzTQ==",
|
||||
"requires": {
|
||||
"@popperjs/core": "^2.9.0"
|
||||
}
|
||||
}
|
||||
}
|
||||
}
|
||||
|
|
@ -0,0 +1,10 @@
|
|||
{
|
||||
"name": "@mtf-wiki/tfsci",
|
||||
"version": "0.0.0",
|
||||
"private": true,
|
||||
"dependencies": {
|
||||
"bulma": "^0.9.4",
|
||||
"throttle-debounce-ts": "^1.1.1",
|
||||
"tippy.js": "^6.3.7"
|
||||
}
|
||||
}
|
||||
|
|
@ -0,0 +1,20 @@
|
|||
乳腺癌 乳癌
|
||||
保法止 柔沛
|
||||
倍美力 普力馬林
|
||||
優思明 悅己
|
||||
卵泡刺激素 濾泡刺激素
|
||||
垂體促性腺激素 性腺激素釋放素
|
||||
天生女性 原生女性
|
||||
性腺性激素 性腺激素
|
||||
抗雄激素 抗雄性素
|
||||
比卡魯胺 可蘇多
|
||||
激光 雷射
|
||||
脫靶活動 脫靶效應
|
||||
色譜龍 安得卡
|
||||
螺內酯 蘇拉通
|
||||
補佳樂 益斯德
|
||||
達芙通 得胎隆
|
||||
適尿通 新髮靈
|
||||
高血鉀癥 高血鉀症
|
||||
睾酮 睪固酮
|
||||
藥物 藥品
|
||||
|
|
@ -0,0 +1,37 @@
|
|||
#!/bin/bash
|
||||
set -euo pipefail
|
||||
|
||||
SCRIPT_DIR=$(cd -- "$(dirname -- "${BASH_SOURCE[0]}")" &>/dev/null && pwd)
|
||||
|
||||
function cc() {
|
||||
local original="$1"
|
||||
local language="$2"
|
||||
local config="$3"
|
||||
local input="content/$original"
|
||||
local output="content.$language/$original"
|
||||
mkdir -p "$(dirname "$output")"
|
||||
opencc \
|
||||
--config "$config" \
|
||||
--input "$input" \
|
||||
--output "$output"
|
||||
}
|
||||
|
||||
files=$(
|
||||
cd content || exit
|
||||
find . -type f -name '*.md'
|
||||
)
|
||||
|
||||
for file in $files; do
|
||||
cc "$file" "zh-tw" "$SCRIPT_DIR/s2twp.json"
|
||||
cc "$file" "zh-hk" "s2hk"
|
||||
done
|
||||
|
||||
opencc \
|
||||
--config "$SCRIPT_DIR/s2twp.json" \
|
||||
--input "data/abbreviation.zh-cn.yaml" \
|
||||
--output "data/abbreviation.zh-tw.yaml"
|
||||
|
||||
opencc \
|
||||
--config "s2hk" \
|
||||
--input "data/abbreviation.zh-cn.yaml" \
|
||||
--output "data/abbreviation.zh-hk.yaml"
|
||||
|
|
@ -0,0 +1,21 @@
|
|||
{
|
||||
"name": "Taiwan",
|
||||
"segmentation": {
|
||||
"type": "mmseg",
|
||||
"dict": { "type": "ocd2", "file": "STPhrases.ocd2" }
|
||||
},
|
||||
"conversion_chain": [
|
||||
{
|
||||
"dict": {
|
||||
"type": "group",
|
||||
"dicts": [
|
||||
{ "type": "ocd2", "file": "STPhrases.ocd2" },
|
||||
{ "type": "ocd2", "file": "STCharacters.ocd2" }
|
||||
]
|
||||
}
|
||||
},
|
||||
{ "dict": { "type": "ocd2", "file": "TWPhrases.ocd2" } },
|
||||
{ "dict": { "type": "ocd2", "file": "TWVariants.ocd2" } },
|
||||
{ "dict": { "type": "text", "file": "CustomTW.txt" } }
|
||||
]
|
||||
}
|
||||
|
|
@ -0,0 +1,5 @@
|
|||
/*
|
||||
Access-Control-Allow-Origin: null
|
||||
Cache-Control: max-age=600
|
||||
X-Content-Type-Options: nosniff
|
||||
X-Frame-Options: DENY
|
||||
|
|
@ -0,0 +1,19 @@
|
|||
/ /zh-cn/
|
||||
/favicon.ico /favicon.png
|
||||
/security.txt https://mtf.wiki/.well-known/security.txt
|
||||
/.well-known/security.txt https://mtf.wiki/.well-known/security.txt
|
||||
/humans.txt https://github.com/mtf-wiki/transfeminine-science/graphs/contributors
|
||||
/about.html /zh-cn/about/ 301
|
||||
/LICENSE.md /zh-cn/misc/license/ 301
|
||||
/articles/bica-adoption.html /zh-cn/articles/bica-adoption/ 301
|
||||
/articles/breast-cancer.html /zh-cn/articles/breast-cancer/ 301
|
||||
/articles/cpa-dosage.html /zh-cn/articles/cpa-dosage/ 301
|
||||
/articles/cpa-meningioma.html /zh-cn/articles/cpa-meningioma/ 301
|
||||
/articles/genital-e2-application.html /zh-cn/articles/genital-e2-application/ 301
|
||||
/articles/injectable-e2-meta-analysis.html /zh-cn/articles/injectable-e2-meta-analysis/ 301
|
||||
/articles/nonbinary-transfem-overview.html /zh-cn/articles/nonbinary-transfem-overview/ 301
|
||||
/articles/oral-p4-low-levels.html /zh-cn/articles/oral-p4-low-levels/ 301
|
||||
/articles/shbg.html /zh-cn/articles/shbg/ 301
|
||||
/articles/sublingual-e2-transfem.html /zh-cn/articles/sublingual-e2-transfem/ 301
|
||||
/articles/sublingual-ev.html /zh-cn/articles/sublingual-ev/ 301
|
||||
/articles/transfem-intro.html /zh-cn/articles/transfem-intro/ 301
|
||||
|
|
@ -0,0 +1,10 @@
|
|||
{{- $created := .Date | time | dateFormat "2006-01-02" -}}
|
||||
---
|
||||
title: {{ .Name }}
|
||||
author: Aly W.
|
||||
published: {{ $created }}
|
||||
updated: {{ $created }}
|
||||
translated: {{ $created }}
|
||||
translators: []
|
||||
draft: true
|
||||
---
|
||||
|
|
@ -0,0 +1,4 @@
|
|||
---
|
||||
title: {{ .Name }}
|
||||
draft: true
|
||||
---
|
||||
Binary file not shown.
|
After Width: | Height: | Size: 59 KiB |
|
|
@ -0,0 +1,27 @@
|
|||
export const ready = new Promise<void>((resolve) => {
|
||||
if (document.readyState === 'complete') {
|
||||
resolve()
|
||||
} else {
|
||||
document.addEventListener('readystatechange', () => {
|
||||
if (document.readyState !== 'complete') return
|
||||
resolve()
|
||||
})
|
||||
}
|
||||
})
|
||||
|
||||
export function on<E extends Event>(
|
||||
element: EventTarget,
|
||||
name: string,
|
||||
selector: string,
|
||||
listener: (event: E) => void,
|
||||
options?: AddEventListenerOptions
|
||||
) {
|
||||
const bound = (event: Event) => {
|
||||
if (event.target === null) return
|
||||
const target = event.target as HTMLElement
|
||||
if (target.closest(selector) === null) return
|
||||
listener(event as E)
|
||||
}
|
||||
element.addEventListener(name, bound, options)
|
||||
return () => element.removeEventListener(name, bound, options)
|
||||
}
|
||||
|
|
@ -0,0 +1,41 @@
|
|||
import { debounce } from 'throttle-debounce-ts'
|
||||
|
||||
history.scrollRestoration = 'manual'
|
||||
|
||||
export function onRestoreAnchor() {
|
||||
let hash = decodeURIComponent(location.hash)
|
||||
if (!hash) return
|
||||
const heading = document.getElementById(hash.slice(1))
|
||||
if (!heading) return
|
||||
heading.scrollIntoView({ block: 'start', inline: 'nearest' })
|
||||
}
|
||||
|
||||
export function onSaveAnchor() {
|
||||
const content = document.querySelector('article.content')
|
||||
if (!content) return
|
||||
// prettier-ignore
|
||||
const headings = Array.from(content.querySelectorAll('[id]'))
|
||||
.filter((element): element is HTMLHeadingElement => /^H\d$/.test(element.tagName))
|
||||
const onScroll = debounce(100, () => {
|
||||
const heading = findHeading(headings)
|
||||
const target = new URL(location.href)
|
||||
target.hash = heading ? `#${heading.id}` : ''
|
||||
history.replaceState(undefined, '', target)
|
||||
})
|
||||
addEventListener('scroll', onScroll, { passive: true })
|
||||
}
|
||||
|
||||
function findHeading(headings: HTMLHeadingElement[]) {
|
||||
const position = scrollY
|
||||
return headings.find((heading, index, headings) => {
|
||||
const current = heading.offsetTop
|
||||
let next: number
|
||||
if (headings[index + 1]) {
|
||||
next = headings[index + 1].offsetTop
|
||||
} else {
|
||||
const parent = heading.parentElement!
|
||||
next = parent.offsetTop + parent.offsetHeight
|
||||
}
|
||||
return position >= current - 1 && position < next - 1
|
||||
})
|
||||
}
|
||||
|
|
@ -0,0 +1,16 @@
|
|||
export function getItem<T>(name: string, defaultValue?: T): T {
|
||||
const value = localStorage.getItem(name)
|
||||
return value ? JSON.parse(value) : defaultValue
|
||||
}
|
||||
|
||||
export function setItem<T>(name: string, value: T) {
|
||||
localStorage.setItem(name, JSON.stringify(value))
|
||||
}
|
||||
|
||||
export function editItem<T>(name: string, editor: (value: T | undefined) => T) {
|
||||
setItem(name, editor(getItem<T>(name, undefined)))
|
||||
}
|
||||
|
||||
export function getPageKey() {
|
||||
return document.querySelector<HTMLMetaElement>('meta[name=page-key]')!.content
|
||||
}
|
||||
|
|
@ -0,0 +1,22 @@
|
|||
declare const MEASUREMENT_ID: string
|
||||
|
||||
// @ts-ignore
|
||||
window.dataLayer = window.dataLayer || []
|
||||
|
||||
function gtag(...values: unknown[]): void
|
||||
function gtag() {
|
||||
// @ts-ignore
|
||||
window.dataLayer.push(arguments)
|
||||
}
|
||||
|
||||
gtag('js', new Date())
|
||||
gtag('config', MEASUREMENT_ID)
|
||||
|
||||
const script = document.createElement('script')
|
||||
script.async = true
|
||||
script.src = 'https://www.googletagmanager.com/gtag/js?id=' + MEASUREMENT_ID
|
||||
script.addEventListener('load', () => script.remove())
|
||||
|
||||
document.currentScript!.remove()
|
||||
|
||||
document.head.append(script)
|
||||
|
|
@ -0,0 +1,80 @@
|
|||
@import 'node_modules/bulma/bulma';
|
||||
@import 'node_modules/tippy.js/dist/tippy';
|
||||
@import 'node_modules/tippy.js/themes/light-border';
|
||||
|
||||
:root {
|
||||
touch-action: manipulation;
|
||||
font-variant-numeric: tabular-nums;
|
||||
scroll-padding-top: $navbar-height + 2rem;
|
||||
}
|
||||
|
||||
body {
|
||||
$font-family: Helvetica, Arial, '-apple-system', 'BlinkMacSystemFont', system-ui, sans-serif;
|
||||
$font-family-tc: 'PingFang TC', 'Apple LiGothic Medium', 'Microsoft JhengHei', 'WenQuanYi Zen Hei', $font-family;
|
||||
|
||||
@at-root :root:lang(zh-cn) & {
|
||||
font-family: 'Noto Sans SC', 'PingFang SC', $font-family;
|
||||
}
|
||||
|
||||
@at-root :root:lang(zh-tw) & {
|
||||
font-family: 'Noto Sans TC', $font-family-tc;
|
||||
}
|
||||
|
||||
@at-root :root:lang(zh-hk) & {
|
||||
font-family: 'Noto Sans HK', $font-family-tc;
|
||||
}
|
||||
|
||||
> main {
|
||||
min-height: 100vh;
|
||||
}
|
||||
}
|
||||
|
||||
main > .container {
|
||||
@include from($tablet) {
|
||||
max-width: $tablet !important;
|
||||
}
|
||||
}
|
||||
|
||||
.content {
|
||||
table.table {
|
||||
width: auto;
|
||||
|
||||
white-space: nowrap;
|
||||
}
|
||||
|
||||
figure {
|
||||
margin-right: 0;
|
||||
margin-left: 0;
|
||||
}
|
||||
|
||||
.card-image img {
|
||||
width: 100%;
|
||||
}
|
||||
|
||||
dl.metadata {
|
||||
display: grid;
|
||||
overflow: hidden;
|
||||
|
||||
word-break: break-all;
|
||||
|
||||
grid-template-columns: max-content auto;
|
||||
|
||||
dt {
|
||||
padding-right: 1em;
|
||||
|
||||
text-align: end;
|
||||
|
||||
grid-column-start: 1;
|
||||
}
|
||||
|
||||
dd {
|
||||
margin-left: 0;
|
||||
|
||||
grid-column-start: 2;
|
||||
}
|
||||
|
||||
span {
|
||||
display: inline-block;
|
||||
}
|
||||
}
|
||||
}
|
||||
|
|
@ -0,0 +1,102 @@
|
|||
import { onRestoreAnchor, onSaveAnchor } from './functions/scroll'
|
||||
import { on, ready } from './functions/browser'
|
||||
import tippy from 'tippy.js'
|
||||
|
||||
ready
|
||||
.then(onTableStyle)
|
||||
.then(onMobileHeader)
|
||||
.then(onLanguageSwitch)
|
||||
.then(onRestoreAnchor)
|
||||
.then(onSaveAnchor)
|
||||
.then(onRestoreEmailAddress)
|
||||
.then(onReferenceLinks)
|
||||
.then(onAbbreviation)
|
||||
|
||||
function onTableStyle() {
|
||||
const content = document.querySelector('article.content')
|
||||
if (!content) return
|
||||
const template = document.createElement('section')
|
||||
template.classList.add('table-container')
|
||||
for (const element of content.querySelectorAll('table')) {
|
||||
element.classList.add('table', 'is-narrow', 'is-hoverable')
|
||||
const container = template.cloneNode()
|
||||
container.appendChild(element.cloneNode(true))
|
||||
element.replaceWith(container)
|
||||
}
|
||||
}
|
||||
|
||||
function onMobileHeader() {
|
||||
on(document, 'click', '.navbar-burger', (event) => {
|
||||
const target = event.target as HTMLElement
|
||||
const menu = target.closest('.navbar')!.querySelector('.navbar-menu')!
|
||||
menu.classList.toggle('is-active')
|
||||
target.closest('.navbar-burger')!.ariaExpanded = String(menu.classList.contains('is-active'))
|
||||
})
|
||||
}
|
||||
|
||||
function onLanguageSwitch() {
|
||||
on(document, 'click', '.navbar-item.language a', (event) => {
|
||||
event.preventDefault()
|
||||
const target = event.target as HTMLAnchorElement
|
||||
const url = new URL(target.href)
|
||||
url.hash = location.hash
|
||||
location.replace(url.toString())
|
||||
})
|
||||
}
|
||||
|
||||
function onRestoreEmailAddress() {
|
||||
const content = document.querySelector('article.content')
|
||||
if (!content) return
|
||||
for (const link of content.querySelectorAll<HTMLAnchorElement>('a[href^="mailto:"]')) {
|
||||
const address = atob(link.pathname)
|
||||
link.href = `mailto:${address}`
|
||||
link.textContent = address
|
||||
}
|
||||
}
|
||||
|
||||
function onReferenceLinks() {
|
||||
const content = document.querySelector('article.content')
|
||||
if (!content) return
|
||||
const citationMap = new Map<string, HTMLElement>()
|
||||
for (const link of content.querySelectorAll<HTMLAnchorElement>('#references + ul a')) {
|
||||
citationMap.set(link.href, link.closest('li')!)
|
||||
}
|
||||
if (citationMap.size === 0) return
|
||||
const links = Array.from(content.querySelectorAll('a'))
|
||||
.filter((link) => link.closest('#references + ul') === null)
|
||||
.filter((link) => citationMap.has(link.href))
|
||||
tippy(links, {
|
||||
touch: 'hold',
|
||||
theme: 'light-border',
|
||||
interactive: true,
|
||||
appendTo: document.body,
|
||||
content(ref) {
|
||||
const cite = citationMap.get((ref as HTMLAnchorElement).href)
|
||||
const citation = document.createDocumentFragment()
|
||||
for (const node of cite!.childNodes) {
|
||||
citation.append(node.cloneNode(true))
|
||||
}
|
||||
return citation
|
||||
},
|
||||
})
|
||||
}
|
||||
|
||||
function onAbbreviation() {
|
||||
const content = document.querySelector('article.content')
|
||||
if (!content) return
|
||||
tippy(content.querySelectorAll('abbr[title][data-origin]'), {
|
||||
touch: 'hold',
|
||||
theme: 'light-border',
|
||||
interactive: true,
|
||||
appendTo: document.body,
|
||||
content(ref) {
|
||||
const fragment = document.createDocumentFragment()
|
||||
fragment.append(
|
||||
ref.getAttribute('data-origin')!,
|
||||
document.createElement('br'),
|
||||
document.createTextNode(`${ref.getAttribute('title')} (${ref.textContent})`)
|
||||
)
|
||||
return fragment
|
||||
},
|
||||
})
|
||||
}
|
||||
|
|
@ -0,0 +1,21 @@
|
|||
comma: 、
|
||||
# language
|
||||
language: 语言
|
||||
# article metadata
|
||||
author: 作者
|
||||
translators: 译者
|
||||
original: 原文
|
||||
keywords: 关键词
|
||||
published: 首次发表于
|
||||
updated: 最后修订于
|
||||
translated: 翻译于
|
||||
word-count: 字数
|
||||
word-count-text: 共 {{ .WordCount }} 字,阅读约 {{ .ReadingTime }} 分钟
|
||||
date-format: 2006 年 1 月 2 日
|
||||
# article notice
|
||||
notice: 注意:
|
||||
# article see-also
|
||||
see-also: 相关文章
|
||||
# 404 page
|
||||
page-not-found: 页面未找到
|
||||
page-not-found-description: 您请求的页面无法找到,<a href="{{ . }}">返回首页</a>
|
||||
|
|
@ -0,0 +1,21 @@
|
|||
comma: 、
|
||||
# language
|
||||
language: 語言
|
||||
# article metadata
|
||||
author: 作者
|
||||
translators: 譯者
|
||||
original: 原文
|
||||
keywords: 關鍵詞
|
||||
published: 首次發表於
|
||||
updated: 最後修訂於
|
||||
translated: 翻譯於
|
||||
word-count: 字數
|
||||
word-count-text: 共 {{ .WordCount }} 字,閲讀約 {{ .ReadingTime }} 分鐘
|
||||
date-format: 2006 年 1 月 2 日
|
||||
# article notice
|
||||
notice: 注意:
|
||||
# article see-also
|
||||
see-also: 相關文章
|
||||
# 404 page
|
||||
page-not-found: 頁面未找到
|
||||
page-not-found-description: 您請求的頁面無法找到,<a href="{{ . }}">返回首頁</a>
|
||||
|
|
@ -0,0 +1,21 @@
|
|||
comma: 、
|
||||
# language
|
||||
language: 語言
|
||||
# article metadata
|
||||
author: 作者
|
||||
translators: 譯者
|
||||
original: 原文
|
||||
keywords: 關鍵詞
|
||||
published: 首次發表於
|
||||
updated: 最後修訂於
|
||||
translated: 翻譯於
|
||||
word-count: 字數
|
||||
word-count-text: 共 {{ .WordCount }} 字,閱讀約 {{ .ReadingTime }} 分鐘
|
||||
date-format: 2006 年 1 月 2 日
|
||||
# article notice
|
||||
notice: 注意:
|
||||
# article see-also
|
||||
see-also: 相關文章
|
||||
# 404 page
|
||||
page-not-found: 頁面未找到
|
||||
page-not-found-description: 您請求的頁面無法找到,<a href="{{ . }}">返回首頁</a>
|
||||
|
|
@ -0,0 +1,13 @@
|
|||
{{- define "title" -}}
|
||||
{{- T "page-not-found" -}}
|
||||
{{- end -}}
|
||||
{{- define "main" }}
|
||||
<section class="container py-4">
|
||||
<header class="page-header">
|
||||
<p class="title">{{ T "page-not-found" }}</p>
|
||||
</header>
|
||||
<article class="content mt-6">
|
||||
<p>{{ T "page-not-found-description" .Site.Home.Permalink | safeHTML }}</p>
|
||||
</article>
|
||||
</section>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,17 @@
|
|||
{{- $index := .Attributes.index }}
|
||||
{{- if not $index }}
|
||||
{{- .Page.Scratch.Add "table-index" 1 -}}
|
||||
{{- $index = .Page.Scratch.Get "table-index" -}}
|
||||
{{- end }}
|
||||
{{- $rows := .Inner | transform.Unmarshal -}}
|
||||
<table id="table-{{ $index }}">
|
||||
<thead>
|
||||
<tr>{{ range (index $rows 0) }}<th>{{ . | markdownify }}</th>{{ end }}</tr>
|
||||
</thead>
|
||||
{{- $rows = after 1 $rows }}
|
||||
<tbody>
|
||||
{{- range $rows }}
|
||||
<tr>{{ range . }}<td>{{ replace . `\n` "\\\n" | markdownify }}</td>{{ end }}</tr>
|
||||
{{- end }}
|
||||
</tbody>
|
||||
</table>
|
||||
|
|
@ -0,0 +1,8 @@
|
|||
{{- if .Title }}
|
||||
<div class="card">
|
||||
<div class="card-image"><figure class="image"><img src="{{ .Destination | safeURL }}" alt="{{ .Text }}"></figure></div>
|
||||
<div class="card-content">{{ .Title }}</div>
|
||||
</div>
|
||||
{{- else }}
|
||||
<figure class="image"><img src="{{ .Destination | safeURL }}" alt="{{ .Text }}"></figure>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,33 @@
|
|||
{{- $text := .Text -}}
|
||||
{{- $destination := .Destination -}}
|
||||
{{- $parsed := urls.Parse $destination -}}
|
||||
{{- if in (slice "http" "https") $parsed.Scheme -}}
|
||||
{{- if eq .Destination .Text -}}
|
||||
{{- $host := replaceRE `^www\.` "" $parsed.Host -}}
|
||||
{{- $onlyPathHosts := slice "doi.org" "reddit.com" "github.com" -}}
|
||||
{{- if in $onlyPathHosts (lower $host) }}
|
||||
{{- $text = slicestr $parsed.Path 1 -}}
|
||||
{{- else -}}
|
||||
{{- $text = print $host $parsed.Path -}}
|
||||
{{- end }}
|
||||
{{- else -}}
|
||||
{{- if and (eq $parsed.Host "transfemscience.org") (hasPrefix $parsed.Path "/articles/") }}
|
||||
{{- $articleName := replaceRE `^/articles/(\S+)/$` "$1" $parsed.Path -}}
|
||||
{{- with .Page.GetPage $articleName -}}
|
||||
{{- if not .Params.hidden -}}
|
||||
{{- $destination = .Permalink -}}
|
||||
{{- with $parsed.Fragment -}}
|
||||
{{- $destination = print $destination "#" $parsed.EscapedFragment -}}
|
||||
{{- end -}}
|
||||
{{- end -}}
|
||||
{{- end -}}
|
||||
{{- end }}
|
||||
{{- end -}}
|
||||
{{- end -}}
|
||||
{{- if eq $parsed.Scheme "mailto" -}}
|
||||
<a href="mailto:{{ $parsed.Opaque | base64Encode }}">{{ cond (eq $text $parsed.Opaque) "" $text | safeHTML }}</a>
|
||||
{{- else if .Title -}}
|
||||
<a href="{{ $destination | safeURL }}" title="{{ .Title }}">{{ $text | safeHTML }}</a>
|
||||
{{- else -}}
|
||||
<a href="{{ $destination | safeURL }}">{{ $text | safeHTML }}</a>
|
||||
{{- end -}}
|
||||
|
|
@ -0,0 +1,20 @@
|
|||
{{- define "main" }}
|
||||
{{- $page := .Site.GetPage "articles" -}}
|
||||
<section class="container py-4">
|
||||
{{ partial "page-header" . }}
|
||||
<article class="content mt-6">
|
||||
{{- .Content }}
|
||||
<ul>
|
||||
{{- range $page.Pages.ByPublishDate.Reverse }}
|
||||
{{- if .Params.hidden }}{{- continue -}}{{- end }}
|
||||
<li data-author="{{ .Params.author }}">
|
||||
<p>
|
||||
<a href="{{ .Permalink }}">{{ .LinkTitle }}</a>
|
||||
<span class="is-inline-block">({{ .Params.author }}, {{ .PublishDate.Format "2006/1" }})</span>
|
||||
</p>
|
||||
</li>
|
||||
{{- end }}
|
||||
</ul>
|
||||
</article>
|
||||
</section>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,25 @@
|
|||
<!DOCTYPE html>
|
||||
<html lang="{{ .Language }}" prefix="og: http://ogp.me/ns#" class="has-navbar-fixed-top">
|
||||
<head>
|
||||
<meta charset="UTF-8">
|
||||
<meta name="viewport" content="width=device-width, initial-scale=1, minimum-scale=1">
|
||||
<title>
|
||||
{{- block "title" . -}}
|
||||
{{- cond .IsHome .Site.Title (print .Title " - " .Site.Title) -}}
|
||||
{{- end -}}
|
||||
</title>
|
||||
{{ partial "head/meta" . }}
|
||||
{{ partial "head/resources" . }}
|
||||
{{ partial "head/opengraph" . }}
|
||||
{{ partial "head/twitter" . }}
|
||||
{{ partial "head/telegram" . }}
|
||||
{{ partial "head/jsonld" . }}
|
||||
</head>
|
||||
<body>
|
||||
{{ partial "header" . }}
|
||||
<main class="section">
|
||||
{{- block "main" . }}{{- end }}
|
||||
</main>
|
||||
{{ partial "footer" . }}
|
||||
</body>
|
||||
</html>
|
||||
|
|
@ -0,0 +1,15 @@
|
|||
{{- define "main" }}
|
||||
<section class="container py-4">
|
||||
{{ partial "page-header" . }}
|
||||
<article class="content mt-6">
|
||||
{{- partial "notice" . }}
|
||||
{{ .Content }}
|
||||
<ul>
|
||||
{{- range .Pages }}
|
||||
{{- if .Params.hidden }}{{- continue -}}{{- end }}
|
||||
<li><a href="{{ .Permalink }}">{{ .Title }}</a></li>
|
||||
{{- end }}
|
||||
</ul>
|
||||
</article>
|
||||
</section>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,16 @@
|
|||
{{- define "main" }}
|
||||
<section class="container py-4">
|
||||
{{ partial "page-header" . }}
|
||||
<article class="content mt-6">
|
||||
{{- if eq .Section "articles" }}
|
||||
{{- partial "metadata" . }}
|
||||
{{- partial "notice" . }}
|
||||
{{ .Content }}
|
||||
{{- partial "related" . }}
|
||||
{{- else }}
|
||||
{{- partial "notice" . }}
|
||||
{{ .Content }}
|
||||
{{- end }}
|
||||
</article>
|
||||
</section>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1 @@
|
|||
{{ .Render "single" }}
|
||||
|
|
@ -0,0 +1,5 @@
|
|||
<footer class="footer">
|
||||
<main class="content has-text-centered">
|
||||
<p class="copyright">{{ .Site.Copyright | markdownify }}</p>
|
||||
</main>
|
||||
</footer>
|
||||
|
|
@ -0,0 +1,4 @@
|
|||
{{- $defines := dict "MEASUREMENT_ID" (jsonify .Site.GoogleAnalytics) -}}
|
||||
{{- with resources.Get "gtag.ts" | js.Build (dict "defines" $defines) | minify | fingerprint }}
|
||||
<script async defer src="{{ .Permalink }}" integrity="{{ .Data.Integrity }}"></script>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,90 @@
|
|||
{{- define "partials/parents.html" -}}
|
||||
{{- $parents := slice . -}}
|
||||
{{- if .Parent -}}
|
||||
{{- $parents = partial "parents.html" .Parent | append $parents -}}
|
||||
{{- end -}}
|
||||
{{- return $parents -}}
|
||||
{{- end -}}
|
||||
{{- define "partials/breadcrumb-items.html" -}}
|
||||
{{- $items := slice -}}
|
||||
{{- range $index, $page := partial "parents" . -}}
|
||||
{{-
|
||||
$item := dict
|
||||
"@type" "ListItem"
|
||||
"position" (add $index 1)
|
||||
"name" $page.Title
|
||||
"item" $page.Permalink
|
||||
-}}
|
||||
{{- $items = $items | append $item -}}
|
||||
{{- end -}}
|
||||
{{- return $items -}}
|
||||
{{- end }}
|
||||
{{- $about := ref . "about" -}}
|
||||
{{-
|
||||
$publisher := dict
|
||||
"@type" "Organization"
|
||||
"name" .Site.Author.name
|
||||
"url" .Site.Author.url
|
||||
"email" .Site.Author.email
|
||||
-}}
|
||||
{{-
|
||||
$creator := dict
|
||||
"@type" "Organization"
|
||||
"name" "Transfeminine Science"
|
||||
"url" "https://transfemscience.org"
|
||||
-}}
|
||||
{{- $authors := slice -}}
|
||||
{{- with .Params.author -}}
|
||||
{{-
|
||||
$author := dict
|
||||
"@type" "Person"
|
||||
"name" .
|
||||
"url" (print $about "#" (. | anchorize))
|
||||
-}}
|
||||
{{- $authors = $authors | append $author -}}
|
||||
{{- end -}}
|
||||
{{- range .Params.translators -}}
|
||||
{{-
|
||||
$author := dict
|
||||
"@type" "Person"
|
||||
"name" .
|
||||
"url" (print $about "#" (. | anchorize))
|
||||
-}}
|
||||
{{- $authors = $authors | append $author -}}
|
||||
{{- end -}}
|
||||
{{-
|
||||
$brand := dict
|
||||
"@context" "https://schema.org"
|
||||
"@type" "Organization"
|
||||
"name" .Site.Title
|
||||
"url" .Site.Home.Permalink
|
||||
"logo" (resources.GetMatch "favicon**").Permalink
|
||||
"email" .Site.Author.email
|
||||
-}}
|
||||
{{-
|
||||
$article := dict
|
||||
"@context" "https://schema.org"
|
||||
"@type" "Article"
|
||||
"name" .Title
|
||||
"url" .Permalink
|
||||
"author" $authors
|
||||
"creator" $creator
|
||||
"headline" .Title
|
||||
"wordCount" .WordCount
|
||||
"publisher" $publisher
|
||||
"maintainer" $publisher
|
||||
"description" .Description
|
||||
"dateCreated" .PublishDate
|
||||
"datePublished" .Date
|
||||
"dateModified" .Lastmod
|
||||
"copyrightNotice" (.Site.Copyright | markdownify | plainify)
|
||||
-}}
|
||||
{{-
|
||||
$breadcrumbs := dict
|
||||
"@context" "https://schema.org"
|
||||
"@type" "BreadcrumbList"
|
||||
"itemListElement" (partial "breadcrumb-items" .)
|
||||
-}}
|
||||
<script type="application/ld+json">
|
||||
{{ slice $brand $article $breadcrumbs | jsonify (dict "indent" " ") | safeJS }}
|
||||
</script>
|
||||
|
|
@ -0,0 +1,22 @@
|
|||
{{ hugo.Generator }}
|
||||
<meta name="page-key" content="{{ .TranslationKey }}">
|
||||
<meta name="google" content="notranslate">
|
||||
{{- with .Site.Params.ContentSecurityPolicy }}
|
||||
{{- $policy := delimit . "; " -}}
|
||||
<meta http-equiv="Content-Security-Policy" content="{{ $policy }}">
|
||||
{{- end }}
|
||||
{{- if .Params.hidden }}
|
||||
<meta name="robots" content="noindex, nofollow">
|
||||
{{- else }}
|
||||
<meta name="robots" content="noarchive">
|
||||
{{- end -}}
|
||||
{{- with .Description | default (cond .IsPage .Summary .Site.Params.description) }}
|
||||
<meta name="description" content="{{ . }}">
|
||||
{{- end }}
|
||||
<link rel="canonical" href="{{ .Permalink }}">
|
||||
{{- range .Translations }}
|
||||
<link rel="alternate" href="{{ .Permalink }}" hreflang="{{ .Language }}">
|
||||
{{- end }}
|
||||
{{- range .AlternativeOutputFormats }}
|
||||
<link rel="{{ .Rel }}" href="{{ .Permalink }}" type="{{ .MediaType.Type }}">
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,37 @@
|
|||
{{- $iso8601 := "2006-01-02T15:04:05Z07:00" -}}
|
||||
<meta property="og:title" content="{{ .Title }}">
|
||||
{{- with .Description | default (cond .IsPage .Summary .Site.Params.description) }}
|
||||
<meta property="og:description" content="{{ . }}">
|
||||
{{- end }}
|
||||
{{- with cond .IsPage "article" "website" }}
|
||||
<meta property="og:type" content="{{ . }}">
|
||||
{{- end }}
|
||||
<meta property="og:url" content="{{ .Permalink }}">
|
||||
<meta property="og:locale" content="{{ .Language }}">
|
||||
{{- range .Translations }}
|
||||
<meta property="og:locale:alternate" content="{{ .Language }}">
|
||||
{{- end }}
|
||||
<meta property="og:site_name" content="{{ .Site.Title }}">
|
||||
{{- with .Lastmod }}
|
||||
<meta property="og:updated_time" content="{{ .Format $iso8601 }}">
|
||||
{{- end }}
|
||||
{{- with resources.GetMatch "favicon**" }}
|
||||
<meta property="og:image" content="{{ .Permalink }}">
|
||||
{{- end }}
|
||||
{{- if .IsPage }}
|
||||
<meta property="article:section" content="{{ .Section }}">
|
||||
{{- with .PublishDate }}
|
||||
<meta property="article:published_time" content="{{ .Format $iso8601 }}">
|
||||
{{- end }}
|
||||
{{- with .Date }}
|
||||
<meta property="article:modified_time" content="{{ .Format $iso8601 }}">
|
||||
{{- end }}
|
||||
{{- with .Params.author }}
|
||||
<meta property="article:author" content="{{ . }}">
|
||||
{{- end }}
|
||||
{{- with .Params.translators }}
|
||||
{{- range . }}
|
||||
<meta property="article:author" content="{{ . }}">
|
||||
{{- end }}
|
||||
{{- end }}
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,12 @@
|
|||
{{- with resources.GetMatch "favicon**" -}}
|
||||
<link rel="icon" href="{{ .Permalink }}" integrity="{{ .Data.Integrity }}">
|
||||
{{- end }}
|
||||
{{- with resources.Get "main.scss" | toCSS | minify | fingerprint }}
|
||||
<link rel="stylesheet" href="{{ .Permalink }}" integrity="{{ .Data.Integrity }}">
|
||||
{{- end }}
|
||||
{{- with resources.Get "main.ts" | js.Build | minify | fingerprint }}
|
||||
<script async defer src="{{ .Permalink }}" integrity="{{ .Data.Integrity }}"></script>
|
||||
{{- end }}
|
||||
{{- if not .Site.IsServer }}
|
||||
{{- partial "head/google-analytics" . }}
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,3 @@
|
|||
{{- with .Site.Social.telegram -}}
|
||||
<meta name="telegram:channel" content="{{ . }}">
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,16 @@
|
|||
<meta name="twitter:card" content="summary">
|
||||
{{- with cond .IsHome .Site.Title (print .Title " - " .Site.Title) }}
|
||||
<meta name="twitter:title" content="{{ . }}">
|
||||
{{- end }}
|
||||
{{- with .Description | default (cond .IsPage .Summary .Site.Params.description) }}
|
||||
<meta name="twitter:description" content="{{ . }}">
|
||||
{{- end }}
|
||||
{{- with .Site.Social.twitter }}
|
||||
<meta name="twitter:site" content="{{ . }}">
|
||||
{{- end }}
|
||||
{{- with .Params.twitter | default .Site.Social.twitter }}
|
||||
<meta name="twitter:creator" content="{{ . }}">
|
||||
{{- end }}
|
||||
{{- with resources.GetMatch "favicon**" | fingerprint }}
|
||||
<meta name="twitter:image" content="{{ .Permalink }}">
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,38 @@
|
|||
{{- $page := . -}}
|
||||
<header class="navbar is-fixed-top" role="navigation" aria-label="main navigation">
|
||||
<main class="container">
|
||||
<section class="navbar-brand">
|
||||
<a class="navbar-item" href="{{ .Site.Home.Permalink }}">{{ .Site.Title }}</a>
|
||||
<a role="button" class="navbar-burger" aria-label="menu" aria-expanded="false">
|
||||
<span aria-hidden="true"></span>
|
||||
<span aria-hidden="true"></span>
|
||||
<span aria-hidden="true"></span>
|
||||
</a>
|
||||
</section>
|
||||
<section class="navbar-menu">
|
||||
<section class="navbar-start">
|
||||
{{- range .Site.Home.Pages }}
|
||||
{{- if .Params.hidden }}{{- continue -}}{{- end }}
|
||||
{{- $active := cond .IsNode (.InSection $page) (eq . $page) }}
|
||||
<a class="navbar-item{{ if $active }} is-active{{ end }}" href="{{ .Permalink }}">{{ .LinkTitle }}</a>
|
||||
{{- end }}
|
||||
</section>
|
||||
{{- if .IsTranslated }}
|
||||
<section class="navbar-end">
|
||||
<div class="navbar-item language has-dropdown is-hoverable">
|
||||
<a class="navbar-link">{{ T "language" }}</a>
|
||||
<nav class="navbar-dropdown">
|
||||
{{- range .AllTranslations }}
|
||||
{{- if eq $page . }}
|
||||
<a hreflang="{{ .Language }}" href="{{ .Permalink }}" class="navbar-item is-active">{{ .Language.LanguageName }}</a>
|
||||
{{- else }}
|
||||
<a hreflang="{{ .Language }}" href="{{ .Permalink }}" class="navbar-item">{{ .Language.LanguageName }}</a>
|
||||
{{- end }}
|
||||
{{- end }}
|
||||
</nav>
|
||||
</div>
|
||||
</section>
|
||||
{{- end }}
|
||||
</section>
|
||||
</main>
|
||||
</header>
|
||||
|
|
@ -0,0 +1,55 @@
|
|||
{{- $about := ref . "about" -}}
|
||||
{{- if or .Params.author .Params.translators }}
|
||||
<dl class="metadata">
|
||||
{{- with .Params.author }}
|
||||
<dt>{{ T "author" }}</dt>
|
||||
<dd><a href="{{ $about }}#{{ . | anchorize }}">{{ . }}</a></dd>
|
||||
{{- end }}
|
||||
{{- with .Params.translators }}
|
||||
<dt>{{- T "translators" -}}</dt>
|
||||
<dd>
|
||||
{{- range $index, $name := . -}}
|
||||
{{- if ne $index 0 -}}{{- T "comma" -}}{{- end -}}
|
||||
<a href="{{ $about }}#{{ $name | anchorize }}">{{ $name }}</a>
|
||||
{{- end -}}
|
||||
</dd>
|
||||
{{- end }}
|
||||
{{- with .Params.original | default (print "https://transfemscience.org/articles/" .File.ContentBaseName) }}
|
||||
<dt>{{ T "original" }}</dt>
|
||||
<dd>{{ . | markdownify }}</dd>
|
||||
{{- end }}
|
||||
{{- with .Params.wordCount | default .WordCount }}
|
||||
<dt>{{ T "word-count" }}</dt>
|
||||
{{- $wordCount := . | lang.FormatNumber 0 }}
|
||||
{{- $readingTime := div . 200 | math.Round }}
|
||||
<dd>{{ T "word-count-text" (dict "WordCount" $wordCount "ReadingTime" $readingTime) }}</dd>
|
||||
{{- end }}
|
||||
{{- with .Params.keywords }}
|
||||
<dt>{{ T "keywords" }}</dt>
|
||||
<dd>
|
||||
{{- range $index, $keyword := . -}}
|
||||
{{- if ne $index 0 -}}{{- T "comma" -}}{{- end -}}
|
||||
<span>{{ $keyword }}</span>
|
||||
{{- end -}}
|
||||
</dd>
|
||||
{{- end }}
|
||||
{{- with .PublishDate }}
|
||||
<dt>{{ T "published" }}</dt>
|
||||
<dd>{{ .Format (T "date-format") }}</dd>
|
||||
{{- end }}
|
||||
{{- if and .Date (ne .PublishDate .Date) }}
|
||||
<dt>{{ T "updated" }}</dt>
|
||||
<dd>{{ .Date.Format (T "date-format") }}</dd>
|
||||
{{- end }}
|
||||
{{- with .Lastmod }}
|
||||
<dt>{{ T "translated" }}</dt>
|
||||
<dd>{{ .Format (T "date-format") }}</dd>
|
||||
{{- end }}
|
||||
{{- with .Params.trackHash }}
|
||||
{{- if site.IsServer }}
|
||||
<dt>Track</dt>
|
||||
<dd><a href="https://github.com/mtf-wiki/tfsci-track/compare/{{ . }}..HEAD">{{ . }}</a></dd>
|
||||
{{- end }}
|
||||
{{- end }}
|
||||
</dl>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,3 @@
|
|||
{{- with .Params.notice }}
|
||||
<p class="notification"><b>{{ T "notice" }}</b>{{ . | markdownify }}</p>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1 @@
|
|||
<header class="page-header"><p class="title">{{ .Title }}</p></header>
|
||||
|
|
@ -0,0 +1,9 @@
|
|||
{{- $related := .Site.RegularPages.Related . | first 5 -}}
|
||||
{{- with $related }}
|
||||
<h2 id="see-also">{{ T "see-also" }}</h2>
|
||||
<ul>
|
||||
{{- range . }}
|
||||
<li><a href="{{ .Permalink }}">{{ .LinkTitle }}</a></li>
|
||||
{{- end }}
|
||||
</ul>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,11 @@
|
|||
{{- if ne (.TableOfContents | plainify | len) 0 -}}
|
||||
<aside class="sidebar">
|
||||
<main>
|
||||
<header>
|
||||
<button class="toggle"><svg><use xlink:href="#sidebar"></use></svg></button>
|
||||
<span>{{ T "table-of-contents" }}</span>
|
||||
</header>
|
||||
{{ .TableOfContents }}
|
||||
</main>
|
||||
</aside>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,2 @@
|
|||
User-agent: *
|
||||
Sitemap: {{ absURL "sitemap.xml" }}
|
||||
|
|
@ -0,0 +1,16 @@
|
|||
{{- $abbr := .Get 0 -}}
|
||||
{{- $abbreviation := index .Site.Data (print "abbreviation." .Page.Language.Lang) -}}
|
||||
{{- if $abbreviation }}
|
||||
{{- with index $abbreviation $abbr -}}
|
||||
{{ $html := printf `<abbr title=%q data-origin=%q>%s</abbr>` .origin .title $abbr }}
|
||||
{{- if .href -}}
|
||||
<a href="{{ .href }}" target="_blank">{{ $html | safeHTML }}</a>
|
||||
{{- else -}}
|
||||
{{ $html | safeHTML }}
|
||||
{{- end -}}
|
||||
{{- else -}}
|
||||
{{- errorf "%q not found with %q" $abbr .Page.Language -}}
|
||||
{{- end -}}
|
||||
{{- else }}
|
||||
<abbr>{{ $abbr }}</abbr>
|
||||
{{- end }}
|
||||
|
|
@ -0,0 +1,8 @@
|
|||
{
|
||||
"compilerOptions": {
|
||||
"target": "ES2020",
|
||||
"module": "ES2020",
|
||||
"moduleResolution": "Node",
|
||||
"strict": true
|
||||
}
|
||||
}
|
||||
Loading…
Reference in New Issue